眼球內源性風險

視網膜剝離
此疾病群的要點
Section titled “此疾病群的要點”1. 什麼是視網膜剝離?
Section titled “1. 什麼是視網膜剝離?”視網膜剝離(retinal detachment; RD)是指神經視網膜(感覺視網膜)從視細胞層內側的部分與視網膜色素上皮(RPE)層分離,兩者之間積聚視網膜下液的狀態。從胚胎學上講,神經視網膜由神經外胚層的內層分化而來,RPE由神經外胚層的外層分化而來,因此兩者的結合原本較弱,容易因各種原因發生剝離。10,20)
當發生視網膜剝離時,感光細胞與來自RPE和脈絡膜的氧氣及營養供應分離。發病早期即開始出現感光細胞外節的變性和脫落,若長期持續,則會進展為不可逆的感光細胞損傷。這種時間依賴性構成了視網膜剝離「緊急性」的依據。特別是當黃斑部(中心凹)剝離時,中心視力會迅速且嚴重下降,術後視力恢復也往往不完全。
視網膜剝離的基本分類
Section titled “視網膜剝離的基本分類”根據發病機轉,大致分為以下三型(也有將外傷性獨立為第四型的觀點)。
| 病型 | 英文名稱 | 主要縮寫 | 裂孔 | 牽引性 | 滲出性 |
|---|---|---|---|---|---|
| 裂孔性 | 裂孔性視網膜剝離 | RRD | ◎ | △(繼發性) | — |
| 牽引性 | 牽引性視網膜剝離 | TRD | — | ◎ | — |
| 滲出性 | 滲出性視網膜剝離 | ERD | — | — | ◎ |
| 外傷性 | 外傷性視網膜剝離 | — | △/◎ | △ | △ |
2. 依病型分類與流行病學
Section titled “2. 依病型分類與流行病學”2-1. 裂孔源性視網膜剝離(RRD)
Section titled “2-1. 裂孔源性視網膜剝離(RRD)”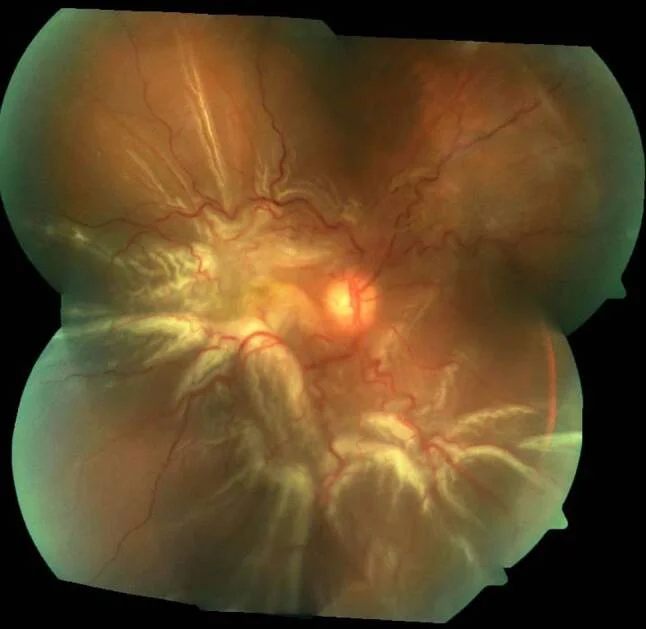
定義與流行病學
裂孔性視網膜剝離(rhegmatogenous retinal detachment; RRD)的名稱源自希臘語「rhegma」,意為「裂孔」。年發生率因地區而異,但通常為每10萬人約10~15例。對側眼視網膜剝離病史或家族史是發病的危險因子。7)
發病年齡呈雙峰分佈:
- 年輕高峰(20多歲):格子狀變性內萎縮性圓孔引起的扁平剝離
- 中老年高峰(50多歲):後玻璃體剝離(PVD)伴瓣狀裂孔引起的高聳剝離
年齡、性別與種族差異
PVD隨年齡增長發生,近視或白內障手術後更容易早期出現。裂孔性視網膜剝離的風險隨高齡、男性、近視、白內障術後、外傷、對側眼裂孔性視網膜剝離病史、格子狀變性等增加,發生率因地區和種族而異。7)
眼軸長度與近視的關聯
隨著眼軸延長,視網膜和玻璃體變性進展,裂孔性視網膜剝離的風險逐步升高。與眼軸長度小於24mm的正視眼相比,眼軸長度26mm以上(相當於高度近視)的周邊視網膜格子狀變性和萎縮性圓孔的出現率高出2-3倍。在日本,高度近視(超過-6屈光度)眼中黃斑圓孔型裂孔性視網膜剝離佔所有裂孔性視網膜剝離的約5%,高於歐美的0.5-2.0%。
發病的必要條件
裂孔性視網膜剝離的發生必須具備以下兩個條件:
- 視網膜的「孔」狀缺損(裂孔或圓孔)
- 玻璃體液化(液化玻璃體流入視網膜下的路徑)
近視是裂孔源性視網膜剝離的重要危險因子,據報告,超過-3屈光度的近視可使發病風險增加約10倍。高度近視眼易早期發生玻璃體後剝離(PVD),玻璃體液化和視網膜牽引進展較快。格子狀變性也是參與裂孔源性視網膜剝離發生的代表性周邊視網膜變性。7, 9)
主要危險因子
醫源性與外部風險
2-2. 牽引性視網膜剝離
Section titled “2-2. 牽引性視網膜剝離”牽引性視網膜剝離是因後玻璃體不完全剝離,導致玻璃體對視網膜產生強烈牽引而發病。大致可分為眼內增殖細胞引起的含新生血管之纖維血管膜型,以及玻璃體視網膜牽引型兩種。
| 類型 | 代表性疾病 | 牽引特徵 |
|---|---|---|
| 纖維血管膜型 | 增殖性糖尿病視網膜病變(PDR)、視網膜靜脈阻塞、早產兒視網膜病變(ROP) | 新生血管和纖維母細胞形成的視網膜前膜 |
| 單純玻璃體牽引型 | 玻璃體黃斑牽引症候群、穿孔性眼外傷 | 無新生血管的純粹牽引 |
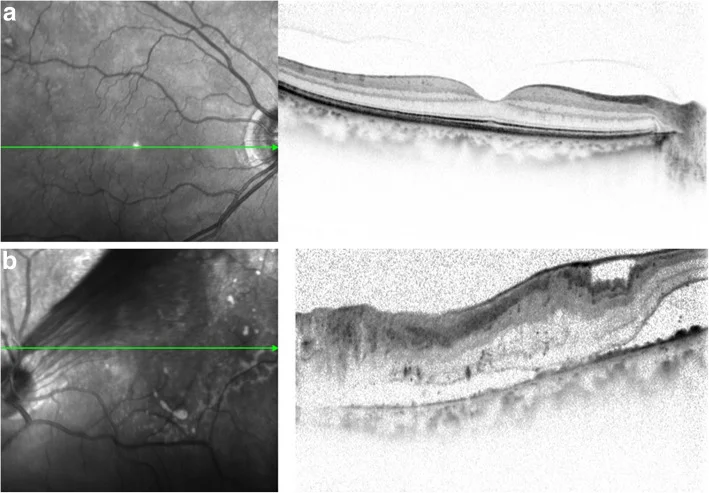
形態特徵
牽引性視網膜剝離無活動性,形態呈反向拱形(concave shape)。在新生血管根部(epicenter)或沿視網膜血管出現帳篷狀剝離,若沾黏廣泛則呈「桌面型(富士山型)」。若剝離呈穹頂狀且有活動性,需懷疑合併裂孔源性視網膜剝離(combined tractional-rhegmatogenous retinal detachment)。
2-3. 滲出性視網膜剝離
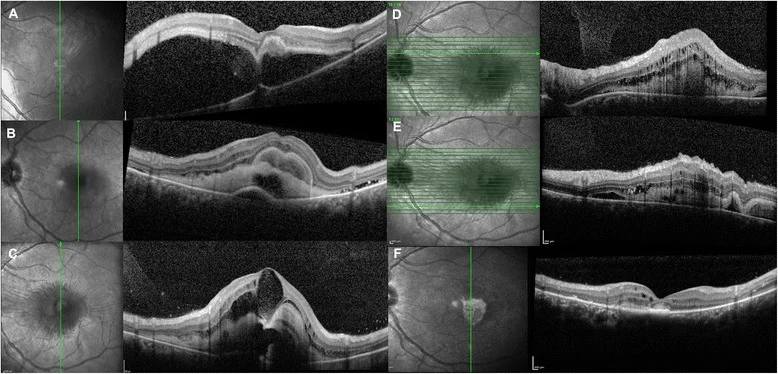
Section titled “2-3. 滲出性視網膜剝離”滲出性視網膜剝離是由於視網膜血管、RPE、脈絡膜等功能障礙導致視網膜下滲出液積聚而形成的非裂孔性視網膜剝離。血-視網膜屏障(BRB)破壞是最終共同病理狀態,原因多種多樣。
典型臨床特徵
- 視網膜剝離面呈穹頂狀突出,表面平滑
- 體位改變時液體移動(shifting fluid):與裂孔性視網膜剝離的重要鑑別要點
- 可能自然消退(因體位改變使液體排出)
主要病因
| 病因分類 | 代表性疾病 |
|---|---|
| 發炎性/免疫性 | Vogt-小柳-原田病(VKH)、後鞏膜炎、交感性眼炎、葡萄膜炎 |
| 血管性 | 中心性漿液性脈絡網膜病變(CSC)、Coats病、滲出型AMD、糖尿病性黃斑水腫 |
| 腫瘤性 | 脈絡膜惡性黑色素瘤、轉移性脈絡膜腫瘤、視網膜母細胞瘤 |
| 藥物性 | MEK抑制劑(如比美替尼)4)、免疫檢查點抑制劑(包括抗PD-1/PD-L1抗體引起的VKH樣症候群)12) |
| 全身性疾病 | 妊娠高血壓症候群/子癇前症(可能引起雙側滲出性視網膜剝離)6)/惡性高血壓 |
| 其他 | 特發性脈絡膜剝離/葡萄膜滲出 |
2-4. 外傷性視網膜剝離
Section titled “2-4. 外傷性視網膜剝離”外傷性視網膜剝離由鈍性或穿孔性眼外傷引起。鈍性外傷後立即發生視網膜剝離的比例為12%,1個月內為30%,8個月內為50%,24個月內達80%,因此需要長期追蹤。一種特殊類型是外傷引起的鋸狀緣斷裂(retinal dialysis)。
3. 症狀與緊急程度
Section titled “3. 症狀與緊急程度”主要自覺症狀
Section titled “主要自覺症狀”前驅症狀(尤其是裂孔性視網膜剝離)
| 症狀 | 機轉 | 注意事項 |
|---|---|---|
| 飛蚊症(突然增加或惡化) | 玻璃體出血或色素細胞漂浮(Shafer’s sign) | 突然飛蚊增加表示視網膜裂孔形成 |
| 閃光感 | 玻璃體牽引視網膜 | 在暗處、閉眼或眼球運動時加劇 |
| 簾狀視野缺損 | 對應剝離區域的敏感度下降 | 易被誤認為青光眼或眼瞼下垂 |
| 視力下降和視物變形 | 黃斑部剝離和水腫 | 黃斑剝離的指標 |
症狀與疾病類型的對應
裂孔性視網膜剝離
- 飛蚊症和閃光感常為前驅症狀
- 青少年型萎縮孔通常無症狀
- 窗簾狀視野缺損發生在剝離對側
- 玻璃體內菸草塵(Shafer氏徵)提示裂孔形成
牽引性視網膜剝離
滲出性視網膜剝離
- 主要表現為視力下降和視物變形
- VKH伴有頭痛、耳鳴和感冒樣全身症狀
- 視野缺損部位可能隨體位改變而變化
- 多為雙眼(尤其VKH和惡性高血壓)
眼壓變化
- 典型裂孔源性視網膜剝離:傾向低眼壓(合併脈絡膜剝離時更明顯)
- Schwartz症候群:感光細胞外節堵塞小樑網導致眼壓升高
- 滲出性視網膜剝離:眼壓隨原發病因變化
4. 檢查方法
Section titled “4. 檢查方法”| 確認事項 | 目的 |
|---|---|
| 症狀的發作形式與經過 | 鑑別急性(裂孔性)與慢性(牽引性/滲出性) |
| 閃光感和飛蚊症的有無及變化 | 估計PVD和裂孔形成的時間 |
| 近視的有無及度數 | 裂孔源性視網膜剝離風險評估 |
| 眼部手術或外傷史 | 醫源性或外傷性風險 |
| 全身性疾病(糖尿病、高血壓、自體免疫疾病) | 牽引性或滲出性視網膜剝離的原因搜尋 |
| 對側眼或家族視網膜剝離病史 | 辨識遺傳性疾病或高風險族群 |
| 懷孕及藥物使用史 | 尋找滲出性視網膜剝離的原因 |
裂隙燈顯微鏡檢查
Section titled “裂隙燈顯微鏡檢查”- 前房:細胞或閃輝(發炎性滲出性視網膜剝離的評估)
- 玻璃體:菸草塵(色素顆粒)= Shafer氏徵強烈暗示裂孔形成
- 眼壓:低眼壓暗示廣泛裂孔源性視網膜剝離合併脈絡膜剝離
散瞳眼底檢查
Section titled “散瞳眼底檢查”使用倒像檢眼鏡(雙眼倒像鏡)和鞏膜壓迫進行周邊部檢查是診斷的核心。
- 檢查剝離視網膜的範圍、形態和色調(混濁、透明度下降)
- 確定病因裂孔的位置、大小和形狀(瓣狀、圓形、巨大裂孔)
- 評估增殖性玻璃體視網膜病變(PVR)的有無及程度
5. 檢查(OCT、超音波、眼底檢查的選擇)
Section titled “5. 檢查(OCT、超音波、眼底檢查的選擇)”光學同調斷層掃描(OCT)
Section titled “光學同調斷層掃描(OCT)”OCT是確診視網膜剝離、鑑別類型、術前規劃及術後追蹤不可或缺的檢查。
| 檢查目的 | 獲得的資訊 |
|---|---|
| 確認黃斑部剝離的有無及程度 | 預測視力預後及判斷手術適應症 |
| 鑑別病型 | 裂孔源性 vs 滲出性(SRF的性質與形態) |
| 牽引性視網膜剝離的評估 | 增殖膜的位置和視網膜牽引模式 |
| 術後監測 | 視網膜復位和黃斑恢復的追蹤 |
OCT應觀察的結構及其意義
在視網膜剝離的術前和術後評估中閱讀OCT時,應關注以下結構。術後橢圓體帶(EZ)恢復取決於剝離的持續時間和範圍,EZ長度的恢復可作為術後視力的指標。3,15)
| 結構 | 所見的意義 |
|---|---|
| 橢圓體帶(ellipsoid zone; EZ) | 感光細胞內節/外節交界的高反射帶。剝離時間越長,越模糊/缺損→術後視力預後的指標 |
| 外界膜(external limiting membrane; ELM) | 位於EZ內層的高反射帶。比EZ更受保護,ELM的恢復先於EZ |
| 視網膜下高反射物質(SHRM) | 剝離視網膜下的PRE細胞與發炎殘留物。術後殘留會妨礙EZ恢復。 |
| 視網膜下液(SRF)的性質 | 裂孔源性視網膜剝離表現為低反射、均勻;滲出性視網膜剝離可呈穹窿狀伴點狀高反射。 |
OCT鑑別診斷要點
- 裂孔源性視網膜剝離:視網膜下液呈淡低反射,剝離邊緣陡峭,外節伸展,SHRM較少。
- 滲出性視網膜剝離:視網膜下液呈圓頂狀且平滑,可能伴有SHRM,反映移動性液體
- 牽引性視網膜剝離:增殖膜從內側牽引,呈凹形,活動性降低
超音波B型檢查
Section titled “超音波B型檢查”當眼底無法透見(玻璃體出血、白內障、角膜混濁)時,這是必需的檢查。將探頭置於角膜或鞏膜上,系統性地拍攝縱切面、橫切面和軸切面。
基本成像技術
- 使用10MHz或更高頻率(眼科高頻)的探頭,觀察眼球壁的動態。
- 讓患者進行眼球運動時:視網膜作為高亮度的硬膜移動(確認後壁附著),玻璃體柔軟地晃動(aftermovement陽性),增殖膜顯示中間運動。
- 透過在視神經乳頭處確認後壁附著,識別完全性視網膜全剝離(V形或T形)。
| 所見 | 意義 |
|---|---|
| 確認視網膜全剝離 | 視神經乳頭處後壁附著→判斷ERG和手術適應症 |
| 牽引性視網膜剝離的評估 | 增殖膜的位置、密度和範圍 |
| 漏斗型閉合性視網膜剝離(PVR D-3)的確認 | 預後不良的掌握 |
| 脈絡膜剝離的檢測 | 裂孔源性視網膜剝離的合併及低眼壓的原因 |
| 排除眼內腫瘤 | 滲出性視網膜剝離的腫瘤性病因鑑別 |
超廣角眼底攝影(UWF)的應用
Section titled “超廣角眼底攝影(UWF)的應用”超廣角雷射眼底相機(OptosSS、Clarijs等)單次拍攝可捕捉視網膜周邊部(近鋸齒緣)80–200°的範圍。
- 檢測傳統眼底攝影(45°)容易遺漏的周邊裂孔和格子狀變性
- 有助於術前客觀記錄裂孔位置和範圍(提高手術計劃精度)
- 術後追蹤時可監測周邊新出現的裂孔與剝離
- 但確認小裂孔(<0.5 DD)必須合併鞏膜壓迫眼底檢查;UWF影像上未見裂孔不能作為排除依據
螢光眼底血管攝影(FA·ICGA)
Section titled “螢光眼底血管攝影(FA·ICGA)”用於尋找滲出性視網膜剝離的原因。
- FA:CSC的RPE滲漏點、VKH的多發性強螢光、腫瘤性病變的染色
- ICGA:脈絡膜層級的循環評估、厚脈絡膜診斷、息肉狀脈絡膜血管病變(PCV)的識別
超廣角眼底攝影和眼底相機
Section titled “超廣角眼底攝影和眼底相機”- 用於術前記錄、追蹤觀察和裂孔位置的記錄
- 超廣角雷射眼底相機(如Optos)可提高周邊裂孔的發現率
- 但小裂孔可能無法透過眼底相機發現,因此必須合併使用鞏膜壓迫眼底檢查
6. 治療方針的考量
Section titled “6. 治療方針的考量”依病型的治療原則
Section titled “依病型的治療原則”| 病型 | 治療原則 | 緊急性 |
|---|---|---|
| 裂孔性視網膜剝離 | 手術封閉裂孔、視網膜復位 | 高(黃斑部剝離前手術) |
| 牽引性視網膜剝離 | 玻璃體手術解除牽引 | 中至高(進展或合併裂孔時緊急) |
| 滲出性視網膜剝離 | 治療原發疾病(內科/腫瘤科協作) | 取決於疾病 |
| 外傷性視網膜剝離 | 依損傷型態進行手術 | 開放性傷口為急症 |
裂孔源性視網膜剝離的手術選擇
Section titled “裂孔源性視網膜剝離的手術選擇”裂孔源性視網膜剝離的治療有三種手術方式。
鞏膜扣帶術(SB)
從眼外以冷凍凝固及鞏膜扣帶(矽膠材質)在裂孔處形成壓痕,使視網膜復位。
適應症:年輕患者、玻璃體未剝離、周邊單純裂孔 優點:保留水晶體、維持接近自然狀態的眼球形態 缺點:不適用於複雜病例或增殖性變化
玻璃體切除術(PPV)
氣性視網膜復位術(PR)
向眼內注入膨脹氣體,封閉裂孔,使視網膜復位。可作為門診手術進行。
適應症:侷限於上半部分的單個裂孔 優點:無需住院、創傷小 缺點:適應症病例有限、成功率略低於其他術式
術式選擇指南
- 年輕患者、玻璃體未剝離、單純裂孔 → 鞏膜扣帶術為首選
- 中老年患者、合併PVD、深部裂孔、多發裂孔、合併PVR → 玻璃體手術為適應症
- 初次手術的解剖學成功率在許多報告中高達80-90%以上,但術式間的優劣取決於病例背景(裂孔部位、PVR、有無人工水晶體等)10, 14)
- 多次手術後最終復位的案例很多,但黃斑部剝離時間和PVR的有無對視功能預後影響很大7, 18)
術後管理與氣體填充注意事項
玻璃體內氣體填充後,需要保持氣體壓迫裂孔位置的體位限制(通常俯臥或頭部傾斜)數天至2週。氣體吸收後眼內再次充滿液體。
| 氣體種類 | 眼內滯留時間 | 膨脹倍率 | 體位限制期間參考 |
|---|---|---|---|
| 空氣 | 5~7天 | 無膨脹 | 3~5天 |
| 20% SF₆ | 10~14天 | 約2倍 | 5~10天 |
| 14% C₃F₈ | 6~8週 | 約4倍 | 10~14天 |
氣體殘留期間的禁忌
- 搭乘飛機/高海拔登山:外界氣壓降低導致氣體膨脹,眼壓急劇升高,引起眼循環障礙(失明風險)。在氣體消失前禁止搭乘飛機,登機前必須經眼科確認。
- MRI檢查:過去使用的氣體是鐵磁性的,但目前使用的眼內氣體(SF₆、C₃F₈)是非磁性的,直接風險較低。但體位限制期間的磁場環境仍令人擔憂,術後管理中需向主治醫師確認。
- 氧化亞氮(笑氣)麻醉:笑氣溶解於眼內氣體,導致氣體急劇膨脹,引起眼壓升高。在氣體殘留期間進行全身麻醉時,務必告知麻醉醫師不要使用笑氣。
術後再剝離風險較高的時期
再剝離常在術後早期至數月內被發現,PVR和新發現或遺漏的裂孔是主要原因。指導患者若出現症狀(飛蚊症增加、視野缺損再次出現)應立即就診,並堅持術後定期追蹤。19, 22)
增殖性玻璃體視網膜病變(PVR)的管理
Section titled “增殖性玻璃體視網膜病變(PVR)的管理”PVR是裂孔性視網膜剝離的嚴重併發症,是阻礙視網膜復位的主要原因。剝離視網膜的傷口癒合過程過度,導致由RPE細胞、膠質細胞、成纖維樣細胞和巨噬細胞組成的增殖膜在視網膜上、下及玻璃體內形成,膜收縮使剝離的視網膜固定。
- 術後5–10%發生19)
- 發生時間:術後2–3週開始,6–8週完成
- 1983年視網膜學會分類(舊分類):Grade A–D
視網膜學會分類(舊分類,1983年)
| 分級 | 所見 |
|---|---|
| A | 玻璃體混濁(色素塊、玻璃體中的色素顆粒、視網膜上的色素塊) |
| B | 視網膜表面皺褶形成、視網膜血管迂曲、裂孔邊緣翹起、玻璃體活動性降低 |
| C-1至C-3 | 視網膜全層皺褶(1至3個象限) |
| D-1至D-3 | 涉及四個象限的固定皺襞(寬漏斗/窄漏斗/閉合漏斗) |
1991年,Machemer等人提出了新分類。新分類考慮了前部PVR和視網膜下病變,並用鐘點方位描述病變範圍。11) 伴有PVR的裂孔源性視網膜剝離通常需要玻璃體切除術,聯合增殖膜剝離、長效氣體或矽油填充,可能需要多次手術。7, 19)
近年來,越來越多的機構首次選擇PPV,導致前部PVR病例增加。玻璃體術後發生的PVR進展迅速,需要早期再次手術。
牽引性視網膜剝離的治療
Section titled “牽引性視網膜剝離的治療”牽引性視網膜剝離的治療原則是通過玻璃體手術解除牽引。增殖膜的處理需運用膜剝離和玻璃體剪,徹底進行眼內光凝和周邊玻璃體切除。若合併裂孔,則參照裂孔源性視網膜剝離追加氣液交換。
術前抗VEGF藥物投予可用於增殖性糖尿病視網膜病變伴隨牽引性視網膜剝離手術,以促使新生血管消退並減少術中出血。但由於纖維血管膜收縮可能加重牽引,需謹慎判斷手術時機與適應症。5)
滲出性視網膜剝離的治療
Section titled “滲出性視網膜剝離的治療”滲出性視網膜剝離的治療以原發病治療為基礎,很少直接進行視網膜手術復位。應確定發炎性、血管性、腫瘤性等原因,並根據各自情況選擇相應的內科與眼科治療。21)
| 原因 | 主要治療 |
|---|---|
| VKH病 | 以全身類固醇為主,復發或遷延病例可考慮免疫抑制劑(VKH是滲出性視網膜剝離的典型發炎性原因)。2, 21) |
| CSC | 觀察、雷射光凝固、光動力療法(PDT)、抗VEGF |
| 惡性高血壓、子癇前症 | 降壓治療、產科管理(分娩) |
| Coats病 | 雷射光凝固、冷凍凝固、抗VEGF、玻璃體手術 |
| 脈絡膜腫瘤 | 依腫瘤類別的腫瘤科治療(放射、摘除等) |
| 藥物性 | 停用致病藥物(MEK抑制劑停藥後數日消退) |
| 葡萄膜滲出 | 鞏膜減壓術(渦靜脈減壓) |
7. 病型別特徵與鑑別流程
Section titled “7. 病型別特徵與鑑別流程”7-0. 基於眼底所見的病型鑑別實務
Section titled “7-0. 基於眼底所見的病型鑑別實務”從眼底所見鑑別視網膜剝離的病型時,從以下三個觀點進行評估。
① 裂孔或圓孔的有無與形狀
| 裂孔類型 | 特徵 | 提示的病型 |
|---|---|---|
| 瓣狀裂孔(馬蹄形) | 玻璃體牽引導致蓋膜殘留;裂孔邊緣隆起 | 裂孔源性視網膜剝離(PVD後);快速進展 |
| 萎縮性圓孔 | 格子狀變性內的圓形全層缺損;邊緣平坦 | 裂孔源性視網膜剝離(青少年型);緩慢進展 |
| 巨大裂孔 | ≥1個象限(90°);邊緣可能翻轉 | 裂孔性視網膜剝離(高度近視);難治 |
| 鋸齒緣斷裂 | 沿鋸齒緣;多見於下耳側 | 外傷性視網膜剝離;年輕男性 |
| 無裂孔 | — | 牽引性視網膜剝離/滲出性視網膜剝離 |
② 增殖膜的有無與形態
- 無:多見於原發性裂孔性視網膜剝離和滲出性視網膜剝離
- 帳篷狀膜(凸型、不可動):牽引性視網膜剝離(增殖性糖尿病視網膜病變、ROP等)
- 固定皺襞(star fold):PVR合併裂孔源性視網膜剝離;處置困難
③ 視網膜下液的性狀與移動性
| 性狀 | 提示的疾病類型 |
|---|---|
| 透明、可移動(shifting fluid) | 滲出性視網膜剝離 |
| 透明,無移動性 | 裂孔源性視網膜剝離 |
| 混濁,黃白色 | 腫瘤性/炎症性滲出性視網膜剝離;陳舊性視網膜剝離 |
| 體位改變時液體移動 | 滲出性視網膜剝離(如VKH、CSC) |
7-1. 裂孔性視網膜剝離
Section titled “7-1. 裂孔性視網膜剝離”裂孔性視網膜剝離是最常見的視網膜剝離類型,是眼科急症的代表性疾病之一。主要亞型包括:
瓣狀裂孔(馬蹄形裂孔)型:因PVD導致視網膜撕裂。在有晶體眼的裂孔性視網膜剝離中約佔30%,表現為快速進展、高度泡狀剝離。
萎縮圓孔型:格子狀變性區內萎縮形成的圓孔。多見於年輕人和近視眼,表現為低平局限性剝離,進展緩慢。
巨大裂孔型:90度(1個象限)以上的裂孔。好發於伴有格子狀變性的高度近視眼。裂孔邊緣捲曲,使用比水重的液體全氟碳(PFC)進行玻璃體手術復位。
黃斑裂孔型:多見於高度近視女性,在日本約佔裂孔性視網膜剝離的5%(高於歐美的0.5%~2.0%)。包括內界膜(ILM)剝離的玻璃體手術為標準術式。
詳細資訊 → 裂孔性視網膜剝離文章
7-2. 牽引性視網膜剝離
Section titled “7-2. 牽引性視網膜剝離”增殖性糖尿病視網膜病變是最常見的原因。含有新生血管的纖維血管膜收縮,形成帳篷狀剝離。最初局限於周邊部,當波及黃斑部時會導致急速的視力下降。
- 增殖性糖尿病視網膜病變(PDR):從反覆玻璃體出血的階段,進展為膜收縮引起的牽引性視網膜剝離。
- 早產兒視網膜病變(第4/5期):周邊視網膜的纖維血管增生膜造成的牽引延伸至水晶體後表面
- 鐮狀細胞疾病、Eales病、視網膜靜脈阻塞等缺血性視網膜疾病:來自缺血性增殖膜的牽引7, 8)
詳細請見 → 牽引性視網膜剝離的文章
7-3. 滲出性視網膜剝離
Section titled “7-3. 滲出性視網膜剝離”非裂孔性、非牽引性的視網膜下液體積聚。體位改變時液體移動(shifting fluid)是其特徵。VKH急性期可出現多發性雙側穹隆狀剝離,適當的免疫抑制治療有望自然消退。腫瘤性原因則優先進行腫瘤的檢查和治療。
詳細請見 → 滲出性視網膜剝離的文章
7-4. 外傷性視網膜剝離及相關病變
Section titled “7-4. 外傷性視網膜剝離及相關病變”鈍性外傷(眼球挫傷)後數週至數月內可能發生視網膜剝離,因此必須長期追蹤觀察。
鋸狀緣斷裂(Retinal Dialysis):沿鋸狀緣(ora serrata)的全層斷裂,多見於年輕男性外傷後。好發於下顳側,因緩慢進展常無症狀。
脈絡膜破裂和視網膜震盪(Berlin水腫):鈍挫傷後立即出現的後極部水腫和出血。光感受器損傷可能永久存在。
相關文章 → 視網膜裂孔、圓孔和格子狀變性
7-5. 兒童視網膜剝離的特殊性
Section titled “7-5. 兒童視網膜剝離的特殊性”兒童視網膜剝離較成人少見,但由於基礎疾病不同,需要特殊考慮。
基礎疾病類型
| 疾病 | 特徵 | 剝離類型 |
|---|---|---|
| 早產兒視網膜病變(ROP)第4/5期 | 增殖膜牽引;可能延伸至水晶體後表面 | 主要為牽引性視網膜剝離 |
| 家族性滲出性玻璃體視網膜病變(FEVR) | 遺傳性(FZD4、LRP5等);周邊無血管區→裂孔/牽引 | 裂孔性視網膜剝離合併牽引性視網膜剝離 |
| Stickler症候群 | 第二型膠原蛋白基因突變;玻璃體變性/格子狀變性;血管旁變性 | 裂孔性視網膜剝離;多發裂孔 |
| Norrie病 | X染色體隱性遺傳;僅見於男性;玻璃體出血、眼球萎縮 | 牽引性視網膜剝離 |
| Bloch-Sulzberger症候群(色素失調症) | 僅見於女性(男性致死);無血管區→新生血管→牽引 | 牽引性視網膜剝離 |
| 先天性視網膜分離症 | X染色體隱性遺傳;黃斑部分離及周邊分離;1%~2%進展為視網膜剝離 | 裂孔源性視網膜剝離,分離型 |
治療的特殊性
- 兒童鞏膜固定容易且眼球順應性高,因此鞏膜扣帶術比成人更受偏好。特別是ROP第4A期,為減輕對增殖膜的牽引,環紮術為首選。
- 用於扣帶的矽膠條會因眼球生長而加重絞扼,因此建議在6個月內取出。
- ROP引起的牽引性視網膜剝離,在Stage 4A時期應在專業機構考慮手術適應症。Stage 4B/5解剖和視功能預後較差,需個別判斷是否保留水晶體。13)
- Stickler症候群確診後,建議進行360°雷射預防性凝固。
7-6. 與特殊病理狀態的關聯
Section titled “7-6. 與特殊病理狀態的關聯”增殖性玻璃體視網膜病變(PVR):裂孔源性視網膜剝離術後最嚴重的併發症。形成固定皺襞,視網膜變硬固定。術後5-10%發生,常需再次手術。
視網膜分裂症:視網膜在內網狀層或外網狀層分離。與視網膜剝離不同,無RPE分離。通過OCT、螢光血管造影和ERG鑑別。
詳情見 → 視網膜分裂症文章
與青光眼的關聯:裂孔源性視網膜剝離可能出現Schwartz症候群(外節碎片阻塞引起的繼發性開放隅角青光眼),合併脈絡膜剝離的視網膜剝離可出現低眼壓。滲出性視網膜剝離可能合併原發疾病引起的繼發性青光眼。
裂孔源性視網膜剝離的預後
Section titled “裂孔源性視網膜剝離的預後”解剖學預後:透過適當的手術,95%以上可實現視網膜解剖復位。首次手術成功率約90%以上,包括多次手術在內的最終復位率約達98%。
功能性預後(視力)
| 黃斑部剝離的有無 | 視力預後 |
|---|---|
| 黃斑部未剝離(macula-on) | 可望維持接近術前視力的視力 |
| 黃斑部剝離(macula-off) | 術後視力約半數在0.5以下,常殘留視野缺損和視物變形 |
術後併發症的發生率
| 併發症 | 發生率/時間 | 處理 |
|---|---|---|
| PVR(增殖性玻璃體視網膜病變) | 術後5%–10%;2–8週內形成19) | 玻璃體再手術、矽油 |
| 視網膜前膜(ERM) | PPV後可能發生(根據報告,頻率大致為10%至百分之十幾)16) | 如果視力或視物變形惡化,則行剝離手術 |
| 囊樣黃斑水腫(CME) | 黃斑剝離型10–20%;術後數月 | 抗VEGF、類固醇眼藥水、NSAIDs |
| 白內障進展 | PPV後2-3年核性白內障進展 | 白內障手術(多在PPV後1-2年) |
| 再剝離(裂孔源性) | 初次手術後5-10%;多數在術後6個月內 | 再次手術(追加鞏膜扣帶或再次PPV) |
復發與長期管理
- PVR導致的再剝離:術後5%~10%。發病時間多在術後2~8週
- 對側眼視網膜剝離:長期風險持續約10%
- 術後追蹤中發現新裂孔:5%~14%(尤其最初幾個月內)1)
- 需指導患者出現症狀時立即就醫
牽引性視網膜剝離的預後
Section titled “牽引性視網膜剝離的預後”原發疾病的控制直接影響視力預後。在糖尿病性牽引性視網膜剝離中,血糖管理和全視網膜光凝是基礎。手術成功率低於裂孔源性視網膜剝離,進展為PVR和再次手術的風險較高。
滲出性視網膜剝離的預後
Section titled “滲出性視網膜剝離的預後”通過治療原發疾病有望改善,但如果發生RPE萎縮或光感受器的器質性損傷,視力恢復將不完全。在VKH中,首次發作的早期治療可獲得良好預後,但復發病例可能出現日落現象、Dalen-Fuchs結節等慢性期變化。在腫瘤性滲出性視網膜剝離中,腫瘤的控制決定預後。
取決於手術方式和有無併發症。鞏膜扣帶術住院時間約1-2週,幾乎不需要體位限制。玻璃體切除術由於術後氣體填充,需要保持體位(俯臥或側臥)數天至2週。氣體殘留期間禁止航空旅行、登山等低氣壓環境。視力恢復在視網膜復位後可能需要數月,尤其是黃斑剝離的病例,需要追蹤半年至1年。
網膜復位(解剖学的成功)と視機能回復(機能的成功)は必ずしも一致しない。特に黄斑部が剥離していた症例では、OCTで確認される楕円体帯(EZ)の回復に数か月〜1年以上かかり、完全に回復しないこともある。剥離期間が長いほどEZの欠損が広くなり、術後視力は低くとどまる傾向がある。また術後に黄斑上膜や嚢胞様黄斑浮腫が生じた場合も視力回復を妨げることがあるため、術後のOCT定期検査が重要である。
PVRとは、網膜剥離の術後に眼内の創傷治癒反応が過剰になり、網膜色素上皮やグリア細胞・線維芽細胞が増殖して網膜の表面や下面に膜を形成した状態である。膜が収縮すると固定皺襞(star fold)が形成され、網膜の可動性が著しく低下して再剥離をきたす。術後5〜10%に発症し、初期の硬化したGrade A〜Bなら強膜バックリング術が奏効することもあるが、重症例(Grade C〜D)では硝子体再手術による増殖膜除去と長期タンポナーデが必要で、複数回の手術を要することも多い。
兒童視網膜剝離的發生率低於成人,但重要的是背景疾病不同。早產兒視網膜病變(ROP)、家族性滲出性玻璃體視網膜病變(FEVR)、Stickler症候群、Norrie病等遺傳性疾病較多,需要與單純裂孔源性視網膜剝離不同的管理。兒童眼鞏膜彈性高,鞏膜扣帶術通常比成人更有效。ROP以牽引性剝離為主,4A期手術是最佳適應症。扣帶術使用的矽膠帶會隨著眼球生長導致絞扼,因此需要在6個月內取出。
9. 相關文章
Section titled “9. 相關文章”- Flaxel CJ, Adelman RA, Bailey ST, et al. Posterior Vitreous Detachment, Retinal Breaks, and Lattice Degeneration Preferred Practice Pattern. Ophthalmology. 2020;127(1):P146-P181. 1)
- Goto H, Mochizuki M, Yamaki K, et al. Epidemiological survey of intraocular inflammation in Japan. Jpn J Ophthalmol. 2007;51(1):41-44. 2)
- Obata R, Yanagi Y, Tamaki Y, et al. Quantitative analysis of optical coherence tomography after vitreous surgery for rhegmatogenous retinal detachment. Am J Ophthalmol. 2005;139(6):1003-1008. 3)
- Urner-Bloch U, Urner M, Stieger P, et al. Transient MEK inhibitor-associated retinopathy in metastatic melanoma. Ann Oncol. 2014;25(7):1473-1476. 4)
- Zhao LQ, Zhu H, Zhao PQ, Hu YQ. A systematic review and meta-analysis of clinical outcomes of vitrectomy with or without intravitreal bevacizumab pretreatment for severe diabetic retinopathy. Br J Ophthalmol. 2011;95(9):1216-1222. doi:10.1136/bjo.2010.189514. PMID: 21216799. 5)
- Mackeen LD. Bilateral retinal detachment in preeclampsia. Am J Obstet Gynecol. 1997;177(4):948-949. 6)
- Xiong J, Mehta N, Sandhu S, et al. A review of rhegmatogenous retinal detachment: past, present and future. Wien Med Wochenschr. 2025;175:146-160. PMCID: PMC12031774. 7)
- Hayreh SS. Ocular vascular occlusive disorders: natural history of visual outcome. Prog Retin Eye Res. 2014;41:1-25. doi:10.1016/j.preteyeres.2014.04.001. PMID: 24769221. 8)
- Akiba J. Prevalence of posterior vitreous detachment in high myopia. Ophthalmology. 1993;100(9):1384-1388. 9)
- Yan X, Xu M, Su F. Surgical managements for rhegmatogenous retinal detachment: a network meta-analysis of randomized controlled trial. PLoS One. 2024;19(11):e0310859. 10)
- Machemer R, Aaberg TM, Freeman HM, et al. An updated classification of retinal detachment with proliferative vitreoretinopathy. Am J Ophthalmol. 1991;112(2):159-165. 11)
- Denu RA, Nair S, Patel S, et al. Vogt-Koyanagi-Harada-Like Uveitis Secondary to Pembrolizumab in Metastatic Gastric Cancer: A Case Report and Review of the Literature. Case Rep Oncol. 2024;17(1):1071-1086. doi:10.1159/000541133. PMID: 39474530. 12)
- Sahin A, Yonekawa Y, et al. Surgical Management and Outcomes for Retinopathy of Prematurity-Associated Retinal Detachment: Lens-Sparing Vitrectomy vs Lensectomy. Retina. 2020;40(4):610-617. doi:10.1097/IAE.0000000000002608. PMID: 31403588. 13)
- Tam AL, Yan P, Gan NY, Lam WC. The current surgical management of rhegmatogenous retinal detachments: a review. Clin Exp Ophthalmol. 2021;49(8):905-917. doi:10.1111/ceo.13976. PMID: 34272822. 14)
- Fawzi AA, Lee NG, Cheng L, et al. Recovery of photoreceptor outer segment length and the ellipsoid zone following surgery for rhegmatogenous retinal detachment. Br J Ophthalmol. 2011;95(4):570-573. 15)
- Wickham L, Bunce C, Wong D, et al. Epiretinal membrane formation and visual outcome after pars plana vitrectomy for primary retinal detachment. Retina. 2016;36(7):1213-1221. doi:10.1097/IAE.0000000000001178. PMID: 27308274. 16)
- Kim J, Ryu SY, Hong JH, Chung EJ. Incidence and risk factors for retinal detachment after cataract surgery in Korea: a nationwide population-based study from 2011 to 2015. Graefes Arch Clin Exp Ophthalmol. 2019;257(10):2193-2202. doi:10.1007/s00417-019-04423-x. PMID: 31388742. 17)
- Schwartz SG, Flynn HW Jr, Lee WH, et al. Primary retinal detachment: scleral buckle or pars plana vitrectomy? Curr Opin Ophthalmol. 2015;26(3):245-250. doi:10.1097/ICU.0000000000000157. PMID: 25789772. 18)
- Pastor JC, de la Rúa ER, Martín F. Proliferative vitreoretinopathy: risk factors and pathobiology. Prog Retin Eye Res. 2002;21(1):127-144. 19)
- Wolfensberger TJ. The historical discovery of the retinal detachment. Doc Ophthalmol. 2003;107(1):1-5. 20)
- Amer R, Nalcı H, Yalçındağ N. Exudative retinal detachment: a systematic approach to diagnosis and management. Curr Opin Ophthalmol. 2020;31(6):455-461. doi:10.1097/ICU.0000000000000731. PMID: 32776566. 21)
- Kunikata H, Nishida K. Long-term follow-up of vitrectomy for recurrent retinal detachment and established proliferative vitreoretinopathy. Jpn J Ophthalmol. 2001;45(6):626-631. PMID: 11792656. 22)
