前部PVR
玻璃體基底部的收縮:前部視網膜和睫狀體被向前牽引。
漏斗狀視網膜剝離:嚴重病例呈前後狹窄的漏斗狀剝離形態。
牽引力強:膜附著於玻璃體基底部,使剝離難以治療。

增殖性玻璃體視網膜病變(Proliferative Vitreoretinopathy; PVR)是由孔源性視網膜剝離(RRD)手術或RD本身引發的異常傷口癒合反應。視網膜色素上皮(RPE)細胞、膠質細胞和肌纖維母細胞增殖,在視網膜前、視網膜後和玻璃體基底部形成纖維收縮膜。這些膜的收縮牽拉視網膜,產生固定皺襞,導致視網膜再次剝離。
PVR是RD手術失敗的主要原因。75%的RD手術失敗歸因於PVR,3) 總體RD中PVR的發生率為5%~10%。3) 常在RD術後30~60天發病。1)
1983年視網膜學會提出了PVR的統一分類,之後1991年發表了Silverstone分類等修訂版。PVR是孔源性視網膜剝離最重要的預後決定因素,早期發現和適當干預直接影響視力預後。
慢性孔源性視網膜剝離、下方孔源性視網膜剝離、眼內炎、葡萄膜炎、急性視網膜壞死(ARN)5) 等是主要風險因素。詳情請參閱「原因與風險因素」一節。
PVR的自覺症狀常與基礎疾病視網膜剝離的症狀重疊。
黃斑部PVR(mPVR)在PPV後10至28天相對早期發生。2) 報告病例中,術後BCVA從20/38降至20/166。2)
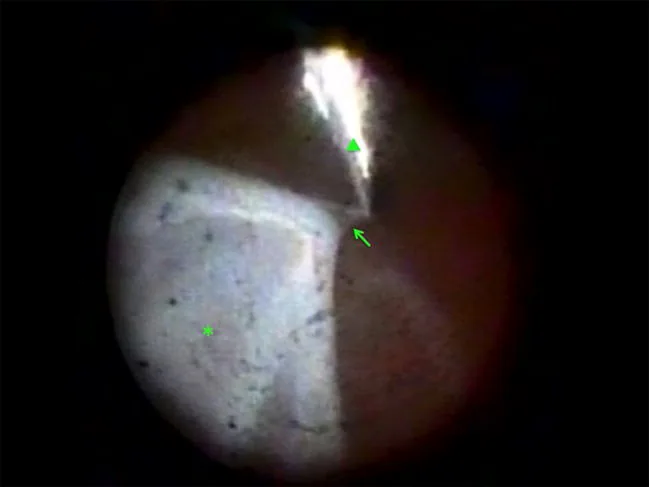
PVR最具特徵性的所見是固定皺褶(星形皺褶)。增殖膜收縮使視網膜折疊,形成即使在玻璃體手術時也無法展開的所謂「固定」皺褶。
前部PVR
玻璃體基底部的收縮:前部視網膜和睫狀體被向前牽引。
漏斗狀視網膜剝離:嚴重病例呈前後狹窄的漏斗狀剝離形態。
牽引力強:膜附著於玻璃體基底部,使剝離難以治療。
後部PVR
黃斑部PVR(mPVR)在OCT檢查中顯示特徵性表現。據報導,中心凹視網膜厚度(CMT)從711μm顯著增厚至354μm,2) 與通常的黃斑前膜(ERM)的鑑別很重要。ERM形成表面光滑的膜,而mPVR可見指狀突起樣結構。2)
超音波檢查可見V字形(後部PVR)或T字形(重度漏斗狀剝離)的特徵性表現。
PVR的根本原因是血-視網膜屏障(BRB)的破壞。BRB破壞後,血清中的生長因子(TGF-β、PDGF、IL-6等)進入玻璃體腔和視網膜下腔,誘導RPE細胞和神經膠質細胞的增殖和遷移。RPE細胞經上皮-間質轉化(EMT)分化為肌纖維母細胞,3) 產生收縮性的細胞外基質(ECM)。
已報導以下風險因素。
| 風險因素 | 分類 |
|---|---|
| 慢性/大型裂孔性視網膜剝離 | 解剖學因素 |
| 下方裂孔性視網膜剝離 | 解剖學因素 |
| 裂孔大或多發 | 解剖學因素 |
| 眼內炎、葡萄膜炎 | 發炎性因素 |
| 急性視網膜壞死(ARN) | 發炎性因素 |
| 糖尿病視網膜病變 | 全身性因素 |
| 腎功能障礙 | 全身性因素 |
| 吸菸 | 生活習慣因素 |
ARN(急性視網膜壞死)會導致血-視網膜屏障(BRB)大規模破壞,並引起嚴重的PVR。ARN後裂孔性視網膜剝離的發生率超過50%。5) 此外,糖尿病患者牽引性視網膜剝離(TRD)術後可能出現持續性視網膜下液(SRF),腎功能障礙是其持續存在的危險因子。4)
PVR的診斷主要透過裂隙燈顯微鏡(合併前房角鏡)和間接檢眼鏡進行眼底檢查。確認固定皺襞是診斷的關鍵。在玻璃體手術中無法展平的固定視網膜皺襞是PVR的確切表現。
PVR的嚴重程度分級廣泛採用視網膜學會(1983年)的以下分類。
| 分級 | 表現 |
|---|---|
| A | 玻璃體混濁、RPE變性、內界膜皺褶(僅少量) |
| B | 視網膜內面皺褶、視網膜裂孔邊緣捲曲、僵硬 |
| C | 固定皺襞(1/4圓周計為1CP) |
| D | 漏斗狀視網膜剝離(廣口型、狹口型、閉鎖型) |
在C級中,皺褶的範圍以其佔據的時鐘方位(CP)來量化,例如「C3」表示固定皺褶佔據3個時鐘方位。
通常在RD術後30至60天的定期追蹤中發現。1) 術前應識別慢性或下方裂孔源性視網膜剝離等風險因素,術後需密切觀察固定皺褶的形成。在mPVR中,OCT上檢測到指狀突起有助於早期診斷。2)
PVR的標準治療是玻璃體切除術(PPV:經睫狀體扁平部玻璃體切除術),包括增殖膜剝離和視網膜復位。主要手術要素如下:
對於黃斑部PVR(mPVR),有報導稱膜剝離後最佳矯正視力從20/166改善至20/57,2) 建議積極手術介入。
關於術後持續性視網膜下液(SRF),糖尿病TRD術後報告顯示術後1個月75%、3個月50%、6個月30%、12個月10%殘留。平均持續時間為4.4±4.7個月。4)
目前尚未建立標準的藥物治療,但已有幾種方法被報導。
| 藥物 | 給藥方式 | 證據等級 |
|---|---|---|
| MTX(甲氨蝶呤) | 玻璃體內注射200–400 μg | 臨床試驗中(研究階段) |
| 矽油 | 玻璃體腔填充 | 標準輔助治療 |
| 類固醇 | - | 非PVR治療標的 3) |
甲氨蝶呤(MTX)是最有希望的候選藥物,但詳情請參閱「最新研究與未來展望」一節。類固醇不被認為是PVR的治療標靶。3)
PVR的核心發病機制是RPE細胞的上皮-間質轉化(EMT)。3) 因RD脫離的RPE細胞釋放到玻璃體腔,在生長因子的刺激下發生以下變化。
PVR膜的主要組成細胞如下。2, 3)
BRB的破壞導致以下因子進入玻璃體腔,誘導增殖。
前部PVR發生在玻璃體基底(睫狀體平坦部至周邊視網膜)。該區域的膜將睫狀體、前部視網膜和玻璃體基底整體向前牽引,導致眼球低眼壓、漏斗狀剝離和完全失明等嚴重病變。解剖上手術難度高,矽油填充尤為重要。
ARN(急性視網膜壞死)後的PVR尤其嚴重。5) ARN病毒(VZV/HSV)引起的大規模BRB破壞導致血清蛋白和發炎性細胞因子大量進入玻璃體腔。這提供了強烈的增殖刺激,使得裂孔性視網膜剝離的發生率超過50%,且發生的PVR往往嚴重。5)
MTX是一種抑制二氫葉酸還原酶的抗葉酸藥物,具有抗增殖和抗發炎作用。通過玻璃體內局部給藥預防或治療PVR的研究正在全球進行。
GUARD試驗(3期RCT):術中及術後給予MTX可顯著降低再剝離率,提供了最可靠的證據。1)
Ambati等人(2024)報告了對先天性無虹膜症背景下的PVR病例,採用MTX 200μg每2週一次共5次,隨後每月一次維持治療。GUARD試驗(3期RCT)顯示術中及術後MTX可顯著降低再剝離率。1)
Babel等人(2022)報告了一例伴有PVR的復發性視網膜剝離,使用矽油1000cSt聯合單次MTX 400μg/0.10mL治療。3) MTX在玻璃體內的半衰期為3-5天,其通過抑制IL-6抑制PVR的機制已被提出。
FIXER試驗(NCT06541574):一項評估MTX預防PVR效果的新3期RCT正在進行中。1) 該試驗的結果可能決定MTX是否被納入標準治療。
局限於黃斑部的PVR(mPVR)近年來作為PPV後10-28天早期發生的獨立病因而受到關注。2) OCT上指狀突起的識別是診斷的關鍵,早期膜剝離可改善視力。2)
Khateb等人(2021)報告了一例PPV後最佳矯正視力從20/38降至20/166的病例,行膜剝離後術後視力改善至20/57。2) CMT從711μm恢復正常至354μm,提示mPVR應被視為獨立的臨床實體。
目前,它仍處於研究或臨床試驗階段,並未納入日本的標準治療。GUARD試驗和FIXER試驗等臨床試驗正在驗證其有效性,1) 可能影響未來的指南修訂。希望接受治療的患者應諮詢主治醫師。