PVR ส่วนหน้า
การหดตัวของฐานน้ำวุ้นตา: จอตาส่วนหน้าและซิลิอารีบอดีถูกดึงไปข้างหน้า
จอตาลอกรูปกรวย: ในรายที่รุนแรง จะมีลักษณะลอกรูปกรวยที่แคบลงจากหน้าไปหลัง
แรงดึงรั้งสูง: เนื่องจากเยื่อยึดติดกับฐานน้ำวุ้นตา การลอกจึงรักษายาก

โรคจอตาเสื่อมชนิดมีเยื่อเจริญ (Proliferative Vitreoretinopathy; PVR) เป็นการตอบสนองการสมานแผลที่ผิดปกติซึ่งเกิดขึ้นหลังการผ่าตัดจอตาลอกชนิดมีรู (RRD) หรือจากจอตาลอกเอง เซลล์เยื่อบุผิวรงควัตถุจอตา (RPE), เซลล์เกลีย และไมโอไฟโบรบลาสต์เพิ่มจำนวนและสร้างเยื่อพังผืดหดรั้งบนผิวหน้าด้านหน้าและด้านหลังของจอตาและฐานน้ำวุ้นตา การหดตัวของเยื่อเหล่านี้ดึงรั้งจอตา ทำให้เกิดรอยพับคงที่ และส่งผลให้จอตาลอกซ้ำ
PVR เป็นสาเหตุหลักของความล้มเหลวในการผ่าตัด RD 75% ของความล้มเหลวในการผ่าตัด RD เกิดจาก PVR3) และรายงานอุบัติการณ์อยู่ที่ 5-10% ของ RD ทั้งหมด3) มักเกิดขึ้นภายใน 30-60 วันหลังการผ่าตัด RD1)
ในปี 1983 Retina Society ได้เสนอการจำแนกประเภทแบบรวมสำหรับ PVR ต่อมาได้มีการตีพิมพ์ฉบับปรับปรุง เช่น การจำแนกของ Silverstone ในปี 1991 PVR เป็นปัจจัยพยากรณ์โรคที่สำคัญที่สุดสำหรับจอตาลอกชนิดมีรู และการตรวจพบตั้งแต่เนิ่นๆ และการแทรกแซงที่เหมาะสมมีความสัมพันธ์โดยตรงกับผลลัพธ์ทางสายตา
จอตาลอกชนิดมีรูเรื้อรัง, จอตาลอกชนิดมีรูส่วนล่าง, ภาวะติดเชื้อในลูกตา, ม่านตาอักเสบ, จอตาตายเฉียบพลัน (ARN)5) เป็นปัจจัยเสี่ยงหลัก ดูรายละเอียดในหัวข้อ “สาเหตุและปัจจัยเสี่ยง”
อาการที่ผู้ป่วยรับรู้ได้ของ PVR มักทับซ้อนกับอาการของจอตาลอกที่เป็นโรคพื้นฐาน
PVR ที่จุดรับภาพ (mPVR) เกิดขึ้นค่อนข้างเร็ว คือ 10-28 วันหลังการตัดน้ำวุ้นตา (PPV) 2) ในรายงาน มีการบันทึกการมองเห็นลดลงจาก 20/38 เป็น 20/166 หลังผ่าตัด 2)
อาการแสดงที่จำเพาะที่สุดของ PVR คือ รอยพับ固定 (star fold) การหดตัวของเยื่อ增生ทำให้จอตาพับ เกิดเป็นรอยพับ “固定” ที่ไม่สามารถกางออกได้แม้ในระหว่างการผ่าตัดน้ำวุ้นตา
PVR ส่วนหน้า
การหดตัวของฐานน้ำวุ้นตา: จอตาส่วนหน้าและซิลิอารีบอดีถูกดึงไปข้างหน้า
จอตาลอกรูปกรวย: ในรายที่รุนแรง จะมีลักษณะลอกรูปกรวยที่แคบลงจากหน้าไปหลัง
แรงดึงรั้งสูง: เนื่องจากเยื่อยึดติดกับฐานน้ำวุ้นตา การลอกจึงรักษายาก
PVR หลัง
รอยพับคงที่: รอยพับจอประสาทตาแนวรัศมีที่หดตัว พบในบริเวณขั้วหลังจนถึงส่วนรอบนอกกลาง
ลักษณะคล้ายเยื่อเหนือจอประสาทตา (ERM): ใน mPVR ที่จำกัดเฉพาะจุดรับภาพ (macula) การตรวจ OCT จะพบโครงสร้างยื่นคล้ายนิ้ว (finger-like projections) 2)
รอยพับรูปดาว: รอยพับที่ขั้วหลังรวมตัวกันเป็นรูปดาว ลักษณะเฉพาะ
PVR จุดรับภาพ (mPVR) แสดงลักษณะเฉพาะในการตรวจ OCT ความหนาจอประสาทตาบริเวณรอยบุ๋ม (CMT) มีรายงานว่าเพิ่มขึ้นอย่างมีนัยสำคัญจาก 711 μm เป็น 354 μm 2) และสิ่งสำคัญคือต้องแยกความแตกต่างจาก ERM ทั่วไป ERM จะสร้างเยื่อที่มีพื้นผิวเรียบ ในขณะที่ mPVR จะพบโครงสร้างยื่นคล้ายนิ้ว 2)
การตรวจอัลตราซาวนด์พบลักษณะเฉพาะรูปตัว V (PVR หลัง) หรือรูปตัว T (จอประสาทตาหลุดแบบกรวยรุนแรง)
ทั้งสองเป็นการสร้างเยื่อบนพื้นผิวจุดรับภาพ แต่ใน PVR การตรวจ OCT จะพบโครงสร้างยื่นคล้ายนิ้ว และมีลักษณะเฉพาะคือเกิดเร็วหลังผ่าตัด (10-28 วัน) 2) ERM จะแสดงเยื่อที่มีพื้นผิวค่อนข้างเรียบและเกิดอย่างช้าๆ การมองเห็นดีขึ้นหลังการลอกเยื่อสามารถคาดหวังได้แม้ใน mPVR 2)
สาเหตุพื้นฐานของ PVR คือ การแตกของสิ่งกีดขวางเลือด-จอประสาทตา (BRB) เมื่อ BRB แตก ปัจจัยการเจริญเติบโตในซีรั่ม (เช่น TGF-β, PDGF, IL-6) จะไหลเข้าสู่ช่องว่างน้ำวุ้นตาและใต้จอประสาทตา กระตุ้นการเพิ่มจำนวนและการย้ายที่ของเซลล์ RPE และเซลล์เกลียประสาท เซลล์ RPE ผ่านกระบวนการเปลี่ยนสภาพเยื่อบุผิวเป็นมีเซนไคม์ (EMT) เพื่อแยกความแตกต่างเป็นไมโอไฟโบรบลาสต์ 3) และผลิตสารนอกเซลล์ (ECM) ที่หดตัวได้
มีรายงานปัจจัยเสี่ยงดังต่อไปนี้
| ปัจจัยเสี่ยง | การจำแนก |
|---|---|
| จอประสาทตาหลุดชนิดรอยฉีกขาดเรื้อรังและขนาดใหญ่ | ปัจจัยทางกายวิภาค |
| จอประสาทตาลอกชนิดมีรอยฉีกขาดตำแหน่งด้านล่าง | ปัจจัยทางกายวิภาค |
| รอยฉีกขาดขนาดใหญ่หรือหลายรอย | ปัจจัยทางกายวิภาค |
| เยื่อบุตาอักเสบหรือม่านตาอักเสบ | ปัจจัยการอักเสบ |
| จอประสาทตาตายเฉียบพลัน (ARN) | ปัจจัยการอักเสบ |
| จอประสาทตาเสื่อมจากเบาหวาน | ปัจจัยทางระบบ |
| การทำงานของไตบกพร่อง | ปัจจัยทางระบบ |
| การสูบบุหรี่ | ปัจจัยการดำเนินชีวิต |
ARN (จอประสาทตาตายเฉียบพลัน) ทำให้เกิดการทำลายสิ่งกีดขวางเลือด-จอประสาทตา (BRB) อย่างกว้างขวาง ส่งผลให้เกิด PVR รุนแรง อุบัติการณ์ของจอประสาทตาลอกชนิดมีรอยฉีกขาดหลัง ARN สูงกว่า 50% 5) นอกจากนี้ ในผู้ป่วยเบาหวาน จอประสาทตาลอกชนิดดึงรั้ง (TRD) หลังผ่าตัดอาจทำให้เกิดของเหลวใต้จอประสาทตา (SRF) ที่คงอยู่ และการทำงานของไตบกพร่องเป็นปัจจัยเสี่ยงต่อการคงอยู่ของภาวะนี้ 4)
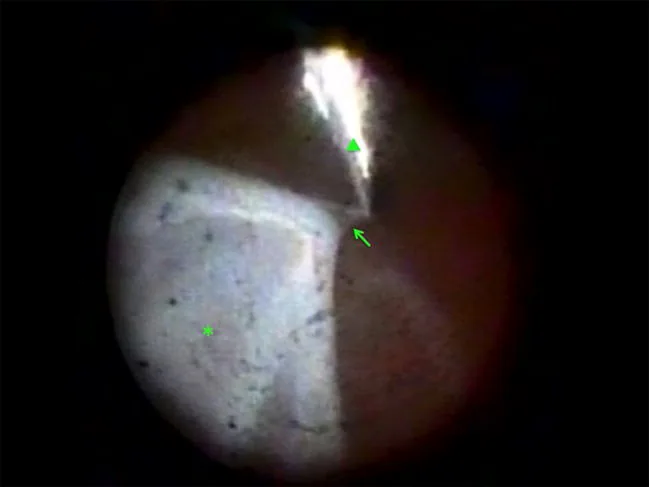
การวินิจฉัย PVR ส่วนใหญ่ทำโดยการตรวจอวัยวะภายในลูกตาด้วยกล้องจุลทรรศน์ชนิดกรีดแสง (ร่วมกับเลนส์ส่วนหน้า) และกล้องตรวจอวัยวะภายในลูกตาแบบกลับภาพ การยืนยัน รอยพับคงที่ เป็นจุดสำคัญของการวินิจฉัย รอยพับจอประสาทตาที่คงที่ซึ่งไม่สามารถยืดออกได้แม้ในระหว่างการผ่าตัดวุ้นตาเป็นสิ่งที่บ่งชี้ถึง PVR อย่างแน่นอน
การจำแนกความรุนแรงของ PVR ตามสมาคมจอประสาทตา (ค.ศ. 1983) ถูกใช้อย่างแพร่หลาย
| ระดับ | สิ่งที่พบ |
|---|---|
| A | ความขุ่นของวุ้นตา, การเสื่อมของเซลล์เยื่อบุผิวรงควัตถุจอประสาทตา, รอยพับของเยื่อลิมิตติ้งชั้นใน (เพียงสงสัย) |
| B | รอยพับบนผิวด้านในของจอประสาทตา, การม้วนของขอบจอประสาทตาฉีกขาด, ความแข็งเกร็ง |
| C | รอยพับคงที่ (หนึ่งในสี่ของวงกลมนับเป็น 1 CP) |
| D | จอประสาทตาลอกแบบกรวย (ชนิดปากกว้าง ปากแคบ ปิด) |
ใน Grade C ขอบเขตของรอยพับจะถูกวัดตามตำแหน่งนาฬิกา (CP: clockhour position) เช่น “C3” หมายถึงรอยพับคงที่ขนาด 3 ชั่วโมงนาฬิกา
มักพบในการตรวจติดตามเป็นระยะภายใน 30-60 วันหลังการผ่าตัดจอประสาทตาลอก 1) ก่อนผ่าตัด ควรระบุปัจจัยเสี่ยง เช่น จอประสาทตาลอกเรื้อรังหรือด้านล่าง และหลังผ่าตัดควรติดตามการเกิดรอยพับคงที่อย่างใกล้ชิด ใน mPVR การยืนยัน finger-like projections ใน OCT มีประโยชน์ต่อการวินิจฉัยระยะแรก 2)
การรักษามาตรฐานสำหรับ PVR คือ การผ่าตัดวุ้นตา (PPV: pars plana vitrectomy) เพื่อลอกเยื่อ增生และจัดจอประสาทตาให้เข้าที่ องค์ประกอบหลักของเทคนิคการผ่าตัดมีดังนี้:
ใน PVR จุดรับภาพ (mPVR) มีรายงานการปรับปรุงค่าสายตาที่ดีที่สุดที่แก้ไขแล้วจาก 20/166 เป็น 20/57 หลังการลอกเยื่อ 2) และแนะนำให้ทำการผ่าตัดเชิงรุก
เกี่ยวกับของเหลวใต้จอประสาทตาที่ยังคงอยู่หลังผ่าตัด รายงานหลังการผ่าตัด TRD จากเบาหวานพบว่ามีของเหลวเหลืออยู่ 75% ที่ 1 เดือน 50% ที่ 3 เดือน 30% ที่ 6 เดือน และ 10% ที่ 12 เดือน ระยะเวลาเฉลี่ยคือ 4.4 ± 4.7 เดือน 4)
ปัจจุบันยังไม่มีการรักษาด้วยยามาตรฐานที่ชัดเจน แต่มีรายงานแนวทางหลายวิธี
| ยา | วิธีการให้ | ระดับหลักฐาน |
|---|---|---|
| MTX (เมโธเทรกเซต) | ฉีดเข้าแก้วตา 200–400 ไมโครกรัม | อยู่ระหว่างการทดลองทางคลินิก (ระยะวิจัย) |
| ซิลิโคนออยล์ | การอุดช่องว่างแก้วตา | การรักษาเสริมมาตรฐาน |
| สเตียรอยด์ | - | ไม่ใช่เป้าหมายการรักษา PVR 3) |
เมโธเทรกเซต (MTX) เป็นยาที่มีแนวโน้มมากที่สุด แต่สำหรับรายละเอียด โปรดดูหัวข้อ “งานวิจัยล่าสุดและแนวโน้มในอนาคต” สเตียรอยด์ไม่ถือเป็นเป้าหมายการรักษาสำหรับ PVR 3)
กลไกหลักของ PVR คือ การเปลี่ยนสภาพของเซลล์เยื่อบุผิวเม็ดสีจอประสาทตาเป็นไมโอไฟโบรบลาสต์ผ่านกระบวนการเยื่อบุผิว-มีเซนไคม์ทรานซิชัน (EMT) 3) เซลล์เยื่อบุผิวเม็ดสีจอประสาทตาที่หลุดลอกเนื่องจากจอประสาทตาลอกจะถูกปล่อยเข้าสู่ช่องว่างน้ำวุ้นตา และภายใต้การกระตุ้นของปัจจัยการเจริญเติบโต จะเกิดการเปลี่ยนแปลงดังต่อไปนี้
เซลล์หลักที่ประกอบเป็นเยื่อ PVR มีดังนี้: 2, 3)
เนื่องจากการแตกของ BRB ปัจจัยต่อไปนี้จะไหลเข้าสู่ช่องว่างน้ำวุ้นตาและกระตุ้นการเจริญ
PVR ส่วนหน้าเกิดขึ้นที่ ฐานน้ำวุ้นตา (จากพาร์สพลานาของซิลิอารีบอดีถึงจอตาส่วนปลาย) เยื่อบริเวณนี้จะดึงซิลิอารีบอดี จอตาส่วนหน้า และฐานน้ำวุ้นตาไปข้างหน้าพร้อมกัน ทำให้เกิดความดันลูกตาต่ำ จอตาลอกแบบกรวย และตาบอดสนิท ทางกายวิภาค การผ่าตัดทำได้ยาก และการอุดด้วยน้ำมันซิลิโคน (SO) มีความสำคัญเป็นพิเศษ
PVR หลัง ARN (acute retinal necrosis) รุนแรงเป็นพิเศษ 5) เนื่องจากการแตกของ BRB อย่างกว้างขวางที่เกิดจากไวรัส ARN (VZV/HSV) ทำให้โปรตีนในซีรัมและไซโตไคน์อักเสบจำนวนมากไหลเข้าสู่ช่องว่างน้ำวุ้นตา สิ่งนี้กระตุ้นการเจริญอย่างรุนแรง ส่งผลให้อุบัติการณ์ของจอตาลอกแบบมีรอยฉีกขาดหลัง ARN สูงกว่า 50% และ PVR ที่เกิดขึ้นมักจะรุนแรง 5)
MTX เป็นยาต้านโฟเลตที่ยับยั้งเอนไซม์ dihydrofolate reductase มีฤทธิ์ต้านการเจริญเติบโตและต้านการอักเสบ ความพยายามในการป้องกันและรักษา PVR โดยการให้ยาเฉพาะที่เข้าแก้วตากำลังดำเนินไปทั่วโลก
การทดลอง GUARD (ระยะที่ 3 RCT): การให้ MTX ระหว่างและหลังการผ่าตัดแสดงให้เห็นว่าลดอัตราการหลุดซ้ำอย่างมีนัยสำคัญ โดยให้หลักฐานที่น่าเชื่อถือที่สุด 1)
รายงานของ Ambati และคณะ (2024) รักษาผู้ป่วย PVR ที่มีภาวะ aniridia แต่กำเนิดด้วย MTX 200 ไมโครกรัมทุก 2 สัปดาห์ จำนวน 5 ครั้ง ตามด้วยการบำรุงรักษารายเดือน การทดลอง GUARD (ระยะที่ 3 RCT) แสดงให้เห็นว่าการให้ MTX ระหว่างและหลังผ่าตัดลดอัตราการหลุดซ้ำอย่างมีนัยสำคัญ 1)
Babel และคณะ (2022) รายงานผู้ป่วยจอประสาทตาหลุดซ้ำที่มี PVR ซึ่งรักษาด้วยซิลิโคนออยล์ 1000 cSt และ MTX ขนาด 400 ไมโครกรัม/0.10 มล. เพียงครั้งเดียว 3) ค่าครึ่งชีวิตของ MTX ในแก้วตาประมาณ 3-5 วัน และมีการเสนอกลไกการยับยั้ง PVR ผ่านการยับยั้ง IL-6
การทดลอง FIXER (NCT06541574): การทดลองระยะที่ 3 RCT ใหม่ที่กำลังดำเนินการเพื่อตรวจสอบผลการป้องกัน PVR ของ MTX 1) ผลการทดลองนี้อาจกำหนดว่า MTX จะถูกรวมเข้าในการรักษามาตรฐานหรือไม่
PVR ที่จำกัดเฉพาะจุดรับภาพ (mPVR) เป็นภาวะอิสระที่เกิดขึ้นเร็ว 10-28 วันหลังการผ่าตัด PPV และเพิ่งได้รับความสนใจเมื่อเร็วๆ นี้ 2) การระบุ finger-like projections ด้วย OCT เป็นกุญแจสำคัญในการวินิจฉัย และการลอกเยื่อหุ้มแต่เนิ่นๆ แสดงให้เห็นว่าช่วยให้การมองเห็นดีขึ้น 2)
รายงานของ Khateb และคณะ (2021) ได้ทำการลอกเยื่อหุ้มในผู้ป่วยที่ค่าการมองเห็นที่ดีที่สุดที่แก้ไขแล้วลดลงจาก 20/38 เป็น 20/166 หลัง PPV และดีขึ้นเป็น 20/57 หลังผ่าตัด 2) ความหนาจุดรับภาพส่วนกลางลดลงจาก 711 ไมครอนเป็น 354 ไมครอน แสดงให้เห็นว่า mPVR ควรได้รับการยอมรับว่าเป็นหน่วยทางคลินิกอิสระ
ในปัจจุบัน เป็นการรักษาในขั้นตอนการวิจัยและการทดลองทางคลินิก ยังไม่รวมอยู่ในการรักษามาตรฐานในญี่ปุ่น ประสิทธิภาพของมันกำลังถูกทดสอบในการทดลองทางคลินิก เช่น GUARD และ FIXER 1) และอาจส่งผลต่อการปรับปรุงแนวทางปฏิบัติในอนาคต ควรปรึกษาแพทย์ผู้รักษาหากคุณต้องการรับการรักษา