จอประสาทตาเสื่อมชนิดสีสะสม (RP ) เป็นโรคจอประสาทตา เสื่อมทางพันธุกรรมที่พบใน 1 ใน 4,000–8,000 คน เป็นสาเหตุอันดับสอง (13.0%) ของความบกพร่องทางการมองเห็น ในผู้ที่ได้รับบัตรผู้พิการทางร่างกายรายใหม่อายุ ≥18 ปี และเป็นสาเหตุอันดับหนึ่งของภาวะตาบอดแต่กำเนิด 9) .
อาการแรกมักเป็นตาบอดกลางคืน (มองเห็นลำบากในที่มืด) ตามด้วยการแคบลงของลานสายตาอย่างค่อยเป็นค่อยไป โรคเริ่มมีอาการในช่วงอายุ 10–20 ปี และดำเนินไปจนถึงตาบอดใช้เวลาหลายสิบปี
มียีนเกี่ยวข้องมากกว่า 100 ยีน โดยมีรูปแบบการถ่ายทอดทางพันธุกรรมแบบออโตโซมอลโดมิแนนต์ ออโตโซมอลรีเซสซีฟ และแบบเชื่อมโยงกับโครโมโซม X กรณีประปรายพบมากที่สุด (48–63%) 9) .
ในชนิดรีเซสซีฟในคนญี่ปุ่น การกลายพันธุ์ของยีน EYS พบบ่อยที่สุด (30–50% ของกรณีที่ระบุยีนก่อโรคได้) 12) 13) .
ปัจจุบันยังไม่มีการรักษาที่หายขาด การดูแลมุ่งเน้นที่การปกป้องเซลล์รับแสง (วิตามินเอ ยูโนพรอสโตน นิลวาดิพีน ฯลฯ) การรักษาภาวะแทรกซ้อน (การรักษาภาวะบวมน้ำจอตาแบบซีสตอยด์ การผ่าตัดต้อกระจก ) และการดูแลผู้มีสายตาเลือนราง
ยาบำบัดด้วยยีน voretigene neparvovec (Luxturna) ได้รับการอนุมัติในญี่ปุ่นในปี 2023 9) จำกัดเฉพาะผู้ป่วยที่มีความแปรผันทางพยาธิวิทยาแบบสองอัลลีลในยีน RPE 65.
ได้รับการกำหนดให้เป็นโรคหายากที่กำหนด (ตั้งแต่วันที่ 1 มกราคม 2015) และมีสิทธิ์ได้รับเงินอุดหนุนค่ารักษาพยาบาล
จอประสาทตาเสื่อมชนิดสีสะสม (RP ) เป็นคำรวมสำหรับกลุ่มโรคทางพันธุกรรมที่มีลักษณะการเสื่อมแบบลุกลามเป็นวงกว้างของเซลล์รับแสง (เซลล์รูปแท่ง และเซลล์รูปกรวย ) และเยื่อบุผิวสีจอตา (RPE ) การเสื่อมของเซลล์รูปแท่ง เกิดขึ้นก่อนการเสื่อมของเซลล์รูปกรวย และชนิดนี้เรียกว่าโรคจอประสาทตา เสื่อมชนิดแท่ง-กรวย ซึ่งเข้าใจในความหมายเดียวกันกับ RP ไม่ใช่โรคเดียวแต่เป็นกลุ่มโรคที่เกี่ยวข้องกับยีนมากกว่า 100 ยีน
ความชุกคือ 1 ใน 4,000–8,000 คน โดยจำนวนผู้ป่วยทั้งหมดในญี่ปุ่นอย่างน้อย 30,000 คน (ผู้รับสิทธิโรคหายากที่กำหนด 20,687 คนในปี 2023) 9) ในส่วนที่เกี่ยวข้องกับความบกพร่องทางการมองเห็น RP เป็นสาเหตุอันดับสอง (13.0% รองจากต้อหิน 40.7% ในปี 2019) ของความบกพร่องทางการมองเห็น ในผู้ที่ได้รับบัตรผู้พิการทางร่างกายรายใหม่อายุ ≥18 ปี และเป็นสาเหตุอันดับหนึ่งของภาวะตาบอดแต่กำเนิด 9) ได้รับการกำหนดให้เป็นโรคหายากที่กำหนดภายใต้พระราชบัญญัติโรคหายากของญี่ปุ่น (ตั้งแต่วันที่ 1 มกราคม 2015) 9) และมีสิทธิ์ได้รับเงินอุดหนุนค่ารักษาพยาบาล
รูปแบบการถ่ายทอดทางพันธุกรรมแบ่งออกเป็นประเภทต่างๆ ดังนี้9) .
รูปแบบการถ่ายทอด ความถี่ ลักษณะ กรณีประปราย 48-63% พบบ่อยที่สุด; รวมถึง AR จำนวนมาก ถ่ายทอดแบบด้อยบนออโตโซม (AR) 20-35% การกลายพันธุ์ของ EYS พบบ่อยที่สุด ถ่ายทอดแบบเด่นบนออโตโซม (AD) 10-23% เริ่มมีอาการช้า พยากรณ์โรคค่อนข้างดี ถ่ายทอดแบบเชื่อมโยงกับโครโมโซม X (XL) 1.5-5% เพศชายรุนแรงกว่า; ดำเนินโรคเร็ว
เชื่อกันว่ากรณีที่เกิดขึ้นประปรายนั้นรวมถึงชนิด AR (ถ่ายทอดทาง autosomal recessive) จำนวนมาก
RP ยังมีชนิดที่เป็นกลุ่มอาการร่วมกับโรคทางระบบอื่นๆ และจัดอยู่ภายใต้แนวคิดที่กว้างขึ้นคือ โรคซิเลีย (ciliopathy) ดังนี้ 9) 2)
โรคซิเลีย (ciliopathy):
กลุ่มอาการอัชเชอร์ (type 1/2/3):RP + การสูญเสียการได้ยิน; โรคหายากที่กำหนด (AR). ใน type 1 จะมีการสูญเสียการได้ยินรุนแรงและความผิดปกติของระบบการทรงตัวตั้งแต่วัยเด็กกลุ่มอาการบาร์เด็ต-บีเดิล: โรคอ้วน, พัฒนาการทางจิตช้า, นิ้วเกิน, อวัยวะเพศเจริญไม่เต็มที่ (AR)กลุ่มอาการซีเนียร์-โลเกน: RP + โรคไตอักเสบในเด็กและวัยรุ่น (AR)กลุ่มอาการอัลสตรอม: RP + โรคอ้วน, การสูญเสียการได้ยิน, เบาหวาน (AR)กลุ่มอาการจูเบิร์ต: RP + สมองน้อยส่วน vermis เจริญไม่เต็มที่ (AR)
ความผิดปกติแต่กำเนิดของเมแทบอลิซึม:
โรคเมือกโพลีแซ็กคาไรด์สะสม (Hurler, Hunter): ร่วมกับความขุ่นของจอตาโรคเรฟซัม (ชนิดผู้ใหญ่และทารก): โรคเพอรอกซิโซม ; การเคลื่อนไหวไม่ประสานของสมองน้อย, โรคเส้นประสาทหลายเส้น (AR)กลุ่มอาการบาสเซน-คอร์นซ์ไวก์: ความผิดปกติของเมแทบอลิซึมไขมัน
โรคไมโทคอนเดรีย:
กลุ่มอาการเคิร์นส์-เซย์รี: กล้ามเนื้อตาภายนอกอ่อนแรงแบบลุกลามทั้งสองข้าง, หนังตาตก , การนำไฟฟ้าหัวใจผิดปกติ
โรคกล้ามเนื้อเสื่อม :
โรคกล้ามเนื้อเสื่อมชนิดไมโอโทนิก : อาจเกิดร่วมกับ RP
นอกจากนี้ การแยกความแตกต่างจากกลุ่มอาการต่างๆ เช่น PHARC (โรคปลายประสาทอักเสบหลายเส้น, หูหนวก, การทรงตัวผิดปกติ, RP , ต้อกระจก ), PCARP และกลุ่มอาการโอลิเวอร์-แมคฟาร์เลนก็มีความสำคัญเช่นกัน 3)
Q
โรคจอประสาทตาเสื่อมชนิดรงควัตถุเป็นโรคทางพันธุกรรมหรือไม่?
A
RP เป็นโรคทางพันธุกรรม แต่ไม่ได้ถ่ายทอดไปยังทุกคนเสมอไป ความเสี่ยงในการถ่ายทอดไปยังบุตรแตกต่างกันไปตามรูปแบบการถ่ายทอดทางพันธุกรรม ในชนิด AD มีโอกาส 50% ที่บุตรจะได้รับโรค ในขณะที่ชนิด AR หรือ XL ความเสี่ยงจะแตกต่างกันไปตามรูปแบบ การเกิดแบบประปราย (48-63% ของทั้งหมด) มักมีความเสี่ยงในการถ่ายทอดไปยังรุ่นต่อไปค่อนข้างต่ำ 9) แนะนำให้ใช้การให้คำปรึกษาทางพันธุกรรม
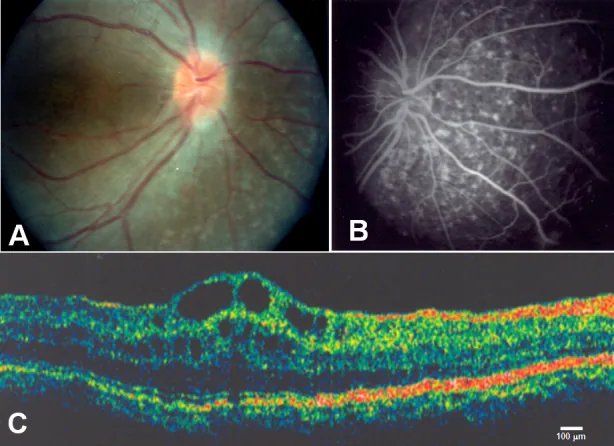
ภาพถ่ายจอประสาทตา, การตรวจหลอดเลือดด้วยฟลูออเรสซีน, และ OCT ของโรคจอประสาทตาเสื่อมชนิดรงควัตถุ Zenteno JC, et al. Compound heterozygosity for a novel and a recurrent MF
RP gene mutation in a family with the nanophthalmos-retinitis pigmentosa complex. Mol Vis. 2009. Figure 1. PM
CI D: PMC2742641. License: CC BY.
A แสดงดรูเซน ของหัวประสาทตาและการฝ่อของเยื่อบุผิวรงควัตถุจอประสาทตา อย่างกว้างขวาง, B แสดงการเรืองแสงของคอรอยด์ ที่สอดคล้องกับการฝ่อของเยื่อบุผิวรงควัตถุจอประสาทตา , C แสดงอาการบวมน้ำที่จุดรับภาพชนิดถุงน้ำและการแยกชั้นในของจอประสาทตา ที่รอยบุ๋มจอประสาทตา สอดคล้องกับอาการบวมน้ำที่จุดรับภาพชนิดถุงน้ำที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
อาการของ RP เปลี่ยนแปลงไปตามระยะของโรค เนื่องจากเซลล์รูปแท่ง เสื่อมก่อน อาการตามัวในที่มืดจึงปรากฏเป็นอาการแรกเริ่ม
ตามัวในที่มืด (night blindness) : การมองเห็น ลดลงหรือมองไม่เห็นในที่มืด ปรากฏเร็วมากเนื่องจากเซลล์รูปแท่ง เสื่อมก่อน 9) ; รับรู้ได้ในช่วงอายุ 10-20 ปี ว่ามองเห็นลำบากในที่แสงสลัว ในระยะแรก การมองเห็น ในเวลากลางวันมักปกติการแคบลงของลานสายตา : ลานสายตาแคบลงทีละน้อยจากรอบนอกเข้าสู่ส่วนกลาง พัฒนาจากจุดบอดรูปวงแหวนไปสู่การแคบลงของลานสายตาแบบศูนย์กลาง (การมองเห็น แบบอุโมงค์) 9) การมองเห็น ลดลงเซลล์รูปกรวย ดำเนินต่อไปหลังจากเซลล์รูปแท่ง การมองเห็น ส่วนกลางก็ลดลงเช่นกัน หากมี CME ร่วมด้วย อาจเกิดการมองเห็น ลดลงระดับปานกลางในระยะค่อนข้างต้น ในบางกรณี การมองเห็น ส่วนกลางอาจคงอยู่จนถึงระยะท้ายกลัวแสง (ตาบอดกลางวัน) : ความไวต่อแสง มากเกินไป เป็นอาการของความผิดปกติของเซลล์รูปกรวย เพิ่มขึ้นเมื่อการเสื่อมของเซลล์รูปกรวย ดำเนินไป สิ่งสำคัญคือต้องแยกความแตกต่างจากการกระจายแสงที่เกิดจากต้อกระจก ภาพแสงวาบ (photopsia) : อาจเกิดขึ้นเนื่องจากการเสื่อมและการสูญเสียเซลล์รับแสง ภาพหลอนทางตา (Charles Bonnet syndrome) : ปรากฏการณ์ที่ผู้ป่วยที่มีการมองเห็น ลดลงเห็นทิวทัศน์หรือบุคคลที่ไม่มีอยู่จริง ไม่ใช่ประสบการณ์ทางพยาธิวิทยา แต่เป็นปรากฏการณ์จากการทำงานมากเกินไปของคอร์เทกซ์การเห็น9)
ด้านล่างเป็นแนวทางการดำเนินของอาการตามระยะของโรค
ระยะ อาการหลัก ช่วงอายุโดยประมาณ ระยะแรก ตาบอดกลางคืน 10–20 ปี ระยะกลาง การแคบลงของลานสายตา (scotoma วงแหวน → เข้าสู่ศูนย์กลาง) 30–40 ปี ระยะปลาย การมองเห็น ลดลง, ความผิดปกติของการมองเห็นสี , กลัวแสง50 ปีขึ้นไป
กลุ่มอาการคลาสสิกสามประการของ RP เป็นที่รู้จักดังนี้
เม็ดสีคล้ายกระดูกชิ้นเล็ก : เม็ดสีลักษณะเฉพาะที่ปรากฏจากบริเวณกึ่งกลางรอบนอกไปจนถึงรอบนอก (รูปแบบ bone spicule)หลอดเลือดแดงจอประสาทตา ตีบแคบ : เกิดขึ้นทุติยภูมิจากการเสื่อมของเซลล์รับแสง จานประสาทตา ซีดคล้ายขี้ผึ้งเส้นประสาทตา
การจำแนกชนิดของโรค แบ่งเป็นชนิดปกติและชนิดผิดปกติ 9) .
RP ชนิดปกติ (rod-cone dystrophy )เซลล์รูปแท่ง ถูกทำลายก่อน ตามด้วยเซลล์รูปกรวย ในภายหลัง
Rod dystrophy (ชนิดย่อย) : เซลล์รูปกรวย ไม่ถูกทำลายจนถึงระยะท้าย; การมองเห็น ส่วนกลางยังคงดีแม้ลานสายตาตีบรุนแรง
RP ชนิดผิดปกติ9) :
RP ไร้เม็ดสี: ไม่พบเม็ดสีRP ข้างเดียว: พบเพียงข้างเดียว หรือความแตกต่างระหว่างสองตามากRP เฉพาะส่วน: จำกัดอยู่ที่ 1-2 จตุภาคของจอประสาทตา ; ดำเนินโรคช้า พยากรณ์โรคดีRP ชนิดกลางและกึ่งกลาง: รอยโรคจอประสาทตา และความผิดปกติของลานสายตาเริ่มจากศูนย์กลางจอประสาทตา อักเสบชนิดจุดขาว: รอยโรคจุดสีขาวถึงเหลืองบนจอประสาทตา
ในเด็ก มักไม่พบลักษณะที่ครบถ้วน และ ERG เป็นกุญแจสำคัญในการวินิจฉัย
ภาวะแทรกซ้อนที่สำคัญมีดังนี้9)
ต้อกระจก ชนิดใต้แคปซูลด้านหลัง (PSC)การมองเห็น ลดลงในที่สว่าง ความกว้างของโซนรูปไข่ (EZ ) ≥600 ไมครอน สามารถทำนายการมองเห็น หลังผ่าตัดต้อกระจก ที่ดีได้ (AUC 0.97)5) จอประสาทตา บวมน้ำชนิดซีสตอยด์ (CME )การมองเห็น ส่วนกลางลดลง9) ต้อหินมุมปิด 9) เยื่อเหนือจอตา (Epiretinal membrane) : พบร่วม 15.6-27.3%9) รูจอตาและรอยแยกที่โฟเวีย : พบได้ค่อนข้างน้อย แต่อาจเป็นข้อบ่งชี้ในการผ่าตัดน้ำวุ้นตา 9)
Q
การมองเห็นดีขึ้นหลังผ่าตัดต้อกระจกหรือไม่?
A
ในการผ่าตัดต้อกระจก ชนิดใต้แคปซูลด้านหลังที่เกิดร่วมกับ RP หากความกว้างของโซนรูปไข่ (EZ ) จากการตรวจ OCT ก่อนผ่าตัด ≥600 ไมครอน สามารถคาดหวังการมองเห็น หลังผ่าตัดที่ดีได้ (AUC 0.97)5) ความกว้างของ EZ เป็นตัวบ่งชี้ทางชีวภาพ ที่มีประโยชน์ในการทำนายการทำงานของการมองเห็น ก่อนผ่าตัด อย่างไรก็ตาม เส้นใยซินน์มักจะอ่อนแอ จึงต้องระวังการหดรัดตัวของแคปซูลด้านหน้าและเลนส์แก้วตาเทียม เคลื่อน ในการป้องกัน CME หลังผ่าตัด (10-14%) แนะนำให้ใช้ยาหยอดตาสเตียรอยด์ และ NSAID เป็นระยะเวลานานกว่าปกติ9)
RP เป็นกลุ่มโรคที่มีความหลากหลายทางพันธุกรรมสูง เกิดจากการกลายพันธุ์ของยีนมากกว่า 100 ยีน9) ด้านล่างนี้คือยีนก่อโรคหลักในคนญี่ปุ่นจำแนกตามรูปแบบการถ่ายทอดทางพันธุกรรม
การเปรียบเทียบยีนก่อโรคหลักแสดงไว้ด้านล่าง
ยีน รูปแบบการถ่ายทอด ความถี่/ลักษณะเฉพาะในคนญี่ปุ่น EYS AR 30-50% ของกรณีที่ระบุยีนก่อโรคได้ (พบมากที่สุดในชนิด AR)12) 13) USH2A AR พบบ่อยเป็นอันดับสองในชนิด AR (4-9%); ยีนหลักของกลุ่มอาการอัชเชอร์ 12) RHO AD พบบ่อยที่สุดในชนิด AD 6) RP GRเชื่อมโยงกับโครโมโซม X ประมาณ 70-75% ในชนิด XL 6) REEP6 AR หนึ่งในยีนก่อโรคชนิด AR 4)
รายละเอียดเพิ่มเติมเกี่ยวกับลักษณะของยีนแต่ละชนิดมีดังนี้
EYS (Eyes Shut Homolog) : ยีนก่อโรคที่พบบ่อยที่สุดในชนิด AR RP ในคนญี่ปุ่น (30-50% ของผู้ป่วยที่ระบุยีนได้) 12) 13) ความถี่นี้ไม่สูงเท่าในประเทศตะวันตก สะท้อนถึงพื้นฐานทางพันธุกรรมที่เป็นเอกลักษณ์ของคนญี่ปุ่นUSH2A : ยีนหลักของกลุ่มอาการอัชเชอร์ (RP + สูญเสียการได้ยิน) และเป็นยีนที่พบบ่อยเป็นอันดับสองในชนิด AR RP ในคนญี่ปุ่นรองจาก EYS (4-9%) 12) RHO (Rhodopsin) : ยีนที่พบบ่อยที่สุดที่ทำให้เกิด RP ชนิด AD 6) กำหนดรหัสโปรตีนรับแสงในเซลล์รูปแท่ง RP GR (Retinitis Pigmentosa GTPase Regulator)RP ชนิด XL 6) มีรายงานผู้ป่วยชายที่มีการกลายพันธุ์ของ RP GR และมีภาวะผิดปกติของซิเลียปฐมภูมิ (PCD) ร่วมด้วย 1) REEP6 (Receptor Expression-Enhancing Protein 6) : หนึ่งในยีนที่ทำให้เกิด RP ชนิด AR 4)
อัตราการตรวจพบยีนก่อโรคในการตรวจทางพันธุกรรมแตกต่างกันไปตามรูปแบบการถ่ายทอดทางพันธุกรรม สำหรับชนิด AD 35-60%, ชนิด AR/ผู้ป่วยประปราย 30-50%, และชนิด XL 16-36% 6)
นอกจากนี้ ใน RP ที่มีกลุ่มอาการ2) การแยกโรคจากกลุ่มอาการต่างๆ เช่น ภาวะเสียการทรงตัวของฟรีดริช (PHARC), PCARP , กลุ่มอาการ Oliver-McFarlane เป็นสิ่งสำคัญ 3)
Q
ควรตรวจพันธุกรรมหรือไม่?
A
การวินิจฉัยทางพันธุกรรมมีความสำคัญต่อการวินิจฉัยที่แน่นอน การให้คำปรึกษาทางพันธุกรรม และการพิจารณาความเหมาะสมในการรักษาด้วยยีน ระบบชุดตรวจ PrismGuide IRD (การวิเคราะห์ลำดับเอ็กซอนของยีนก่อโรคจอประสาทตา ทางพันธุกรรม 82 ยีนอย่างครอบคลุม) ได้รับการอนุมัติให้ครอบคลุมโดยประกันในปี 2023 แต่ ณ เดือนมิถุนายน 2025 มีไว้สำหรับผู้ป่วยอายุน้อยที่สงสัยว่าเป็น IRD ที่เกี่ยวข้องกับ RPE 65 เท่านั้น 9) แนะนำให้ทำร่วมกับการให้คำปรึกษาทางพันธุกรรม สามารถรับคำปรึกษาทางพันธุกรรมได้โดยไม่ต้องตรวจวินิจฉัยทางพันธุกรรม
การวินิจฉัย RP ทำได้โดยการรวมผลการตรวจทางคลินิก การตรวจทางไฟฟ้าสรีรวิทยา การตรวจภาพ และการตรวจทางพันธุกรรม
เกณฑ์การวินิจฉัย (เกณฑ์การรับรอง) 9) ประกอบด้วยองค์ประกอบต่อไปนี้:
ก. อาการ (อย่างน้อย 1 ข้อ) :
อาการที่ผู้ป่วยรู้สึกได้เองและดำเนินไป
อย่างน้อย 1 ข้อจาก: ตาบอดกลางคืน , การมองเห็น แคบลง, สายตาเลือนลาง, กลัวแสง
ข. ผลการตรวจ (อย่างน้อย 2 ข้อ) :
(1) ผลการตรวจอวัยวะภายในตา: หลอดเลือดจอประสาทตา ตีบ, สีจอประสาทตา หยาบ, เม็ดสีรูปกระดูก, จุดขาวหลายจุด, เส้นประสาทตา ฝ่อ, จุดรับภาพเสื่อม
(2) ความผิดปกติของ ERG
(3) ความผิดปกติของผล FAF
(4) ความผิดปกติของ EZ (ellipsoid zone) ใน OCT
ค. การตรวจทางพันธุกรรม (เสริม)
ง. การแยกโรคอื่นออก
การจำแนกระดับความรุนแรง 9) 10) :
ระดับ I : สายตาที่แก้ไขแล้ว ≥ 0.7, ไม่มีการแคบของลานสายตาระดับ II : สายตาที่แก้ไขแล้ว ≥ 0.7, มีการแคบของลานสายตา (เข้าข่ายโรคหายากที่กำหนด)ระดับ III : สายตาที่แก้ไขแล้ว < 0.7 และ ≥ 0.2 (เข้าข่ายโรคหายากที่กำหนด)ระดับ IV : สายตาที่แก้ไขแล้ว < 0.2 (เข้าข่ายโรคหายากที่กำหนด)
วิธีการตรวจหลักแสดงไว้ด้านล่าง
การตรวจ บทบาทหลัก ข้อสังเกตพิเศษ การตรวจคลื่นไฟฟ้าจอตา (ERG ) การวินิจฉัยที่แน่นอน การตอบสนองของเซลล์รูปแท่ง ลดลงก่อนการตอบสนองของเซลล์รูปกรวย 6) 9) OCT การประเมินสภาพและการพยากรณ์โรค ความกว้าง EZ : ตัวบ่งชี้ทางชีวภาพ สำหรับการพยากรณ์5) ; การบางลงของชั้นเม็ดเล็กด้านนอก FAF การประเมินกิจกรรมของโรค วงแหวนเรืองแสงผิดปกติ (AF ring) เป็นตัวบ่งชี้ระยะโรค6) การตรวจลานสายตา การประเมินการดำเนินโรค เครื่องวัดลานสายตา Goldmann; โปรแกรม HFA 10-2 ก็มีประโยชน์9) 10) การตรวจการมองเห็น สี การประเมินการทำงานของเซลล์รูปกรวย ความผิดปกติแบบน้ำเงิน-เหลืองที่เกิดขึ้นภายหลังพบบ่อย; การทดสอบ Panel D-15 และ 100 Hue9) การทดสอบการปรับตัวในที่มืด การประเมินการทำงานของเซลล์รูปแท่ง ไม่พบจุดหักเหของ Kohlrausch10) การตรวจยีน NGS การวินิจฉัยทางพันธุกรรม ชุดตรวจ PrismGuide IRD (82 ยีน) 9)
รายละเอียดของการตรวจแต่ละรายการแสดงไว้ด้านล่าง
การตรวจคลื่นไฟฟ้าจอตา (ERG ) : จำเป็นสำหรับการวินิจฉัยที่แน่นอน 6) 9) การตอบสนองของเซลล์รูปแท่ง (ERG ในที่มืด) ลดลงตั้งแต่แรกเริ่ม และเมื่อโรคดำเนินไป การตอบสนองของเซลล์รูปกรวย (ERG ในที่สว่าง) ก็ลดลงเช่นกัน ERG แบบเต็มลานตาเป็นมาตรฐานพื้นฐาน มักจะไม่สามารถบันทึกสัญญาณได้แล้วเมื่อมาตรวจครั้งแรกOCT (เครื่องตรวจชั้นจอตาด้วยแสง)EZ (โซนรูปไข่) ความกว้างของ EZ มีประโยชน์เป็นตัวบ่งชี้ทางชีวภาพ เชิงปริมาณสำหรับการทำงานของการมองเห็น และการพยากรณ์โรค และยังใช้ในการพิจารณาความเหมาะสมของการผ่าตัดต้อกระจก 5) พบการบางลงของชั้นนิวเคลียสชั้นนอกและการหายไปของ EZ ตั้งแต่ระยะแรกการตรวจการเรืองแสงเองของจอตา (FAF ) : พบวงแหวนเรืองแสงเองผิดปกติ (วงแหวน AF) รอบจอประสาทตา ซึ่งเป็นตัวบ่งชี้การดำเนินโรคและจอตาที่ยังมีหน้าที่เหลืออยู่ 6) การตรวจลานสายตา การตรวจลานสายตา แบบพลวัตด้วยเครื่องวัดลานสายตา Goldmann เป็นมาตรฐาน เมื่อโรคดำเนินไป จะเป็นไปตามแบบ scotoma วงแหวน → การแคบเข้าหาศูนย์กลางของลานสายตา 10) โปรแกรม HFA 10-2 มีประโยชน์ในการประเมินการทำงานของเซลล์รูปกรวย ส่วนกลางที่เหลืออยู่ 9) การตรวจการมองเห็น สี : มักพบความผิดปกติแบบสีน้ำเงิน-เหลืองที่เกิดขึ้นภายหลัง ประเมินด้วยการทดสอบ Panel D-15 และการทดสอบ 100 Hue 9) การตรวจการปรับตัวในที่มืด : ไม่พบจุดหักเหของ Kohlrausch (จุดเปลี่ยนระหว่างเซลล์รูปแท่ง และเซลล์รูปกรวย ) 10) เครื่องหาลำดับเบสรุ่นใหม่ (NGS) : ระบบชุดตรวจ PrismGuide IRD สามารถวิเคราะห์ลำดับเอ็กซอนของยีนก่อโรค 82 ยีนได้อย่างครอบคลุม 9) นอกจากนี้ยังจำเป็นสำหรับการพิจารณาความเหมาะสมของการรักษาด้วยยีน
โรคที่ต้องวินิจฉัยแยกโรคหลักตาม GL2026 แสดงไว้ด้านล่าง 9)
โรคทางพันธุกรรม : จอประสาทตา เสื่อมชนิดเซลล์รูปกรวย , จอประสาทตา เสื่อมชนิดเซลล์รูปกรวย -แท่ง, โรคสตาร์การ์ดต์ (ยีน ABCA4; จอประสาทตา เสื่อมเฉพาะที่), โรคโอกุจิ (จอตาดุจแผ่นทองคำ; ปรากฏการณ์มิซูโอะ-นากามูระ), ตามัวในที่มืดแต่กำเนิดชนิดคงที่ (จอตาปกติถึงสายตาสั้น ; คลื่น b ลบ), จอตามีจุดขาวกระจาย (fundus albipunctatus; ยีน RDH5), จอตาฉีกขาดแต่กำเนิด (ชนิด XL; เพศชาย), คอรอยเดอเรเมีย (คอรอยด์ ฝ่อกระจาย; ยีน CHM), จอตาและคอรอยด์ ฝ่อแบบวงแหวน (ornithine ในเลือดสูง; OAT บกพร่อง), จอตาเสื่อมแบบผลึก
โรคที่เกิดขึ้นภายหลัง : จอประสาทตา อักเสบจากภูมิต้านตนเอง (AIR), จอประสาทตาเสื่อมที่สัมพันธ์กับมะเร็ง (CAR), จอประสาทตาเสื่อมที่สัมพันธ์กับมะเร็ง ผิวหนังชนิดเมลาโนมา (MAR) (เริ่มต้นค่อนข้างเฉียบพลัน; ค้นหาแอนติบอดีต่อจอตา), จอประสาทตาเสื่อมจากยา (คลอโรควิน, เมลาโทนิน ฯลฯ), จอประสาทตา เสื่อมจากการบาดเจ็บ, การติดเชื้อ (หัดเยอรมัน, ซิฟิลิส, ทอกโซพลาสมา), AZOOR (ลานสายตาบอดเฉียบพลัน; จอตาปกติในระยะแรก)
ปัจจุบันยังไม่มีการรักษาที่หายขาดสำหรับ RP 6) 9) การรักษามุ่งเน้นที่การรักษาการทำงานของการมองเห็น การจัดการภาวะแทรกซ้อน และการสนับสนุนการใช้ชีวิตในสังคม
การปกป้องเซลล์รับแสง
วิตามินเอ (15,000 IU/วัน) : มีรายงานว่าการรับประทานชะลอการเสื่อมของ ERG ได้ไม่กี่เปอร์เซ็นต์ 14) ไม่ช่วยปรับปรุงการมองเห็น หรือลานสายตา จำเป็นต้องติดตามการทำงานของตับเมื่อใช้ระยะยาว ห้ามใช้ในระหว่างตั้งครรภ์เนื่องจากเสี่ยงต่อการทำให้ทารกพิการ ในผู้ที่มีการกลายพันธุ์ ABCA4 อาจทำให้โรคดำเนินเร็วขึ้น 14) ข้อควรระวัง: วิตามินอีอาจทำให้โรคดำเนินเร็วขึ้น จึงต้องระมัดระวัง 14)
ยาหยอดตา Unoprostone : แสดงแนวโน้มการปรับปรุงความไวที่ขึ้นกับขนาดยา แต่ไม่มีนัยสำคัญทางสถิติในตัวชี้วัดหลักของการทดลองระยะที่ 2 (ความไวของจอประสาทตา ส่วนกลาง 2 องศา) 16)
Nilvadipine (ยาปิดกั้นช่องแคลเซียม) : รายงานระยะยาวบ่งชี้ว่าชะลออัตราการดำเนินของความบกพร่องของลานสายตา 15) รายงานเหล่านี้มาจากศูนย์เดียวและมีจำนวนผู้ป่วยน้อย ยังไม่มีการทดลองแบบหลายศูนย์
N-acetylcysteine (NAC) : ยับยั้งความเครียดออกซิเดชัน การทดลองระยะที่ 1 รายงานว่าช่วยปรับปรุงการมองเห็น 17) และกำลังมีการทดลองระยะที่ 3 ในปี 2025
DHA และลูทีน : ปกป้องเซลล์รับแสง บริเวณจอประสาทตา ส่วนกลางจากความเครียดออกซิเดชัน การเพิ่ม DHA ลงในวิตามินเอไม่พบประโยชน์เพิ่มเติม
Helenien (Adaptinol) : ได้รับการอนุมัติให้ใช้ปรับปรุงลานสายตาและการปรับตัวในที่มืดชั่วคราวใน RP ยังไม่มีการประเมินประสิทธิผลตามมาตรฐานการแพทย์สมัยใหม่
แว่นตาป้องกันแสง : ลดความเครียดออกซิเดชันจากรังสียูวีและแสงจ้า แนะนำให้ใช้ทุกวัน
การรักษาภาวะแทรกซ้อน
การรักษาภาวะจอประสาทตา บวมน้ำชนิดซีสต์ (CME ) :
ทางเลือกแรกคือยับยั้งเอนไซม์คาร์บอนิกแอนไฮเดรส (CAI)
ใช้ dorzolamide (Trusopt) ยาหยอดตาหรือ acetazolamide (Diamox) รับประทาน การปรับปรุงความหนาจอประสาทตา ส่วนกลาง (CMT) ทำได้ประมาณ 40% เกิดการกลับเป็นซ้ำประมาณ 30% 9)
หากดื้อต่อ CAI ให้พิจารณาสเตียรอยด์
ใช้ triamcinolone acetonide (Macuoid) ฉีดเข้าแก้วตา หรือ dexamethasone ฝังในแก้วตา (Ozurdex )
ไม่แนะนำให้ใช้ยาต้าน VEGF ใน RP -CME เนื่องจากการผลิต VEGF ลดลง 9)
โปรดทราบว่าไม่มีวิธีการใดที่ได้รับการอนุมัติจากประกันสำหรับ RP -CME และใช้เป็นการใช้นอกเหนือข้อบ่งชี้
การผ่าตัดต้อกระจก : ดำเนินการในผู้ป่วยที่มีต้อกระจก ชนิดใต้แคปซูลด้านหลัง ความกว้างของ EZ ≥600 μm จากการตรวจ OCT ก่อนผ่าตัดเป็นปัจจัยพยากรณ์การมองเห็น หลังผ่าตัดที่ดี 5) ในกรณีที่เอ็นซินน์อ่อนแอ ให้พิจารณาใช้วงแหวนขยายแคปซูลเลนส์ เพื่อป้องกัน CME หลังผ่าตัด (10-14%) ให้ใช้ยาหยอดตาสเตียรอยด์ และ NSAID เป็นระยะเวลานานกว่าปกติ 9)
ต้อหินมุมปิด ต้อหินมุมปิดปฐมภูมิ สูงในผู้ป่วย RP ช่องหน้าม่านตา จะตื้นขึ้นเรื่อย ๆ ทำการตัดม่านตาด้วยเลเซอร์ เพื่อป้องกันหรือผ่าตัดต้อกระจก 9)
เยื่อเหนือจอตา (GL2026 CQ4) : การตัดแก้วตา การมองเห็น ดีขึ้นได้ในกรณีที่เส้น EZ ต่อเนื่อง ในกรณีที่เส้น EZ ไม่ต่อเนื่อง การฟื้นตัวมีจำกัด มีรายงานการฝ่อของจอประสาทตา อย่างรุนแรงในระยะยาวหลังผ่าตัด ดังนั้นควรประเมินในสถานพยาบาลเฉพาะทาง 9)
รูที่จอตา : การตัดแก้วตาเป็นการรักษาที่หายขาดเพียงวิธีเดียว การศึกษาเกี่ยวกับผลลัพธ์หลังผ่าตัดมีจำกัด 9)
การสนับสนุนและการฟื้นฟู
การดูแลผู้มีสายตาเลือนราง การมองเห็น เป็นสิ่งสำคัญ แนะนำให้ใช้ Smart Site (แนะนำสถานที่ปรึกษาสายตาเลือนรางในแต่ละภูมิภาค)
การให้คำปรึกษาทางพันธุกรรม
ระบบโรคหายาก : สามารถใช้ระบบช่วยเหลือค่าใช้จ่ายทางการแพทย์สำหรับโรคหายากที่กำหนด 9) ควรพิจารณาขอบัตรประจำตัวคนพิการทางกายและการสนับสนุนการดูแลตนเองด้วย
Voretigene neparvovec (Luxturna) : ยารักษาด้วยยีนที่สามารถให้แก่ผู้ป่วยที่มีความแปรปรวนทางพยาธิแบบสองอัลลีลในยีน RPE 65 และมีเซลล์จอประสาทตา ที่มีชีวิตเพียงพอ ได้รับการอนุมัติในญี่ปุ่นในปี 2023 9) ในการทดลองระยะที่ 3 ของสหรัฐอเมริกา (การศึกษา 301) มีผู้ลงทะเบียน 31 ราย และการวิเคราะห์ mITT (กลุ่มแทรกแซง 20 ราย กลุ่มควบคุม 9 ราย) แสดงให้เห็นการปรับปรุงอย่างมีนัยสำคัญใน MLMT และ FST แสงสีขาวเมื่อเทียบกับกลุ่มควบคุม 18) ในการทดลองระยะที่ 3 ในประเทศ (การศึกษา A11301) พบว่าความไว FST เพิ่มขึ้นและลานสายตาขยายในผู้ป่วยญี่ปุ่น 4 ราย 19) ผลในการปรับปรุงการมองเห็น มีจำกัด และมีรายงานการฝ่อของคอรอยด์ และจอประสาทตา เป็นภาวะแทรกซ้อนระยะยาวในมากกว่า 20% 9)
ดำเนินการทุก 6 เดือนถึง 1 ปี: การมองเห็น , กล้องจุลทรรศน์ชนิดกรีด, จอตา, การวัดลานสายตา Humphrey (HFA 10-2), OCT 9)
การรับประทานวิตามินเอมากเกินไปมีความเสี่ยงต่อพิษต่อตับและทำให้ทารกพิการ อย่าเพิ่มขนาดยาเอง 14)
ในจีโนไทป์เช่นการกลายพันธุ์ ABCA4 วิตามินเออาจส่งเสริมการดำเนินโรค ดังนั้นจึงสำคัญที่จะปรึกษาผู้เชี่ยวชาญหลังการวินิจฉัยทางพันธุกรรม 14)
การฉีดสเตียรอยด์ เข้าแก้วตาเพื่อรักษาภาวะจอประสาทตา บวมน้ำชนิดถุงน้ำมีความเสี่ยงต่อความดันลูกตา สูงและการดำเนินของต้อกระจก
ข้อบ่งชี้ในการผ่าตัดต้อกระจก จะพิจารณาหลังจากการประเมิน ERG และความกว้างของ EZ อย่างรอบคอบ
ไม่มียาใดสำหรับรักษาภาวะจอประสาทตา บวมน้ำชนิดถุงน้ำที่ได้รับการอนุมัติจากประกันสุขภาพสำหรับ RP -CME ดังนั้นจึงเป็นการใช้นอกข้อบ่งชี้ 9)
Q
ยาชนิดใดที่ใช้รักษาภาวะจอประสาทตาบวมน้ำ?
A
การรักษาทางเลือกแรกสำหรับ RP -CME คือยับยั้งเอนไซม์คาร์บอนิกแอนไฮเดรส เช่น ยาหยอดตาดอร์โซลาไมด์ หรือยาเม็ดอะเซตาโซลาไมด์ รับประทาน 9) การปรับปรุง CMT ทำได้ประมาณ 40% ของกรณี แต่ประมาณ 30% เกิดการกลับเป็นซ้ำ หากไม่ดีขึ้นด้วย CAI อาจเลือกใช้การฉีดไตรแอมซิโนโลน อะซีโทไนด์เข้าแก้วตา หรือการฝังเดกซาเมทาโซนเข้าแก้วตา (Ozurdex ) ไม่แนะนำให้ใช้ยา anti-VEGF สำหรับ RP -CME ควรทราบว่าทั้งหมดนี้เป็นการใช้นอกข้อบ่งชี้ที่ได้รับการอนุมัติ
วิถีร่วมสุดท้ายของการตายของเซลล์รับแสง ใน RP คืออะพอพโทซิส แม้ว่าชนิดของการกลายพันธุ์ทางพันธุกรรมจะหลากหลาย แต่สุดท้ายแล้วจะมาบรรจบกันที่วิถีการตายของเซลล์ร่วมกัน
ใน RP เซลล์รูปแท่ง จะเสื่อมและหายไปก่อน ตามด้วยการเสื่อมทุติยภูมิของเซลล์รูปกรวย 7) เซลล์รูปกรวย ต้องพึ่งพาปัจจัยโภชนาการที่ผลิตโดยเซลล์รูปแท่ง (RdCVF) เพื่อความอยู่รอด ดังนั้นหลังจากเซลล์รูปแท่ง หายไป เซลล์รูปกรวย ก็จะสูญเสียการทำงานเช่นกัน 7) 11)
จอประสาทตา เป็นเนื้อเยื่อที่มีการเผาผลาญสูงที่สุดชนิดหนึ่ง โดยเปลี่ยนกลูโคส 80-90% เป็นแลคเตทผ่านไกลโคไลซิสแบบใช้ออกซิเจน (Warburg effect) เซลล์รูปกรวย มีความไวต่อความเครียดจากการเผาผลาญมากกว่าเซลล์รูปแท่ง และความไวต่อการเผาผลาญนี้ยังเป็นปัจจัยในการเสื่อมทุติยภูมิของเซลล์รูปกรวย 11)
การอักเสบยังได้รับการยอมรับว่าเป็นปัจจัยหลักในการดำเนินของ RP โดยการกระตุ้นไมโครเกลียและการแทรกซึมของแมคโครฟาจทำให้ความเสียหายของจอประสาทตา แย่ลง 11) ความเครียดออกซิเดชันยังทำหน้าที่เป็นตัวขับเคลื่อนทางชีวภาพของการเสื่อมทุติยภูมิของเซลล์รูปกรวย
กลไกการเสื่อมแตกต่างกันไปตามยีน
การกลายพันธุ์ RHO : โรดอปซินที่พับผิดรูปทำให้เกิดความเครียดของเอนโดพลาสมิกเรติคูลัม → การตอบสนองต่อโปรตีนที่พับผิดรูป → อะพอพโทซิส 11) การกลายพันธุ์ REEP6 : REEP6 เข้ารหัสโปรตีนที่เกี่ยวข้องกับการรักษาสัณฐานของ ER การกลายพันธุ์ที่ก่อโรคทำให้เกิดการสร้าง inclusion ใน ER ที่ส่วนนอกของเซลล์รูปแท่ง นำไปสู่การเสื่อมของเซลล์รับแสง 4) การกลายพันธุ์ RP GR : RP GR เกี่ยวข้องกับโครงสร้าง axoneme ของซิเลียปฐมภูมิ และการกลายพันธุ์ทำให้การขนส่งสารไปยังส่วนนอกของเซลล์รับแสง บกพร่อง1)
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
การบำบัดด้วยยีน เป็นแนวทางที่มีแนวโน้มมากที่สุดในการรักษาโรคจอประสาทตา ทางพันธุกรรม8)
Luxturna (voretigene neparvovec) : ยารักษาด้วยยีนที่สามารถให้แก่ผู้ป่วยที่มีความแปรผันทางพยาธิวิทยาแบบสองอัลลีลในยีน RPE 65 ในการทดลองระยะที่ 3 ของสหรัฐอเมริกา (การศึกษา 301) มีผู้ลงทะเบียน 31 ราย และการวิเคราะห์ mITT (กลุ่มแทรกแซง 20 ราย กลุ่มควบคุม 9 ราย) แสดงให้เห็นการปรับปรุงอย่างมีนัยสำคัญใน MLMT และ FST แสงสีขาวเมื่อเทียบกับกลุ่มควบคุม18) ในการทดลองระยะที่ 3 ในประเทศ (การศึกษา A11301) มีการยืนยันการเพิ่มความไวของ FST และการขยายลานสายตาในชาวญี่ปุ่น 4 ราย19) ได้รับการอนุมัติในญี่ปุ่นในปี 2023 และทำหน้าที่เป็นสะพานเชื่อมระหว่างการรักษามาตรฐานและการรักษาวิจัย
การบำบัดด้วยยีน RP GRการบำบัดด้วยยีน ที่ใช้ AAV เป็นพาหะสำหรับ XL-RP เนื่องจากการกลายพันธุ์ RP GR ได้ก้าวหน้าไปสู่การทดลองทางคลินิกระยะที่ 1/2/38)
CRISPR/Cas9 : การวิจัยกำลังดำเนินการเพื่อแก้ไขการกลายพันธุ์ที่ก่อโรคโดยตรงหรือยับยั้งการกลายพันธุ์แบบเด่นเชิงลบ8)
RdCVF เป็นโปรตีนที่หลั่งจากเซลล์รูปแท่ง และรักษาการอยู่รอดของเซลล์รูปกรวย 7) 11) การทดลองทางคลินิกของการบำบัดปกป้องเซลล์รูปกรวย โดยใช้ RdCVF กำลังดำเนินอยู่ และเป็นกลยุทธ์การรักษาอิสระเพื่อรักษาการทำงานของเซลล์รูปกรวย หลังการเสื่อมของเซลล์รูปแท่ง
NAC เป็นยาที่ยับยั้งความเครียดออกซิเดชัน และการทดลองระยะที่ 1 รายงานว่ามีการปรับปรุงการมองเห็น 17) ณ ปี 2025 การทดลองระยะที่ 3 กำลังดำเนินอยู่
การศึกษาในร่างกายเมื่อเร็วๆ นี้ (แบบจำลองหนู rd10) แสดงให้เห็นว่า dexamethasone ชนิดฉีดเข้าแก้วตา ช่วยปกป้องเซลล์รับแสง รูปกรวยและเยื่อบุผิวเม็ดสีจอประสาทตา 11) กลูโคคอร์ติคอยด์มีศักยภาพในการนำกลับมาใช้ใหม่สูงในฐานะการรักษาที่ไม่ขึ้นกับการกลายพันธุ์ อย่างไรก็ตาม หลักฐานในปัจจุบันจำกัดอยู่เพียงแบบจำลองสัตว์ และจำเป็นต้องมีการตรวจสอบเพิ่มเติมสำหรับการประยุกต์ใช้ทางคลินิกในมนุษย์
การปลูกถ่ายจอประสาทตา จากเซลล์ iPS : การวิจัยเกี่ยวกับการปลูกถ่ายแผ่นเซลล์รับแสง ที่สร้างจากเซลล์ iPS ของผู้ป่วยเองกำลังดำเนินอยู่จอประสาทตา เทียม (อุปกรณ์เทียมจอประสาทตา )RP ระยะสุดท้าย Argus II และอื่นๆ ได้ถูกนำมาใช้จริงในต่างประเทศ และการทดลองทางคลินิกของวิธีการกระตุ้นผ่านคอรอยด์ -จอประสาทตา กำลังดำเนินอยู่ในญี่ปุ่น
Q
การบำบัดด้วยยีนมีให้บริการในญี่ปุ่นด้วยหรือไม่?
A
Voretigene neparvovec (Luxturna) ได้รับการอนุมัติในญี่ปุ่นในปี 2023 แต่จำกัดเฉพาะจอประสาทตา เสื่อมที่มีความแปรปรวนทางพยาธิวิทยาแบบสองอัลลีลในยีน RPE 65 9) 18) 19) การบำบัดด้วยยีน สำหรับ RP ที่มีการกลายพันธุ์ของยีนอื่นๆ รวมถึงการกลายพันธุ์ RP GR ยังอยู่ในขั้นตอนการทดลองทางคลินิก 7) และยังไม่ได้รับการอนุมัติให้เป็นการรักษาทั่วไปในญี่ปุ่น
Q
จะได้รับการรักษาในขั้นตอนการวิจัยได้อย่างไร?
A
การเข้าร่วมการทดลองทางคลินิกจำกัดเฉพาะการทดลองอย่างเป็นทางการที่ได้รับอนุมัติจากคณะกรรมการจริยธรรมของสถาบันการแพทย์ นอกจากการปรึกษาแพทย์ผู้รักษาแล้ว ยังสามารถค้นหาข้อมูลการทดลองได้จากเว็บไซต์ข้อมูลการทดลองทางคลินิก (jRCT) ที่ดำเนินการโดยศูนย์มะเร็งแห่งชาติ หรือ clinicaltrials.gov ของสหรัฐอเมริกา
Baz-Redon N, et al. Primary Ciliary Dyskinesia and Retinitis Pigmentosa: Novel RP GR Variant and Possible Modifier Gene. Cells. 2024;13(6):524.
Holanda IP, et al. Syndromic Retinitis Pigmentosa: A 15-Patient Study Exploring Clinical and Genetic Features. Genes. 2024;15(4):516.
Wawrocka A, et al. Retinitis Pigmentosa and Ataxia in PHARC, PCARP , and Oliver-McFarlane Syndrome. Int J Mol Sci. 2024;25(11):5759.
Zhang L, et al. Autosomal Recessive Retinitis Pigmentosa Associated with REEP6 Variants in a Chinese Population. Genes. 2021;12(4):537.
Sakai D, et al. Ellipsoid zone width for predicting visual prognosis after cataract surgery in retinitis pigmentosa. Eye. 2023;37(1):42-47.
日本眼科学会. 網膜色素変性診療ガイドライン. 日眼会誌. 2016;120:846-861.
Campochiaro PA, Mir TA. The mechanism of cone cell death in Retinitis Pigmentosa. Prog Retin Eye Res. 2018;62:24-37. doi:10.1016/j.preteyeres.2017.08.004.
Liu Y, Zong X, Cao W, Zhang W, Zhang N, Yang N. Gene therapy for retinitis pigmentosa: current challenges and new progress. Biomolecules. 2024;14(8):903. PMID: 39199291. PMCI D: PMC11352491. doi:10.3390/biom14080903.
厚生労働科学研究費補助金難治性疾患政策研究事業網膜脈絡膜・視神経萎縮症に関する調査研究班. 網膜色素変性診療ガイドライン2026. 日眼会誌. 2026.
厚生労働科学研究費補助金難治性疾患政策研究事業網膜脈絡膜・視神経萎縮症に関する調査研究班. 網膜色素変性診療ガイドライン(旧版). 日眼会誌.
Napoli D, Di Marco B, Salamone G, et al. Keeping the lights on: a new role for an old drug to support cone survival in Retinitis Pigmentosa. Prog Retin Eye Res. 2025.
Koyanagi Y, Akiyama M, Nishiguchi KM, et al. Genetic characteristics of retinitis pigmentosa in 1204 Japanese patients. J Med Genet. 2019;56:662-670.
Numa S, Oishi A, Higasa K, et al. EYS is a major gene involved in retinitis pigmentosa in Japan: genetic landscapes revealed by stepwise genetic screening. Sci Rep. 2020;10:20770.
Berson EL, Rosner B, Sandberg MA, et al. A randomized trial of vitamin A and vitamin E supplementation for retinitis pigmentosa. Arch Ophthalmol. 1993;111:761-772.
Nakazawa M, Suzuki Y, Ito T, et al. Long-term effects of nilvadipine against progression of the central visual field defect in retinitis pigmentosa: an extended study. Biomed Res Int. 2013;2013:585729.
Yamamoto S, Sugawara T, Murakami A, et al. Topical isopropyl unoprostone for retinitis pigmentosa: microperimetric results of the phase 2 clinical study. Ophthalmol Ther. 2012;1:5.
Campochiaro PA, Iftikhar M, Hafiz G, et al. Oral N-acetylcysteine improves cone function in retinitis pigmentosa patients in phase I trial. J Clin Invest. 2020;130:1527-1541.
Russell S, Bennett J, Wellman JA, et al. Efficacy and safety of voretigene neparvovec (AAV2-hRPE 65v2) in patients with RPE 65-mediated inherited retinal dystrophy: a randomised, controlled, open-label, phase 3 trial. Lancet. 2017;390:849-860.
Fujinami K, Akiyama K, Tsunoda K, et al. Efficacy and safety of voretigene neparvovec in RPE 65-retinopathy: results of a phase 3 trial in Japan. Ophthalmol Sci. 2025;5:100876.