อาการบวมน้ำที่จอประสาทตา ชนิดถุงน้ำ (CME ) เป็นภาวะที่มีของเหลวสะสมในจอประสาทตา เนื่องจากการแตกของสิ่งกีดขวางเลือด-จอตา (BRB)
สาเหตุมีหลากหลาย เช่น จอประสาทตา จากเบาหวาน การอุดตันของหลอดเลือดดำจอตา หลังผ่าตัดต้อกระจก และจากยา การระบุสาเหตุเป็นกุญแจสำคัญในการรักษา
ผู้ป่วยส่วนใหญ่หายได้เองภายใน 3-4 เดือน แต่หากกลายเป็นเรื้อรังอาจทำให้เซลล์รับแสง เสียหายถาวร
OCT เป็นเครื่องมือหลักในการวินิจฉัยและประเมินประสิทธิภาพการรักษา ตำแหน่งของถุงน้ำที่แยกตามชั้นเป็นเบาะแสในการสันนิษฐานสาเหตุการรักษาจะเลือกตามสาเหตุ เช่น ยาหยอดตา NSAIDs, สเตียรอยด์ หรือการฉีด anti-VEGF ใน CME ที่เกิดจากยา การหยุดยาที่เป็นสาเหตุเป็นสิ่งสำคัญที่สุด
ความเสียหายของ EZ (ellipsoid zone) และ ELM (external limiting membrane) เป็นตัวบ่งชี้ทางชีวภาพ จาก OCT ที่บ่งชี้การพยากรณ์โรคที่ไม่ดี 13)
ภาวะจอประสาทตา ส่วนกลางบวมน้ำชนิดถุงน้ำ (Cystoid Macular Edema; CME ) เป็นภาวะที่มีการรั่วของของเหลวจากเส้นเลือดฝอยบริเวณจอประสาทตา ส่วนกลาง (รอบรอยบุ๋มจอตา ) เนื่องจากการแตกของสิ่งกีดขวางระหว่างเลือดและจอตา (blood-retinal barrier; BRB) ทำให้เกิดการสะสมของของเหลวเป็นถุงน้ำในชั้น plexiform ชั้นนอกและชั้น nuclear ชั้นใน ผนังของถุงน้ำประกอบด้วยเซลล์ Müller และเส้นใยประสาทแอกซอน และของเหลวจะสะสมตามแนวชั้นเส้นใย Henle ทำให้เกิดรูปแบบคล้ายกลีบดอกไม้ที่มีลักษณะเฉพาะ
CME เป็นสาเหตุหลักประการหนึ่งของความบกพร่องทางการมองเห็น ส่วนกลางในประเทศที่พัฒนาแล้ว และอาจเกิดจากโรคตาต่างๆ โรคทางระบบ และยา มีกลไกพื้นฐานสามประการของ CME : ① แบบมีการรั่วซึม (การรั่วของหลอดเลือดเนื่องจากการแตกของ BRB), ② แบบเสื่อม (การสะสมของของเหลวภายในเซลล์เนื่องจากความเสียหายของเซลล์ Müller), และ ③ แบบมีการดึงรั้ง (การผิดรูปเชิงกลเนื่องจากการดึงรั้งของวุ้นตา -จอประสาทตา ส่วนกลาง หรือเยื่อเหนือจอตา) 3)
ตำแหน่งของของเหลวที่แยกตามชั้นใน OCT เป็นเบาะแสในการสันนิษฐานสาเหตุ การจำกัดอยู่ที่ชั้น nuclear ชั้นในบ่งชี้กลไกแบบเสื่อม การจำกัดอยู่ที่ชั้น nuclear ชั้นนอกบ่งชี้ภาวะเซลล์ Müller บวมน้ำเฉียบพลันหรือกลไกแบบมีการดึงรั้ง ส่วนการกระจายทั้งสองชั้นบ่งชี้กลไกแบบมีการรั่วซึม 3)
Q
ภาวะจอประสาทตาส่วนกลางบวมน้ำชนิดถุงน้ำสามารถหายได้เองหรือไม่?
A
ส่วนใหญ่จะหายได้เองภายใน 3-4 เดือน อย่างไรก็ตาม หากกลายเป็นเรื้อรัง (มากกว่า 6-9 เดือน) อาจเกิดความเสียหายถาวรต่อเซลล์รับแสง การระบุสาเหตุและการแทรกแซงการรักษาที่เหมาะสมเป็นสิ่งสำคัญ สำหรับรายละเอียด โปรดดูหัวข้อ “การรักษามาตรฐาน”
การมองเห็น ลดลงภาพบิดเบี้ยว (Metamorphopsia)ภาพเล็ก (Micropsia) : วัตถุดูเล็กลงจุดบอดกลาง (Central scotoma)รอยบุ๋มจอตา รุนแรง จะเกิดการมองเห็น ส่วนกลางลำบากการลดลงของความไวต่อคอนทราสต์และการมองเห็น สี : มักเกิดขึ้นพร้อมกับการมองเห็น ที่ลดลง
ระดับของการรั่วซึมในการตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA ) ไม่จำเป็นต้องสัมพันธ์กับระดับการมองเห็น ที่ลดลง
การหายไปของรีเฟล็กซ์โฟเวีย (foveal reflex) จากการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp) เป็นอาการแสดงเริ่มต้นที่สำคัญ ความหนาของโฟเวีย ≥300 ไมครอน ถือเป็นอาการบวมน้ำที่มีนัยสำคัญทางคลินิก แสงสีเขียว (แสงที่ไม่ใช่สีแดง) จะช่วยเน้นขอบของถุงน้ำ
ในจอประสาทตา จะเกิดถุงน้ำเรียงตัวเป็นกลีบดอกไม้รอบโฟเวีย มักสังเกตเห็นเป็นรูปแบบรังผึ้ง ในกรณีรุนแรง การรวมตัวของถุงน้ำจะเกิดเป็นถุงน้ำขนาดใหญ่
สาเหตุหลักของ CME จัดกลุ่มโดยใช้คำย่อ “DEPRIVENS”: D iabetes (เบาหวานขึ้นจอประสาทตา ), E pinephrine (อีพิเนฟริน), P ars planitis (ม่านตาอักเสบส่วนกลาง ), R etinitis pigmentosa (จอประสาทตา เสื่อมชนิดสี), I rvine-Gass syndrome (หลังผ่าตัดต้อกระจก ), V ein occlusion (หลอดเลือดดำอุดตัน), N icotinic acid (กรดนิโคตินิก), E xternal beam radiation (การฉายรังสี), S urgery (การผ่าตัด)
CME หลังผ่าตัดต้อกระจก พบได้บ่อยที่สุด เกิดขึ้นในตาที่ใส่เลนส์แก้วตาเทียม (IOL ) มากถึง 20% แต่การมองเห็น ลดลงพบเพียง 1-20% การแตกของแคปซูลเลนส์ด้านหลังเป็นปัจจัยเสี่ยงสูง อาการมักเริ่ม 6-10 สัปดาห์หลังผ่าตัด และ 95% หายได้เองภายใน 6 เดือน อุบัติการณ์ของ CME หลังผ่าตัดรูรั่วที่จอประสาทตา ส่วนกลางน้อยกว่า 10% 14)
มีรายงานสะสมเกี่ยวกับยาต่อไปนี้
ยา ข้อบ่งใช้ ลักษณะเฉพาะ ลาทาโนพรอสต์ ต้อหิน เกิดขึ้นแม้ในตาที่ยังมีเลนส์ธรรมชาติ รายงานครั้งแรกหลังใช้ 22 ปี1) ฟิงโกลิโมด โรคปลอกประสาทเสื่อมแข็ง 0.5 มก.: ME 0.4% การผ่าตัดต้อกระจก เป็นตัวกระตุ้น8) ไซโปนิโมด โรคปลอกประสาทเสื่อมแข็ง ในการศึกษา EXPAND: CME 2% เกิดขึ้นภายใน 1 สัปดาห์หลังจากเริ่ม4) นา-พาคลิแทกเซล มะเร็งเต้านม ไม่มีการรั่วซึมในการตรวจ FA (พิษต่อเซลล์มุลเลอร์)2) ไอบรูทินิบ มะเร็งเม็ดเลือดขาวชนิดลิมโฟไซต์เรื้อรัง ความหนาจอประสาทตา ส่วนโฟเวีย 600 μm หายไป 6 เดือนหลังจากหยุด7) เพนโทซานโพลีซัลเฟต (PPS ) กระเพาะปัสสาวะอักเสบชนิดคั่นระหว่าง เกิดขึ้นแม้ 10 ปีหลังจากหยุด พบร่วม 17% ของโรคจอประสาทตา เสื่อม10)
ยาที่เกี่ยวข้องกับพรอสตาแกลนดิน (PGA) ทำให้อุปสรรคเลือด-อารมณ์ขันเสียหายและกระตุ้นให้เกิด CME ในการทบทวนของ Warwar และคณะเกี่ยวกับ latanoprost พบว่า 2.1% ของผู้ป่วย 94 รายเกิด CME และในการทบทวนของ Hu และคณะ พบว่า 47 ใน 48 ตาเป็นตาปลอมหรือตาไม่มีเลนส์ 1) การเกิดในตาที่มีเลนส์ธรรมชาติพบได้น้อย แต่มีรายงานกรณีหลังการใช้เป็นเวลานานถึง 22 ปี 1)
การอุดตันของหลอดเลือดดำจอตา (RVO ) : ทั้งการอุดตันของแขนงและส่วนกลางมักเกิดร่วมกับ CME ภาวะโฮโมซิสเทอีนในเลือดสูง (23.3 ไมโครโมล/ลิตร สูงกว่าค่าปกติ 5–13 ไมโครโมล/ลิตร) เพิ่มความเสี่ยง RVO ผ่านการแข็งตัวของเลือดมากเกินไป และอาจทำลาย BRB โดยตรงทำให้เกิด CME 6) การอุดตันของหลอดเลือดแดงจอตาส่วนกลาง (CRAO ) : ในระยะเฉียบพลัน อาจเกิด CME ที่จำกัดอยู่ที่ชั้นนิวเคลียสชั้นนอกและหายได้เองภายใน 2 สัปดาห์ ในระยะเรื้อรัง เกิด CME แบบเสื่อมที่จำกัดอยู่ที่ชั้นนิวเคลียสชั้นในโดยไม่มีการรั่วซึมในการตรวจฟลูออเรสซีน แองจิโอกราฟี 3) ม่านตาอักเสบ (ยูเวียอักเสบ)CME ถึง 20 เท่า 5) อุปกรณ์ต้อหิน : มีรายงานกลไกการงอของ Hydrus Microstent → การเสียดสีของม่านตา → ม่านตาอักเสบ เฉียบพลันร่วมกับซิลิอารีบอดี → CME 9)
หลอดเลือด
จอประสาทตาเสื่อมจากเบาหวาน
การอุดตันของหลอดเลือดดำจอตา : ทั้งการอุดตันของแขนงและส่วนกลางพบบ่อย
การอุดตันของหลอดเลือดแดง (CRAO ) : ระยะเฉียบพลันอยู่ที่ชั้นนิวเคลียสชั้นนอก ระยะเรื้อรังอยู่ที่ชั้นนิวเคลียสชั้นใน 3)
การอักเสบ
ม่านตาอักเสบ (ยูเวียอักเสบ)CME 20 เท่า 5)
การอักเสบหลังผ่าตัด : หลังผ่าตัดต้อกระจก ต้อหิน จอตาแก้วตา
ภาวะแทรกซ้อนจากอุปกรณ์ : การงอของ Hydrus → ม่านตาอักเสบ → CME 9)
จากยา
ยาหยอดตา PGA : สามารถเกิดได้แม้ในตาที่ยังมีเลนส์แก้วตา เดิม 1)
ยาปรับ受体 S1P : Fingolimod, Siponimod 4, 8)
ยาต้านมะเร็ง : กลุ่ม taxane, ยายับยั้ง BTK, PPS 2, 7, 10)
หลังผ่าตัด/การดึงรั้ง
Irvine-Gass syndrome เลนส์แก้วตาเทียม
การดึงรั้งของวุ้นตา -จอตา (VMT ) : CME จากการดึงรั้ง
เยื่อเหนือจอตา (ERM ) : CME จากการเสียรูปเชิงกล
หากคุณรู้สึกว่าการมองเห็น ลดลงหรือภาพบิดเบี้ยว ขณะใช้ยาหยอดตารักษาโรคต้อหิน อย่าหยุดยาเอง ควรปรึกษาจักษุแพทย์โดยเร็ว หลังผ่าตัดต้อกระจก การใช้ยาหยอดตาตามที่กำหนดอย่างต่อเนื่องเป็นสิ่งสำคัญในการป้องกัน CME หลังผ่าตัด เมื่อเริ่มหรือเปลี่ยนยารักษาโรคปลอกประสาทเสื่อมแข็ง (เช่น fingolimod, siponimod) ควรตรวจตาเป็นประจำ
Q
โอกาสเกิด CME หลังผ่าตัดต้อกระจกเท่าไร?
A
CME (Irvine-Gass syndrome ) เกิดขึ้นในตาที่ใส่เลนส์แก้วตาเทียม ได้ถึง 20% แต่การมองเห็น ลดลงจริงเกิดขึ้น 1-20% ความเสี่ยงเพิ่มขึ้นหากมีถุงเลนส์แตก 95% หายได้เองภายใน 6 เดือนหลังผ่าตัด แต่แนะนำให้ใช้ NSAID ป้องกันในกรณีที่มีความเสี่ยงสูง 12)
Q
ยารับประทานสามารถทำให้เกิด CME ได้หรือไม่?
A
มีรายงานกับ fingolimod, siponimod (ยารักษาโรคปลอกประสาทเสื่อมแข็ง), nab-paclitaxel (ยาต้านมะเร็ง), ibrutinib (ยารักษามะเร็งเม็ดเลือด) และ pentosan polysulfate (ยารักษากระเพาะปัสสาวะอักเสบชนิดคั่นระหว่างหน้า) การหยุดยาที่เป็นสาเหตุเป็นการรักษาที่มีประสิทธิภาพที่สุด ดูรายละเอียดในหัวข้อ “การรักษามาตรฐาน”
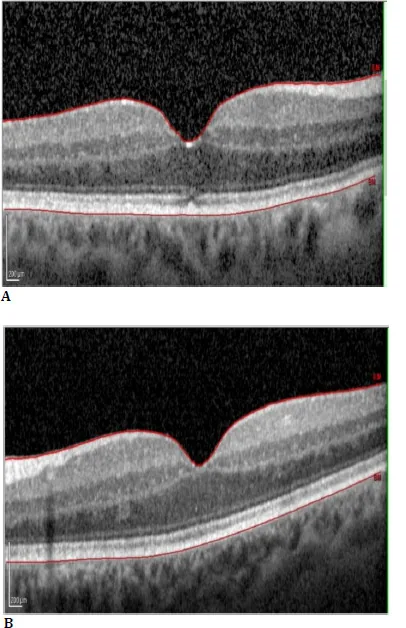
ภาพจอประสาทตาบวมน้ำชนิดซีสตอยด์ Radomir Babovic; Ben Burton; Nimesha Alex; Lakshmi Harihar; Tihomir Dugandzija. Unraveling the Mystery of Taxol-Induced Cystoid Macular Oedema: Case Report and Literature Review. Rom J Ophthalmol. 2025 Jan-Mar; 69(1):3-9. Figure 5. PM
CI D: PMC12049643. License: CC BY.
ภาพตัดขวาง SD-OCT ของตาขวา (A) และตาซ้าย (B) แสดงการหายไปของจอประสาทตา บวมน้ำชนิดซีสตอยด์อย่างสมบูรณ์หลังจากหยุดการรักษาด้วยยาแพคลิแทกเซล
การตรวจวินิจฉัย CME ใช้การตรวจภาพหลายวิธี ต่อไปนี้เป็นวิธีการหลัก:
วิธีการตรวจ ลักษณะเฉพาะ การใช้งานหลัก OCT ไม่รุกราน ประเมินเชิงปริมาณ การวินิจฉัยที่แน่นอนและการประเมินผลการรักษา การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) ใช้สารทึบแสง ยืนยันรูปแบบการรั่ว การเรืองแสงอัตโนมัติของจอตา (FAF ) ไม่รุกราน ประเมินความผิดปกติของ RPE
วิธีการตรวจที่สำคัญที่สุด สามารถประเมินตำแหน่ง การกระจาย และความหนาของจอประสาทตา ของซีสต์ได้ในเชิงปริมาณ และจำเป็นสำหรับการติดตามผลการรักษาเมื่อเวลาผ่านไป ผล OCT พื้นฐานของ CME มี 3 ชนิด: ① จอประสาทตา บวม (แบบกระจาย), ② ภาวะบวมน้ำแบบซีสต์ (การเกิดซีสต์), ③ จอประสาทตาลอก แบบมีน้ำใต้จอประสาทตา
การระบุตำแหน่งตามชั้นมีประโยชน์ในการประมาณสาเหตุ; การจำกัดอยู่ที่ชั้นนิวเคลียสชั้นในบ่งชี้กลไกเสื่อม ในขณะที่การจำกัดอยู่ที่ชั้นนิวเคลียสชั้นนอกบ่งชี้ภาวะบวมน้ำของเซลล์มุลเลอร์เฉียบพลัน 3) OCT แบบเอนเฟซมีประโยชน์ในการแสดงรูปแบบการกระจายของ CME 3)
ในการทบทวนวรรณกรรมอย่างเป็นระบบเกี่ยวกับตัวบ่งชี้ทางชีวภาพ OCT สำหรับการตอบสนองต่อการรักษา ได้แสดงดังต่อไปนี้: 13)
ของเหลวใต้จอประสาทตา ดีขึ้นใน 67% ของกรณี, ซีสต์ในจอประสาทตา ดีขึ้นใน 76% ในขณะที่ความผิดปกติของโซนรูปไข่ (EZ ) ไม่เปลี่ยนแปลงหรือแย่ลงใน 64%, ความผิดปกติของเยื่อหุ้มจำกัดชั้นนอก (ELM) ไม่เปลี่ยนแปลงหรือแย่ลงใน 67%, จุดสะท้อนแสงสูง ไม่เปลี่ยนแปลงหรือแย่ลงใน 63%, และความไม่เป็นระเบียบของชั้นในจอประสาทตา (DRIL) ไม่เปลี่ยนแปลงหรือแย่ลงใน 50% 13)
การมีความผิดปกติของ EZ และ ELM เป็นตัวบ่งชี้ทางชีวภาพ ของการพยากรณ์โรคที่ไม่ดี ซึ่งบ่งชี้ว่าการฟื้นฟูการมองเห็น หลังการรักษาไม่ดี 13)
ในระยะปลาย (10-20 นาที) การรั่วซึมรูปกลีบดอกไม้ตามแนวเส้นใยเฮนล์เป็นลักษณะเฉพาะ อย่างไรก็ตาม ใน CME ที่เกิดจากยาเคมีบำบัดกลุ่มแทกเซน มักไม่พบการรั่วซึมใน FA (เนื่องจากกลไกเสื่อม) และไม่สามารถแยก CME ออกได้แม้ว่า FA จะเป็นลบ 2)
ในจอประสาทตา เสื่อมที่เกี่ยวข้องกับเพนโทซานโพลีซัลเฟต (PPS ) จะพบรูปแบบ FAF ผิดปกติที่มีลักษณะเฉพาะ และมักถูกวินิจฉัยผิดว่าเป็น AMD 10) มีประโยชน์ในการประเมินความผิดปกติของ RPE มากกว่าตัว CME เอง
Q
OCT บอกอะไรได้บ้าง?
A
สามารถประเมินตำแหน่ง การกระจาย ขนาดของซีสต์ และความหนาของจอประสาทตา ได้ในเชิงปริมาณ และจำเป็นสำหรับการตัดสินผลการรักษาเมื่อเวลาผ่านไป การระบุตำแหน่งตามชั้น (ชั้นนิวเคลียสชั้นในหรือชั้นนอก) ให้เบาะแสในการประมาณสาเหตุ ความผิดปกติของ EZ และ ELM ได้รับการประเมินเป็นตัวบ่งชี้ทางชีวภาพ ที่ส่งผลต่อการพยากรณ์การมองเห็น 13)
การรักษาจะเลือกตามโรคที่เป็นสาเหตุและสภาพ ใน CME ที่เกิดจากยา การหยุดยาที่เป็นสาเหตุเป็นทางเลือกแรก
ใช้คีโตโรแลค 0.5%, เนปาฟีแนค 0.1%, โบรมีฟีแนค 0.07% และอื่นๆ โดยการยับยั้งไซโคลออกซีจีเนส (COX) จะยับยั้งการผลิตพรอสตาแกลนดินและทำให้สิ่งกีดขวางเลือด-จอประสาทตา (BRB) คงที่
แนะนำให้ใช้ NSAIDs ป้องกันในระยะผ่าตัดสำหรับตาที่มีความเสี่ยงสูง (เช่น กรณี capsular rupture, ตาเดียว, เบาหวาน) การเริ่มก่อนผ่าตัดและต่อเนื่องทันทีหลังผ่าตัดช่วยฟื้นฟูการมองเห็น 12)
ในกรณี CME จากการงอของ Hydrus Microstent มีรายงานการหายสนิทด้วยยาหยอดตา ketorolac + prednisolone นาน 2 เดือน (สายตาจาก 20/60 เป็น 20/25) 9)
การฉีด triamcinolone ใต้ Tenon capsule : ฤทธิ์ต้านการอักเสบเฉพาะที่ มักต้องฉีดหลายครั้งการฉีด triamcinolone เข้าแก้วตา : การนำส่งยาโดยตรง ต้องระวังความดันลูกตา สูงและต้อกระจก ที่ลุกลามสเตียรอยด์ ทั้งระบบCME อักเสบรุนแรง แต่การใช้ระยะยาวต้องจัดการผลข้างเคียง
สเตียรอยด์ กระตุ้นสัญญาณ adenosine ใน Müller cell เพื่อลดการผลิต VEGF ใน CME ที่เกี่ยวข้องกับ IRU ซึ่งห้ามใช้สเตียรอยด์ เนื่องจาก femoral head necrosis สามารถใช้ tocilizumab ทดแทนได้ (จะกล่าวถึงภายหลัง)
การรักษาหลักสำหรับ macular edema จากเบาหวานและ CME ที่เกี่ยวข้องกับ RVO ใช้ bevacizumab 1.25 มก./0.05 มล., ranibizumab 0.5 มก., aflibercept 2 มก. เป็นต้น
มีรายงานกรณี CME ที่เกี่ยวข้องกับ PPS หายสนิทหลังฉีด bevacizumab 1.25 มก./0.05 มล. สองครั้ง กรณีที่ไม่ตอบสนองต่อยาหยอด NSAIDs และสเตียรอยด์ นี้ได้ผลลัพธ์ที่ดี 10)
ในกรณี venous stasis ทั้งสองข้างและ CME ร่วมกับ hyperhomocysteinemia ดีขึ้นหลังฉีด anti-VEGF สองครั้ง 6)
เพิ่มการทำงานของปั๊ม RPE และเร่งการดูดซึมของเหลวใต้จอประสาทตา ให้เป็นยาหยอดตา (dorzolamide, brinzolamide) หรือรับประทาน (acetazolamide) ใน CME ที่เกิดจาก latanoprost มีรายงานการหายภายใน 1 เดือนหลังจากเปลี่ยนจาก latanoprost เป็น dorzolamide (CMT 319→218 μm, 326→227 μm) 1)
ใน CME ที่เกิดจากยา การหยุดยาสาเหตุเป็นการรักษาที่มีประสิทธิภาพที่สุด
Latanoprost → การหยุดหรือเปลี่ยนยาทำให้หายภายใน 1 เดือน 1)
Fingolimod → บางครั้งรอให้หายเองขณะใช้ยาต่อเนื่องเนื่องจากเสี่ยงต่อการกำเริบของ MS มีรายงานหายเองหลังจาก 13 เดือน 8)
Siponimod → ดีขึ้นชัดเจน 1 สัปดาห์หลังหยุด หายสนิทใน 1 เดือน 4)
Nab-paclitaxel → ดีขึ้น 2 เดือนหลังหยุดเคมีบำบัด Triamcinolone ใต้ Tenon ไม่ได้ผล 2)
Ibrutinib → หายสนิท 6 เดือนหลังหยุด (สายตา 6/15 → 6/12) NSAIDs + ยาหยอดสเตียรอยด์ 2 ปี ได้ผลเพียงบางส่วน 7)
PPS → CME อาจเกิดขึ้นได้แม้หลังหยุดยา โดยมีรายงานเกิดหลังจาก 10 ปี 10)
ใน CME ชนิดดึงรั้งร่วมกับ VMT การตัดน้ำวุ้นตา ช่วยให้ CME ดีขึ้น 80-92% Ocriplasmin (ยาสลายน้ำวุ้นตา แบบเอนไซม์) ในการทดลองระยะ 2 และ 3 แสดงการปลด VMT ภายใน 1 เดือนใน 58%
Q
ทางเลือกในการรักษา CME มีอะไรบ้าง?
A
ขึ้นอยู่กับสาเหตุ ทางเลือกได้แก่: ยาหยอด NSAID, สเตียรอยด์ (ใต้ Tenon/ฉีดในน้ำวุ้นตา ), การฉีด anti-VEGF ในน้ำวุ้นตา , ยายับยั้ง carbonic anhydrase, และการตัดน้ำวุ้นตา ใน CME ที่เกิดจากยา การหยุดยาสาเหตุเป็นการรักษาอันดับแรกที่มีประสิทธิภาพที่สุด ดูรายละเอียดการรักษาในหัวข้อ “การรักษามาตรฐาน”
BRB ประกอบด้วยสองชั้น BRB ด้านใน (tight junction ระหว่างเซลล์บุผนังหลอดเลือดจอประสาทตา ) และ BRB ด้านนอก (tight junction ระหว่างเซลล์เยื่อบุผิวรงควัตถุจอประสาทตา ) รักษาสมดุลของน้ำในจอประสาทตา เมื่อ tight junction อ่อนแอลงเนื่องจากการอักเสบ ภาวะขาดเลือด หรือสารพิษ โปรตีนในซีรัมและไขมันจะรั่วไหล ทำให้เกิดความดันออสโมติกเพิ่มขึ้น 11)
เซลล์ Müller ป้องกันการสะสมของของเหลวในสภาวะปกติผ่านกลไกระบายน้ำที่ใช้ช่อง aquaporin-4 และ Kir4.1 เมื่อการสลาย BRB รุนแรง กลไกระบายน้ำชดเชยนี้จะอิ่มตัว และ CME จะปรากฏชัดเจน 11)
ชนิด渗出 (Exudative)
การสลาย BRB : การอ่อนแอของ tight junction ของบุผนังหลอดเลือดและ RPE
ส่วนประกอบของเหลว : การรั่วไหลของโปรตีนในซีรัมและไขมัน การตรวจ FA พบการรั่วไหลเป็นรูปกลีบดอกไม้
โรคที่เป็นตัวแทน : จอประสาทตาเสื่อมจากเบาหวาน , RVO , ม่านตาอักเสบ 11)
ชนิดเสื่อม (Degenerative)
ความผิดปกติของเซลล์ Müller : ยากลุ่ม taxane, ระยะเรื้อรังของ CRAO
ลักษณะเฉพาะ : ไม่มีการรั่วไหลในการตรวจ FA มักจำกัดอยู่ที่ชั้นนิวเคลียสชั้นใน 2, 3)
ตัวอย่าง : CME ที่เกิดจาก Nab-PTX, CME ชั้นนิวเคลียสชั้นใน 28 เดือนหลัง CRAO
ชนิดดึงรั้ง (Tractional)
การเสียรูปเชิงกล : เนื่องจาก VMT หรือ ERM
ลักษณะ : พบมากในชั้นกรานูลาร์ชั้นนอก ดีขึ้นหลังการผ่าตัดวุ้นตา
การรักษา : การผ่าตัดวุ้นตา (ดีขึ้น 80-92%), ocriplasmin
ยาปรับเปลี่ยนรีเซพเตอร์ S1P (fingolimod, siponimod) : ยับยั้งการควบคุม cadherin ของเซลล์บุผนังหลอดเลือด ทำให้การซึมผ่านของหลอดเลือดเพิ่มขึ้น และทำลาย Blood-Retinal Barrier 4) ในการทดลอง EXPAND พบ CME ในกลุ่ม siponimod 2% (เทียบกับยาหลอก <1%) 4)
Ibrutinib (ยับยั้ง BTK) : เนื่องจากสามารถผ่าน Blood-Brain Barrier ได้ จึงอาจทำลาย Blood-Retinal Barrier เช่นกัน ในการทดลองระยะที่ 3 กลุ่ม ibrutinib รายงานตามัว 10% (เทียบกับ ofatumumab 3%) 7)
ระยะเฉียบพลันของ Central Retinal Artery Occlusion : ภาวะขาดเลือดทำให้สมดุลไอออนนอกเซลล์เสีย ส่งผลให้ไอออนไหลเข้าสู่เซลล์ Müller อย่างรวดเร็ว ส่งผลให้การแสดงออกของ aquaporin-4 และช่อง Kir4.1 เพิ่มขึ้น ทำให้เกิดอาการบวมของเซลล์ Müller (จำกัดเฉพาะชั้นกรานูลาร์ชั้นนอก) 3)
มีรายงานผู้ป่วย CME ภายหลัง uveitis จากการฟื้นตัวของภูมิคุ้มกัน (IRU) ที่ตอบสนองต่อ tocilizumab
Nguyen และคณะ (2024) รายงานหญิงอายุ 17 ปีที่มี CME หลังการรักษามะเร็งเม็ดเลือดขาวชนิดลิมโฟบลาสติกเฉียบพลันชนิด T-cell, CMV retinitis และ IRU (ห้ามใช้สเตียรอยด์ ทั้งระบบเนื่องจาก femoral head necrosis) ได้รับ tocilizumab 8 มก./กก. ทางหลอดเลือดดำเดือนละครั้ง จำนวน 2 รอบ หลังจาก 2 รอบ CME ดีขึ้นอย่างชัดเจน 5)
การทดลอง STOP-UVEITIS แสดงให้เห็นว่า tocilizumab ช่วยให้ CME ดีขึ้น จึงคาดว่าจะเป็นทางเลือกในการรักษาในกรณีที่ห้ามใช้สเตียรอยด์ ผลการค้นพบนี้บ่งชี้ว่า IL-6 เกี่ยวข้องโดยตรงในการเกิดโรค CME 5)
โรคจอประสาทตา เสื่อมที่เกี่ยวข้องกับ PPS เป็นแนวคิดโรคที่ค่อนข้างใหม่ ซึ่งได้รับการยอมรับครั้งแรกในปี 2018 รอยโรคสามารถดำเนินไปและ CME สามารถเกิดขึ้นได้แม้หลังจากหยุด PPS ไปแล้วมากกว่า 10 ปี ซึ่งบ่งชี้ถึงความสำคัญของการติดตามผลระยะยาว 10)
Szelog และคณะ (2023) รายงานหญิงอายุ 57 ปีที่เกิด CME 10 ปีหลังจากหยุดใช้ PPS เป็นเวลา 3 ปี ตอนแรกได้รับการวินิจฉัยผิดว่าเป็น AMD ยาหยอด NSAIDs และสเตียรอยด์ ไม่ได้ผล แต่การฉีด bevacizumab 1.25 มก./0.05 มล. สองครั้งทำให้หายเป็นปกติ หลังจาก 5 เดือน ตาอีกข้างก็เกิด CME เช่นกัน 10)
มีรายงานว่า 17% ของโรคจอประสาทตา เสื่อมที่เกี่ยวข้องกับ PPS มี CME ร่วมด้วย และการใช้สะสมมากกว่า 500 กรัมทำให้เกิดโรคจอประสาทตา เสื่อมในมากกว่า 10% ของกรณี 10)
การศึกษาที่ประเมินการตอบสนองต่อการรักษาอย่างเป็นระบบจากผล OCT แสดงให้เห็นว่าตัวบ่งชี้ทางชีวภาพ ต่อไปนี้มีประโยชน์ในการทำนายพยากรณ์โรค 13)
ในการทบทวนวรรณกรรมอย่างเป็นระบบที่ตีพิมพ์ใน Survey of Ophthalmology ปี 2025 ถุงน้ำในจอประสาทตา (ดีขึ้น 76%) และของเหลวใต้จอประสาทตา (ดีขึ้น 67%) แสดงการตอบสนองต่อการรักษาสูง ในขณะที่ความผิดปกติของ EZ (ไม่เปลี่ยนแปลง/แย่ลง 64%) ความผิดปกติของ ELM (ไม่เปลี่ยนแปลง/แย่ลง 67%) จุดสะท้อนแสงสูง (ไม่เปลี่ยนแปลง/แย่ลง 63%) และ DRIL (ไม่เปลี่ยนแปลง/แย่ลง 50%) บ่งชี้ถึงพยากรณ์โรคที่ไม่ดี 13)
มีแนวโน้มเพิ่มขึ้นในการนำการมีหรือไม่มีความผิดปกติของ EZ และ ELM มาใช้ในการตัดสินใจวางแผนการรักษา
การวิเคราะห์รูปแบบการกระจายของ CME โดยใช้ En face OCT กำลังระบุลักษณะภาพที่มีประโยชน์ในการแยกแยะโรคที่เป็นสาเหตุ 3) โดยเฉพาะอย่างยิ่ง ความแตกต่างในการกระจายตามชั้นในระยะเฉียบพลันและเรื้อรังของ CME ที่เกิดร่วมกับ CRAO กำลังได้รับความสนใจในฐานะวิธีการประมาณสาเหตุแบบไม่รุกราน
Lin WC, Hsieh JW, Tsai SH, Lan YW. Latanoprost-associated cystoid macular edema in a patient with phakic eyes. Taiwan J Ophthalmol. 2023;13:242-244.
Yamane H, Itagaki T, Kajitani K, et al. Cystoid macular edema following treatment with nanoparticle albumin-bound paclitaxel and atezolizumab for metastatic breast cancer. Case Rep Oncol. 2023;16:1121-1128.
Estawro R, Abraham N, Fouad Y, Bousquet E, Sarraf D. Cystoid macular edema as a complication of central retinal artery occlusion. Am J Ophthalmol Case Rep. 2024;33:101998.
Kim MY, Alkhabaz A, Smith SJ, Liao YJ. Siponimod-associated cystoid macular edema without known risk factors. Am J Ophthalmol Case Rep. 2024;36:102124.
Nguyen BT, Hung JH, Thng ZX, et al. Tocilizumab for cystoid macular edema secondary to immune recovery uveitis in a patient with contraindications to long-term systemic corticosteroid. Yale J Biol Med. 2024;97:423-430.
Chaloulis SK, Tsaousis KT. Cystoid macular edema associated with venous stasis in a patient with previously undiagnosed hyperhomocysteinemia. Cureus. 2021;13(12):e20782.
Ben-Avi R, Dori D, Chowers I. Cystoid macular edema secondary to ibrutinib. Am J Ophthalmol Case Rep. 2022;26:101436.
Fukuoka H, Kojima K, Iwama A, Okumura T, Sotozono C. Fingolimod-associated severe bilateral cystoid macular edema. Am J Ophthalmol Case Rep. 2022;26:101553.
Karaca I, Korot E, Ghoraba H, et al. Acute iridocyclitis and cystoid macular edema related to kinked Hydrus Microstent in advanced glaucoma. Saudi J Ophthalmol. 2022;36:390-393.
Szelog JT, Shah NS, Camejo MD. Cystoid macular edema arising 10 years after cessation of pentosan polysulfate sodium successfully treated with bevacizumab. J Vitreoret Dis. 2023;7(1):83-86.
Cunha-Vaz J, et al. Blood-retinal barrier. Prog Retin Eye Res. 2024. [出典: 1-s2.0-S1350946224000107-main.pdf]
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022. [出典: PIIS0161642021007508.pdf]
OCT biomarkers systematic review. Surv Ophthalmol. 2025. [出典: PIIS0039625725001766.pdf]Royal College of Ophthalmologists. DRAFT Clinical Guideline on Idiopathic Full-Thickness Macular Holes. 2024.