RRMS
ชนิดเป็นซ้ำ-ทุเลา (Relapsing-Remitting MS): ชนิดย่อยที่พบบ่อยที่สุด อาการกำเริบนานกว่า 24 ชั่วโมง และมีการทุเลาแบบสมบูรณ์หรือบางส่วนระหว่างการกำเริบ

โรคปลอกประสาทเสื่อมแข็ง (Multiple Sclerosis; MS) เป็นโรคอักเสบทำลายปลอกไมอีลินในเนื้อขาวของระบบประสาทส่วนกลาง (CNS) ทำให้เกิดอาการทางระบบประสาทหลากหลายที่กำเริบและทุเลาสลับกัน มีลักษณะเฉพาะคือรอยโรคแข็งจากพังผืดเกลีย และโดยปกติจะเกิดเฉพาะใน CNS โดยไม่ทำลายระบบประสาทส่วนปลาย
ความชุกโดยประมาณในสหรัฐอเมริกาคือ 1-1.5 ต่อ 1,000 คน 1) ทั่วโลกมีผู้ป่วย 2.1 ล้านคน พบมากในพื้นที่ละติจูดสูงของซีกโลกเหนือและซีกโลกใต้ อายุเฉลี่ยเมื่อเริ่มป่วยคือ 15-45 ปี อายุเฉลี่ยเมื่อวินิจฉัยคือ 30 ปี ช่วงอายุที่พบบ่อยคือ 15-50 ปี พบในผู้หญิงมากกว่า (สูงสุดช่วงปลายอายุ 20 ปี) โดยอัตราส่วนชาย:หญิงคือ 1:2.9
โรคปลอกประสาทเสื่อมแข็ง (MS) มีชนิดย่อยหลัก 4 ชนิด ได้แก่ RRMS (ชนิดเป็นซ้ำ-ทุเลา) มักเริ่มมีอาการเมื่ออายุ 25–29 ปี ส่วน SPMS (ชนิดทุติยภูมิแบบค่อยเป็นค่อยไป) มักเริ่มเมื่ออายุ 40–49 ปี1)
RRMS
ชนิดเป็นซ้ำ-ทุเลา (Relapsing-Remitting MS): ชนิดย่อยที่พบบ่อยที่สุด อาการกำเริบนานกว่า 24 ชั่วโมง และมีการทุเลาแบบสมบูรณ์หรือบางส่วนระหว่างการกำเริบ
SPMS
PPMS
ชนิดปฐมภูมิแบบค่อยเป็นค่อยไป (Primary Progressive MS): ความพิการสะสมแบบค่อยเป็นค่อยไปตั้งแต่เริ่มแรก ดำเนินไปช้าๆ โดยไม่มีการกำเริบ
CIS
กลุ่มอาการเดี่ยวทางคลินิก (Clinically Isolated Syndrome): อาการทางคลินิกครั้งแรกที่อาจนำไปสู่ MS ทำให้สามารถเริ่มการรักษาได้เร็ว
ในผู้ป่วย 75% อาการเริ่มแรกเป็นข้อร้องเรียนเดียว โดย 45% เป็นอาการทางการเคลื่อนไหว/ความรู้สึก และ 20% เป็นอาการทางสายตา
อาการทางตา
อาการทางระบบประสาททั่วร่างกาย
อาการกำเริบเกิดขึ้นแบบเฉียบพลันถึงกึ่งเฉียบพลันและคงอยู่นานหลายวันถึงหลายเดือน ใน 85% อาการดีขึ้นหรือหายไป แต่ใน 10-15% มีอาการตกค้าง
มักเริ่มต้นเป็นการสูญเสียการมองเห็นอย่างเจ็บปวดในตาข้างเดียว พบอาการปวดเบ้าตาใน 92% แย่ลงเมื่อขยับตา ปรากฏการณ์ Uhthoff (อาการแย่ลงชั่วคราวเมื่ออุณหภูมิร่างกายสูงขึ้น เช่น อาบน้ำอุ่น ออกกำลังกาย) ก็พบได้เช่นกัน
ไม่ทราบสาเหตุที่แน่ชัดของ MS แต่เชื่อว่ากลไกภูมิต้านตนเองมีส่วนเกี่ยวข้องกับการเกิดโรค
ปัจจัยทางพันธุกรรมมีส่วนเกี่ยวข้อง แต่อัตราความสอดคล้องในฝาแฝดเหมือนกันอยู่ที่เพียง 25-30% มีการระบุความหลากหลายของ HLA และตำแหน่งเสี่ยงมากกว่า 100 ตำแหน่ง แต่เชื่อว่าปัจจัยด้านสิ่งแวดล้อมนอกเหนือจากความโน้มเอียงทางพันธุกรรมก็มีบทบาทสำคัญในการเกิดโรค
ใช้เกณฑ์ McDonald 2017 (ฉบับปรับปรุง 2024) หลักการคือการพิสูจน์การกระจายตัวของรอยโรคทำลายไมอีลินในระบบประสาทส่วนกลางทั้งในด้านเวลาและพื้นที่ (DIT/DIS) ในการปรับปรุงปี 2024 ได้เพิ่มเส้นประสาทตาเป็นตำแหน่งทางกายวิภาคที่ห้า ในญี่ปุ่นก็มีเกณฑ์การวินิจฉัยโรคปลอกประสาทเสื่อมแข็งของกระทรวงสาธารณสุข แรงงาน และสวัสดิการ ปี 2015 เช่นกัน
ตำแหน่งทางกายวิภาคทั้งห้าสำหรับการกระจายตัวในพื้นที่ (DIS) มีดังนี้:
หลักฐานการกระจายตามเวลา (DIT): การโจมตีสองครั้งขึ้นไป หรือการมีรอยโรคที่เสริมและไม่เสริมสัญญาณพร้อมกันใน MRI, รอยโรค T2 ใหม่ หรือสามารถแทนที่ด้วยแถบโอลิโกโคลนอลในน้ำไขสันหลัง 1).
สำหรับการวินิจฉัย PPMS นอกเหนือจากความพิการที่ดำเนินไปนาน ≥1 ปี จำเป็นต้องมีผลการตรวจอย่างน้อยสองข้อต่อไปนี้: รอยโรค T2 ในสมอง, รอยโรค T2 ในไขสันหลัง (≥2), หรือแถบโอลิโกโคลนอลในน้ำไขสันหลัง 1).
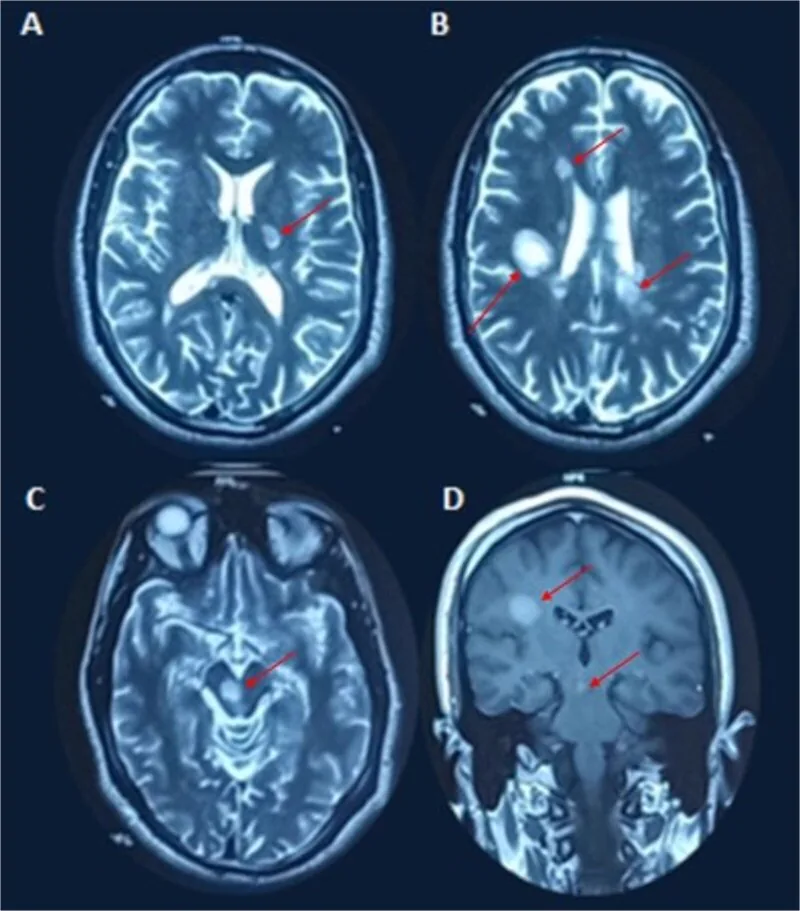
แผ่นคราบดีไมอีลิเนชันถูกตรวจพบเป็นรอยโรคสัญญาณสูงใน T2 หรือรอยโรคที่เสริมด้วยแกโดลิเนียม
มีประโยชน์เมื่อ MRI ไม่สามารถสรุปได้หรือเพื่อทำนายการดำเนินของโรค 1) สามารถตรวจพบการทำลายไมอีลินระยะแรกที่ไม่มีอาการก่อนที่จะเห็นได้ด้วย MRI ใน 65% พบว่ามีการยืดเวลาของแฝงและการลดลงของแอมพลิจูด
สิ่งสำคัญคือต้องแยกโรคจากโรคต่อไปนี้ และในกรณีที่ไม่ปกติ ให้ทำการตรวจเพิ่มเติม
| หมวดหมู่โรค | โรคที่ต้องแยกหลัก |
|---|---|
| โรคทำลายไมอีลิน | NMO (โรคเดวิก), ADEM, MOGAD |
| ติดเชื้อ | ซาร์คอยโดซิส วัณโรค ซิฟิลิส โรคไลม์ |
| ภูมิต้านตนเอง | SLE, กลุ่มอาการโจเกรน, โรคเบห์เซ็ต |
| โรคเส้นประสาทตา | NAION, LHON, โรคเส้นประสาทตาจากพิษ/เมตาบอลิก |
การตรวจเพิ่มเติมในกรณีที่ไม่ปกติ: แอนติบอดีต่อ AQP4 (เพื่อแยก NMO), แอนติบอดีต่อ MOG (เพื่อแยก MOGAD), การตรวจ NfL ในซีรั่ม, การตรวจซีรั่มซิฟิลิส (VDRL/RPR/FTA-ABS), ANA (สำหรับ SLE), ACE/lysozyme (สำหรับซาร์คอยโดซิส)
การรักษามาตรฐานในญี่ปุ่นคือการให้สเตียรอยด์แบบพัลส์ด้วย methylprednisolone 1,000 มก./วัน ทางหลอดเลือดดำเป็นเวลา 3 วันติดต่อกัน ไม่มีการให้ prednisolone รับประทานหลังการให้ยา ไม่ควรให้สเตียรอยด์แบบรับประทานเพราะเพิ่มอัตราการกลับเป็นซ้ำ
แม้ไม่ได้รับการรักษา ประมาณ 80% ของผู้ป่วยจะเริ่มมีการมองเห็นดีขึ้นภายใน 3 สัปดาห์หลังจากเริ่มมีอาการ แต่การให้สเตียรอยด์แบบพัลส์จะทำให้ระยะเวลาการดีขึ้นสั้นลง คาดว่าการมองเห็นจะฟื้นตัวในมากกว่า 90% ของผู้ป่วยโรคประสาทตาอักเสบ
หากการให้สเตียรอยด์แบบพัลส์ไม่ได้ผล ให้ทำการฟอกเลือด (พลาสมาเฟเรซิส) ในต่างประเทศใช้ methylprednisolone 500-1,000 มก./วัน เป็นเวลา 3-5 วัน ในการทดลองรักษาโรคประสาทตาอักเสบ (ONTT) การให้ methylprednisolone ทางหลอดเลือดดำขนาดสูงช่วยให้เวลาฟื้นตัวของการมองเห็น ความไวต่อคอนทราสต์ และการมองเห็นสีดีขึ้น แต่ไม่แสดงการปรับปรุงผลลัพธ์การมองเห็นสุดท้าย
หลังจากที่การสูญเสียการมองเห็นและความบกพร่องของลานสายตาดีขึ้น ควรพิจารณาการรักษาปรับเปลี่ยนโรคร่วมกับแพทย์ระบบประสาทเพื่อป้องกันการกลับเป็นซ้ำ
ด้านล่างนี้คือการรักษาปรับเปลี่ยนโรคหลักและประสิทธิผล
| ยา | กลไกการออกฤทธิ์ | วิธีการให้ยา | การลดความเสี่ยงสัมพัทธ์ |
|---|---|---|---|
| อินเตอร์เฟอรอนเบตา | ปรับเปลี่ยนการทำงานของเซลล์ T/B และการหลั่งไซโตไคน์ | ฉีดเอง | ความพิการลุกลาม RR 0.71 |
| กลาติราเมอร์ อะซิเตท | ควบคุมเซลล์ T ควบคุม | ฉีดเอง | การกลับเป็นซ้ำ RR 0.82 |
| นาตาลิซูแมบ | ยับยั้งการเข้าสู่ระบบประสาทส่วนกลางของเซลล์อักเสบ | หยดเข้าหลอดเลือดดำ | การกลับเป็นซ้ำ RR 0.56 |
| ฟิงโกลิโมด | ตัวปรับ受体 S1P | รับประทาน | RR ของรอยโรค T2 ใหม่ 0.65 |
| เทริฟลูโนไมด์ | ยับยั้งการสังเคราะห์ไพริมิดีน | รับประทาน | RR ของความพิการที่แย่ลง 0.76 |
| ไดเมทิลฟูมาเรต | ลดความเครียดออกซิเดชันและการอักเสบ | รับประทาน | RR ของการกลับเป็นซ้ำ 0.64 |
| อาเล็มทูซูแมบ | แอนติบอดีต่อต้าน CD52 | หยดเข้าหลอดเลือดดำ | RR ของความพิการที่แย่ลง 0.44 |
แอนติบอดีโมโนโคลนอลที่ต่อต้าน CD20 (ocrelizumab, rituximab, ofatumumab) ได้กลายเป็นการรักษามาตรฐานสำหรับ MS ชนิดกำเริบ 3)
แม้ในกรณีเส้นประสาทตาอักเสบที่ไม่มีรอยโรคในสมอง 25% จะพัฒนาเป็น MS ภายใน 15 ปี และหากมีรอยโรคในสมอง 78% จะเปลี่ยนเป็น MS
MS ถือเป็นโรคภูมิต้านตนเอง ทีลิมโฟไซต์จดจำไมอีลินว่าเป็นสิ่งแปลกปลอม กระตุ้นมาโครฟาจ ไซโตไคน์ และแอนติบอดีให้ทำลายไมอีลินและแอกซอน การสูญเสียไมอีลินทำให้การนำกระแสประสาทบกพร่อง ส่งผลให้การส่งสัญญาณประสาทผิดปกติ
แผ่นคราบจุลินทรีย์ที่ยังทำงาน (Active plaque)
มาโครฟาจแบบฟอง (Foamy macrophages): การสะสมของมาโครฟาจที่กินไมอีลิน
การแทรกซึมรอบหลอดเลือด (Perivascular cuffing): ลิมโฟไซต์ล้อมรอบหลอดเลือด เป็นลักษณะเฉพาะ
รอยโรคทำลายไมอีลินเฉพาะที่แบบบวมน้ำ (Edematous focal demyelinating lesions): พบในระยะกำเริบเฉียบพลัน
แผ่นคราบจุลินทรีย์เรื้อรัง (Chronic plaque)
การสูญเสียไมอีลิน: ยืนยันได้ด้วยการย้อม Luxol fast blue แอกซอนยังคงอยู่แต่การสร้างไมอีลินใหม่ไม่สมบูรณ์
รอยโรค NAWM (Normal-Appearing White Matter): การเกิดไกลโอซิสแบบกระจาย การกระตุ้นไมโครเกลีย และการทำลายเลือด-สมองในสารสีขาวที่ดูปกติ มีความสัมพันธ์กับความบกพร่องทางคลินิกสูงกว่ารอยโรคสารสีขาวเฉพาะที่
โอลิโกเดนโดรไซต์ทำหน้าที่สร้างไมอีลินใหม่ในระบบประสาทส่วนกลาง 1) ขึ้นอยู่กับเซลล์ตั้งต้นของโอลิโกเดนโดรไซต์ในผู้ใหญ่ (OPC) แต่โอลิโกเดนโดรไซต์ที่เจริญเต็มที่ที่มีอยู่แล้วไม่มีส่วนในการสร้างไมอีลินใหม่ 1)
สาเหตุหลักของความล้มเหลวในการสร้างไมอีลินใหม่มีดังนี้ 1)
นอกจากนี้ ยังพบความเสียหายของเนื้อเทาในคอร์เทกซ์และใต้คอร์เทกซ์ และเป็นที่ทราบกันว่าการสร้างโครงสร้างน้ำเหลืองคล้ายฟอลลิเคิลของเซลล์บีในเยื่อหุ้มสมองนำไปสู่การดำเนินโรคทางคลินิกที่รุนแรงขึ้น1)
แนวทางใหม่ที่ยับยั้ง CD40L เพื่อปิดกั้นการกระตุ้นร่วมระหว่างทีเซลล์และเซลล์นำเสนอแอนติเจน (รวมถึงบีเซลล์)
ในการทดลองระยะที่ 2 โดย Vermersch และคณะ (N Engl J Med 2024) frexalimab แสดงประสิทธิภาพที่ชัดเจนเมื่อเทียบกับยาหลอกในผลลัพธ์ MRI (รอยโรคที่เพิ่มความเข้มด้วยแกโดลิเนียมใหม่ในช่วงสัปดาห์ที่ 8-12) และยังยืนยันการลดลงของ NfL ในซีรั่ม ซึ่งเป็นตัวบ่งชี้ทางชีวภาพของความเสียหายของเนื้อเยื่อประสาท3) สำหรับ MS ชนิดลุกลาม คาดว่าจะมีผลในการยับยั้งไมโครเกลียและมาโครฟาจ และในทางทฤษฎี สามารถปกป้องเซลล์ประสาทได้โดยการปิดกั้นสัญญาณ CD40L บนไมโครเกลียที่ขอบของแผ่นคราบจุลินทรีย์3)
การสร้างความเหนือกว่าทางคลินิกเหนือ DMT ที่มีประสิทธิภาพสูงในปัจจุบัน (anti-CD20) ถือเป็นความท้าทายในอนาคต3)
พบว่า ferroptosis ซึ่งเป็นการตายของเซลล์ที่ขึ้นกับเหล็ก มีส่วนเกี่ยวข้องกับการตายของเซลล์ประสาทใน MS
Tang et al. (2025) อธิบายการศึกษาของ Woo et al. (Cell, 2024) และรายงานลำดับเหตุการณ์: ความเป็นพิษต่อเซลล์ประสาทจากกลูตาเมต → ภาวะแคลเซียมเกิน → ความเครียดของเอนโดพลาสมิกเรติคูลัม → STING1 หลุดจาก STIM1 → การกระตุ้นวิถีที่ไม่ใช่แบบดั้งเดิม → ออโตฟาจี → การสลาย GPX4 (เอนไซม์ทำให้เป็นกลางของลิพิดเปอร์ออกซิเดชัน) โดยออโตฟาจี → เฟอร์รอปโทซิส 4) พบการเพิ่มขึ้นของการแสดงออกของ STING1 ในเซลล์ประสาททั้งในตัวอย่าง MS ของมนุษย์และแบบจำลองหนู ยับยั้ง STING1 (C176, H151) ลดการสลาย GPX4 ที่ขึ้นกับออโตฟาจีและแสดงผลป้องกันระบบประสาทในแบบจำลองสัตว์ 4)
ในขั้นตอนการวิจัย การป้องกันระบบประสาทผ่านการยับยั้งไมโครเกลียและมาโครฟาจโดยยา frexalimab ซึ่งยับยั้ง CD40L 3) และการยับยั้งเฟอร์รอปโทซิส (การตายของเซลล์ที่ขึ้นกับเหล็ก) โดยการยับยั้ง STING1 4) ถือว่ามีแนวโน้มดี ทั้งสองอย่างอยู่ในขั้นตอนการทดลองทางคลินิกและการวิจัย ยังไม่ใช่การรักษามาตรฐาน