РРРС
Рецидивирующе-ремиттирующий РС (РРРС) : самый распространенный подтип. Рецидивы длятся более 24 часов, между ними наблюдается полная или частичная ремиссия.

Рассеянный склероз (РС) — это заболевание, при котором в белом веществе центральной нервной системы (ЦНС) возникают воспалительные демиелинизирующие очаги, вызывающие разнообразные неврологические симптомы с рецидивами и ремиссиями. Характерны склеротические рубцовые изменения вследствие глиоза, обычно поражается только ЦНС, периферическая нервная система не затрагивается.
Расчетная распространенность в США составляет 1–1,5 на 1000 человек1). В мире насчитывается 2,1 миллиона больных, с более частым распространением в высоких широтах Северного и Южного полушарий. Средний возраст начала заболевания — 15–45 лет, средний возраст на момент диагностики — 30 лет. Чаще болеют в возрасте 15–50 лет, женщины (пик в конце 20-х годов), соотношение мужчин и женщин 1:2,9.
РС имеет четыре основных подтипа. РРРС (рецидивирующе-ремиттирующий) обычно начинается в возрасте 25–29 лет, а ВПРС чаще встречается в возрасте 40–49 лет1).
РРРС
Рецидивирующе-ремиттирующий РС (РРРС) : самый распространенный подтип. Рецидивы длятся более 24 часов, между ними наблюдается полная или частичная ремиссия.
ВПРС
Вторично-прогрессирующий РС (ВПРС) : переход из РРРС. Прогрессирующее накопление инвалидности даже в периоды ремиссии.
ППРС
Первично-прогрессирующий РС (ППРС) : прогрессирующее накопление инвалидности с самого начала, без рецидивов, медленное прогрессирование.
КИС
Клинически изолированный синдром (КИС) : первый клинический эпизод, который может перейти в РС. Позволяет начать раннее лечение.
РС делится на четыре подтипа: РРРС (рецидивирующе-ремиттирующий), ВПРС (вторично-прогрессирующий), ППРС (первично-прогрессирующий) и КИС (клинически изолированный синдром). Наиболее распространен РРРС, характеризующийся рецидивами и ремиссиями. ВПРС развивается из РРРС, а ППРС прогрессирует с самого начала.
У 75% пациентов первым симптомом является единственная жалоба, у 45% — двигательные/сенсорные симптомы, у 20% — зрительные симптомы.
Глазные симптомы
Общие неврологические симптомы
Обострение начинается остро или подостро и длится от нескольких дней до нескольких месяцев. В 85% случаев симптомы улучшаются или исчезают, но в 10–15% остаются остаточные явления.
Часто проявляется односторонним болезненным снижением зрения. Глазничная боль наблюдается в 92% случаев, усиливается при движениях глаз. Также наблюдается феномен Утгоффа, когда повышение температуры тела (ванна, физическая нагрузка) временно ухудшает симптомы.
Точная причина РС неизвестна, но считается, что в его развитии участвует аутоиммунный механизм.
Генетические факторы вовлечены, но уровень конкордантности у однояйцевых близнецов составляет всего 25–30%. Хотя были идентифицированы полиморфизм HLA и более 100 локусов риска, считается, что не только генетическая предрасположенность, но и факторы окружающей среды играют важную роль в развитии заболевания.
Используются критерии Макдональда 2017 года (пересмотр 2024 года). Основным является доказательство временной и пространственной диссеминации (DIT/DIS) демиелинизирующих поражений центральной нервной системы. В пересмотре 2024 года зрительный нерв был добавлен в качестве пятой топографической области. В Японии также существуют диагностические критерии рассеянного склероза Министерства здравоохранения, труда и социального обеспечения 2015 года.
Пять топографических областей пространственной диссеминации (DIS) следующие:
Доказательство диссеминации во времени (DIT): ≥2 атак, или одновременное наличие накапливающих и не накапливающих контраст очагов на МРТ, новые очаги в режиме Т2, или олигоклональные полосы в ЦСЖ 1).
Для диагностики ППМС, помимо прогрессирования инвалидности ≥1 года, необходимы как минимум 2 из следующих признаков: очаги в головном мозге в режиме Т2, очаги в спинном мозге в режиме Т2 (≥2), или олигоклональные полосы в ЦСЖ 1).
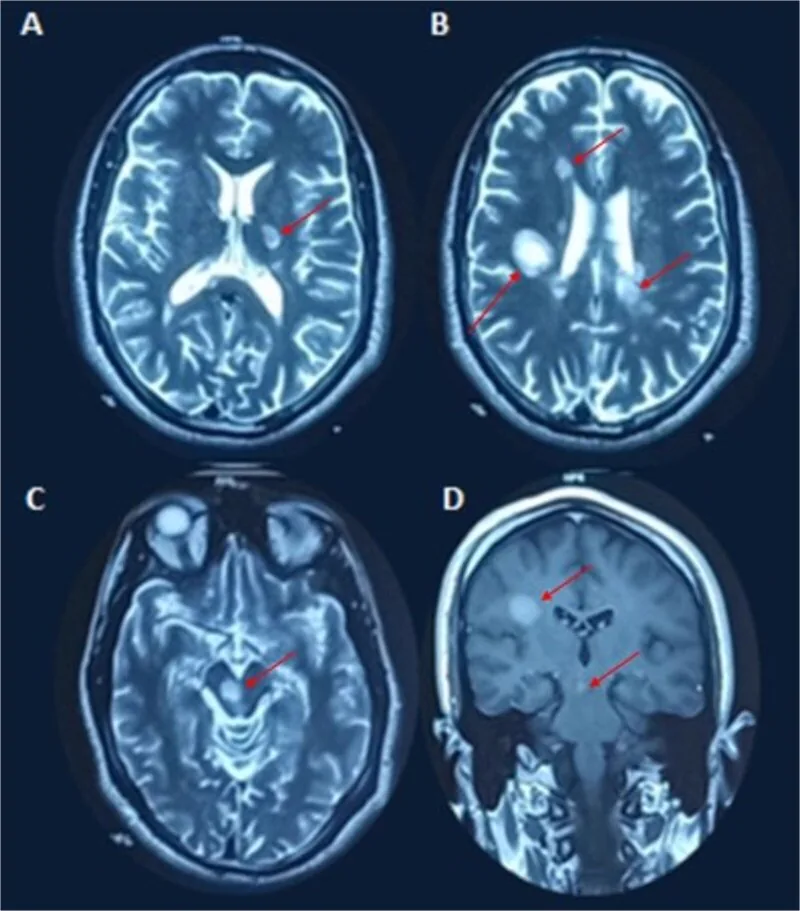
Бляшки демиелинизации выявляются как гиперинтенсивные очаги в режиме Т2 или очаги, накапливающие гадолиний.
Полезны, когда МРТ неинформативна или для прогнозирования прогрессирования заболевания 1). Могут выявить раннюю бессимптомную демиелинизацию до ее визуализации на МРТ. В 65% случаев отмечается удлинение латентности и снижение амплитуды.
Важно дифференцировать следующие заболевания; в нетипичных случаях проводятся дополнительные исследования.
| Категория заболевания | Основные дифференциальные диагнозы |
|---|---|
| Демиелинизирующие заболевания | NMO (болезнь Девика), ADEM, MOGAD |
| Инфекционные | Саркоидоз, туберкулез, сифилис, болезнь Лайма |
| Аутоиммунные | СКВ, синдром Шегрена, болезнь Бехчета |
| Заболевания зрительного нерва | NAION, LHON, токсическая/метаболическая оптическая нейропатия |
Дополнительные исследования при атипичных случаях: антитела к AQP4 (для исключения NMO), антитела к MOG (для исключения MOGAD), уровень NfL в сыворотке, серология сифилиса (VDRL/RPR/FTA-ABS), ANA (для СКВ), ACE и лизоцим (для саркоидоза).
Стандартным лечением в Японии является пульс-терапия метилпреднизолоном в дозе 1000 мг/сут внутривенно капельно в течение 3 дней подряд. После 3-дневной инфузии пероральный прием преднизолона (последующая терапия) не проводится. Пероральная стероидная терапия повышает частоту рецидивов и не должна применяться.
Даже без лечения примерно у 80% пациентов улучшение зрения начинается в течение 3 недель от начала заболевания, но пульс-терапия сокращает период улучшения. Более чем в 90% случаев неврита зрительного нерва можно ожидать восстановления зрения.
При неэффективности пульс-терапии стероидами проводится гемокоррекция (плазмаферез). За рубежом применяют метилпреднизолон в дозе 500–1000 мг/сут в течение 3–5 дней. В исследовании лечения неврита зрительного нерва (ONTT) высокие дозы внутривенного метилпреднизолона улучшали время восстановления зрительных функций, контрастной чувствительности и цветового зрения, но не показали улучшения конечного зрительного прогноза.
После улучшения снижения зрения и дефектов поля зрения следует рассмотреть DMT для профилактики рецидивов в сотрудничестве с неврологом.
Основные DMT и их эффективность приведены ниже.
| Препарат | Механизм действия | Путь введения | Снижение относительного риска |
|---|---|---|---|
| Интерферон бета | Модуляция активности T/B-клеток и секреции цитокинов | Самостоятельная инъекция | ОР прогрессирования инвалидности 0,71 |
| Глатирамера ацетат | Регуляция регуляторных T-клеток | Самостоятельная инъекция | ОР рецидива 0,82 |
| Натализумаб | Ингибирование проникновения воспалительных клеток в ЦНС | Инфузия | ОР рецидива 0,56 |
| Финголимод | Модуляция S1P-рецепторов | Перорально | Новые очаги T2 RR 0,65 |
| Терифлуномид | Ингибирование синтеза пиримидинов | Перорально | Прогрессирование инвалидности RR 0,76 |
| Диметилфумарат | Снижение окислительного стресса и воспаления | Перорально | Рецидив RR 0,64 |
| Алемтузумаб | Анти-CD52 моноклональное антитело | Инфузия | Прогрессирование инвалидности RR 0,44 |
Анти-CD20 моноклональные антитела (окрелизумаб, ритуксимаб, офатумумаб) стали стандартной терапией рецидивирующего рассеянного склероза3).
Даже при отсутствии поражений головного мозга у 25% пациентов с невритом зрительного нерва через 15 лет развивается РС, а при наличии поражений головного мозга переход в РС наблюдается у 78%.
Даже при отсутствии поражений на МРТ головного мозга через 15 лет у 25% развивается РС, а при наличии поражений головного мозга переход в РС наблюдается у 78%. Пациентам с невритом зрительного нерва следует рассмотреть возможность применения ПИТРС для профилактики рецидивов в сотрудничестве с неврологом.
РС считается аутоиммунным заболеванием. Т-лимфоциты распознают миелин как чужеродный и активируют макрофаги, цитокины и антитела, разрушающие миелин и аксоны. Потеря миелина нарушает проведение электрических импульсов и ухудшает передачу нервных сигналов.
Активная бляшка
Пенистые макрофаги : скопление макрофагов, фагоцитировавших миелиновую оболочку.
Периваскулярная инфильтрация (perivascular cuffing) : характерный признак – лимфоциты, окружающие кровеносные сосуды.
Отечные очаговые демиелинизирующие поражения : наблюдаются во время острых обострений.
Хроническая бляшка
Потеря миелина : подтверждается окрашиванием Luxol fast blue. Аксоны сохраняются, но ремиелинизация неполная.
Поражения NAWM : диффузный глиоз, активация микроглии и разрушение ГЭБ в нормально выглядящем белом веществе. Они сильнее коррелируют с клиническими нарушениями, чем очаговые поражения белого вещества.
Олигодендроциты отвечают за ремиелинизацию в ЦНС1). Она зависит от взрослых клеток-предшественников олигодендроцитов (OPC), но существующие зрелые олигодендроциты не могут участвовать в ремиелинизации1).
Основные причины неудачи ремиелинизации следующие1).
Кроме того, наблюдаются поражения коркового и подкоркового серого вещества, и известно, что формирование В-клеточных фолликулоподобных лимфоидных структур в мозговых оболочках приводит к более тяжелому клиническому течению 1).
Это новый подход, который блокирует костимуляцию между Т-клетками и антигенпрезентирующими клетками (включая В-клетки) путем ингибирования CD40L.
В исследовании фазы 2 Vermersch et al. (N Engl J Med 2024) фрексалимаб показал четкую эффективность по сравнению с плацебо по данным МРТ (новые очаги, накапливающие гадолиний, на 8–12 неделе), также было подтверждено снижение сывороточного NfL, биомаркера повреждения нервной ткани 3). Для прогрессирующего РС также ожидается эффект инактивации микроглии и макрофагов, и теоретически возможна нейропротекция за счет блокирования сигнала CD40L на микроглии по краю бляшки 3).
Установление клинического преимущества перед существующими высокоэффективными ПИТРС (анти-CD20 препаратами) считается будущей задачей 3).
Было показано, что ферроптоз, железозависимая клеточная гибель, участвует в гибели нейронов при РС.
Tang et al. (2025) комментируют исследование Woo et al. (Cell, 2024) и сообщают о каскаде: глутаматная эксайтотоксичность → перегрузка кальцием → стресс эндоплазматического ретикулума → диссоциация STING1 от STIM1 → активация неканонического пути → аутофагия → аутофагическая деградация GPX4 (фермента, нейтрализующего перекисное окисление липидов) → ферроптоз 4). Повышение экспрессии STING1 в нейронах было подтверждено как в образцах РС человека, так и на мышиных моделях. Ингибиторы STING1 (C176, H151) уменьшали аутофагическую деградацию GPX4 на животных моделях и оказывали нейропротекторное действие 4).
На стадии исследований нейропротекция путем инактивации микроглии и макрофагов с помощью ингибитора CD40L фрексалимаба 3) и подавление ферроптоза (железозависимой клеточной гибели) с помощью ингибирования STING1 4) считаются многообещающими. Оба подхода в настоящее время находятся на стадии клинических испытаний/исследований и не являются стандартной терапией.