EMRR
Esclerose Múltipla Remitente-Recorrente (EMRR): Subtipo mais comum. As recaídas duram mais de 24 horas, com remissão completa ou parcial entre os surtos.

A esclerose múltipla (EM) é uma doença desmielinizante inflamatória da substância branca do sistema nervoso central (SNC), que causa diversos sintomas neurológicos com surtos e remissões. Caracteriza-se por lesões escleróticas devido à gliose, e geralmente afeta apenas o SNC, poupando o sistema nervoso periférico.
A prevalência estimada nos EUA é de 1 a 1,5 por 1000 pessoas 1). Mundialmente, 2,1 milhões de pessoas são afetadas, com maior distribuição em regiões de alta latitude nos hemisférios norte e sul. A idade média de início é de 15 a 45 anos, e a idade média ao diagnóstico é de 30 anos. A faixa etária mais comum é de 15 a 50 anos, mais frequente em mulheres (pico no final dos 20 anos) com proporção homem:mulher de 1:2,9.
A EM tem quatro subtipos principais. A EMRR (Esclerose Múltipla Remitente-Recorrente) geralmente surge entre 25 e 29 anos, enquanto a EMSP (Esclerose Múltipla Secundariamente Progressiva) surge frequentemente entre 40 e 49 anos1).
EMRR
Esclerose Múltipla Remitente-Recorrente (EMRR): Subtipo mais comum. As recaídas duram mais de 24 horas, com remissão completa ou parcial entre os surtos.
EMSP
Esclerose Múltipla Secundariamente Progressiva (EMSP): Transição da EMRR. A incapacidade progride mesmo durante a remissão.
EMPP
Esclerose Múltipla Primariamente Progressiva (EMPP): A incapacidade progride desde o início. Avança lentamente sem recaídas.
CIS
Síndrome Clínica Isolada (CIS): Primeiro episódio clínico que pode evoluir para EM. Permite início precoce do tratamento.
A EM é classificada em quatro subtipos: EMRR (Remitente-Recorrente), EMSP (Secundariamente Progressiva), EMPP (Primariamente Progressiva) e CIS (Síndrome Clínica Isolada). O mais comum é a EMRR, com recaídas e remissões alternadas. A EMSP é a transição da EMRR, enquanto a EMPP progride desde o início.
Em 75% dos pacientes, o sintoma inicial é uma queixa única, sendo 45% sintomas motores/sensitivos e 20% sintomas visuais.
Sintomas Oculares
Sintomas Neurológicos Sistêmicos
A exacerbação é aguda a subaguda e dura de alguns dias a vários meses. Em 85% dos casos, os sintomas melhoram ou desaparecem, mas em 10-15% persistem sequelas.
Frequentemente se inicia como perda visual dolorosa unilateral. Dor orbitária é encontrada em 92% dos casos, piorando com o movimento ocular. O fenômeno de Uhthoff (piora temporária com aumento da temperatura corporal, como banho ou exercício) também é observado.
A causa exata da EM é desconhecida, mas mecanismos autoimunes estão implicados no seu início.
Fatores genéticos estão envolvidos, mas a taxa de concordância em gêmeos idênticos é de apenas 25-30%. Polimorfismos HLA e mais de 100 loci de risco foram identificados, mas acredita-se que fatores ambientais, além da predisposição genética, desempenham um papel importante no início da doença.
Os critérios de McDonald 2017 (revisão 2024) são utilizados. O princípio é demonstrar a disseminação temporal e espacial (DIT/DIS) das lesões desmielinizantes no sistema nervoso central. Na revisão de 2024, o nervo óptico foi adicionado como o quinto sítio anatômico. No Japão, também existem os critérios diagnósticos de esclerose múltipla do Ministério da Saúde, Trabalho e Bem-Estar de 2015.
Os cinco sítios anatômicos para disseminação espacial (DIS) são os seguintes:
Evidência de disseminação temporal (DIT): dois ou mais surtos, ou presença simultânea de lesões com e sem realce na RM, novas lesões T2, ou pode ser substituída por bandas oligoclonais no LCR 1).
Para o diagnóstico de PPMS, além da progressão da incapacidade por ≥1 ano, são necessários dois ou mais dos seguintes achados: lesões T2 cerebrais, lesões T2 na medula espinhal (≥2), ou bandas oligoclonais no LCR 1).
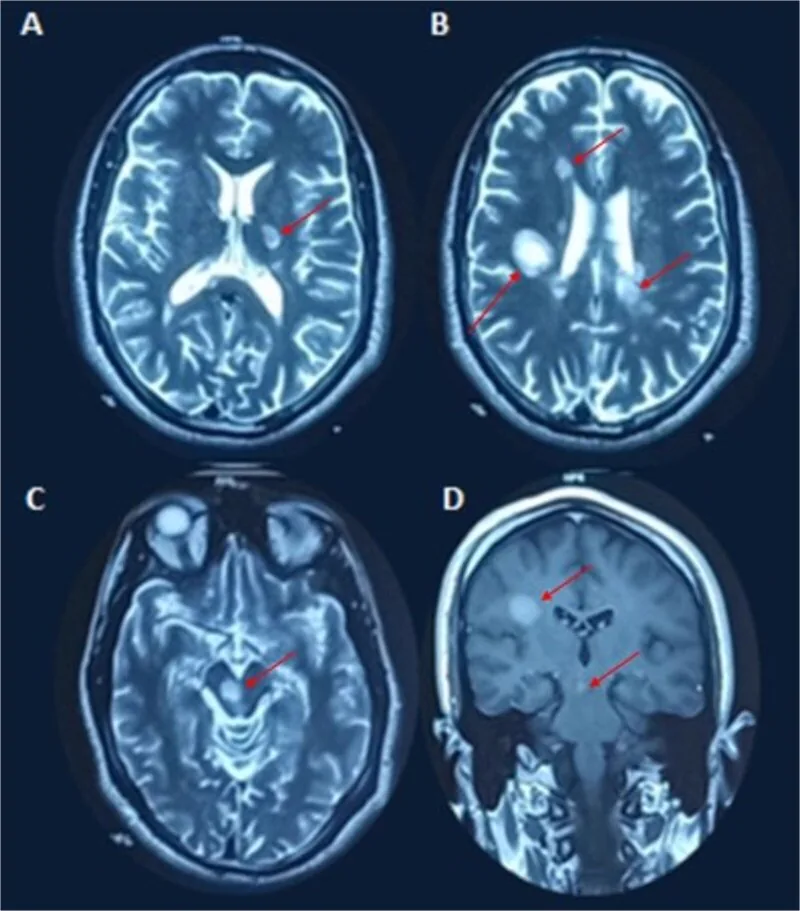
As placas de desmielinização são detectadas como lesões hiperintensas em T2 ou lesões com realce pelo gadolínio.
Útil quando a RM é inconclusiva ou para prever a progressão da doença 1). Pode detectar desmielinização precoce assintomática antes da visualização por RM. Em 65% dos casos, observa-se prolongamento da latência e redução da amplitude.
É importante diferenciar das seguintes doenças, e em casos atípicos, exames adicionais são realizados.
| Categoria da Doença | Principais Diagnósticos Diferenciais |
|---|---|
| Doenças Desmielinizantes | NMO (doença de Devic), ADEM, MOGAD |
| Infeccioso | Sarcoidose, tuberculose, sífilis, doença de Lyme |
| Autoimune | LES, síndrome de Sjögren, doença de Behçet |
| Doenças do nervo óptico | NAION, LHON, neuropatia óptica tóxica/metabólica |
Exames adicionais em casos atípicos: anticorpo anti-AQP4 (para excluir NMO), anticorpo anti-MOG (para excluir MOGAD), exame de NfL sérico, sorologia para sífilis (VDRL/RPR/FTA-ABS), FAN (para LES), ECA/lisozima (para sarcoidose).
O tratamento padrão no Japão é a pulsoterapia com metilprednisolona 1000 mg/dia intravenosa por 3 dias consecutivos. Não é administrada prednisolona oral após a infusão. A terapia com corticosteroides orais não deve ser realizada, pois aumenta a taxa de recorrência.
Mesmo sem tratamento, a melhora visual começa em cerca de 80% dos casos dentro de 3 semanas do início, mas a pulsoterapia encurta o período de melhora. A recuperação visual é esperada em mais de 90% dos casos de neurite óptica.
Se a pulsoterapia com corticosteroides for ineficaz, realiza-se terapia de purificação sanguínea (troca plasmática). No exterior, utiliza-se metilprednisolona 500-1000 mg/dia por 3-5 dias. No ensaio clínico de tratamento da neurite óptica (ONTT), a metilprednisolona intravenosa em alta dose melhorou o tempo de recuperação da função visual, sensibilidade ao contraste e visão de cores, mas não demonstrou melhora no resultado visual final.
Após a melhora da perda visual e dos defeitos de campo visual, a terapia modificadora da doença deve ser considerada em colaboração com o neurologista para prevenir recorrências.
Abaixo estão as principais terapias modificadoras da doença e sua eficácia.
| Medicamento | Mecanismo de ação | Via de administração | Redução do risco relativo |
|---|---|---|---|
| Interferon beta | Modulação da atividade de células T/B e secreção de citocinas | Autoinjeção | Progressão da incapacidade RR 0,71 |
| Acetato de glatirâmer | Regulação de células T reguladoras | Autoinjeção | Recaída RR 0,82 |
| Natalizumabe | Inibição da entrada de células inflamatórias no SNC | Infusão | Recaída RR 0,56 |
| Fingolimode | Modulador do receptor S1P | Oral | RR de novas lesões T2 0,65 |
| Teriflunomida | Inibição da síntese de pirimidina | Oral | RR de progressão da incapacidade 0,76 |
| Dimetilfumarato | Redução do estresse oxidativo e inflamação | Oral | RR de recaída 0,64 |
| Alemtuzumabe | Anticorpo monoclonal anti-CD52 | Infusão | RR de progressão da incapacidade 0,44 |
Os anticorpos monoclonais anti-CD20 (ocrelizumabe, rituximabe, ofatumumabe) tornaram-se tratamento padrão para a EM surto-remissão 3).
Mesmo na neurite óptica sem lesões cerebrais, 25% desenvolvem EM após 15 anos, e com lesões cerebrais, 78% evoluem para EM.
Mesmo sem lesões na ressonância magnética cerebral, 25% desenvolvem EM após 15 anos, e com lesões cerebrais, 78% evoluem para EM. Pacientes com neurite óptica devem considerar o uso de DMT para prevenção de surtos em conjunto com o neurologista.
A EM é considerada uma doença autoimune. Os linfócitos T reconhecem a mielina como estranha, ativando macrófagos, citocinas e anticorpos para destruir a mielina e os axônios. A perda de mielina prejudica a condução dos impulsos elétricos, comprometendo a transmissão dos sinais nervosos.
Placa ativa
Macrófagos espumosos: Acúmulo de macrófagos que fagocitam mielina.
Infiltrado perivascular (perivascular cuffing): Linfócitos circundando os vasos sanguíneos, achado característico.
Lesões de desmielinização focal edematosa: Observadas durante a fase de exacerbação aguda.
Placa crônica
Perda de mielina: Confirmada pela coloração Luxol fast blue. Os axônios são preservados, mas a remielinização é incompleta.
Lesões NAWM (substância branca de aparência normal): Gliose difusa, ativação microglial e ruptura da barreira hematoencefálica na substância branca de aparência normal. Correlacionam-se mais fortemente com o comprometimento clínico do que as lesões focais da substância branca.
Os oligodendrócitos são responsáveis pela remielinização do SNC 1). Dependem de células precursoras de oligodendrócitos adultos (OPC), mas os oligodendrócitos maduros existentes não contribuem para a remielinização 1).
As principais causas de falha na remielinização são as seguintes 1).
Além disso, danos à substância cinzenta cortical e subcortical também são observados, e sabe-se que a formação de estruturas linfoides semelhantes a folículos de células B nas meninges leva a um curso clínico mais grave1).
Uma nova abordagem que inibe o CD40L para bloquear a coestimulação entre células T e células apresentadoras de antígeno (incluindo células B).
No ensaio de fase 2 por Vermersch et al. (N Engl J Med 2024), o frexalimabe mostrou eficácia clara em relação ao placebo nos desfechos de RM (novas lesões realçadas por gadolínio entre 8-12 semanas), e também foi confirmada a redução do NfL sérico, um biomarcador de dano ao tecido nervoso3). Para a EM progressiva, espera-se também um efeito de inativação de micróglia e macrófagos, e teoricamente, a neuroproteção pode ser alcançada pelo bloqueio da sinalização de CD40L na micróglia na borda da placa3).
O estabelecimento da superioridade clínica em relação às DMTs de alta eficácia atuais (anti-CD20) é considerado um desafio futuro3).
Foi demonstrado que a ferroptose, uma morte celular dependente de ferro, está envolvida na morte neuronal na EM.
Tang et al. (2025) explicaram o estudo de Woo et al. (Cell, 2024) e relataram a cascata: excitotoxicidade do glutamato → sobrecarga de cálcio → estresse do retículo endoplasmático → dissociação de STING1 de STIM1 → ativação da via não canônica → autofagia → degradação autofágica de GPX4 (enzima neutralizante da peroxidação lipídica) → ferroptose 4). O aumento da expressão de STING1 em neurônios foi confirmado tanto em amostras de EM humana quanto em modelos murinos. Os inibidores de STING1 (C176, H151) reduziram a degradação de GPX4 dependente de autofagia e mostraram efeito neuroprotetor em modelos animais 4).
Em fase de pesquisa, a neuroproteção através da inativação de micróglia e macrófagos pelo inibidor de CD40L frexalimab 3) e a inibição da ferroptose (morte celular dependente de ferro) pela inibição de STING1 4) são consideradas promissoras. Ambas estão atualmente em fase de ensaios clínicos e pesquisa, não sendo tratamento padrão.