RRMS
रिलैप्सिंग-रेमिटिंग MS (RRMS) : सबसे सामान्य उपप्रकार। रिलैप्स 24 घंटे से अधिक रहते हैं और उनके बीच पूर्ण या आंशिक छूट होती है।

मल्टीपल स्केलेरोसिस (MS) केंद्रीय तंत्रिका तंत्र (CNS) के श्वेत पदार्थ में सूजन संबंधी विमाइलिनीकरण घावों का कारण बनने वाला रोग है, जिसमें विविध तंत्रिका संबंधी लक्षण पुनरावृत्ति और छूट के साथ होते हैं। ग्लियोसिस के कारण निशान-कठोर घाव इसकी विशेषता है, और आमतौर पर केवल CNS प्रभावित होता है, परिधीय तंत्रिका तंत्र अप्रभावित रहता है।
अमेरिका में अनुमानित प्रसार 1-1.5 प्रति 1,000 व्यक्ति है1)। दुनिया भर में 2.1 मिलियन लोग प्रभावित हैं, जो उत्तरी और दक्षिणी गोलार्ध के उच्च अक्षांश क्षेत्रों में अधिक पाए जाते हैं। औसत आयु 15-45 वर्ष है, और निदान के समय औसत आयु 30 वर्ष है। सामान्य आयु सीमा 15-50 वर्ष है, महिलाओं में अधिक (20 के दशक के अंत में चरम), और लिंग अनुपात 1:2.9 है।
MS के चार मुख्य उपप्रकार हैं। RRMS (रिलैप्सिंग-रेमिटिंग) आमतौर पर 25-29 वर्ष की आयु में शुरू होता है, जबकि SPMS 40-49 वर्ष की आयु में अधिक पाया जाता है1)।
RRMS
रिलैप्सिंग-रेमिटिंग MS (RRMS) : सबसे सामान्य उपप्रकार। रिलैप्स 24 घंटे से अधिक रहते हैं और उनके बीच पूर्ण या आंशिक छूट होती है।
SPMS
सेकेंडरी प्रोग्रेसिव MS (SPMS) : RRMS से संक्रमण। छूट के दौरान भी विकलांगता धीरे-धीरे बढ़ती है।
PPMS
प्राइमरी प्रोग्रेसिव MS (PPMS) : शुरुआत से ही विकलांगता धीरे-धीरे बढ़ती है, बिना रिलैप्स के।
CIS
क्लिनिकली आइसोलेटेड सिंड्रोम (CIS) : पहला क्लिनिकल एपिसोड जो MS बन सकता है। प्रारंभिक उपचार संभव बनाता है।
75% रोगियों में प्रारंभिक लक्षण एक एकल शिकायत होती है, 45% में मोटर/संवेदी लक्षण और 20% में दृश्य लक्षण होते हैं।
नेत्र लक्षण
सामान्य तंत्रिका संबंधी लक्षण
तीव्रता तीव्र से अर्धतीव्र रूप में शुरू होती है और कुछ दिनों से लेकर कुछ महीनों तक रहती है। 85% मामलों में लक्षणों में सुधार या गायब हो जाता है, लेकिन 10-15% में अवशेष बने रहते हैं।
अक्सर एकतरफा दर्दनाक दृष्टि हानि के रूप में शुरू होता है। 92% में कक्षीय दर्द पाया जाता है, जो नेत्र गति से बढ़ जाता है। इसके अलावा, शरीर के तापमान में वृद्धि (स्नान, व्यायाम) से लक्षणों का अस्थायी रूप से बिगड़ना (उहथॉफ घटना) भी देखा जाता है।
MS का सटीक कारण अज्ञात है, लेकिन ऑटोइम्यून तंत्र इसकी शुरुआत में शामिल माना जाता है।
आनुवंशिक कारक शामिल हैं, लेकिन समान जुड़वां बच्चों में भी सहमति दर केवल 25-30% है। HLA बहुरूपता और 100 से अधिक जोखिम जीन स्थानों की पहचान की गई है, लेकिन ऐसा माना जाता है कि रोग की शुरुआत में न केवल आनुवंशिक प्रवृत्ति बल्कि पर्यावरणीय कारक भी महत्वपूर्ण भूमिका निभाते हैं।
2017 मैकडॉनल्ड मानदंड (2024 संशोधन) का उपयोग किया जाता है। केंद्रीय तंत्रिका तंत्र के डिमाइलिनेटिंग घावों के अस्थायी और स्थानिक प्रसार (DIT/DIS) को साबित करना मौलिक है। 2024 के संशोधन में ऑप्टिक तंत्रिका को पांचवें स्थलाकृतिक स्थल के रूप में जोड़ा गया था। जापान में, 2015 के स्वास्थ्य, श्रम और कल्याण मंत्रालय के मल्टीपल स्केलेरोसिस निदान मानदंड भी हैं।
स्थानिक प्रसार (DIS) के पांच स्थलाकृतिक स्थल इस प्रकार हैं:
समय में फैलाव (DIT) का प्रमाण: ≥2 दौरे, या MRI पर एक साथ बढ़ने वाले और न बढ़ने वाले घावों की उपस्थिति, नए T2 घाव, या CSF ओलिगोक्लोनल बैंड 1).
PPMS के निदान के लिए, ≥1 वर्ष की विकलांगता प्रगति के अलावा, निम्न में से कम से कम 2 की आवश्यकता है: मस्तिष्क T2 घाव, रीढ़ की हड्डी के T2 घाव (≥2), या CSF ओलिगोक्लोनल बैंड 1).
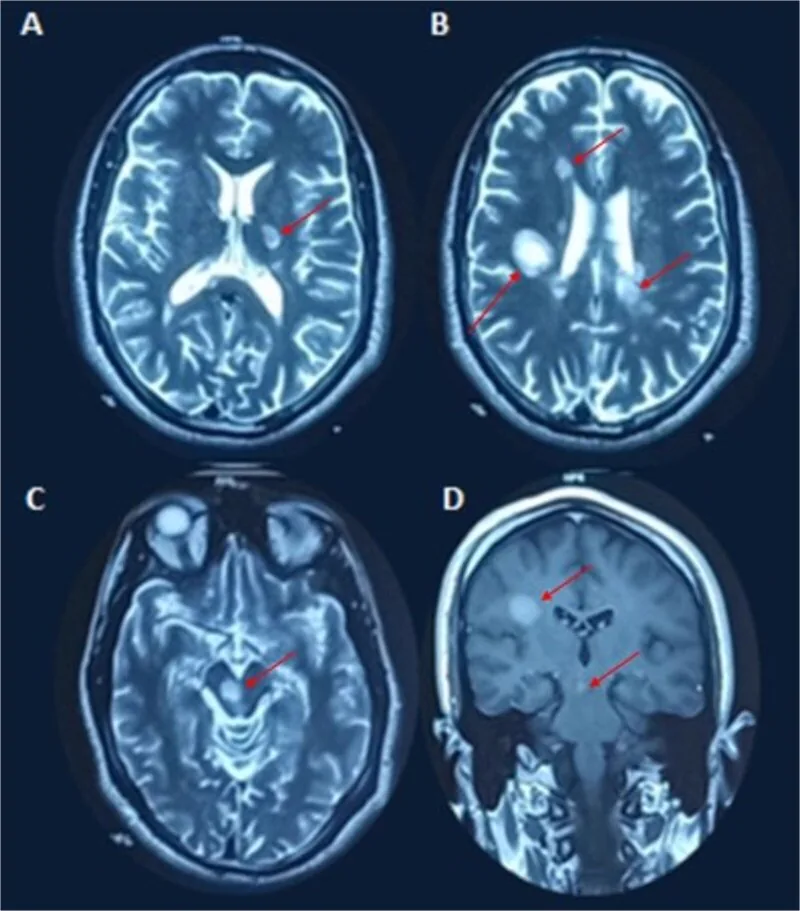
डिमाइलिनेशन प्लेक T2 हाइपरइंटेंस घावों या गैडोलीनियम-बढ़ाने वाले घावों के रूप में पाए जाते हैं।
MRI अनिर्णायक होने पर या रोग की प्रगति की भविष्यवाणी के लिए उपयोगी 1)। MRI दृश्यता से पहले प्रारंभिक, स्पर्शोन्मुख डिमाइलिनेशन का पता लगा सकता है। 65% में विलंबता लंबी और आयाम कम होता है।
निम्नलिखित रोगों से अंतर करना महत्वपूर्ण है; असामान्य मामलों में अतिरिक्त परीक्षण किए जाते हैं।
| रोग श्रेणी | मुख्य विभेदक निदान |
|---|---|
| डिमाइलिनेटिंग रोग | NMO (डेविक रोग), ADEM, MOGAD |
| संक्रामक | सारकॉइडोसिस, तपेदिक, उपदंश (सिफलिस), लाइम रोग |
| स्वप्रतिरक्षी | एसएलई (SLE), शेग्रेन सिंड्रोम, बेहसेट रोग |
| ऑप्टिक तंत्रिका रोग | NAION, LHON, विषाक्त/चयापचयी ऑप्टिक न्यूरोपैथी |
असामान्य मामलों में अतिरिक्त परीक्षण: एंटी-AQP4 एंटीबॉडी (NMO को बाहर करने के लिए), एंटी-MOG एंटीबॉडी (MOGAD को बाहर करने के लिए), सीरम NfL परीक्षण, उपदंश सीरोलॉजी (VDRL/RPR/FTA-ABS), ANA (SLE के लिए), ACE और लाइसोजाइम (सारकॉइडोसिस के लिए)।
जापान में मानक उपचार मिथाइलप्रेडनिसोलोन 1,000 मिलीग्राम/दिन का अंतःशिरा जलसेक लगातार 3 दिनों तक (स्टेरॉयड पल्स थेरेपी) है। 3 दिनों के जलसेक के बाद प्रेडनिसोलोन का मौखिक सेवन (अनुवर्ती चिकित्सा) नहीं किया जाता है। मौखिक स्टेरॉयड थेरेपी से पुनरावृत्ति दर बढ़ने का खतरा होता है, इसलिए इसका उपयोग नहीं किया जाना चाहिए।
उपचार के बिना भी, लगभग 80% रोगियों में लक्षण शुरू होने के 3 सप्ताह के भीतर दृष्टि में सुधार शुरू हो जाता है, लेकिन पल्स थेरेपी से सुधार की अवधि कम हो जाती है। ऑप्टिक न्यूरिटिस के 90% से अधिक मामलों में दृष्टि वापसी की उम्मीद की जा सकती है।
यदि स्टेरॉयड पल्स थेरेपी अप्रभावी है, तो रक्त शुद्धिकरण चिकित्सा (प्लाज्मा विनिमय) की जाती है। विदेशों में, मिथाइलप्रेडनिसोलोन 500-1,000 मिलीग्राम/दिन × 3-5 दिनों का उपयोग किया जाता है। ऑप्टिक न्यूरिटिस उपचार परीक्षण (ONTT) में, उच्च खुराक अंतःशिरा मिथाइलप्रेडनिसोलोन ने दृश्य कार्य, कंट्रास्ट संवेदनशीलता और रंग दृष्टि की वसूली के समय में सुधार किया, लेकिन अंतिम दृष्टि पूर्वानुमान में सुधार नहीं दिखाया गया।
दृष्टि हानि और दृश्य क्षेत्र दोषों में सुधार के बाद, पुनरावृत्ति को रोकने के लिए एक न्यूरोलॉजिस्ट के सहयोग से DMT पर विचार किया जाना चाहिए।
प्रमुख DMT और उनकी प्रभावशीलता नीचे दी गई है।
| दवा | क्रिया का तंत्र | प्रशासन का मार्ग | सापेक्ष जोखिम में कमी |
|---|---|---|---|
| इंटरफेरॉन बीटा | T/B कोशिका गतिविधि और साइटोकाइन स्राव का संशोधन | स्व-इंजेक्शन | विकलांगता प्रगति RR 0.71 |
| ग्लैटीरामर एसीटेट | नियामक T कोशिका नियमन | स्व-इंजेक्शन | पुनरावृत्ति RR 0.82 |
| नतालिज़ुमैब | CNS में सूजन कोशिका प्रवेश का अवरोध | अंतःशिरा जलसेक | पुनरावृत्ति RR 0.56 |
| फिंगोलिमोड | S1P रिसेप्टर मॉड्यूलेशन | मौखिक | नए T2 घाव RR 0.65 |
| टेरिफ्लुनोमाइड | पाइरीमिडीन संश्लेषण अवरोध | मौखिक | विकलांगता प्रगति RR 0.76 |
| डाइमिथाइल फ्यूमरेट | ऑक्सीडेटिव तनाव और सूजन में कमी | मौखिक | पुनरावृत्ति RR 0.64 |
| एलेमटुज़ुमैब | एंटी-CD52 मोनोक्लोनल एंटीबॉडी | अंतःशिरा जलसेक | विकलांगता प्रगति RR 0.44 |
एंटी-CD20 मोनोक्लोनल एंटीबॉडी (ओक्रेलिज़ुमैब, रीटक्सिमैब, ओफ़ाटुमुमैब) रिलैप्सिंग MS के मानक उपचार के रूप में स्थापित हो गए हैं3)।
मस्तिष्क के घावों के बिना ऑप्टिक न्यूरिटिस में भी 15 वर्षों के बाद 25% में MS विकसित होता है, और मस्तिष्क के घावों के साथ 78% में MS में संक्रमण देखा जाता है।
मस्तिष्क MRI में घाव न होने पर भी 15 वर्षों में 25% में MS विकसित होता है, और मस्तिष्क घाव होने पर 78% में MS में संक्रमण देखा जाता है। ऑप्टिक न्यूरिटिस के रोगियों को न्यूरोलॉजी के सहयोग से पुनरावृत्ति रोकथाम के लिए DMT पर विचार करना चाहिए।
MS को एक ऑटोइम्यून बीमारी माना जाता है। T लिम्फोसाइट्स माइलिन को विदेशी के रूप में पहचानते हैं और मैक्रोफेज, साइटोकाइन और एंटीबॉडी को सक्रिय करके माइलिन और एक्सॉन को नष्ट करते हैं। माइलिन के नष्ट होने से विद्युत आवेगों का संचालन बाधित होता है और तंत्रिका संकेत संचरण ख़राब होता है।
सक्रिय प्लाक
फोमी मैक्रोफेज : माइलिन आवरण को फैगोसाइट करने वाले मैक्रोफेज का संचय।
पेरिवैस्कुलर कफिंग : रक्त वाहिकाओं के चारों ओर लिम्फोसाइटों का विशिष्ट घेरा।
एडेमेटस फोकल डिमाइलिनेशन घाव : तीव्र प्रकोप के दौरान देखे जाते हैं।
क्रोनिक प्लाक
माइलिन हानि : लक्सोल फास्ट ब्लू धुंधलापन से पुष्टि। एक्सॉन संरक्षित रहते हैं लेकिन पुनर्माइलिनीकरण अपूर्ण होता है।
NAWM घाव : सामान्य दिखने वाले श्वेत पदार्थ में फैली हुई ग्लियोसिस, माइक्रोग्लिया सक्रियण और BBB टूटना। ये फोकल श्वेत पदार्थ घावों की तुलना में नैदानिक हानि से अधिक संबंधित होते हैं।
ऑलिगोडेंड्रोसाइट्स CNS के पुनर्माइलिनीकरण के लिए जिम्मेदार हैं1)। यह वयस्क ऑलिगोडेंड्रोसाइट अग्रदूत कोशिकाओं (OPC) पर निर्भर करता है, लेकिन मौजूदा परिपक्व ऑलिगोडेंड्रोसाइट्स पुनर्माइलिनीकरण में योगदान नहीं दे सकते1)।
पुनर्माइलिनीकरण विफलता के मुख्य कारण निम्नलिखित हैं1)।
इसके अलावा, कॉर्टिकल और सबकॉर्टिकल ग्रे मैटर की क्षति भी देखी जाती है, और जब मेनिन्जेस में B कोशिका कूपिक लिम्फॉइड संरचनाएं बनती हैं, तो यह अधिक गंभीर नैदानिक पाठ्यक्रम की ओर ले जाती है 1).
CD40L को अवरुद्ध करके, T कोशिकाओं और प्रतिजन प्रस्तुत करने वाली कोशिकाओं (B कोशिकाओं सहित) के बीच सह-उत्तेजना को बाधित करने वाला एक नया दृष्टिकोण है।
Vermersch et al. (N Engl J Med 2024) द्वारा चरण 2 परीक्षण में, frexalimab ने MRI परिणामों (8-12 सप्ताह में नए गैडोलीनियम-वर्धित घाव) में प्लेसीबो की तुलना में स्पष्ट प्रभावकारिता दिखाई, और तंत्रिका ऊतक क्षति के बायोमार्कर सीरम NfL में कमी भी पुष्टि की गई 3)। प्रगतिशील MS के लिए, माइक्रोग्लिया और मैक्रोफेज के निष्क्रियीकरण का प्रभाव भी अपेक्षित है, और प्लाक किनारे पर माइक्रोग्लिया में CD40L सिग्नल को अवरुद्ध करके न्यूरोप्रोटेक्शन सैद्धांतिक रूप से संभव माना जाता है 3).
वर्तमान उच्च-प्रभावकारिता DMT (एंटी-CD20 दवाओं) पर नैदानिक श्रेष्ठता स्थापित करना भविष्य की चुनौती माना जाता है 3).
लौह-निर्भर कोशिका मृत्यु, फेरोप्टोसिस, MS न्यूरोनल मृत्यु में शामिल पाया गया है।
Tang et al. (2025) ने Woo et al. (Cell, 2024) के अध्ययन की व्याख्या करते हुए एक कैस्केड की रिपोर्ट की: ग्लूटामेट उत्तेजक विषाक्तता → कैल्शियम अधिभार → एंडोप्लाज्मिक रेटिकुलम तनाव → STING1 का STIM1 से पृथक्करण → गैर-विशिष्ट मार्ग सक्रियण → ऑटोफैजी → GPX4 (लिपिड पेरोक्सीडेशन को निष्क्रिय करने वाला एंजाइम) का ऑटोफैजिक अपघटन → फेरोप्टोसिस 4)। मानव MS नमूनों और माउस मॉडल दोनों में न्यूरॉन्स में STING1 अभिव्यक्ति में वृद्धि की पुष्टि हुई। STING1 अवरोधक (C176, H151) ने पशु मॉडलों में ऑटोफैजी-निर्भर GPX4 अपघटन को कम किया और न्यूरोप्रोटेक्टिव प्रभाव दिखाया 4)।
अनुसंधान स्तर पर, CD40L अवरोधक frexalimab द्वारा माइक्रोग्लिया और मैक्रोफेज के निष्क्रियीकरण के माध्यम से न्यूरोप्रोटेक्शन 3) और STING1 अवरोध द्वारा फेरोप्टोसिस (लौह-निर्भर कोशिका मृत्यु) का दमन 4) आशाजनक माना जाता है। दोनों वर्तमान में परीक्षण/अनुसंधान चरण में हैं और मानक उपचार नहीं हैं।