RRMS
Thể tái phát-thuyên giảm (Relapsing-Remitting MS): Phân nhóm phổ biến nhất. Các đợt tái phát kéo dài hơn 24 giờ, với sự thuyên giảm hoàn toàn hoặc một phần giữa các đợt.

Đa xơ cứng (Multiple Sclerosis; MS) là bệnh viêm thoái hóa myelin ở chất trắng của hệ thần kinh trung ương (CNS), gây ra các triệu chứng thần kinh đa dạng với các đợt tái phát và thuyên giảm. Đặc trưng bởi các tổn thương xơ cứng do tăng sinh thần kinh đệm, và thường chỉ ảnh hưởng đến CNS mà không tổn thương hệ thần kinh ngoại biên.
Tỷ lệ hiện mắc ước tính tại Mỹ là 1-1,5/1000 người 1). Trên toàn thế giới, 2,1 triệu người mắc bệnh, phân bố nhiều ở các vùng vĩ độ cao của bán cầu Bắc và Nam. Tuổi khởi phát trung bình là 15-45 tuổi, tuổi chẩn đoán trung bình là 30 tuổi. Độ tuổi thường gặp là 15-50 tuổi, nữ nhiều hơn nam (đỉnh ở cuối độ tuổi 20) với tỷ lệ nam:nữ là 1:2,9.
MS có bốn phân nhóm chính. RRMS (Thể tái phát-thuyên giảm) thường khởi phát ở độ tuổi 25–29, trong khi SPMS (Thể tiến triển thứ phát) thường khởi phát ở độ tuổi 40–491).
RRMS
Thể tái phát-thuyên giảm (Relapsing-Remitting MS): Phân nhóm phổ biến nhất. Các đợt tái phát kéo dài hơn 24 giờ, với sự thuyên giảm hoàn toàn hoặc một phần giữa các đợt.
SPMS
Thể tiến triển thứ phát (Secondary Progressive MS): Chuyển từ RRMS. Khuyết tật tích lũy dần dần ngay cả trong giai đoạn thuyên giảm.
PPMS
Thể tiến triển nguyên phát (Primary Progressive MS): Khuyết tật tích lũy dần dần ngay từ đầu. Tiến triển chậm mà không có tái phát.
CIS
Hội chứng cô lập lâm sàng (Clinically Isolated Syndrome): Đợt lâm sàng đầu tiên có thể dẫn đến MS. Cho phép bắt đầu điều trị sớm.
MS được phân loại thành bốn phân nhóm: RRMS (Tái phát-thuyên giảm), SPMS (Tiến triển thứ phát), PPMS (Tiến triển nguyên phát) và CIS (Hội chứng cô lập lâm sàng). Phổ biến nhất là RRMS, với các đợt tái phát và thuyên giảm xen kẽ. SPMS là chuyển tiếp từ RRMS, trong khi PPMS tiến triển ngay từ đầu.
Ở 75% bệnh nhân, triệu chứng khởi phát là một phàn nàn đơn độc, 45% là triệu chứng vận động/cảm giác, 20% là triệu chứng thị giác.
Triệu chứng mắt
Triệu chứng thần kinh toàn thân
Đợt cấp xảy ra cấp tính đến bán cấp và kéo dài từ vài ngày đến vài tháng. 85% trường hợp cải thiện hoặc hết triệu chứng, nhưng 10-15% để lại di chứng.
Thường khởi phát là giảm thị lực đau đớn một bên mắt. Đau hốc mắt gặp ở 92% trường hợp, nặng hơn khi cử động mắt. Hiện tượng Uhthoff (nặng tạm thời khi tăng thân nhiệt như tắm nước nóng, tập thể dục) cũng được quan sát.
Nguyên nhân chính xác của MS chưa rõ, nhưng cơ chế tự miễn được cho là có liên quan đến khởi phát.
Yếu tố di truyền có liên quan, nhưng tỷ lệ tương hợp ở cặp song sinh cùng trứng chỉ là 25-30%. Đa hình HLA và hơn 100 locus nguy cơ đã được xác định, nhưng người ta cho rằng các yếu tố môi trường cùng với yếu tố di truyền đóng vai trò quan trọng trong khởi phát bệnh.
Tiêu chuẩn McDonald 2017 (bản sửa đổi 2024) được sử dụng. Nguyên tắc cơ bản là chứng minh sự đa dạng về thời gian và không gian (DIT/DIS) của các tổn thương mất myelin ở hệ thần kinh trung ương. Trong bản sửa đổi 2024, dây thần kinh thị giác được thêm vào như vị trí giải phẫu thứ năm. Tại Nhật Bản, cũng có tiêu chuẩn chẩn đoán bệnh đa xơ cứng của Bộ Y tế, Lao động và Phúc lợi năm 2015.
Năm vị trí giải phẫu cho sự đa dạng về không gian (DIS) như sau:
Bằng chứng về sự đa ổ theo thời gian (DIT): hai hoặc nhiều đợt tấn công, hoặc sự hiện diện đồng thời của các tổn thương có và không bắt thuốc trên MRI, tổn thương T2 mới, hoặc có thể thay thế bằng dải oligoclonal trong dịch não tủy 1).
Để chẩn đoán PPMS, ngoài tiến triển khuyết tật ≥1 năm, cần có hai hoặc nhiều hơn các dấu hiệu sau: tổn thương T2 não, tổn thương T2 tủy sống (≥2), hoặc dải oligoclonal trong dịch não tủy 1).
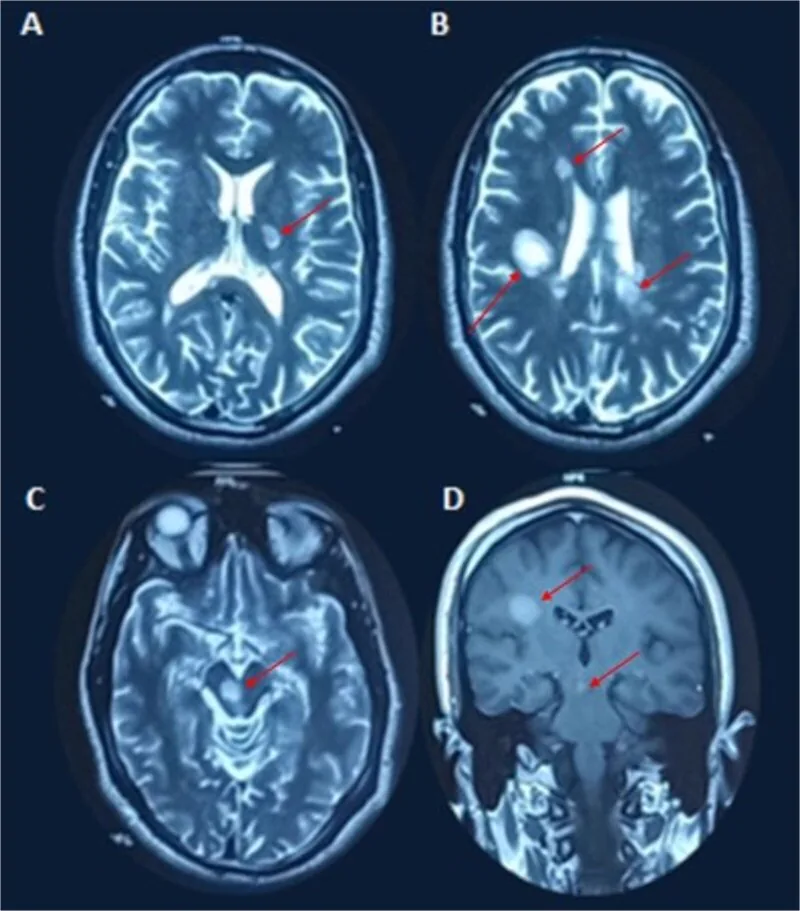
Các mảng mất myelin được phát hiện dưới dạng tổn thương tăng tín hiệu trên T2 hoặc tổn thương bắt thuốc gadolinium.
Hữu ích khi MRI không kết luận được hoặc để dự đoán tiến triển bệnh 1). Có thể phát hiện sự hủy myelin sớm không triệu chứng trước khi thấy trên MRI. 65% trường hợp có kéo dài thời gian tiềm và giảm biên độ.
Cần phân biệt với các bệnh sau, và trong trường hợp không điển hình, tiến hành xét nghiệm bổ sung.
| Nhóm Bệnh | Các Bệnh Cần Phân Biệt Chính |
|---|---|
| Bệnh hủy myelin | NMO (bệnh Devic), ADEM, MOGAD |
| Nhiễm trùng | Sarcoidosis, lao, giang mai, bệnh Lyme |
| Tự miễn | SLE, hội chứng Sjögren, bệnh Behçet |
| Bệnh thần kinh thị giác | NAION, LHON, bệnh thần kinh thị giác do nhiễm độc/chuyển hóa |
Xét nghiệm bổ sung trong trường hợp không điển hình: kháng thể kháng AQP4 (để loại trừ NMO), kháng thể kháng MOG (để loại trừ MOGAD), xét nghiệm NfL huyết thanh, xét nghiệm huyết thanh giang mai (VDRL/RPR/FTA-ABS), ANA (để loại trừ SLE), ACE/lysozyme (để loại trừ sarcoidosis).
Phương pháp điều trị tiêu chuẩn tại Nhật Bản là liệu pháp xung steroid với methylprednisolone 1000 mg/ngày tiêm tĩnh mạch trong 3 ngày liên tiếp. Không dùng prednisolone đường uống sau khi truyền. Không nên thực hiện liệu pháp steroid đường uống vì làm tăng tỷ lệ tái phát.
Ngay cả khi không điều trị, khoảng 80% trường hợp cải thiện thị lực trong vòng 3 tuần kể từ khi khởi phát, nhưng liệu pháp xung giúp rút ngắn thời gian cải thiện. Hơn 90% trường hợp viêm dây thần kinh thị giác có thể phục hồi thị lực.
Nếu liệu pháp xung steroid không hiệu quả, tiến hành liệu pháp thanh lọc máu (trao đổi huyết tương). Ở nước ngoài, sử dụng methylprednisolone 500-1000 mg/ngày trong 3-5 ngày. Trong thử nghiệm điều trị viêm dây thần kinh thị giác (ONTT), methylprednisolone tĩnh mạch liều cao cải thiện thời gian phục hồi chức năng thị giác, độ nhạy tương phản và thị lực màu sắc, nhưng không cải thiện kết quả thị lực cuối cùng.
Sau khi cải thiện mất thị lực và khiếm khuyết thị trường, cần xem xét liệu pháp điều chỉnh bệnh phối hợp với bác sĩ thần kinh để ngăn ngừa tái phát.
Dưới đây là các liệu pháp điều chỉnh bệnh chính và hiệu quả của chúng.
| Thuốc | Cơ chế tác dụng | Đường dùng | Giảm nguy cơ tương đối |
|---|---|---|---|
| Interferon beta | Điều chỉnh hoạt động tế bào T/B và tiết cytokine | Tự tiêm | Tiến triển khuyết tật RR 0,71 |
| Glatiramer acetate | Điều hòa tế bào T điều hòa | Tự tiêm | Tái phát RR 0,82 |
| Natalizumab | Ức chế sự xâm nhập của tế bào viêm vào hệ thần kinh trung ương | Truyền tĩnh mạch | Tái phát RR 0,56 |
| Fingolimod | Điều biến thụ thể S1P | Đường uống | RR tổn thương T2 mới 0,65 |
| Teriflunomide | Ức chế tổng hợp pyrimidine | Đường uống | RR tiến triển tàn tật 0,76 |
| Dimethyl fumarate | Giảm stress oxy hóa và viêm | Đường uống | RR tái phát 0,64 |
| Alemtuzumab | Kháng thể đơn dòng kháng CD52 | Truyền tĩnh mạch | RR tiến triển tàn tật 0,44 |
Các kháng thể đơn dòng kháng CD20 (ocrelizumab, rituximab, ofatumumab) đã trở thành phương pháp điều trị tiêu chuẩn cho MS tái phát 3).
Ngay cả trong viêm dây thần kinh thị giác không có tổn thương não, 25% phát triển MS sau 15 năm, và với tổn thương não, 78% chuyển thành MS.
MS được coi là bệnh tự miễn. Tế bào lympho T nhận diện myelin là vật lạ, kích hoạt đại thực bào, cytokine và kháng thể để phá hủy myelin và sợi trục. Mất myelin làm suy giảm dẫn truyền xung điện, gây rối loạn truyền tín hiệu thần kinh.
Mảng hoạt động
Đại thực bào bọt: Tích tụ các đại thực bào thực bào myelin.
Thâm nhiễm quanh mạch (perivascular cuffing): Tế bào lympho bao quanh mạch máu, dấu hiệu đặc trưng.
Tổn thương khử myelin khu trú phù nề: Xuất hiện trong giai đoạn cấp tính.
Mảng mãn tính
Mất myelin: Có thể xác nhận bằng nhuộm Luxol fast blue. Sợi trục được bảo tồn nhưng quá trình tái tạo myelin không hoàn chỉnh.
Tổn thương NAWM (chất trắng có vẻ bình thường): Tăng sinh thần kinh đệm lan tỏa, hoạt hóa vi đệm và phá vỡ hàng rào máu não ở chất trắng có vẻ bình thường. Tương quan cao hơn với suy giảm lâm sàng so với tổn thương chất trắng khu trú.
Tế bào oligodendrocyte chịu trách nhiệm tái tạo myelin trong hệ thần kinh trung ương 1). Phụ thuộc vào tế bào tiền thân oligodendrocyte trưởng thành (OPC), nhưng các oligodendrocyte trưởng thành hiện có không đóng góp vào quá trình tái tạo myelin 1).
Các nguyên nhân chính của thất bại tái tạo myelin như sau 1).
Ngoài ra, tổn thương chất xám ở vỏ não và dưới vỏ cũng được ghi nhận, và việc hình thành các cấu trúc lympho dạng nang tế bào B ở màng não được biết là dẫn đến diễn tiến lâm sàng nặng hơn1).
Một phương pháp mới ức chế CD40L để chặn sự đồng kích thích giữa tế bào T và tế bào trình diện kháng nguyên (bao gồm tế bào B).
Trong thử nghiệm giai đoạn 2 của Vermersch và cộng sự (N Engl J Med 2024), frexalimab cho thấy hiệu quả rõ rệt so với giả dược trên các kết quả MRI (tổn thương mới bắt gadolinium ở tuần 8-12), và cũng xác nhận sự giảm NfL huyết thanh, một dấu ấn sinh học của tổn thương mô thần kinh3). Đối với MS tiến triển, tác dụng bất hoạt microglia và đại thực bào cũng được kỳ vọng, và về mặt lý thuyết, có thể đạt được bảo vệ thần kinh bằng cách chặn tín hiệu CD40L trên microglia ở rìa mảng3).
Việc thiết lập ưu thế lâm sàng so với các DMT hiệu quả cao hiện tại (kháng CD20) được coi là thách thức trong tương lai3).
Ferroptosis, một dạng chết tế bào phụ thuộc sắt, đã được chứng minh có liên quan đến chết tế bào thần kinh trong MS.
Tang et al. (2025) đã giải thích nghiên cứu của Woo et al. (Cell, 2024) và báo cáo dòng thác: độc tính kích thích glutamate → quá tải canxi → stress lưới nội chất → STING1 tách khỏi STIM1 → kích hoạt con đường không điển hình → tự thực → phân giải GPX4 (enzyme trung hòa peroxid hóa lipid) qua tự thực → ferroptosis 4). Sự gia tăng biểu hiện STING1 ở tế bào thần kinh đã được xác nhận trên cả mẫu MS người và mô hình chuột. Các chất ức chế STING1 (C176, H151) làm giảm phân giải GPX4 phụ thuộc tự thực và cho thấy tác dụng bảo vệ thần kinh trên mô hình động vật 4).
Ở giai đoạn nghiên cứu, bảo vệ thần kinh thông qua bất hoạt microglia và đại thực bào bởi thuốc ức chế CD40L frexalimab 3) và ức chế ferroptosis (chết tế bào phụ thuộc sắt) bằng ức chế STING1 4) được xem là triển vọng. Cả hai hiện đang trong giai đoạn thử nghiệm lâm sàng và nghiên cứu, chưa phải là điều trị tiêu chuẩn.