RRMS
Relapsing-Remitting MS (Ataklı-Düzelmeli MS): En sık görülen alt tip. Ataklar 24 saatten uzun sürer ve ataklar arasında tam veya kısmi düzelme görülür.

Multipl skleroz (MS), merkezi sinir sistemi (MSS) beyaz cevherinde inflamatuar demiyelinizan lezyonların oluştuğu ve çeşitli nörolojik semptomların atak ve remisyonlarla tekrarladığı bir hastalıktır. Gliyozise bağlı skar dokusu ile karakterizedir ve genellikle sadece MSS etkilenir, periferik sinir sistemi zarar görmez.
ABD’de tahmini prevalans 1000 kişide 1-1.5’tir1). Dünya genelinde 2.1 milyon kişi etkilenmiştir ve kuzey ve güney yarımkürenin yüksek enlem bölgelerinde daha sık görülür. Ortalama başlangıç yaşı 15-45, tanı anında ortalama yaş 30’dur. Sık görülen yaş aralığı 15-50’dir ve kadınlarda (20’li yaşların sonunda pik) daha sıktır; kadın/erkek oranı 1:2.9’dur.
MS’in dört ana alt tipi vardır. RRMS (Relapsing-Remitting) genellikle 25-29 yaşlarında, SPMS ise 40-49 yaşlarında başlar1).
RRMS
Relapsing-Remitting MS (Ataklı-Düzelmeli MS): En sık görülen alt tip. Ataklar 24 saatten uzun sürer ve ataklar arasında tam veya kısmi düzelme görülür.
SPMS
Sekonder Progresif MS (İkincil İlerleyici MS): RRMS’den geçiş yapar. Düzelme döneminde bile ilerleyici özürlülük birikir.
PPMS
Primer Progresif MS (Birincil İlerleyici MS): Başlangıçtan itibaren ilerleyici özürlülük birikir. Atak olmaksızın yavaş ilerler.
CIS
Klinik İzole Sendrom (Clinically Isolated Syndrome): MS’e dönüşebilecek ilk klinik epizod. Erken tedavi başlanmasını sağlar.
MS, RRMS (Ataklı-Düzelmeli), SPMS (Sekonder Progresif), PPMS (Primer Progresif) ve CIS (Klinik İzole Sendrom) olmak üzere dört alt tipe ayrılır. En sık görüleni RRMS’dir ve ataklar ve düzelmelerle seyreder. SPMS, RRMS’den geçiş yapar; PPMS ise başlangıçtan itibaren ilerleyici özürlülük biriktirir.
Hastaların %75’inde ilk semptom tek bir şikayettir; %45’i motor/duyusal semptomlar, %20’si görsel semptomlar olarak ortaya çıkar.
Göz semptomları
Genel nörolojik semptomlar
Alevlenme akut ila subakut başlangıçlı olup birkaç gün ila birkaç ay sürer. %85’inde semptomlar düzelir veya kaybolur, ancak %10-15’inde sekel kalır.
Sıklıkla tek taraflı ağrılı görme azalması olarak başlar. Orbital ağrı %92’sinde bulunur ve göz hareketleriyle kötüleşir. Ayrıca vücut ısısının yükselmesiyle (banyo, egzersiz) semptomların geçici olarak kötüleştiği Uhthoff fenomeni de görülür.
MS’in kesin nedeni bilinmemekle birlikte, otoimmün mekanizmaların hastalığın başlangıcında rol oynadığı düşünülmektedir.
Genetik faktörler rol oynar, ancak tek yumurta ikizlerinde uyum oranı yalnızca %25-30’dur. HLA polimorfizmi ve 100’den fazla risk lokusu tanımlanmıştır, ancak genetik yatkınlığın yanı sıra çevresel faktörlerin de hastalığın başlamasında önemli rol oynadığı düşünülmektedir.
2017 McDonald kriterleri (2024 revizyonu) kullanılır. Santral sinir sistemindeki demiyelinizan lezyonların zamansal ve mekansal yayılımının (DIT/DIS) kanıtlanması esastır. 2024 revizyonunda optik sinir beşinci anatomik bölge olarak eklenmiştir. Japonya’da ayrıca 2015 Sağlık, Çalışma ve Refah Bakanlığı multipl skleroz tanı kriterleri de bulunmaktadır.
Mekansal yayılım (DIS) için beş anatomik bölge şunlardır:
Zamansal yayılımın (DIT) kanıtı: İki veya daha fazla atak, MRG’de kontrastlanan ve kontrastlanmayan lezyonların eşzamanlı varlığı, yeni T2 lezyonları veya BOS’ta oligoklonal bant ile ikame edilebilir 1).
PPMS tanısı için, en az bir yıllık özürlülük ilerlemesine ek olarak, aşağıdakilerden en az ikisinin bulunması gerekir: beyin T2 lezyonları, spinal T2 lezyonları (iki veya daha fazla) veya BOS’ta oligoklonal bant 1).
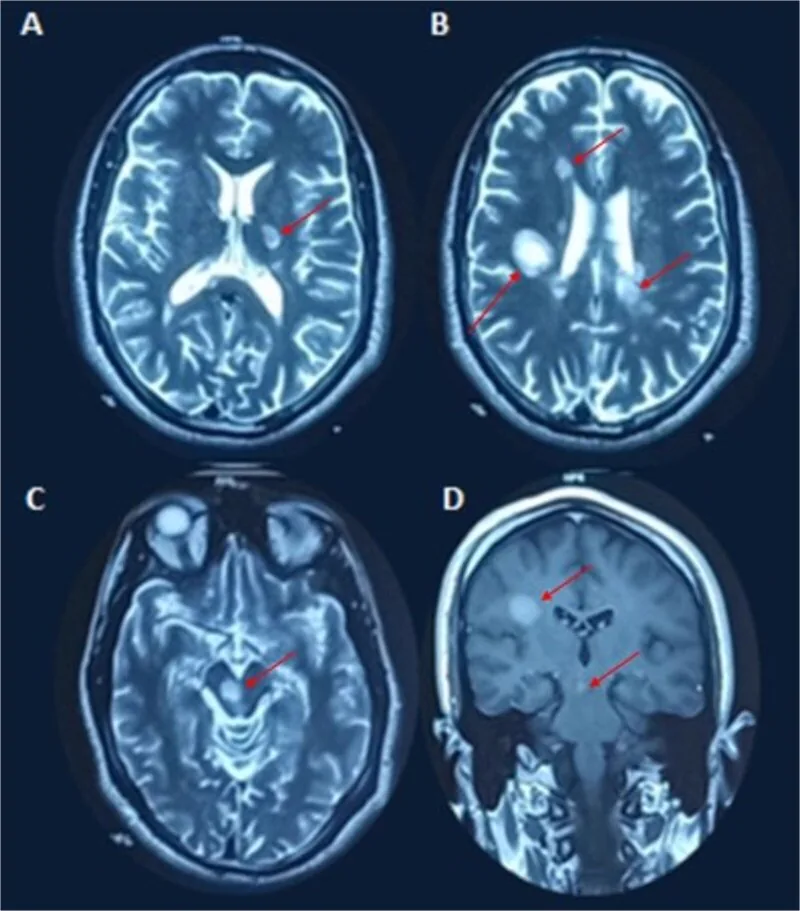
Demiyelinizan plaklar, T2 hiperintens lezyonlar veya gadolinyum tutan lezyonlar olarak saptanır.
MRI’nın kesin olmadığı durumlarda veya hastalık ilerlemesini tahmin etmede faydalıdır 1). Erken ve asemptomatik demiyelinizasyonu MRI’da görünür hale gelmeden önce tespit edebilir. %65 oranında gecikme uzaması ve amplitüd azalması görülür.
Aşağıdaki hastalıklarla ayırıcı tanı önemlidir ve atipik vakalarda ek testler yapılır.
| Hastalık kategorisi | Başlıca ayırıcı tanılar |
|---|---|
| Demiyelinizan hastalıklar | NMO (Devic hastalığı), ADEM, MOGAD |
| Enfeksiyöz | Sarkoidoz, tüberküloz, sifiliz, Lyme hastalığı |
| Otoimmün | SLE, Sjögren sendromu, Behçet hastalığı |
| Optik sinir hastalıkları | NAION, LHON, toksik/metabolik optik nöropati |
Atipik vakalarda ek testler: Anti-AQP4 antikoru (NMO’yu dışlamak için), anti-MOG antikoru (MOGAD’ı dışlamak için), serum NfL testi, sifiliz serolojisi (VDRL/RPR/FTA-ABS), ANA (SLE için), ACE ve lizozim (sarkoidoz için).
Japonya’da standart tedavi, 3 gün boyunca günde 1000 mg metilprednizolon intravenöz infüzyonu ile steroid pulse tedavisidir. 3 günlük infüzyondan sonra oral prednizolon (idame tedavisi) uygulanmaz. Oral steroid tedavisinin nüks oranını artırdığı düşünülür ve uygulanmamalıdır.
Tedavisiz bile, vakaların yaklaşık %80’inde başlangıçtan itibaren 3 hafta içinde görme iyileşmesi başlar, ancak pulse tedavisi iyileşme süresini kısaltır. Optik nörit vakalarının %90’ından fazlasında görme geri kazanımı beklenebilir.
Steroid pulse tedavisine yanıt alınamazsa plazmaferez (plazma değişimi) uygulanır. Yurtdışında metilprednizolon 500-1000 mg/gün, 3-5 gün süreyle kullanılır. Optik Nörit Tedavi Çalışması’nda (ONTT), yüksek doz intravenöz metilprednizolon görme fonksiyonu, kontrast duyarlılığı ve renk görme iyileşme süresini iyileştirmiş ancak nihai görme prognozunda iyileşme göstermemiştir.
Görme azalması ve görme alanı defektinin iyileşmesinden sonra, nüksü önlemek için nöroloji uzmanı ile işbirliği içinde DMT düşünülür.
Başlıca DMT’ler ve etkinlikleri aşağıda gösterilmiştir.
| İlaç | Etki mekanizması | Uygulama yolu | Göreceli risk azalması |
|---|---|---|---|
| İnterferon beta | T/B hücre aktivitesi ve sitokin salınımının düzenlenmesi | Kendi kendine enjeksiyon | Özürlülük ilerlemesi RR 0.71 |
| Glatiramer asetat | Düzenleyici T hücrelerinin modülasyonu | Kendi kendine enjeksiyon | Nüks RR 0.82 |
| Natalizumab | İnflamatuar hücrelerin CNS’e girişinin inhibisyonu | İntravenöz infüzyon | Nüks RR 0.56 |
| Fingolimod | S1P reseptör modülasyonu | Oral | Yeni T2 lezyon RR 0.65 |
| Teriflunomid | Pirimidin sentezi inhibisyonu | Oral | Engellilik ilerlemesi RR 0.76 |
| Dimetil fumarat | Oksidatif stres ve inflamasyonu azaltma | Oral | Nüks RR 0.64 |
| Alemtuzumab | Anti-CD52 monoklonal antikor | İnfüzyon | Engellilik ilerlemesi RR 0.44 |
Anti-CD20 monoklonal antikorlar (okrelizumab, rituksimab, ofatumumab) tekrarlayan MS için standart tedavi haline gelmiştir 3).
Beyin lezyonu olmayan optik nöritte bile 15 yıl sonra %25’inde MS gelişirken, beyin lezyonu varlığında %78’inde MS’e dönüşüm görülür.
Beyin MRG’sinde lezyon olmasa bile 15 yıl sonra %25’inde MS gelişir, beyin lezyonu varsa %78’inde MS’e dönüşüm görülür. Optik nörit geçiren hastalar, nöroloji ile işbirliği içinde nüks önleme için DMT uygunluğu açısından değerlendirilmelidir.
MS otoimmün bir hastalık olarak kabul edilir. T lenfositleri miyelin yabancı bir madde olarak tanır ve makrofajları, sitokinleri ve antikorları aktive ederek miyelin ve aksonları tahrip eder. Miyelin kaybı, elektriksel impulsların iletimini bozarak sinir sinyal iletimini engeller.
Aktif plak
Köpüksü makrofajlar: Miyelini fagosite etmiş makrofajların birikimi.
Perivasküler kılıflanma (perivascular cuffing): Lenfositlerin damar çevresini sarması karakteristik bir bulgudur.
Ödemli sınırlı demiyelinizan lezyonlar: Akut atak döneminde görülür.
Kronik plak
Miyelin kaybı: Luxol fast blue boyaması ile doğrulanabilir. Aksonlar korunur ancak remiyelinizasyon yetersizdir.
NAWM lezyonları: Normal görünen beyaz cevherde yaygın gliozis, mikroglial aktivasyon ve BBB yıkımı. Sınırlı beyaz cevher lezyonlarına göre klinik engellilik ile daha yüksek korelasyon gösterir.
Oligodendrositler, CNS’de remiyelinizasyondan sorumludur1). Bu süreç, yetişkin oligodendrosit öncü hücrelerine (OPC) bağımlıdır, ancak mevcut olgun oligodendrositler remiyelinizasyona katkıda bulunamaz1).
Remiyelinizasyon başarısızlığının başlıca nedenleri şunlardır1).
Ayrıca, kortikal ve subkortikal gri madde hasarı da gözlenir ve meninkslerde B hücreli folikül benzeri lenfoid yapılar oluştuğunda daha şiddetli bir klinik seyir ortaya çıktığı bilinmektedir 1).
CD40L’yi inhibe ederek T hücreleri ve antijen sunan hücreler (B hücreleri dahil) arasındaki kostimülasyonu bloke eden yeni bir yaklaşımdır.
Vermersch ve ark. (N Engl J Med 2024) tarafından yapılan faz 2 çalışmasında, frexalimab MRI sonuçlarında (8-12. haftalarda yeni gadolinyum tutan lezyonlar) plaseboya karşı net bir etkinlik göstermiş ve nöral doku hasarının biyobelirteci olan serum NfL’de azalma da doğrulanmıştır 3). Progresif MS için mikroglia/makrofaj inaktivasyonu etkisi de beklenmekte olup, plak kenarındaki mikroglialara CD40L sinyalinin bloke edilmesiyle nöroproteksiyon teorik olarak mümkün kabul edilmektedir 3).
Mevcut yüksek etkili DMT’lere (anti-CD20 ilaçları) karşı klinik üstünlüğün kanıtlanması gelecekteki bir zorluk olarak değerlendirilmektedir 3).
Demire bağımlı bir hücre ölümü olan ferroptozun, MS’te nöron ölümünde rol oynadığı gösterilmiştir.
Tang ve ark. (2025), Woo ve ark. (Cell, 2024) çalışmasını yorumlayarak şu kaskadı rapor etmiştir: glutamat eksitotoksisitesi → kalsiyum aşırı yüklenmesi → endoplazmik retikulum stresi → STING1’in STIM1’den ayrışması → atipik yolak aktivasyonu → otofaji → GPX4’ün (lipid peroksidasyonunu nötralize eden enzim) otofajik degradasyonu → ferroptoz 4). Hem insan MS örneklerinde hem de fare modellerinde nöronlarda STING1 ekspresyonunda artış doğrulanmıştır. STING1 inhibitörleri (C176, H151), hayvan modellerinde otofaji bağımlı GPX4 degradasyonunu azaltmış ve nöroprotektif etki göstermiştir 4).
Araştırma aşamasında, CD40L inhibitörü frexalimab ile mikroglia ve makrofaj inaktivasyonu yoluyla nöroproteksiyon 3) ve STING1 inhibisyonu ile ferroptozun (demir bağımlı hücre ölümü) baskılanması 4) umut verici görünmektedir. Her ikisi de şu anda klinik deney/araştırma aşamasındadır ve standart tedavi değildir.