RRMS
Relapsing-Remitting MS (RRMS): Subtipe paling umum. Kekambuhan berlangsung lebih dari 24 jam, dengan remisi lengkap atau sebagian di antara serangan.

Sklerosis multipel (MS) adalah penyakit demielinasi inflamasi pada substansia alba sistem saraf pusat (SSP) yang menyebabkan berbagai gejala neurologis dengan serangan berulang dan remisi. Ditandai dengan lesi sklerotik akibat gliosis, dan biasanya hanya menyerang SSP tanpa melibatkan sistem saraf perifer.
Perkiraan prevalensi di AS adalah 1-1,5 per 1000 orang 1). Di seluruh dunia, 2,1 juta orang menderita MS, dengan distribusi lebih banyak di daerah lintang tinggi belahan bumi utara dan selatan. Usia rata-rata onset adalah 15-45 tahun, dan usia rata-rata diagnosis adalah 30 tahun. Usia tersering adalah 15-50 tahun, lebih sering pada wanita (puncak akhir usia 20-an) dengan rasio pria:wanita 1:2,9.
MS memiliki empat subtipe utama. RRMS (Relapsing-Remitting) biasanya muncul pada usia 25–29 tahun, sedangkan SPMS sering muncul pada usia 40–49 tahun1).
RRMS
Relapsing-Remitting MS (RRMS): Subtipe paling umum. Kekambuhan berlangsung lebih dari 24 jam, dengan remisi lengkap atau sebagian di antara serangan.
SPMS
Secondary Progressive MS (SPMS): Transisi dari RRMS. Disabilitas berkembang secara progresif bahkan selama remisi.
PPMS
Primary Progressive MS (PPMS): Disabilitas berkembang secara progresif sejak awal. Berlangsung lambat tanpa kekambuhan.
CIS
Clinically Isolated Syndrome (CIS): Episode klinis pertama yang dapat menjadi MS. Memungkinkan inisiasi pengobatan dini.
MS diklasifikasikan menjadi empat subtipe: RRMS (Relapsing-Remitting), SPMS (Secondary Progressive), PPMS (Primary Progressive), dan CIS (Clinically Isolated Syndrome). Yang paling umum adalah RRMS, dengan kekambuhan dan remisi yang bergantian. SPMS adalah transisi dari RRMS, sedangkan PPMS berkembang progresif sejak awal.
Pada 75% pasien, gejala awal adalah keluhan tunggal, 45% berupa gejala motorik/sensorik, dan 20% berupa gejala visual.
Gejala Mata
Gejala Neurologis Sistemik
Eksaserbasi terjadi akut hingga subakut dan berlangsung selama beberapa hari hingga beberapa bulan. Pada 85% kasus, gejala membaik atau hilang, tetapi pada 10-15% terdapat gejala sisa.
Sering dimulai sebagai penurunan penglihatan nyeri pada satu mata. Nyeri orbita ditemukan pada 92% kasus, memburuk dengan gerakan mata. Fenomena Uhthoff (perburukan sementara dengan peningkatan suhu tubuh, seperti mandi atau olahraga) juga diamati.
Penyebab pasti MS tidak diketahui, tetapi mekanisme autoimun diduga berperan dalam onsetnya.
Faktor genetik berperan, namun tingkat konkordansi pada kembar identik hanya 25-30%. Polimorfisme HLA dan lebih dari 100 lokus risiko telah diidentifikasi, tetapi diyakini bahwa faktor lingkungan selain predisposisi genetik juga memainkan peran penting dalam timbulnya penyakit.
Kriteria McDonald 2017 (revisi 2024) digunakan. Dasarnya adalah membuktikan penyebaran lesi demielinasi di sistem saraf pusat dalam waktu dan ruang (DIT/DIS). Dalam revisi 2024, saraf optik ditambahkan sebagai lokasi anatomis kelima. Di Jepang, juga terdapat kriteria diagnosis multiple sclerosis dari Kementerian Kesehatan, Tenaga Kerja, dan Kesejahteraan tahun 2015.
Lima lokasi anatomis untuk penyebaran dalam ruang (DIS) adalah sebagai berikut:
Bukti diseminasi temporal (DIT): dua atau lebih serangan, atau adanya lesi yang diperkuat dan tidak diperkuat secara bersamaan pada MRI, lesi T2 baru, atau dapat digantikan oleh pita oligoklonal CSF 1).
Untuk diagnosis PPMS, selain perkembangan disabilitas selama ≥1 tahun, diperlukan dua atau lebih temuan berikut: lesi T2 otak, lesi T2 medula spinalis (≥2), atau pita oligoklonal CSF 1).
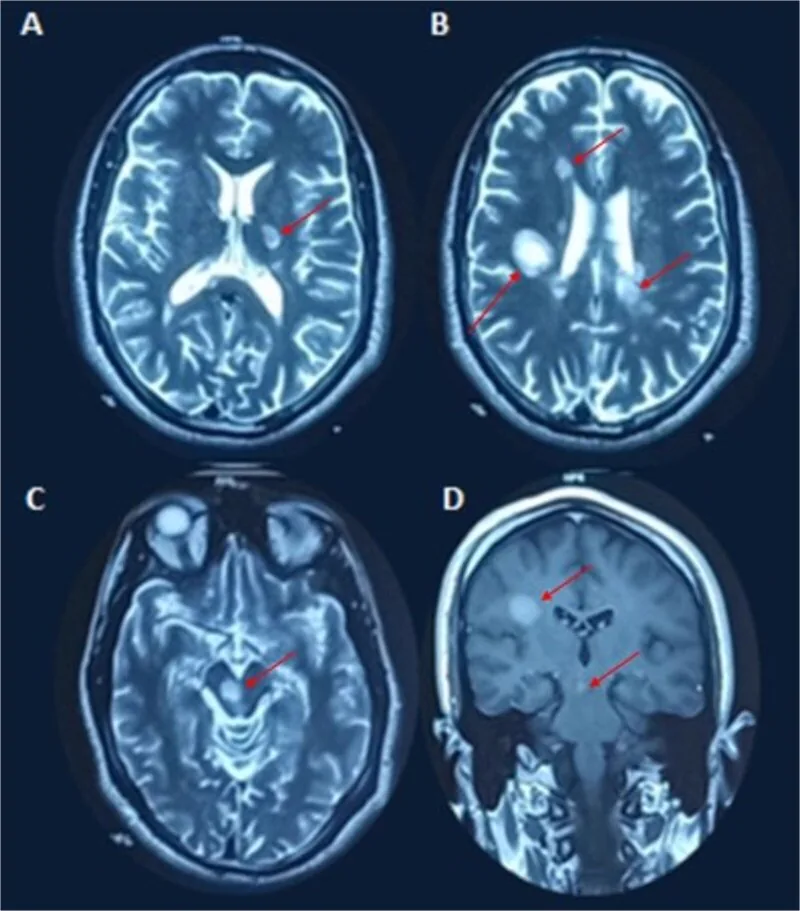
Plak demielinasi terdeteksi sebagai lesi hiperintens T2 atau lesi yang diperkuat gadolinium.
Berguna jika MRI tidak meyakinkan atau untuk memprediksi perkembangan penyakit 1). Dapat mendeteksi demielinasi dini asimtomatik sebelum terlihat pada MRI. Pada 65% kasus, ditemukan perpanjangan latensi dan penurunan amplitudo.
Penting untuk membedakan dari penyakit berikut, dan pada kasus atipikal dilakukan pemeriksaan tambahan.
| Kategori Penyakit | Penyakit Banding Utama |
|---|---|
| Penyakit Demielinasi | NMO (penyakit Devic), ADEM, MOGAD |
| Infeksi | Sarkoidosis, tuberkulosis, sifilis, penyakit Lyme |
| Autoimun | SLE, sindrom Sjögren, penyakit Behçet |
| Penyakit saraf optik | NAION, LHON, neuropati optik toksik/metabolik |
Pemeriksaan tambahan pada kasus atipikal: antibodi anti-AQP4 (untuk menyingkirkan NMO), antibodi anti-MOG (untuk menyingkirkan MOGAD), pemeriksaan NfL serum, tes serologi sifilis (VDRL/RPR/FTA-ABS), ANA (untuk SLE), ACE/lysozyme (untuk sarkoidosis).
Pengobatan standar di Jepang adalah terapi steroid pulsa dengan metilprednisolon 1000 mg/hari intravena selama 3 hari berturut-turut. Tidak diberikan prednisolon oral setelah infus. Terapi steroid oral tidak boleh dilakukan karena meningkatkan angka kekambuhan.
Bahkan tanpa pengobatan, perbaikan penglihatan dimulai pada sekitar 80% kasus dalam 3 minggu setelah onset, tetapi terapi pulsa memperpendek periode perbaikan. Pemulihan penglihatan diharapkan pada lebih dari 90% kasus neuritis optik.
Jika terapi steroid pulsa tidak efektif, dilakukan terapi pemurnian darah (tukar plasma). Di luar negeri, digunakan metilprednisolon 500-1000 mg/hari selama 3-5 hari. Dalam uji coba pengobatan neuritis optik (ONTT), metilprednisolon intravena dosis tinggi memperbaiki waktu pemulihan fungsi visual, sensitivitas kontras, dan penglihatan warna, tetapi tidak menunjukkan perbaikan dalam hasil visual akhir.
Setelah perbaikan kehilangan penglihatan dan defek lapang pandang, terapi modifikasi penyakit harus dipertimbangkan bekerja sama dengan dokter saraf untuk mencegah kekambuhan.
Berikut adalah terapi modifikasi penyakit utama dan efektivitasnya.
| Obat | Mekanisme kerja | Cara pemberian | Penurunan risiko relatif |
|---|---|---|---|
| Interferon beta | Modulasi aktivitas sel T/B dan sekresi sitokin | Suntik sendiri | Perkembangan kecacatan RR 0.71 |
| Glatiramer asetat | Regulasi sel T regulator | Suntik sendiri | Kekambuhan RR 0.82 |
| Natalizumab | Penghambatan masuknya sel inflamasi ke SSP | Infus | Kekambuhan RR 0.56 |
| Fingolimod | Modulator reseptor S1P | Oral | RR lesi T2 baru 0.65 |
| Teriflunomide | Inhibisi sintesis pirimidin | Oral | RR progresi disabilitas 0.76 |
| Dimetil fumarat | Mengurangi stres oksidatif dan inflamasi | Oral | RR kekambuhan 0.64 |
| Alemtuzumab | Antibodi monoklonal anti-CD52 | Infus | RR progresi disabilitas 0.44 |
Antibodi monoklonal anti-CD20 (ocrelizumab, rituximab, ofatumumab) telah menjadi terapi standar untuk MS relaps 3).
Bahkan pada neuritis optik tanpa lesi otak, 25% berkembang menjadi MS setelah 15 tahun, dan dengan lesi otak, 78% beralih ke MS.
Bahkan tanpa lesi pada MRI otak, 25% berkembang menjadi MS setelah 15 tahun, dan dengan lesi otak, 78% beralih ke MS. Pasien dengan neuritis optik harus mempertimbangkan penggunaan DMT untuk pencegahan kekambuhan dengan bekerja sama dengan dokter saraf.
MS dianggap sebagai penyakit autoimun. Limfosit T mengenali mielin sebagai benda asing, mengaktifkan makrofag, sitokin, dan antibodi untuk menghancurkan mielin dan akson. Hilangnya mielin mengganggu konduksi impuls listrik, sehingga transmisi sinyal saraf terganggu.
Plak aktif
Makrofag berbusa: Akumulasi makrofag yang memfagosit mielin.
Infiltrasi perivaskular (perivascular cuffing): Limfosit mengelilingi pembuluh darah, temuan khas.
Lesi demielinasi fokal edematosa: Terlihat selama fase eksaserbasi akut.
Plak kronis
Hilangnya mielin: Dapat dikonfirmasi dengan pewarnaan Luxol fast blue. Akson dipertahankan tetapi remielinasi tidak sempurna.
Lesi NAWM (Normal-Appearing White Matter): Gliosis difus, aktivasi mikroglia, dan kerusakan sawar darah-otak pada materi putih yang tampak normal. Berkorelasi lebih tinggi dengan gangguan klinis dibandingkan lesi materi putih fokal.
Oligodendrosit bertanggung jawab untuk remielinasi SSP 1). Bergantung pada sel prekursor oligodendrosit dewasa (OPC), tetapi oligodendrosit matang yang sudah ada tidak berkontribusi pada remielinasi 1).
Penyebab utama kegagalan remielinasi adalah sebagai berikut 1).
Selain itu, kerusakan materi abu-abu di korteks dan subkorteks juga diamati, dan diketahui bahwa pembentukan struktur limfoid mirip folikel sel B di meningen menyebabkan perjalanan klinis yang lebih parah1).
Pendekatan baru yang menghambat CD40L untuk memblokir kostimulasi antara sel T dan sel penyaji antigen (termasuk sel B).
Dalam uji coba fase 2 oleh Vermersch dkk. (N Engl J Med 2024), frexalimab menunjukkan efektivitas yang jelas dibandingkan plasebo pada hasil MRI (lesi baru yang diperkuat gadolinium pada minggu ke-8 hingga ke-12), dan penurunan NfL serum, biomarker kerusakan jaringan saraf, juga dikonfirmasi3). Untuk MS progresif, efek inaktivasi mikroglia dan makrofag juga diharapkan, dan secara teoritis, perlindungan saraf dapat dicapai dengan memblokir sinyal CD40L pada mikroglia di tepi plak3).
Penetapan keunggulan klinis dibandingkan DMT efektivitas tinggi saat ini (anti-CD20) dianggap sebagai tantangan di masa depan3).
Telah ditunjukkan bahwa feroptosis, kematian sel yang bergantung pada besi, terlibat dalam kematian neuron pada MS.
Tang et al. (2025) menjelaskan penelitian Woo et al. (Cell, 2024) dan melaporkan kaskade: eksitotoksisitas glutamat → kelebihan kalsium → stres retikulum endoplasma → STING1 terlepas dari STIM1 → aktivasi jalur non-kanonik → autophagy → degradasi GPX4 (enzim penetral peroksidasi lipid) melalui autophagy → ferroptosis 4). Peningkatan ekspresi STING1 pada neuron dikonfirmasi baik pada sampel MS manusia maupun model tikus. Inhibitor STING1 (C176, H151) mengurangi degradasi GPX4 yang bergantung pada autophagy dan menunjukkan efek neuroprotektif pada model hewan 4).
Pada tahap penelitian, neuroproteksi melalui inaktivasi mikroglia dan makrofag oleh inhibitor CD40L frexalimab 3) dan penghambatan ferroptosis (kematian sel tergantung besi) melalui inhibisi STING1 4) dipandang menjanjikan. Keduanya saat ini masih dalam tahap uji klinis dan penelitian, bukan terapi standar.