RRMS
재발 완화형 MS: 가장 흔한 아형입니다. 재발이 24시간 이상 지속되며, 발작 사이에 완전 또는 부분적인 완화가 나타납니다.

다발성 경화증(Multiple Sclerosis; MS)은 중추신경계(CNS) 백질에 염증성 탈수초 병변이 발생하여 다양한 신경 증상이 재발과 관해를 반복하는 질환입니다. 신경교증으로 인한 반흔 경화성 병변이 특징이며, 일반적으로 중추신경만 침범하고 말초신경계는 손상되지 않습니다.
미국에서의 추정 유병률은 11.5/1,000명입니다1). 전 세계적으로 210만 명이 이환되어 있으며, 북반구와 남반구의 고위도 지역에 많이 분포합니다. 발병 평균 연령은 1545세이고, 진단 시 평균 연령은 30세입니다. 호발 연령은 15~50세이며 여성(20대 후반이 피크)에 많고, 남녀 비는 1:2.9입니다.
MS에는 다음과 같은 4가지 주요 아형이 있습니다. RRMS(재발 완화형)는 2529세에 발병하고, SPMS는 4049세에 발병하는 경우가 많습니다1).
RRMS
재발 완화형 MS: 가장 흔한 아형입니다. 재발이 24시간 이상 지속되며, 발작 사이에 완전 또는 부분적인 완화가 나타납니다.
SPMS
이차 진행형 MS: RRMS에서 전환됩니다. 완화기에도 진행성으로 장애가 축적됩니다.
PPMS
일차 진행형 MS: 발병 초기부터 진행성으로 장애가 축적됩니다. 재발 없이 서서히 진행됩니다.
CIS
임상적 고립 증후군: MS가 될 수 있는 첫 임상 에피소드입니다. 조기 치료 시작을 가능하게 합니다.
환자의 75%에서 초발 증상은 단일 호소이며, 45%는 운동/감각 증상, 20%는 시각 증상으로 발현됩니다.
안구 증상
전신 신경 증상
악화는 급성아급성으로 발병하여 수일수개월 지속됩니다. 85%에서 증상이 호전·소실되지만, 10~15%에서는 후유증이 남습니다.
단안성 통증을 동반한 시력 저하로 발병하는 경우가 많습니다. 안와통은 92%에서 나타나며, 안구 운동 시 악화되는 것이 특징입니다. 또한, 체온 상승(목욕·운동)으로 증상이 일시적으로 악화되는 Uhthoff 현상도 나타납니다.
MS의 정확한 원인은 알려져 있지 않지만, 자가면역 기전이 발병에 관여하는 것으로 생각됩니다.
유전적 요인이 관여하지만, 일란성 쌍둥이에서도 일치율은 25~30%에 불과합니다. HLA 다형성 및 100개 이상의 위험 유전자좌가 확인되었지만, 유전적 소인뿐만 아니라 환경 요인도 발병에 중요한 역할을 하는 것으로 생각됩니다.
2017년 McDonald 기준(2024년 개정판)이 사용됩니다. 중추신경계의 탈수초 병변의 시간적 및 공간적 다발성(DIT/DIS)을 증명하는 것이 기본입니다. 2024년 개정에서는 시신경이 다섯 번째 지형적 부위로 추가되었습니다. 일본에서는 2015년 후생노동성의 다발성 경화증 진단 기준도 있습니다.
공간적 다발성(DIS)의 다섯 가지 지형적 부위는 다음과 같습니다.
시간적 다발성(DIT)의 증명: 2회 이상의 발작, 또는 MRI에서 조영증강 및 비조영증강 병변의 동시 존재, 새로운 T2 병변, CSF 올리고클론 밴드로 대체 가능 1).
PPMS 진단에는 1년 이상의 장애 진행 외에도 뇌 T2 병변, 척수 T2 병변(2개 이상), CSF 올리고클론 밴드 중 2개 이상의 소견이 필요합니다 1).
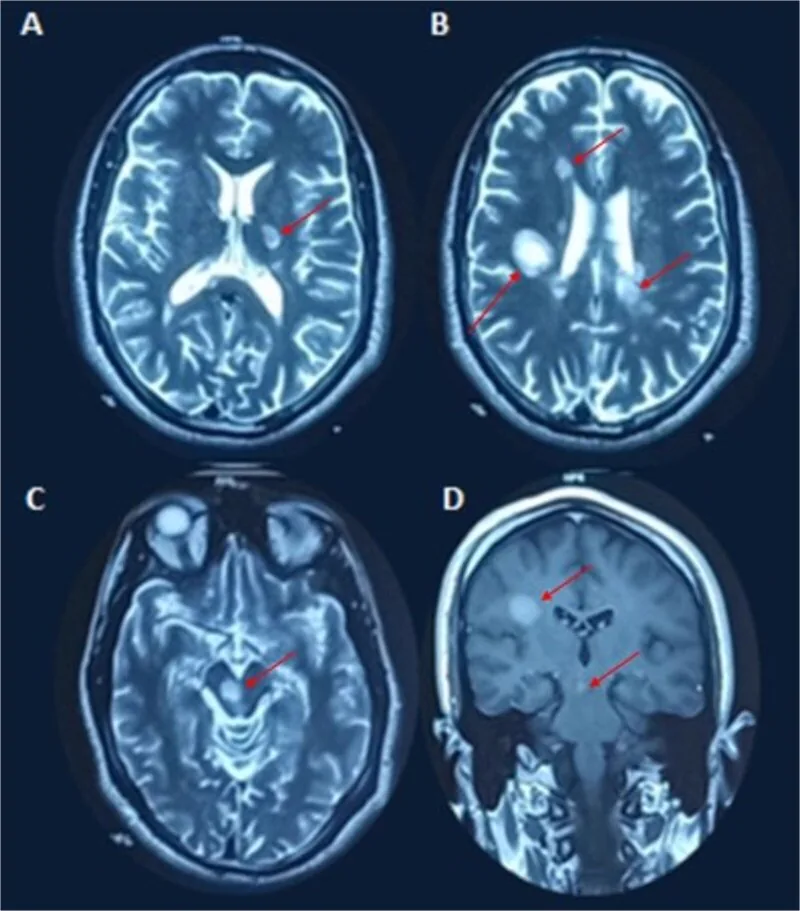
탈수초 플라크는 T2 고신호 병변 또는 가돌리늄 조영증강 병변으로 검출됩니다.
MRI가 불확실하거나 질병 진행 예측에 유용합니다1). MRI 가시화 전에 조기, 무증상 탈수초를 검출할 수 있습니다. 65%에서 잠복기 연장 및 진폭 감소가 인정됩니다.
다음 질환과의 감별이 중요하며, 비전형적인 경우 추가 검사를 시행합니다.
| 질환 범주 | 주요 감별 질환 |
|---|---|
| 탈수초 질환 | NMO(데빅병), ADEM, MOGAD |
| 감염성 | 유육종증, 결핵, 매독, 라임병 |
| 자가면역 | SLE, 쇼그렌 증후군, 베체트병 |
| 시신경 질환 | NAION, LHON, 중독성/대사성 시신경병증 |
비전형적 사례의 추가 검사: 항AQP4 항체(NMO 배제), 항MOG 항체(MOGAD 배제), 혈청 NfL 검사, 매독 혈청 검사(VDRL/RPR/FTA-ABS), ANA(SLE), ACE/리소자임(유육종증).
일본의 표준 치료는 메틸프레드니솔론 1,000mg/일을 3일 연속 정맥 주입하는 스테로이드 펄스 요법입니다. 3일 주입 후 프레드니솔론 경구 투여(후속 요법)는 시행하지 않습니다. 경구 스테로이드 요법은 재발률을 높이는 것으로 알려져 있으므로 시행해서는 안 됩니다.
치료를 하지 않아도 발병 후 3주 이내에 약 80%에서 시력 개선이 시작되지만, 펄스 요법으로 회복 기간이 단축됩니다. 시신경염의 90% 이상에서 시력 회복이 기대됩니다.
스테로이드 펄스 요법이 효과가 없는 경우 혈액 정화 요법(혈장 교환)을 시행합니다. 해외에서는 메틸프레드니솔론 5001,000mg/일을 35일간 사용합니다. 시신경염 치료 시험(ONTT)에서 고용량 메틸프레드니솔론 정맥 주사는 시기능, 대비 감도, 색각의 회복 시간을 개선했지만 최종 시력 예후의 개선은 입증되지 않았습니다.
시력 저하 및 시야 장애가 개선된 후에는 재발 예방을 위해 신경과 의사와 협력하여 DMT를 고려합니다.
주요 DMT와 그 유효성은 아래와 같습니다.
| 약물 | 작용 기전 | 투여 방법 | 상대 위험 감소 |
|---|---|---|---|
| 인터페론 베타 | T/B 세포 활성 및 사이토카인 분비 조절 | 자가 주사 | 장애 진행 RR 0.71 |
| 글라티라머 아세테이트 | 조절 T 세포 조절 | 자가 주사 | 재발 RR 0.82 |
| 나탈리주맙 | 중추신경계로의 염증 세포 유입 억제 | 정맥 주입 | 재발 RR 0.56 |
| 핑골리모드 | S1P 수용체 조절제 | 경구 | 새 T2 병변 RR 0.65 |
| 테리플루노마이드 | 피리미딘 합성 억제제 | 경구 | 장애 진행 RR 0.76 |
| 다이메틸 푸마레이트 | 산화 스트레스 및 염증 감소 | 경구 | 재발 RR 0.64 |
| 알렘투주맙 | 항CD52 단일클론항체 | 정맥 주입 | 장애 진행 RR 0.44 |
항CD20 단클론항체(오크렐리주맙, 리툭시맙, 오파투무맙)는 재발형 MS의 표준 치료로 자리 잡고 있습니다3).
뇌 병변이 없는 시신경염에서도 15년 후 25%에서 MS가 발생하며, 뇌 병변이 있는 경우 78%에서 MS로 전환됩니다.
뇌 MRI에 병변이 없더라도 15년 후 25%에서 MS가 발생하고, 뇌 병변이 있는 경우 78%에서 MS로 전환됩니다. 시신경염이 발생한 환자는 신경과와 협력하여 재발 예방을 위한 DMT 적용을 고려해야 합니다.
MS는 자가면역 질환으로 간주됩니다. T 림프구가 수초를 이물질로 인식하고 대식세포, 사이토카인, 항체를 활성화하여 수초와 축삭을 파괴합니다. 수초 소실로 인해 전기 자극 전도가 손상되고 신경 신호 전달이 장애됩니다.
활동성 플라크
거품 대식세포: 수초를 탐식한 대식세포가 축적됩니다.
혈관주위 침윤 (perivascular cuffing): 림프구가 혈관 주위를 둘러싸는 특징적인 소견.
부종성 국소 탈수초 병변: 급성 악화기에 나타납니다.
만성 플라크
수초 소실: Luxol fast blue 염색으로 확인 가능합니다. 축삭은 보존되지만 재수초화가 불완전합니다.
NAWM 병변: 정상으로 보이는 백질의 미만성 신경아교증, 미세아교세포 활성화, 혈액뇌장벽 파괴. 국소 백질 병변보다 임상적 장애와 더 높은 상관관계를 보입니다.
희소돌기아교세포가 중추신경계의 재수초화를 담당합니다1). 성체 희소돌기아교세포 전구세포(OPC)에 의존하지만, 기존의 성숙 희소돌기아교세포는 재수초화에 기여할 수 없습니다1).
재수초화 실패의 주요 원인은 다음과 같습니다1).
또한 피질 및 피질하 회백질 손상이 관찰되며, 수막에 B세포 여포양 림프 구조가 형성되면 더 심각한 임상 경과로 이어지는 것으로 알려져 있습니다1).
CD40L을 억제하여 T세포와 항원제시세포(B세포 포함)의 공동자극을 차단하는 새로운 접근법입니다.
Vermersch 등(N Engl J Med 2024)의 2상 시험에서 frexalimab은 MRI 결과(8~12주에서 새로운 가돌리늄 조영 병변)에서 위약에 비해 명확한 유효성을 보였으며, 신경 조직 손상의 바이오마커인 혈청 NfL의 감소도 확인되었습니다3). 진행성 MS에 대해서는 미세아교세포와 대식세포의 불활성화 효과도 기대되며, 플라크 가장자리의 미세아교세포에 대한 CD40L 신호 차단을 통한 신경 보호가 이론적으로 가능합니다3).
현재 고효능 DMT(항CD20 약물)에 대한 임상적 우월성 확립이 향후 과제로 남아 있습니다3).
철 의존성 세포 사멸인 페롭토시스가 MS 신경 세포 사멸에 관여하는 것으로 나타났습니다.
Tang et al.(2025)은 Woo et al.(Cell, 2024)의 연구를 해설하며, 글루타메이트 흥분독성 → 칼슘 과부하 → 소포체 스트레스 → STING1이 STIM1에서 해리 → 비정형 경로 활성화 → 오토파지 → GPX4(지질 과산화 중화 효소)의 오토파지 분해 → 페롭토시스(철 의존성 세포 사멸)라는 캐스케이드를 보고했습니다4). 인간 MS 검체와 마우스 모델 모두에서 신경 세포의 STING1 발현 증가가 확인되었습니다. STING1 억제제(C176, H151)는 동물 모델에서 오토파지 의존성 GPX4 분해를 감소시키고 신경 보호 효과를 나타냈습니다4).
연구 단계에서는 CD40L 억제제 frexalimab에 의한 미세아교세포 및 대식세포의 불활성화를 통한 신경 보호3)와 STING1 억제를 통한 페롭토시스(철 의존성 세포 사멸) 억제4)가 유망한 것으로 간주됩니다. 둘 다 현재 임상 시험 또는 연구 단계에 있으며 표준 치료는 아닙니다.