진피내 모반
외관: 돔형 또는 결절형 융기성 병변. 색소가 적고, 살색~연한 갈색이 많습니다.
특징: 모발을 동반할 수 있습니다. 소아기부터 인지되는 경우가 많습니다.
악성화 위험: 거의 없습니다.

눈꺼풀 모반은 미성숙 색소 세포(모반 세포)가 표피 기저층에서 진피 내로 증식한 양성 종양입니다. 표피에 가까울수록 멜라닌 색소가 풍부하고, 진피 깊은 층으로 갈수록 색소가 적어집니다. 모반 세포 집락의 주된 위치가 표층에서 심층으로 이동함에 따라 조직학적으로 경계 모반, 복합 모반, 진피내 모반으로 분류됩니다.
눈꺼풀 양성 종양의 병리 진단별 빈도에서 가장 흔하며, 64안 중 14안(22%)을 차지합니다. 소아기부터 존재하는 경우가 많으며, 문진이 진단에 도움이 됩니다. 아형 중에서는 진피내 모반이 가장 흔합니다. 일반적인 피부 모반은 1인당 평균 1040개입니다1). 오타 모반은 아시아인에서 비교적 흔하며, 0.10.6%의 빈도가 보고되었습니다2).
눈꺼풀에 발생하는 모반의 주요 조직학적 아형은 아래와 같습니다.
경계모반 (접합부모반) junctional nevus: 표피 깊은 층에서 진피와의 경계부에 발생합니다. 경계가 명확하고 편평한 종양으로, 색소를 많이 함유하여 짙은 갈색에서 검은색을 띱니다. 악성화될 수 있습니다.
진피내모반 intradermal nevus: 진피 내에 발생하며 발생 빈도가 가장 높습니다. 융기성·결절성 병변이 많지만 갈색조는 적습니다. 모발을 가질 수도 있습니다. 악성화는 거의 없습니다.
복합모반 compound nevus: 경계모반과 진피내모반의 두 가지 성질을 모두 가지며, 색조는 다양합니다. 악성화될 수 있습니다.
청색모반 blue nevus: 진피 내에 멜라닌세포를 가지며, 청색에서 청갈색조를 띱니다.
오타모반 nevus of Ota: 삼차신경 제1·제2지 영역에 미만성으로 발생하는 청색모반입니다. 공막·홍채에도 색소침착을 일으키는 경우가 많습니다. 여성에 많고, 편측성으로 나타납니다.
아형에 따라 다릅니다. 진피내모반은 악성화되지 않으므로, 미용적 문제가 없다면 경과 관찰이 가능합니다. 단, 급속한 증대·색조 변화·출혈·가려움이 발생한 경우에는 안과를 진료받으십시오. 경계모반이나 복합모반은 드물게 악성 흑색종으로 전환될 수 있으므로, 경과 관찰과 함께 완전 절제를 고려합니다.
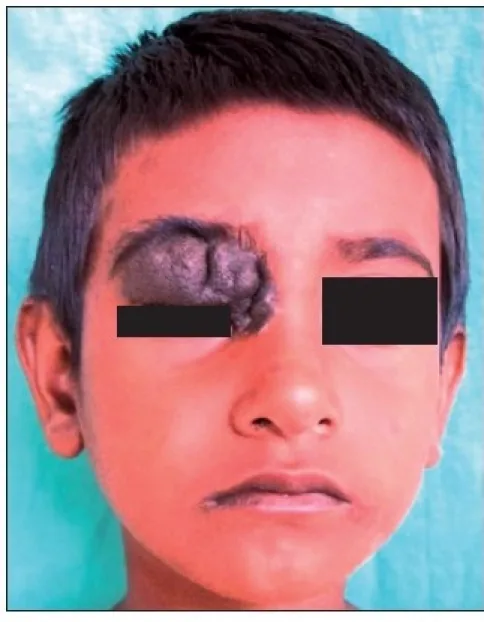
눈꺼풀 모반의 대부분은 무증상입니다. 주요 호소는 미용적 문제(안면의 색소성 융기)이며, 통증이나 시기능 장애는 보통 동반되지 않습니다. 환자 자신이 소아기부터 종괴의 존재를 자각하고 있는 경우가 많으며, 문진이 진단의 단서가 됩니다.
눈꺼풀 가장자리에서 속눈썹 사이에 호발하지만, 눈물점 부근에 발생하기도 합니다. 모반 중에서는 진피내모반이 가장 많으며, 진피 내의 모반 세포가 증식하여 표피를 돔 모양으로 밀어 올립니다. 복합모반은 갈색의 융기성 종양을, 경계모반은 검은색의 편평한 병변을 나타냅니다. 색조는 얕은 층에 위치할수록 짙고(검은색), 깊은 층에서는 옅은 경향이 있습니다.
각 아형의 임상적 특징을 아래에 제시합니다.
진피내 모반
외관: 돔형 또는 결절형 융기성 병변. 색소가 적고, 살색~연한 갈색이 많습니다.
특징: 모발을 동반할 수 있습니다. 소아기부터 인지되는 경우가 많습니다.
악성화 위험: 거의 없습니다.
복합 모반 및 경계 모반
외관: 복합 모반은 갈색의 융기성 종괴입니다. 경계 모반은 검은색이며 편평합니다.
특징: 색소가 풍부하여 검은색~진한 갈색조가 많습니다. 윤곽이 비교적 명확합니다.
악성화 위험: 드물게 악성 흑색종으로 전환됩니다.
오타 모반
외관: 삼차신경 제1,2지 영역에 미만성 청회색~청갈색 색소 침착.
특징: 공막과 홍채에도 색소 침착. 여성에 많고, 편측성. 선천성 또는 청년기 발병.
악성화 위험: 포도막 흑색종의 위험이 보고되었습니다.
오타 모반에서는 홍채·공막의 색소 침착을 동반할 수 있으며, 색소성 녹내장(멜라닌 세포성 녹내장)의 위험이 지적되고 있습니다. 또한 오타 모반과 포도막 악성 흑색종의 연관성도 보고되어9), 정기적인 안과 추적 관찰이 권장됩니다.
눈꺼풀 모반의 발생에는 다음 요인이 관여합니다.
눈꺼풀 모반의 진단에서는 다음 정보가 중요합니다.
눈꺼풀 모반과 감별이 필요한 주요 질환은 다음과 같습니다.
| 감별 질환 | 감별 포인트 |
|---|---|
| 악성 흑색종 | 색소 불균일, 경계 불규칙, 급속 변화, ABCDE 해당 |
| 기저 세포 암종 | 중심 궤양, 진주 광택, 급속 증대 |
| 지루성 각화증 | 표면 각화/사마귀 모양, 노인 |
| 청색 모반 | 청색조, 진피 심부 |
| 혈관종 | 적색, 압박 시 퇴색 |
임상적 감별에는 ABCDE 기준(비대칭, 경계 불규칙, 색조 불균일, 직경 6mm 초과, 변화)이 유용하며, 피부경 검사에서 비전형적 패턴이 있으면 악성을 의심합니다3,4). 또한 소아기부터 존재하는 병변은 양성일 가능성이 높습니다(문진이 중요). 최종 확진은 병리조직검사에 의합니다. 급속한 변화가 있는 경우 망설이지 않고 절제 생검을 시행합니다.
안검 모반의 치료는 아형과 악성화 위험에 기반하여 결정합니다. 아형별 치료 방침을 아래 표에 제시합니다.
| 아형 | 치료법 | 악성화 위험 |
|---|---|---|
| 진피내 모반 | 미용적 희망 시 셰이빙(개방 치료) | 거의 없음 |
| 복합 모반 | 완전 절제 권장 | 드물게 악성 흑색종 |
| 경계모반 | 완전 절제 권장 | 드물게 악성 흑색종 |
| 청색모반 | 경과 관찰 또는 절제 | 극히 드물 |
| 오타모반 | Q스위치 레이저 | 포도막 흑색종 보고 있음 |
진피내 모반의 치료: 악성화되지 않으므로, 미용적 이유로 절제를 원하는 경우에만 수술 적응이 됩니다. 환자는 어릴 때부터 얼굴의 일부로 함께해 온 경우가 많아 절제를 원하지 않는 경우도 많습니다. 일반적인 수술 방법은 종양의 융기된 부분만 부분 절제(shaving)하고 개방창으로 두는 open treatment입니다.
복합모반 및 경계모반의 치료: 드물지만 악성 흑색종으로 전환될 위험이 있으므로, 경과를 보면서 완전 절제를 권장합니다. 절제 검체는 반드시 병리조직검사에 제출합니다.
오타모반의 치료: Q스위치 루비 레이저나 Q스위치 알렉산드라이트 레이저가 효과적이라고 보고되었습니다5). 레이저 조사로 진피 멜라닌 세포를 선택적으로 파괴하여 색소 침착을 개선합니다. 여러 번의 조사가 필요한 경우가 많습니다.
선천성 거대 색소성 모반의 치료: 계획적 단계 절제나 조직 확장기의 적용이 이루어집니다6). 눈꺼풀에 합병된 경우 재건 수술이 복잡해지므로 전문 시설에서의 대응이 바람직합니다.
오타 모반에는 Q스위치 루비 레이저나 Q스위치 알렉산드라이트 레이저가 효과적인 것으로 알려져 있으며, 여러 번 조사로 색소 침착 개선을 기대할 수 있습니다5). 일반적인 진피 내 모반, 복합 모반, 경계 모반에 대해서는 절제(shaving 또는 완전 절제)가 표준 치료이며, 레이저는 일차 선택이 아닙니다.
모반 세포는 신경능선에서 이동한 멜라닌세포 전구체를 기원으로 하는 미성숙 색소 세포입니다1). 모반 세포 집락의 깊이에 따라 조직학적 아형이 결정됩니다. 표피 기저층에 모반 세포 집락이 국한되면 경계 모반, 진피 내에 국한되면 진피 내 모반, 둘 다에 걸치면 복합 모반이 됩니다. 세포의 위치가 얕을수록 멜라닌 색소가 풍부하고, 깊은 층에서는 색소가 적어집니다. 이 색소 구배가 아형 간 육안적 색조 차이를 만듭니다.
후천성 모반의 약 80%에서 BRAF V600E 변이가 발견됩니다7). BRAF 변이는 세포 증식 신호(MAPK 경로)를 활성화하지만, 단독으로는 악성화에 이르지 않으며 종양유전자 유도 노화(oncogene-induced senescence)를 일으키는 경우가 많습니다. 악성 흑색종으로의 전환은 BRAF 변이에 추가로 TERT 프로모터 변이나 CDKN2A 결실 등의 추가 변이가 축적되어 발생합니다7). 일반적인 점이 악성 흑색종으로 전환될 확률은 0.0005% 미만/개/년으로 추정되며, 위험은 매우 낮습니다1).
오타 모반은 진피 내 멜라닌세포의 과형성으로 발생합니다. 삼차신경 제1·2지 영역의 진피에 산재한 멜라닌세포가 증식하여 청색~청회색 색소 침착을 나타냅니다. 눈꺼풀 피부뿐만 아니라 공막, 홍채, 안저에도 색소 침착이 생길 수 있습니다. 백인의 안피부 흑색증(oculodermal melanocytosis) 환자에서는 포도막 흑색종의 평생 발생률이 유의하게 높다고 보고되어9), 정기적인 안저 및 안압 검사가 권장됩니다.
딥러닝을 이용한 피부 종양 영상 진단 시스템이 개발되었으며, 피부과 전문의 수준의 분류 정확도가 보고되었습니다8). 피부경 영상과 결합하면 모반과 악성 흑색종의 감별 정확도가 더욱 향상될 것으로 기대됩니다. 눈꺼풀 부위로의 적용은 향후 과제입니다.
선천성 거대 색소성 모반에 대한 조직 확장기를 이용한 단계적 절제술에 대한 체계적 문헌고찰에서 기능적·미용적 재건의 개선이 보고되었습니다6). 눈꺼풀을 침범한 경우 시각 기능에 미치는 영향을 최소화하면서 절제 및 재건을 수행하는 기술적 개선이 진행되고 있습니다.
안피부 흑색증을 가진 백인 환자를 대상으로 한 연구에서 포도막 흑색종의 평생 발생률이 약 1/400으로 보고되었으며, 오타 모반 환자에서도 정기적인 안저 검사의 유용성이 지적되었습니다9).
Tsao H, Bevona C, Goggins W, et al. The transformation rate of moles (melanocytic nevi) into cutaneous melanoma. Arch Dermatol. 2003;139(3):282-288.
Hidano A, Kajima H, Ikeda S, et al. Natural history of nevus of Ota. Arch Dermatol. 1967;95(2):187-195.
Abbasi NR, Shaw HM, Rigel DS, et al. Early diagnosis of cutaneous melanoma: revisiting the ABCD criteria. JAMA. 2004;292(22):2771-2776.
Argenziano G, Soyer HP, Chimenti S, et al. Dermoscopy of pigmented skin lesions: results of a consensus meeting. J Am Acad Dermatol. 2003;48(5):679-693.
Chan HH, Kono T. The use of lasers and intense pulsed light sources for the treatment of pigmentary lesions. Skin Therapy Lett. 2004;9(8):5-7.
Kishi K, Matsuda N, Kubota Y, et al. Systematic review: staged excision and tissue expansion for giant congenital melanocytic nevi. J Plast Reconstr Aesthet Surg. 2022;75(1):1-15.
Shain AH, Yeh I, Kovalyshyn I, et al. The genetic evolution of melanoma from precursor lesions. N Engl J Med. 2015;373(20):1926-1936.
Esteva A, Kuprel B, Novoa RA, et al. Dermatologist-level classification of skin cancer with deep neural networks. Nature. 2017;542(7639):115-118.
Singh AD, De Potter P, Fijal BA, et al. Lifetime prevalence of uveal melanoma in white patients with oculo(dermal) melanocytosis. Ophthalmology. 1998;105(1):195-198.