الوحمة الجلدية
المظهر: آفة بارزة على شكل قبة أو عقدة. قليلة الصباغ، غالباً بلون الجلد أو بني فاتح.
الخصائص: قد تكون مصحوبة بشعر. غالباً ما تُلاحظ منذ الطفولة.
خطر التحول الخبيث: لا يوجد تقريباً.

وحمة الجفن هي ورم حميد ناتج عن تكاثر الخلايا الصباغية غير الناضجة (خلايا الوحمة) من الطبقة القاعدية للبشرة إلى داخل الأدمة. كلما اقتربت من البشرة، زادت صبغة الميلانين، وكلما تعمقت في الأدمة، قلت الصبغة. مع انتقال موقع تجمعات خلايا الوحمة من السطح إلى العمق، تُصنف نسيجيًا إلى وحمة حدية، وحمة مركبة، وحمة داخل الأدمة.
من حيث التوزيع حسب التشخيص المرضي لأورام الجفن الحميدة، فهي الأكثر شيوعًا، حيث تمثل 14 عينًا من أصل 64 عينًا (22%). توجد غالبًا منذ الطفولة، ويساعد التاريخ المرضي في التشخيص. النوع الفرعي الأكثر شيوعًا هو الوحمة داخل الأدمة. يبلغ متوسط عدد الوحمات الجلدية العامة 10-40 وحمة لكل شخص 1). وحمة أوتا شائعة نسبيًا بين الآسيويين، ويُبلغ عن تواترها بنسبة 0.1-0.6% 2).
فيما يلي الأنواع الفرعية النسيجية الرئيسية للوحمات التي تحدث في الجفن.
الوحمة الحدودية (الوحمة الوصلية) junctional nevus: تحدث في الطبقة العميقة من البشرة عند الحدود مع الأدمة. وهي كتلة مسطحة واضحة الحدود، تحتوي على الكثير من الصبغة وتظهر بلون بني غامق إلى أسود. قد تصبح خبيثة.
الوحمة داخل الأدمة intradermal nevus: تحدث داخل الأدمة، وهي الأكثر شيوعًا. غالبًا ما تكون آفات بارزة وعقيدية ولكن لونها بني قليل. قد تحتوي على شعر. نادرًا ما تصبح خبيثة.
الوحمة المركبة compound nevus: لها خصائص كل من الوحمة الحدودية والوحمة داخل الأدمة، ويختلف لونها. قد تصبح خبيثة.
الوحمة الزرقاء blue nevus: تحتوي على خلايا ميلانينية في الأدمة، وتظهر بلون أزرق إلى بني مزرق.
وحمة أوتا nevus of Ota: وحمة زرقاء منتشرة في منطقة الفرعين الأول والثاني للعصب ثلاثي التوائم. غالبًا ما يصاحبها تصبغ في الصلبة والقزحية. أكثر شيوعًا عند النساء، وتظهر في جانب واحد.
يختلف ذلك حسب النوع الفرعي. الوحمة داخل الأدمة لا تصبح خبيثة، لذا يمكن متابعتها إذا لم تكن هناك مشكلة تجميلية. ومع ذلك، إذا حدث نمو سريع أو تغير في اللون أو نزيف أو حكة، يجب استشارة طبيب عيون. الوحمات الحدودية والمركبة قد تتحول نادرًا إلى ميلانوما خبيثة، لذا يُنصح بالمتابعة والنظر في الاستئصال الكامل.
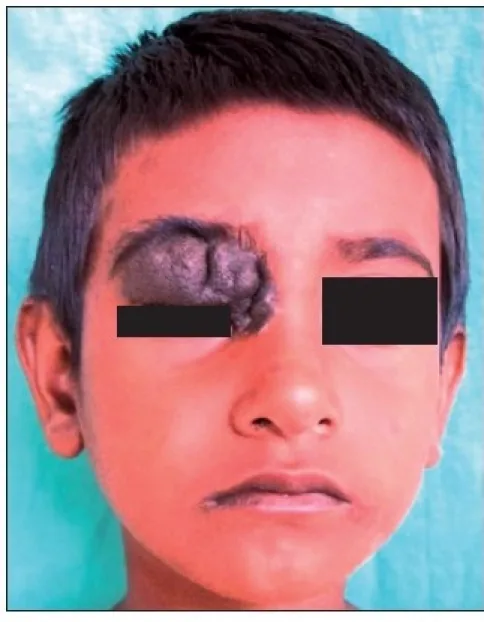
معظم وحمات الجفن لا تسبب أعراضًا. الشكوى الرئيسية هي مشكلة تجميلية (نتوء مصطبغ على الوجه)، وعادة لا يصاحبها ألم أو ضعف بصري. غالبًا ما يكون المريض على علم بوجود الكتلة منذ الطفولة، ويساعد التاريخ المرضي في التشخيص.
تحدث غالبًا على حافة الجفن بين الرموش، ولكن قد تحدث أيضًا بالقرب من نقطة الدمع. أكثر أنواع الوحمات شيوعًا هي الوحمة داخل الأدمة، حيث تتكاثر خلايا الوحمة داخل الأدمة مما يرفع البشرة على شكل قبة. الوحمة المركبة تظهر ككتلة بارزة بنية اللون، بينما الوحمة الحدودية تظهر كآفة مسطحة سوداء. يميل اللون إلى أن يكون أغمق (أسود) في الطبقات السطحية وأفتح في الطبقات العميقة.
فيما يلي الخصائص السريرية لكل نوع فرعي.
الوحمة الجلدية
المظهر: آفة بارزة على شكل قبة أو عقدة. قليلة الصباغ، غالباً بلون الجلد أو بني فاتح.
الخصائص: قد تكون مصحوبة بشعر. غالباً ما تُلاحظ منذ الطفولة.
خطر التحول الخبيث: لا يوجد تقريباً.
الوحمة المركبة والحدودية
المظهر: الوحمة المركبة هي كتلة بارزة بنية اللون. الوحمة الحدودية سوداء ومسطحة.
الخصائص: غنية بالصباغ، غالباً سوداء إلى بنية داكنة. محيطها واضح نسبياً.
خطر التحول الخبيث: نادراً ما تتحول إلى ميلانوما خبيثة.
وحمة أوتا
المظهر: تصبغ منتشر بلون رمادي مزرق إلى بني مزرق في منطقة توزيع العصب ثلاثي التوائم (الفرعين الأول والثاني).
الخصائص: تصبغ في الصلبة والقزحية أيضاً. أكثر شيوعاً عند النساء، أحادي الجانب. خلقي أو يظهر في مرحلة الشباب.
خطر التحول الخبيث: تم الإبلاغ عن خطر الإصابة بالميلانوما العنبية.
قد يصاحب وحمة أوتا تصبغ في القزحية والصلبة، مما يزيد من خطر الإصابة بالجلوكوما الصباغية (جلوكوما الخلايا الميلانينية). كما تم الإبلاغ عن ارتباط بين وحمة أوتا والميلانوما الخبيثة العنبية9)، ويوصى بالمتابعة الدورية لطب العيون.
تتضمن العوامل التالية في حدوث وحمة الجفن:
في تشخيص وحمة الجفن، المعلومات التالية مهمة:
فيما يلي الأمراض الرئيسية التي تتطلب تمييزها عن شامة الجفن.
| مرض تفريقي | نقطة التمييز |
|---|---|
| الورم الميلانيني الخبيث | عدم تجانس اللون، حدود غير منتظمة، تغير سريع، ينطبق عليه ABCDE |
| سرطان الخلايا القاعدية | تقرح مركزي، لمعان لؤلؤي، نمو سريع |
| التقرن الدهني | سطح متقرن/ثؤلولي، كبار السن |
| الوحمة الزرقاء | لون أزرق، عمق الأدمة |
| الورم الوعائي | لون أحمر، يتلاشى بالضغط |
في التشخيص السريري، يُستخدم معيار ABCDE (عدم التماثل، حدود غير منتظمة، لون غير متجانس، قطر >6 مم، تغير) وهو مفيد، وإذا كان هناك نمط غير نمطي في تنظير الجلد، يُشتبه في الورم الخبيث3,4). كما أن الآفات الموجودة منذ الطفولة غالبًا ما تكون حميدة (التاريخ المرضي مهم). التشخيص النهائي يعتمد على الفحص النسيجي المرضي. في حالة التغير السريع، يجب إجراء خزعة استئصالية دون تردد.
يعتمد علاج وحمة الجفن على النوع الفرعي وخطر التحول الخبيث. يوضح الجدول التالي خطة العلاج حسب النوع الفرعي.
| النوع الفرعي | طريقة العلاج | خطر التحول الخبيث |
|---|---|---|
| الوحمة داخل الأدمة | عند الرغبة التجميلية: الحلاقة (العلاج المفتوح) | يكاد لا يوجد |
| الوحمة المركبة | يوصى بالاستئصال الكامل | نادرًا ما يتحول إلى ورم ميلانيني خبيث |
| الوحمة الحدودية | يوصى بالاستئصال الكامل | نادرًا ما يتحول إلى ميلانوما خبيثة |
| الوحمة الزرقاء | المراقبة أو الاستئصال | نادر جدًا |
| وحمة أوتا | ليزر Q-switched | تم الإبلاغ عن ميلانوما العنبية |
علاج الوحمة الجلدية: نظرًا لعدم تحولها إلى خبيث، فإن الجراحة تكون فقط إذا رغب المريض في الإزالة لأسباب تجميلية. غالبًا ما يكون المرضى غير راغبين في الإزالة لأن الوحمة كانت جزءًا من وجههم منذ الطفولة. الإجراء الشائع هو الاستئصال الجزئي (shaving) للجزء البارز فقط وترك الجرح مفتوحًا (open treatment).
علاج الوحمة المركبة والوحمة الحدودية: نظرًا لخطر التحول إلى ميلانوما خبيثة، وإن كان نادرًا، يُنصح بالاستئصال الكامل مع المراقبة. يجب إرسال العينة المستأصلة للفحص النسيجي المرضي.
علاج وحمة أوتا: تم الإبلاغ عن فعالية ليزر Q-switched ruby و Q-switched alexandrite 5). يعمل الليزر على تدمير الخلايا الصباغية الجلدية بشكل انتقائي وتحسين التصبغ. غالبًا ما تكون هناك حاجة لجلسات متعددة.
علاج الوحمة الصباغية الخلقية العملاقة: يتم إجراء الاستئصال التدريجي المخطط أو استخدام موسعات الأنسجة 6). في الحالات التي تصيب الجفن، تكون الجراحة الترميمية معقدة، لذا يُفضل العلاج في مراكز متخصصة.
بالنسبة لوحمة أوتا، يُعتبر ليزر Q-switch روبي وليزر Q-switch ألكسندريت فعالين، ويمكن أن يؤدي العلاج المتعدد إلى تحسن التصبغ 5). بالنسبة للشامات الجلدية العادية والمركبة والحدودية، يعتبر الاستئصال (shaving أو الاستئصال الكامل) هو العلاج القياسي، والليزر ليس الخيار الأول.
خلايا الشامة هي خلايا صبغية غير ناضجة تنشأ من الخلايا السلفية للخلايا الصبغية المهاجرة من العرف العصبي 1). يتم تحديد النوع الفرعي النسيجي حسب عمق تجمعات خلايا الشامة. إذا كانت التجمعات موضعية في الطبقة القاعدية للبشرة، فهي شامة حدية؛ إذا كانت في الأدمة، فهي شامة جلدية؛ وإذا كانت في كليهما، فهي شامة مركبة. كلما كانت الخلايا في طبقة سطحية، زادت كمية الميلانين، وفي الطبقات العميقة يقل الصباغ. هذا التدرج الصباغي يؤدي إلى اختلافات في اللون الظاهري بين الأنواع الفرعية.
حوالي 80% من الشامات المكتسبة تحمل طفرة BRAF V600E 7). طفرة BRAF تنشط إشارات تكاثر الخلايا (مسار MAPK)، ولكنها وحدها لا تؤدي إلى التحول الخبيث، بل غالبًا ما تسبب شيخوخة الخلايا (oncogene-induced senescence). يحدث التحول إلى الورم الميلانيني الخبيث عندما تتراكم طفرات إضافية مثل طفرة محفز TERT أو فقدان CDKN2A بالإضافة إلى طفرة BRAF 7). يُقدر احتمال تحول الشامة العادية إلى ورم ميلانيني خبيث بأقل من 0.0005% لكل شامة سنويًا، وهو خطر منخفض جدًا 1).
تحدث وحمة أوتا بسبب فرط تنسج الخلايا الصبغية في الأدمة. تتكاثر الخلايا الصبغية المنتشرة في أدمة منطقة العصب ثلاثي التوائم (الفروع الأولى والثانية)، مما يؤدي إلى تصبغ أزرق إلى رمادي مزرق. قد يحدث التصبغ ليس فقط في جلد الجفن، ولكن أيضًا في الصلبة والقزحية وقاع العين. في المرضى البيض المصابين بتصبغ جلدي عيني (oculodermal melanocytosis)، يُبلغ عن ارتفاع معدل الإصابة بسرطان العنبية مدى الحياة بشكل ملحوظ 9)، ويُوصى بإجراء فحوصات دورية لقاع العين وضغط العين.
تم تطوير أنظمة تشخيص صور أورام الجلد باستخدام التعلم العميق، وقد تم الإبلاغ عن دقة تصنيف على مستوى أطباء الجلد المتخصصين 8). من المتوقع أن يؤدي الجمع مع صور منظار الجلد إلى تحسين دقة التمييز بين الشامات والورم الميلانيني الخبيث. تطبيق هذه التقنية على منطقة الجفن هو تحدٍ مستقبلي.
تم إجراء مراجعة منهجية لطريقة الاستئصال التدريجي باستخدام موسعات الأنسجة للوحمة الخلقية العملاقة المصطبغة، وتم الإبلاغ عن تحسن في إعادة البناء الوظيفي والتجميلي 6). في الحالات التي تشمل الجفن، تتقدم التحسينات التقنية للاستئصال وإعادة البناء مع تقليل التأثير على الوظيفة البصرية.
في دراسة أجريت على مرضى بيض مصابين بتصبغ جلدي عيني، كان معدل الإصابة مدى الحياة بالورم الميلانيني العنبي حوالي 1/400، مما يشير إلى فائدة الفحص الدوري لقاع العين لدى المرضى الذين يعانون من وحمة أوتا 9).
Tsao H, Bevona C, Goggins W, et al. The transformation rate of moles (melanocytic nevi) into cutaneous melanoma. Arch Dermatol. 2003;139(3):282-288.
Hidano A, Kajima H, Ikeda S, et al. Natural history of nevus of Ota. Arch Dermatol. 1967;95(2):187-195.
Abbasi NR, Shaw HM, Rigel DS, et al. Early diagnosis of cutaneous melanoma: revisiting the ABCD criteria. JAMA. 2004;292(22):2771-2776.
Argenziano G, Soyer HP, Chimenti S, et al. Dermoscopy of pigmented skin lesions: results of a consensus meeting. J Am Acad Dermatol. 2003;48(5):679-693.
Chan HH, Kono T. The use of lasers and intense pulsed light sources for the treatment of pigmentary lesions. Skin Therapy Lett. 2004;9(8):5-7.
Kishi K, Matsuda N, Kubota Y, et al. Systematic review: staged excision and tissue expansion for giant congenital melanocytic nevi. J Plast Reconstr Aesthet Surg. 2022;75(1):1-15.
Shain AH, Yeh I, Kovalyshyn I, et al. The genetic evolution of melanoma from precursor lesions. N Engl J Med. 2015;373(20):1926-1936.
Esteva A, Kuprel B, Novoa RA, et al. Dermatologist-level classification of skin cancer with deep neural networks. Nature. 2017;542(7639):115-118.
Singh AD, De Potter P, Fijal BA, et al. Lifetime prevalence of uveal melanoma in white patients with oculo(dermal) melanocytosis. Ophthalmology. 1998;105(1):195-198.