Dermaler Nävus
Aussehen : Kuppel- oder knotenförmige erhabene Läsion. Wenig Pigment, meist hautfarben bis hellbraun.
Merkmale : Kann behaart sein. Wird oft seit der Kindheit bemerkt.
Malignitätsrisiko : Kaum vorhanden.

Der Lidnävus ist ein gutartiger Tumor, der durch die Proliferation unreifer Pigmentzellen (Nävuszellen) von der Basalschicht der Epidermis bis in die Dermis entsteht. Je näher an der Epidermis, desto melaninreicher; je tiefer in der Dermis, desto pigmentärmer. Je nachdem, wo sich die Nävuszellnester hauptsächlich befinden, werden sie histologisch als Junktionsnävus, Compoundnävus und dermaler Nävus klassifiziert.
Unter den gutartigen Lidtumoren ist der Lidnävus der häufigste; er macht 14 von 64 Augen (22 %) aus. Er besteht oft seit der Kindheit, und die Anamnese ist diagnostisch hilfreich. Der häufigste Subtyp ist der dermale Nävus. Im Durchschnitt hat ein Mensch 10–40 Hautnävi1). Der Ota-Nävus tritt bei Asiaten relativ häufig auf, mit einer berichteten Häufigkeit von 0,1–0,6 %2).
Die wichtigsten histologischen Subtypen der Lidnävi sind im Folgenden aufgeführt.
Junktionsnävus (Grenznävus) : Entsteht in der tiefen Schicht der Epidermis an der Grenze zur Dermis. Es handelt sich um einen gut abgegrenzten, flachen Tumor, der reich an Pigmenten ist und eine dunkelbraune bis schwarze Farbe aufweist. Er kann bösartig werden.
Intradermaler Nävus : Entsteht in der Dermis und ist der häufigste Typ. Er tritt oft als erhabene oder knotige Läsion auf, hat aber weniger braune Tönung. Er kann Haare enthalten. Eine maligne Entartung ist sehr selten.
Compound-Nävus (kombinierter Nävus) : Besitzt Eigenschaften sowohl des Junktions- als auch des intradermalen Nävus, die Farbe ist variabel. Er kann bösartig werden.
Blauer Nävus : Enthält Melanozyten in der Dermis und zeigt eine blaue bis blau-braune Farbe.
Nävus Ota : Diffuser blauer Nävus im Bereich des ersten und zweiten Astes des Trigeminusnervs. Häufig kommt es auch zu Pigmentierungen der Sklera und Iris. Tritt einseitig auf, häufiger bei Frauen.
Das hängt vom Subtyp ab. Der intradermale Nävus entartet nicht, daher ist eine Beobachtung möglich, wenn kein kosmetisches Problem besteht. Bei schnellem Wachstum, Farbveränderung, Blutung oder Juckreiz sollte jedoch ein Augenarzt aufgesucht werden. Junktions- und Compound-Nävi können selten in ein malignes Melanom übergehen, daher sollten sie überwacht und eine vollständige Exzision in Betracht gezogen werden.
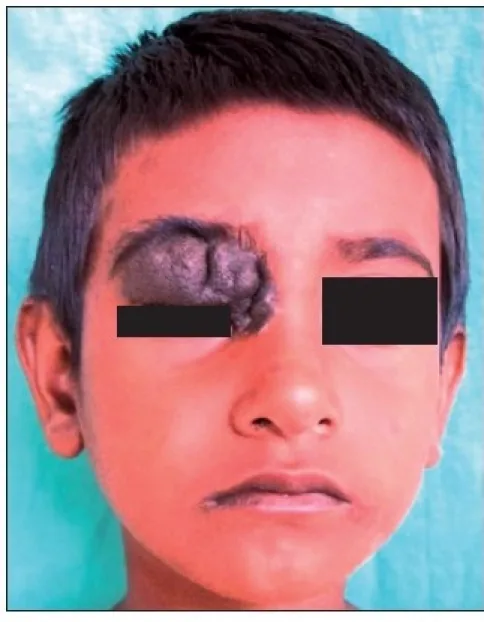
Die meisten Lidnävi sind asymptomatisch. Die Hauptbeschwerde ist kosmetischer Natur (pigmentierte Erhebung im Gesicht), Schmerzen oder Sehstörungen treten in der Regel nicht auf. Der Patient ist sich des Tumors oft seit der Kindheit bewusst, und die Anamnese ist ein diagnostischer Hinweis.
Sie treten häufig am Lidrand zwischen den Wimpern auf, können aber auch in der Nähe des Tränenpunkts vorkommen. Der intradermale Nävus ist der häufigste; die Nävuszellen in der Dermis proliferieren und wölben die Epidermis kuppelförmig vor. Der Compound-Nävus erscheint als braune, erhabene Masse, während der Junktionsnävus eine schwarze, flache Läsion ist. Die Farbe ist in oberflächlichen Schichten dunkler (schwarz) und in tiefen Schichten heller.
Die klinischen Merkmale der einzelnen Subtypen sind unten aufgeführt.
Dermaler Nävus
Aussehen : Kuppel- oder knotenförmige erhabene Läsion. Wenig Pigment, meist hautfarben bis hellbraun.
Merkmale : Kann behaart sein. Wird oft seit der Kindheit bemerkt.
Malignitätsrisiko : Kaum vorhanden.
Compound- und Junktionsnävus
Aussehen : Der Compound-Nävus ist ein brauner, erhabener Tumor. Der Junktionsnävus ist schwarz und flach.
Merkmale : Reich an Pigment, oft schwarz bis dunkelbraun. Relativ scharfe Begrenzung.
Malignitätsrisiko : Selten Übergang in malignes Melanom.
Nävus Ota
Aussehen : Diffuse blaugraue bis blaugraue Pigmentierung im Bereich des 1. und 2. Trigeminusasts.
Merkmale : Auch Pigmentierung von Sklera und Iris. Häufiger bei Frauen, einseitig. Angeboren oder im Jugendalter auftretend.
Malignitätsrisiko : Ein Risiko für ein Aderhautmelanom wurde berichtet.
Der Nävus Ota kann mit einer Pigmentierung von Iris und Sklera einhergehen, und es wird auf ein Risiko für ein Pigmentglaukom (melanozytäres Glaukom) hingewiesen. Zudem wurde ein Zusammenhang zwischen Nävus Ota und uvealem malignem Melanom berichtet9), weshalb regelmäßige augenärztliche Kontrollen empfohlen werden.
Folgende Faktoren sind an der Entstehung eines Lidnävus beteiligt.
Für die Diagnose eines Lidnävus sind folgende Informationen wichtig.
Die wichtigsten Erkrankungen, die vom Lidnävus abgegrenzt werden müssen, sind im Folgenden aufgeführt.
| Differenzialdiagnose | Abgrenzungsmerkmale |
|---|---|
| Malignes Melanom | Ungleichmäßige Pigmentierung, unregelmäßige Begrenzung, schnelle Veränderung, ABCDE-Kriterien erfüllt |
| Basalzellkarzinom | Zentrale Ulzeration, perlmuttartiger Glanz, schnelles Wachstum |
| Seborrhoische Keratose | Oberflächliche Keratose / warzenartig, ältere Patienten |
| Blauer Nävus | Bläulicher Farbton, tiefe Dermis |
| Hämangiom | Rot, blasst bei Druck ab |
Für die klinische Unterscheidung ist das ABCDE-Kriterium (Asymmetrie, unregelmäßige Begrenzung, ungleichmäßige Farbe, Durchmesser > 6 mm, Veränderung) nützlich. Ein atypisches Muster in der Dermatoskopie lässt Malignität vermuten 3,4). Läsionen, die seit der Kindheit bestehen, sind wahrscheinlich gutartig (Anamnese wichtig). Die endgültige Diagnose erfolgt durch histopathologische Untersuchung. Bei schneller Veränderung sollte ohne Zögern eine Exzisionsbiopsie durchgeführt werden.
Die Behandlung des Lidnävus wird basierend auf dem Subtyp und dem Malignitätsrisiko festgelegt. Die Behandlungsschemata nach Subtyp sind in der folgenden Tabelle dargestellt.
| Subtyp | Behandlung | Malignitätsrisiko |
|---|---|---|
| Intradermaler Nävus | Shaving (offene Behandlung) bei kosmetischem Wunsch | Kaum vorhanden |
| Compound-Nävus | Vollständige Exzision empfohlen | Selten malignes Melanom |
| Junktionsnävus | Vollständige Exzision empfohlen | Selten malignes Melanom |
| Blauer Nävus | Beobachtung oder Exzision | Äußerst selten |
| Nävus Ota | Q-switch-Laser | Berichte über Aderhautmelanom |
Behandlung des intradermalen Nävus: Da er nicht bösartig wird, ist eine Operation nur indiziert, wenn der Patient aus kosmetischen Gründen eine Entfernung wünscht. Da der Nävus seit der Kindheit als Teil des Gesichts besteht, ist der Wunsch nach Entfernung oft gering. Die übliche Operationstechnik ist die partielle Resektion (Shaving) des erhabenen Tumoranteils und die offene Wundbehandlung.
Behandlung des kombinierten und Junktionsnävus: Aufgrund des seltenen Risikos einer Umwandlung in ein malignes Melanom wird nach Beobachtung eine vollständige Exzision empfohlen. Das Exzisionspräparat muss zwingend zur histopathologischen Untersuchung eingeschickt werden.
Behandlung des Nävus Ota: Q-switch-Rubinlaser und Q-switch-Alexandritlaser gelten als wirksam5). Die Laserbestrahlung zerstört selektiv dermale Melanozyten und verbessert die Pigmentierung. Oft sind mehrere Sitzungen erforderlich.
Behandlung des kongenitalen riesigen pigmentierten Nävus: Geplante schrittweise Exzision oder Anwendung von Gewebeexpandern werden durchgeführt6). Bei Beteiligung des Augenlids ist die Rekonstruktion komplex, daher ist eine Behandlung in einem spezialisierten Zentrum wünschenswert.
Für den Nävus Ota gelten der Q-switch-Rubinlaser und der Q-switch-Alexandritlaser als wirksam, und mehrere Sitzungen können eine Verbesserung der Pigmentierung erwarten lassen 5). Bei gewöhnlichen intradermalen Nävi, zusammengesetzten Nävi und Junktionsnävi ist die Exzision (Shaving oder vollständige Exzision) die Standardbehandlung, und der Laser ist nicht die erste Wahl.
Nävuszellen sind unreife Pigmentzellen, die aus Melanozytenvorläufern stammen, die aus der Neuralleiste eingewandert sind 1). Die Tiefe der Nävuszellnester bestimmt den histologischen Subtyp. Wenn die Nävuszellnester in der Basalschicht der Epidermis lokalisiert sind, handelt es sich um einen Junktionsnävus; wenn sie in der Dermis liegen, um einen intradermalen Nävus; und wenn sie beide betreffen, um einen zusammengesetzten Nävus. Je oberflächlicher die Zellen liegen, desto reichhaltiger ist das Melanin; in tieferen Schichten ist das Pigment spärlicher. Dieser Pigmentgradient führt zu den makroskopischen Farbunterschieden zwischen den Subtypen.
Etwa 80 % der erworbenen Nävi weisen eine BRAF V600E-Mutation auf 7). Die BRAF-Mutation aktiviert den Zellproliferationssignalweg (MAPK-Weg), führt aber allein nicht zur Malignität; sie verursacht häufig eine zelluläre Seneszenz (Onkogen-induzierte Seneszenz). Die Umwandlung in ein malignes Melanom erfolgt durch die Akkumulation zusätzlicher Mutationen wie TERT-Promotormutationen oder CDKN2A-Deletionen zusätzlich zur BRAF-Mutation 7). Das Risiko der Umwandlung eines gewöhnlichen Muttermals in ein malignes Melanom wird auf weniger als 0,0005 % pro Muttermal pro Jahr geschätzt, was extrem niedrig ist 1).
Der Nävus Ota wird durch eine Hyperplasie dermaler Melanozyten verursacht. Melanozyten, die in der Dermis der ersten und zweiten Äste des Trigeminusnervs verstreut sind, proliferieren und verursachen eine bläuliche bis blaugraue Pigmentierung. Neben der Augenlidhaut kann es auch zu Pigmentierungen in Sklera, Iris und Augenhintergrund kommen. Bei kaukasischen Patienten mit okulodermaler Melanozytose ist das Lebenszeitrisiko für ein Aderhautmelanom signifikant erhöht 9), und regelmäßige Augenuntersuchungen des Augenhintergrunds und des Augeninnendrucks werden empfohlen.
Es wurden Bilddiagnosesysteme für Hauttumoren mittels Deep Learning entwickelt, und es wurde über eine Klassifikationsgenauigkeit auf dem Niveau eines Dermatologen berichtet 8). In Kombination mit dermatoskopischen Bildern wird eine weitere Verbesserung der Unterscheidungsgenauigkeit zwischen Nävi und malignen Melanomen erwartet. Die Anwendung im Augenlidbereich ist eine zukünftige Herausforderung.
Eine systematische Übersicht über die schrittweise Exzision mittels Gewebeexpander bei kongenitalen riesigen pigmentierten Nävi wurde durchgeführt, und es wurde über eine Verbesserung der funktionellen und ästhetischen Rekonstruktion berichtet 6). Bei Fällen mit Beteiligung der Augenlider sind technische Verbesserungen im Gange, um die Auswirkungen auf die Sehfunktion zu minimieren und gleichzeitig Exzision und Rekonstruktion durchzuführen.
In einer Studie an weißen Patienten mit okulokutaner Melanose beträgt das Lebenszeitrisiko für ein uveales Melanom etwa 1/400, und die Nützlichkeit regelmäßiger Fundusuntersuchungen bei Patienten mit Naevus Ota wurde betont 9).
Tsao H, Bevona C, Goggins W, et al. The transformation rate of moles (melanocytic nevi) into cutaneous melanoma. Arch Dermatol. 2003;139(3):282-288.
Hidano A, Kajima H, Ikeda S, et al. Natural history of nevus of Ota. Arch Dermatol. 1967;95(2):187-195.
Abbasi NR, Shaw HM, Rigel DS, et al. Early diagnosis of cutaneous melanoma: revisiting the ABCD criteria. JAMA. 2004;292(22):2771-2776.
Argenziano G, Soyer HP, Chimenti S, et al. Dermoscopy of pigmented skin lesions: results of a consensus meeting. J Am Acad Dermatol. 2003;48(5):679-693.
Chan HH, Kono T. The use of lasers and intense pulsed light sources for the treatment of pigmentary lesions. Skin Therapy Lett. 2004;9(8):5-7.
Kishi K, Matsuda N, Kubota Y, et al. Systematic review: staged excision and tissue expansion for giant congenital melanocytic nevi. J Plast Reconstr Aesthet Surg. 2022;75(1):1-15.
Shain AH, Yeh I, Kovalyshyn I, et al. The genetic evolution of melanoma from precursor lesions. N Engl J Med. 2015;373(20):1926-1936.
Esteva A, Kuprel B, Novoa RA, et al. Dermatologist-level classification of skin cancer with deep neural networks. Nature. 2017;542(7639):115-118.
Singh AD, De Potter P, Fijal BA, et al. Lifetime prevalence of uveal melanoma in white patients with oculo(dermal) melanocytosis. Ophthalmology. 1998;105(1):195-198.