0~1기
0기(정상): 비측, 상측, 하측 경계 불명확. 방사상 신경섬유층.
1기(매우 초기): 유두 비측 경계의 불명확화. 경계 융기 없음. 미묘한 회색 후광. 동심원 또는 방사상 맥락막 주름.

유두부종은 두개내압(ICP) 항진으로 인한 양안의 유두 부종입니다. “papilledema(choked disc)“라는 용어는 ICP 항진에 한정하여 사용되며, 다른 원인에 의한 유두 종창은 “시신경유두 부종(optic disc edema)“과 구별됩니다. 시신경 주위 지주막하 공간의 압력이 상승하여 시신경이 조여지고 축삭류가 정체되어 유두 부종이 발생합니다.
IIH의 연간 발병률은 1.15/10만 명(미국 19972016년 데이터, 여성 1.97 대 남성 0.36)이며 2), 1844세에서 가장 많습니다(2.47/10만 명). 미국 1855세 여성의 유병률은 3.44/10,000명(95%CI 2.615.39)입니다 3). 인종별로는 흑인 2.05 > 백인 1.04 > 히스패닉 0.67 > 아시아태평양 섬주민 0.16(/10만 명) 순이며 2), 비만 유병률과 지리적으로 대체로 일치합니다(Moran I=0.20, P=0.03) 3).
정상 ICP는 성인 <250 mmH2O, 소아 <280 mmH2O입니다. 전격성 IIH(FIH)는 전체 IIH 환자의 2~3%에서 발생하며, 증상 발현 4주 이내 급속한 시력 장애를 특징으로 하는 응급 질환입니다. 1)
유두부종(papilledema)은 두개내압 상승에 국한된 용어이며, 다른 원인(시신경염, 허혈, 침윤성 병변 등)에 의한 유두 종창은 ‘시신경유두부종(optic disc edema)‘으로 구분하여 부릅니다. 이러한 용어 구분은 원인 규명과 적절한 치료법 선택에 직접 연결되므로 중요합니다.
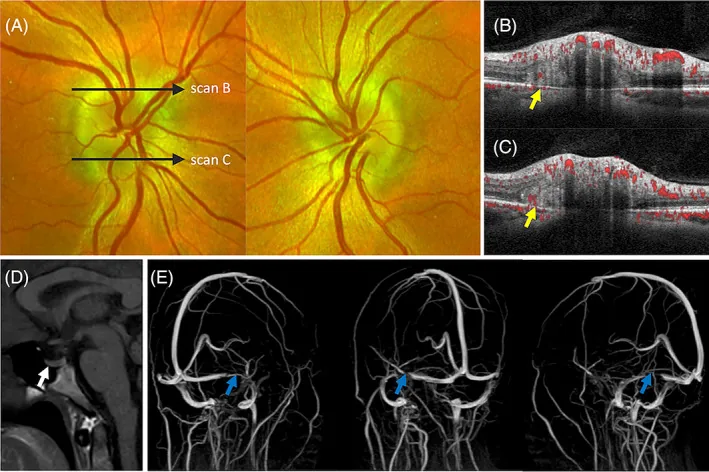
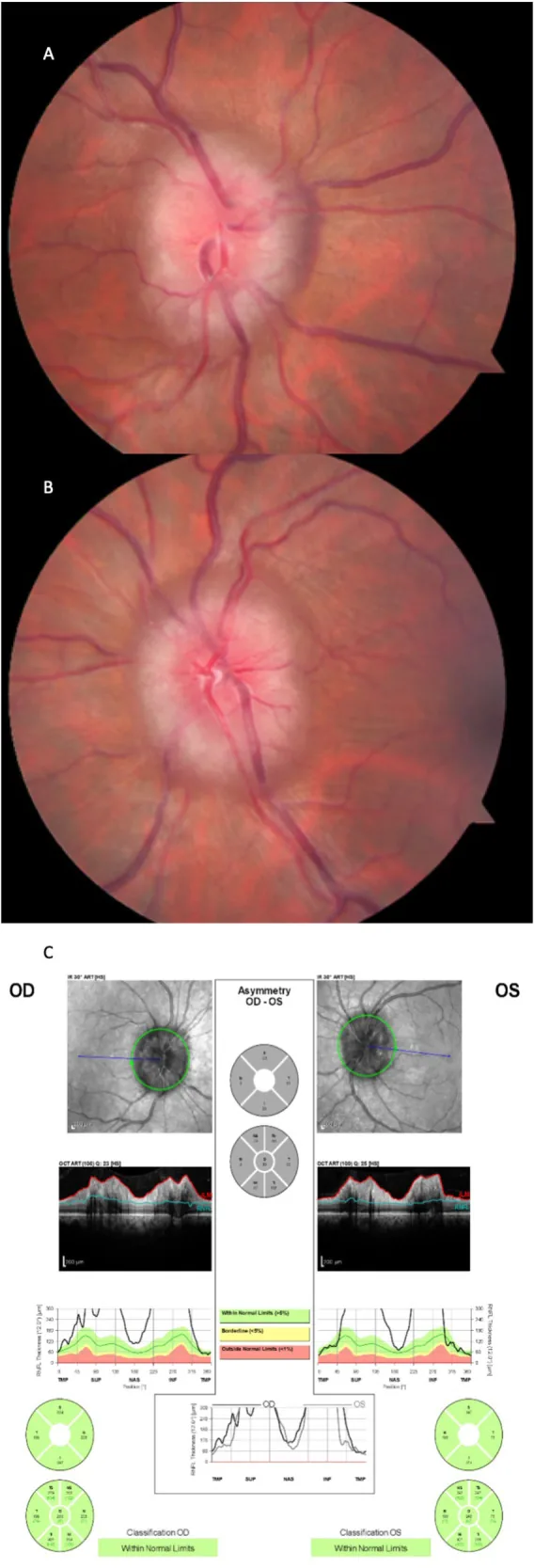
급성기 유두부종은 초기에는 자각 증상이 거의 없으며, 구심성 시기능(최대교정시력, 색각)은 일반적으로 유지됩니다.
소아에서는 양측 외전신경 마비에 동반된 내사시로 두개내압 항진이 발견되는 경우가 많습니다.
급성 유두부종의 안저 소견:
만성 유두부종의 추가 소견: 시신경 유두 창백, 신경교증, optociliary shunt vessel, 굴절체. 만성기에는 죽은 신경 섬유가 부종되지 않으므로 두개내압 상승이 지속되어도 부종이 소실될 수 있음(위축성 말기).
양안성 시신경 유두 발적이면서 시력이 양호한 경우, 울혈 유두를 반드시 감별에 포함해야 함. 울혈 유두는 말기에 이르지 않는 한 시력이 정상에 가깝습니다.
유두부종의 중증도는 Frisén 척도(0~5기)로 평가하며, 시기능 예후의 지표로 사용됩니다.
0~1기
0기(정상): 비측, 상측, 하측 경계 불명확. 방사상 신경섬유층.
1기(매우 초기): 유두 비측 경계의 불명확화. 경계 융기 없음. 미묘한 회색 후광. 동심원 또는 방사상 맥락막 주름.
2~3기
2기(초기): 모든 경계의 불명확화. 코쪽 경계의 융기. 완전한 유두주변 후광.
3기(중등도): 유두 직경 증가. 주요 혈관의 일부 분절 불명확화. 후광 외연에 손가락 모양 연장.
4~5기
4기(현저): 유두 전체의 융기. 유두 위 주요 혈관 분절의 완전 불명확화.
5기(중증): 돔 모양 돌출. 후광은 좁고 경계가 매끄러움. 생리적 함몰 소실.
TVO는 유두부종의 특징적인 증상이지만, 그 자체가 시력 상실의 직접적인 예후 인자는 아닙니다. 그러나 두개내압 항진이 장기간 지속되면 심한 주변 시야 결손에서 중심 시력 저하로 진행될 수 있습니다. TVO가 자주 나타나는 경우 신속히 전문의를 방문하여 원인을 정밀 검사하는 것이 중요합니다.
유두부종의 형성 속도는 두개내압 상승 속도에 의존합니다. 완만한 ICP 상승에서는 수주에 걸쳐 나타나고, 급격한 상승에서는 수시간~1일 이내에 나타나기도 합니다.
IIH의 경우, 5~10%의 체중 감소가 ICP 증상과 유두부종을 개선시킵니다. ICP 정상화(관해)에는 체중의 24% 감량이 필요하며(IIHWT의 per protocol 분석)15), 생활습관 개선만으로 어려운 경우 비만 수술도 선택지가 됩니다. 체중 관리는 보존적 치료의 일부이며, 유두부종의 정도와 시기능 장애 유무에 따라 약물 치료나 수술적 치료와 병행이 필요할 수 있습니다.
검안경으로 양안의 유두부종을 확인한 후, 형광안저촬영, OCT, CT/MRI+조영 MRV, 요추천자(LP) 순서로 평가합니다. 먼저 악성 고혈압 배제를 위해 혈압을 측정하고, 응급 영상 검사(CT→MRI+조영 MRV)로 점유 병변과 정맥동 혈전증을 평가합니다. 뇌탈출 위험이 없음을 확인한 후 LP를 시행합니다.
MRI+조영 MRV가 최적이며, IIH에서는 정맥동 협착·폐쇄 평가가 필수입니다. 고ICP 징후로 다음을 평가합니다.
| 기준 | 내용 |
|---|---|
| 1. 유두부종 | 양안성 유두부종 존재 |
| 2. 신경학적 검사 | 뇌신경 이상 외에는 정상 |
| 3. 신경영상 | 뇌실질 정상, 뇌실 확장 없음, 종괴 없음, 비정상 조영 증강 없음 |
| 4. 뇌척수액 조성 | 정상 |
| 5. 뇌척수액 초기압력 | 성인 ≥250 mmH2O, 소아 ≥280 mmH2O |
의심 진단: 양측 유두부종 존재 + 기준 1-4 충족하나 뇌척수액 압력이 기준 미만인 경우. 25-30 cmH2O는 회색 지대로 재평가 권장.
IIH 진단의 17.8%가 부정확하거나 성급하며, 13.0%가 오진이라는 보고가 있습니다18). 비전형 환자(남성, 정상 BMI, 소아)에서 MRV 미시행(42.4%)이 가장 흔한 오진 원인이며, CVST 누락이 가장 많습니다.
가성유두부종은 고도 원시, 드루젠, 경사 시신경유두, 유수신경섬유, 과오종 등이 원인이 될 수 있습니다. 다음 소견이 가성유두부종을 시사합니다.
감별 진단 목록: 매몰 드루젠, 경사 유두, 당뇨병성 유두병증, 고혈압성 유두병증, 후부 공막염, 시신경주위염, 포도막염(유육종증, VKH), 시신경염, 갑상선 안병증, CRVO, NAION, 침윤성 시신경병증, 시신경초 수막종.
유두부종 환자의 10%에서 치료 가능한 철결핍성 빈혈이 발견된다고 보고되어 있으며, 선별검사가 권장됩니다.
울혈유두(ICP 상승으로 인한 유두부종)에서는 초기에 시력이 정상으로 유지될 수 있습니다. 이는 ICP 상승이 시신경유두의 축삭류를 정체시키더라도 구심성 시기능에 미치는 영향이 경미한 단계이기 때문입니다. 반면, 시신경염에서는 급성 시력 저하가 발생하기 쉬우며, 이 차이가 감별의 단서가 됩니다.
치료의 세 가지 목표는 ① 근본 원인의 치료, ② 시기능의 보존, ③ 증상 완화(두통 등)입니다.
조기에 두개내압이 하강하면 유두부종은 신속히 흡수되어 시기능 장애를 남기지 않습니다. 치료가 지연되어 시기능 장애가 나타나면 비가역적이 됩니다.
| 약제 | 용량 | 비고 |
|---|---|---|
| 아세타졸아미드 (1차 선택) | 250 | IIHTT(2014)에서 경도 시야장애 IIH에 유효성 입증16). 두통에 대한 일관된 효과 없음. 일본에서는 보험 적용 안 됨. |
| 토피라메이트 (2차 선택) | 개별 조정 | ICP 감소 + 체중 감량 촉진 효과. 편두통성 두통에도 유용. 기형 유발 가능성 → 임신부 금기. |
| 푸로세미드 | 보조적 사용 | ACZ 불내성 시 대체 약물. |
| 메틸프레드니솔론 IV | 1 g/일 x 3일 | 전격형 IIH에 한해 일시적 조치. 북미에서 사용되는 관행 있음. |
ACZ의 주요 부작용: 감각 이상 (손발 저림), 미각 장애 (금속 맛), 소화기 증상 (메스꺼움, 구토, 설사), 피로, 신장 결석. 만성 보상성 대사성 산증, 경도 저칼륨혈증.
| 술식 | 시력 개선율 | 두통 개선율 | 주요 합병증 |
|---|---|---|---|
| 시신경초 개창술(ONSF) | 59% | 44% | 합병증 10 |
| 뇌척수액 단락술(LPS/VPS) | 54% | 80% | 단락 실패 43~50%, 감염, 전위1) |
| 경질막 정맥동 스텐트 삽입술(VSS) | 78% | 82~83% | 수술 후 6개월간 항혈소판 요법 필수. 재수술률 10~18%1) |
| 비만 수술 | — | — | IIHWT 무작위 대조 시험에서 2년간 ICP 감소 및 체중 감소 지속15) |
VSS(경막정맥동 스텐트)의 적응증: 횡정맥동 협착 및 압력 구배 >8 mmHg 확인 시. ONSF는 ICP를 낮추지 않습니다. 편측 ONSF만으로는 반대측에 대한 효과가 불충분할 수 있습니다. 요추-복막(LP) 션트가 IIH의 일차 수술적 중재로 자주 선택됩니다.
IIH 환자의 2~3%. 증상 발현 후 4주 이내의 급속한 시력 장애가 특징입니다. 입원 관리를 원칙으로 적극적인 내과 및 외과 치료를 시행합니다.
CSF 개방압 평균은 54.1 cmH2O(범위 29~70)6)로 매우 높습니다. Thambisetty 등의 16례 시리즈6)에서는 적극적 치료에도 불구하고 50%가 법적 실명에 이르렀고, 전례에서 잔여 시야 결손 및 시신경 위축이 남았습니다. HVF 기준 MD가 -7 dB 미만인 경우 시력 회복이 어렵습니다.1) 초기 pRNFL이 높을수록 장기 시력 예후가 불량합니다.1)
아세타졸아미드 최대 4 g/일 단독으로 FIH가 회복된 보고가 있습니다(36세 남성, BMI 47.3, CSF OP 45 cmH2O → 4개월 후 유두부종 소실, 6개월 후 양안 20/20 회복)8). FIH와 악성 고혈압이 동반된 경우 진단 지연이 평균 3.2개월이며, 최종 시력이 20/400~광각으로 매우 불량한 예후를 보일 수 있습니다7).
임신 중 IIH 유병률은 16/10만입니다. 증례의 61%가 첫 삼분기에 발생합니다9). 임신 자체는 IIH의 병인 인자로 간주되지 않습니다. 시각적 예후는 비임신 시와 동등하며, 일반적으로 고위험 임신으로 간주되지 않습니다.
예후: IIH 재발률 9~28%2). 예후 불량 인자: 체중 증가, 유두부종 중증도, 기준 두통 정도2).
아세타졸아미드는 IIH에 대한 일차 선택 약물로 효과가 입증되었지만, 뇌정맥혈전증이 원인인 경우 병태를 악화시킬 수 있으므로 금기입니다. 크립토코쿠스 수막염에서도 사용이 금기입니다. 먼저 원인을 확인하고 근본 원인별로 치료법을 선택하는 것이 필수적입니다. 일본에서는 보험 적용이 되지 않는다는 점에도 주의해야 합니다.
FDA 카테고리 C로 분류되지만, 체계적 문헌고찰에서는 선천 기형과의 인과관계가 부정적입니다9). 임신 초기에도 대량 사용(1g/일 이상)에서 기형 위험 증가가 인정되지 않았습니다. 반드시 산부인과 의사와 협의하여 사용해야 하며, 대부분의 경우 임신 20주 이후로 제한됩니다.
전격성 IIH(FIH)는 IIH의 아형으로, 증상 발현 후 4주 이내에 급속하고 심각한 시력 장애를 초래한다는 점이 다릅니다. IIH 환자의 2~3%에서 발생합니다. 일반 IIH가 비교적 완만하게 진행되는 반면, FIH는 수일 단위로 시력이 악화되며 신속한 중재 없이는 비가역적 실명에 이를 수 있습니다6).
시신경 주위 지주막하 공간의 압력이 상승하여 시신경이 압박되고 축삭류가 정체되면서 유두부종이 발생합니다. 구체적으로는 다음과 같은 경로를 따릅니다.
ICP 상승 → 시신경 주위 지주막하강 압력 상승 → 시신경 압박 → 순행성 축삭 수송 정체 → 신경 부종 (유두부종). 압력 지속 → 신경내 허혈 → 축삭 소실 → 시신경 위축 → 시력 장애. 위축기에는 죽은 신경 섬유가 부어오르지 않으므로 ICP 상승이 지속되어도 유두부종이 사라질 수 있습니다 (위축성 말기).
CSF 배출 장애 가설
거미막 과립 및 림프관 경로에서의 CSF 배출 지연이 ICP 상승을 유발합니다. 미노사이클린은 거미막 과립의 cAMP 신호를 교란하여 CSF 흡수를 감소시킵니다 13).
정맥동 압력 상승 가설
IIH 환자의 90% 이상에서 양측 횡정맥동 협착이 관찰됩니다 2). 연쇄: 비만 → 복강 내압 상승 → 흉강 내압 상승 → 뇌정맥 환류 장애 → ICP 상승. VSS의 효과가 이 가설을 지지합니다.
대사 및 호르몬 이상 가설
안드로겐 조절 이상이 관여하는 것으로 제시됩니다 2). 렙틴 과잉 → 맥락총 과활성화 → CSF 과잉 생성. GLP-1 수용체가 맥락총에 존재하며, GLP-1 RA가 랫트 모델에서 CSF 생성을 감소시키는 것으로 나타났습니다.
비만 수술 대 지역사회 체중 관리 중재의 무작위 대조 시험에서, 비만 수술군이 2년 동안 ICP 감소와 체중 감소를 지속했습니다15). 5년 후 비용 효율성도 식이 요법보다 우월했습니다. ICP 감소량은 체중 감소 폭과 상관관계가 있습니다.
엑세나타이드 등의 GLP-1RA가 IIH 치료의 새로운 후보로 주목받고 있습니다. Na⁺/K⁺-ATPase 활성 감소를 통해 맥락총에서 CSF 분비가 감소합니다. 인간에서 투여 2.5시간 후 ICP가 5.7±2.9 cmH₂O 감소(P=0.048)했다는 보고가 있습니다. 체중 감소 촉진 효과와 ICP 직접 감소 효과의 이중 메커니즘이 기대됩니다. 다만 중단 후 체중 반등 → IIH 발병 위험에도 주의가 필요합니다.
횡정맥동 스텐트 삽입은 안전하고 효과적이라는 보고가 축적되고 있습니다4, 5). 영국에서 VSS 대 VPS를 비교하는 RCT가 진행 중입니다. VSS의 시력 개선율 78%, 두통 개선율 8283%(메타분석). 재수술률은 1018% 범위입니다.
11β-HSD1(11β-하이드록시스테로이드 탈수소효소 1형) 억제제가 IIH의 새로운 치료 표적으로 연구 중입니다1).
“4주 이내”라는 시간 기준 대신 “시력 위협성”에 기반한 정의를 제안하는 논의가 있습니다1). 시간 기준으로는 빠른 진행에도 불구하고 진단에서 누락되는 사례가 있을 수 있습니다.
기존 위험 프로필에 해당하지 않는 환자에서 유두부종이 보고되었습니다1). 비비만·비여성에서의 IIH, MIS-C(소아 다계통 염증 증후군) 관련, 아스트라제네카 백신 후 VITT 등이 있습니다.
미국 내에서 유의한 주 간 차이가 확인되었습니다(Moran I = 0.20, P = 0.03)3). 텍사스, 오클라호마 등에서는 비만율이 높지만 IIH가 낮은 불일치도 관찰되었으며, 그 원인은 아직 밝혀지지 않았습니다.
Bonelli L, Menon V, Arnold AC, Mollan SP. Managing idiopathic intracranial hypertension in the eye clinic. Eye. 2024;38:2472-2481.
Toshniwal SS, Kinkar J, Chadha Y, et al. Navigating the enigma: a comprehensive review of idiopathic intracranial hypertension. Cureus. 2024;16(3):e56256.
Fraz MA, Kim BM, Chen JJ, et al. Nationwide prevalence and geographic variation of idiopathic intracranial hypertension among women in the United States. Ophthalmology. 2025;132:476-483.
Ghorbani M, Griessenauer CJ, Wipplinger C, et al. Intracranial hypertension and papilledema secondary to an unruptured arteriovenous malformation: review of the literature. Neuroradiol J. 2025;38(4):387-393.
Waser B, Wood HM, Mews P, Lalloo S. Transverse sinus stenting for treatment of papilloedema secondary to a large brain herniation into a dural venous sinus with associated tectal plate lesion: case report and literature review. Interv Neuroradiol. 2021;27(6):756-762.
Thambisetty M, Lavin PJ, Newman NJ, Biousse V. Fulminant idiopathic intracranial hypertension. Neurology. 2007;68(3):229-232.
Aldhahwani B, Shah SM, Jiang H, Lam BL. Severe visual loss from concurrent fulminant idiopathic intracranial hypertension and malignant arterial hypertension: prompt suspicion matters. Am J Ophthalmol Case Reports. 2024;36:102201.
Srivastava O, Micieli JA. Resolution of fulminant idiopathic intracranial hypertension treated with acetazolamide. Case Rep Neurol. 2022;14:432-436.
Palermo M, Trevisi G, D’Arrigo S, Sturiale CL. Idiopathic intracranial hypertension in pregnancy: a systematic review on clinical course, treatments, delivery and maternal-fetal outcome. Eur J Neurol. 2025;32:e70186.
Alves S, Sousa N, Cardoso L, Alves J. Multidisciplinary management of idiopathic intracranial hypertension in pregnancy: case series and narrative review. Braz J Anesthesiol. 2022;72(6):790-794.
Regev T, Fried-Regev N, Leeman S, et al. Transverse venous sinus stenting for fulminant idiopathic intracranial hypertension during pregnancy: a report of two cases and literature review. Quant Imaging Med Surg. 2025;15(5):4796-4815.
Selvaraj J, Veeranki V, Kommaraju SY, et al. Abortion and fulminant idiopathic intracranial hypertension. Cureus. 2021;13(2):e13501.
Paramo R, Leishangthem L. Optic atrophy secondary to minocycline-induced idiopathic intracranial hypertension. BMJ Case Rep. 2023;16:e252731.
Mollan SP, Davies B, Silver NC, et al. Idiopathic intracranial hypertension: consensus guidelines on management. J Neurol Neurosurg Psychiatry. 2018;89(10):1088-1100.
Mollan SP, Mitchell JL, Ottridge RS, et al. Effectiveness of bariatric surgery vs community weight management intervention for the treatment of idiopathic intracranial hypertension: a randomized clinical trial. JAMA Neurol. 2021;78:678-686.
Wall M, McDermott MP, Kieburtz KD, et al. Effect of acetazolamide on visual function in patients with idiopathic intracranial hypertension and mild visual loss: the idiopathic intracranial hypertension treatment trial. JAMA. 2014;311:1641-1651.
Pasricha SV, Bhayana R, Wu PE. Supine headache and papilledema: a case and review of cerebral venous sinus thrombosis. Clin Case Rep. 2023;11:e07329.
Fisayo A, Bruce BB, Newman NJ, Biousse V. Overdiagnosis of idiopathic intracranial hypertension. Neurology. 2016;86:341-350.