Evre 0-1
Evre 0 (Normal): Nazal, üst ve alt sınırlar bulanık. Radyal sinir lifi tabakası.
Evre 1 (Çok erken): Disk nazal sınırında bulanıklaşma. Sınırda kabarıklık yok. Hafif gri hale. Eşmerkezli ve radyal koroid kıvrımları.

Papilödem, kafa içi basıncının (ICP) artmasına bağlı iki taraflı optik disk ödemidir. «Papilödem (choked disc)» terimi yalnızca ICP artışı için kullanılır; diğer nedenlere bağlı disk şişmesi «optik disk ödemi (optic disc edema)» olarak adlandırılır. Optik sinir çevresindeki subaraknoid boşlukta basınç artışı siniri sıkıştırarak aksoplazmik akımı durdurur ve disk ödemine yol açar.
IIH’nin yıllık insidansı 1.15/100.000’dir (ABD 1997-2016 verileri, kadınlarda 1.97, erkeklerde 0.36) 2) ve en sık 18-44 yaş arasında görülür (2.47/100.000). ABD’de 18-55 yaş kadınlarda prevalans 3.44/10.000’dir (%95 GA 2.61-5.39) 3). Irksal olarak, insidans siyahlarda 2.05 > beyazlarda 1.04 > Hispaniklerde 0.67 > Asya/Pasifik Adalılarında 0.16 (100.000’de) şeklindedir 2) ve obezite prevalansı ile coğrafi olarak kabaca uyumludur (Moran I=0.20, P=0.03) 3).
Normal ICP erişkinlerde <250 mmH2O, çocuklarda <280 mmH2O’dur. Fulminan IIH (FIH), tüm IIH hastalarının %2-3’ünde görülür ve semptom başlangıcından itibaren 4 hafta içinde hızlı görme kaybı ile karakterize acil bir durumdur. 1)
Papilödem (papilledema) terimi yalnızca kafa içi basınç (KİB) artışına bağlı durumlar için kullanılır; diğer nedenlerle (optik nörit, iskemi, infiltratif lezyonlar vb.) oluşan optik disk şişmesi ise «optik disk ödemi (optic disc edema)» olarak adlandırılır. Bu terim ayrımı, etiyolojinin belirlenmesi ve uygun tedavinin seçimi açısından önemlidir.
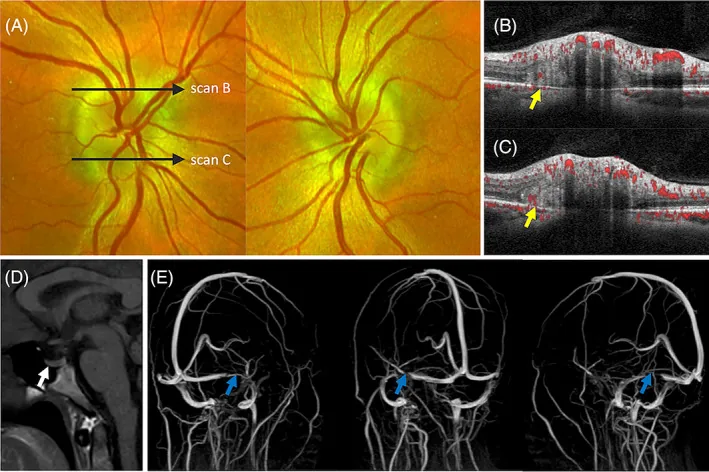
Akut papilödem erken dönemde genellikle semptomsuzdur ve santral görme fonksiyonu (en iyi düzeltilmiş görme keskinliği, renk görme) genellikle korunur.
Çocuklarda, iki taraflı abdusens sinir felcine bağlı içe şaşılık ile kafa içi basınç artışı sıklıkla tespit edilir.
Akut papilödemde fundus bulguları:
Kronik papilödemde ek bulgular: Optik disk solukluğu, gliozis, optosilier şant damarları, refraktil cisimler. Kronik evrede ölü sinir lifleri şişmez, bu nedenle kafa içi basınç artışı devam etse bile ödem kaybolabilir (atrofik son dönem).
Çift taraflı optik disk kızarıklığı ve iyi görme keskinliği varsa, mutlaka konjestif papilödem ayırıcı tanıya dahil edilmelidir. Konjestif papilödemde görme, son döneme kadar normale yakındır.
Papilödem şiddeti Frisén skalası (evre 0-5) ile değerlendirilir ve görsel prognoz göstergesi olarak kullanılır.
Evre 0-1
Evre 0 (Normal): Nazal, üst ve alt sınırlar bulanık. Radyal sinir lifi tabakası.
Evre 1 (Çok erken): Disk nazal sınırında bulanıklaşma. Sınırda kabarıklık yok. Hafif gri hale. Eşmerkezli ve radyal koroid kıvrımları.
Evre 2-3
Evre 2 (erken): Tüm sınırların bulanıklaşması. Nazal sınırda kabarıklık. Tam peripapiller hale.
Evre 3 (orta): Papil çapında artış. Ana damarların bazı segmentlerinin bulanıklaşması. Halenin dış kenarında parmak şeklinde uzantılar.
Evre 4-5
Evre 4 (belirgin): Tüm papilin kabarıklığı. Papil üzerindeki ana damar segmentlerinin tamamen bulanıklaşması.
Evre 5 (şiddetli): Kubbe şeklinde çıkıntı. Hale dar ve sınırları düzgün. Fizyolojik çukurluğun kaybolması.
TVO, papil ödeminin karakteristik bir belirtisidir ancak kendi başına görme kaybının doğrudan bir habercisi değildir. Bununla birlikte, kafa içi basınç artışı uzun süre devam ederse, ciddi periferik görme alanı defektinden merkezi görme azalmasına ilerleyebilir. TVO sık görülüyorsa, nedenin araştırılması için hızlıca bir uzmana başvurmak önemlidir.
Papil ödeminin oluşma hızı, kafa içi basıncının yükselme hızına bağlıdır. Yavaş KİBAS artışında haftalar içinde ortaya çıkarken, ani artışta birkaç saat ila bir gün içinde ortaya çıkabilir.
IIH durumunda, %5-10 kilo kaybı ICP semptomlarını ve papilödemini iyileştirir. ICP’nin normalleşmesi (remisyon) için vücut ağırlığının %24 oranında azaltılması gerekir (IIHWT per protokol analizi)15) ve yalnızca yaşam tarzı değişiklikleriyle bunu başarmak zorsa, obezite cerrahisi de bir seçenektir. Kilo yönetimi yalnızca konservatif tedavinin bir parçasıdır ve papilödemin derecesine ve görme bozukluğunun varlığına bağlı olarak ilaç tedavisi veya cerrahi tedavi ile kombinasyon gerekebilir.
Değerlendirme sırası: Oftalmoskopla iki taraflı papilödemin doğrulanması → Floresein anjiyografi → OCT → BT/MRG + kontrastlı MRV → Lomber ponksiyon (LP). Önce malign hipertansiyonu dışlamak için kan basıncı ölçülür ve acil görüntüleme (BT → MRG + kontrastlı MRV) ile yer kaplayan lezyonlar ve venöz sinüs trombozu değerlendirilir. Beyin hernisi riski olmadığı onaylandıktan sonra LP yapılır.
MRG + kontrastlı MRV en iyisidir ve IIH’de venöz sinüs darlığı/tıkanıklığının değerlendirilmesi zorunludur. Yüksek ICP belirtileri şunları içerir:
| Kriter | İçerik |
|---|---|
| 1. Papilödem | Bilateral papilödem mevcut |
| 2. Nörolojik muayene | Kranial sinir anormalliği dışında normal |
| 3. Nörogörüntüleme | Beyin parankimi normal, ventriküler genişleme yok, kitle yok, anormal kontrast tutulumu yok |
| 4. BOS bileşimi | Normal |
| 5. BOS açılış basıncı | Erişkin ≥250 mmH2O, çocuk ≥280 mmH2O |
Şüpheli tanı: Bilateral papilödem + kriter 1-4’ü karşılar ancak BOS basıncı kriterin altındadır. 25-30 cmH2O gri bölge olarak kabul edilir ve yeniden değerlendirme önerilir.
IIH tanılarının %17.8’inin yanlış veya aceleyle konulduğu ve %13.0’ının hatalı olduğu bildirilmiştir 18). Atipik hastalarda (erkek, normal BMI, çocuk) en sık hata nedeni MRV yapılmamasıdır (%42.4) ve en sık CVST’nin gözden kaçırılmasıdır.
Psödoödem papilla, yüksek hipermetropi, drusen, eğimli disk, miyelinli sinir lifleri, hamartom gibi nedenlerden kaynaklanabilir. Aşağıdaki bulgular psödoödem papilla’yı düşündürür:
Ayırıcı tanı listesi: Gömülü drusen, eğimli disk, diyabetik papillopati, hipertansif papillopati, arka sklerit, perinörit, üveit (sarkoidoz, VKH), optik nörit, tiroid oftalmopatisi, CRVO, NAION, infiltratif optik nöropati, optik sinir kılıfı menenjiyomu.
Papilödemli hastaların %10’unda tedavi edilebilir demir eksikliği anemisi olduğu bildirilmiştir ve tarama önerilir.
Konjestif papilödemde (ICP artışına bağlı papilödem) erken dönemde görme normal kalabilir. Bunun nedeni, ICP artışının optik diskte aksoplazmik akışı durdurmasına rağmen, afferent görme fonksiyonu üzerindeki etkinin erken evrede hafif olmasıdır. Öte yandan, optik nöritte akut görme azalması sık görülür ve bu fark ayırıcı tanıda ipucu sağlar.
Tedavinin üç hedefi: ① Altta yatan nedenin tedavisi, ② Görme fonksiyonunun korunması, ③ Semptomların hafifletilmesi (baş ağrısı gibi).
Kafa içi basıncı erken düşürülürse papilödem hızla emilir ve görme fonksiyon bozukluğu kalmaz. Tedavi gecikir ve görme fonksiyon bozukluğu ortaya çıkarsa, bu geri dönüşümsüz olur.
| İlaç | Doz | Notlar |
|---|---|---|
| Asetazolamid (birinci basamak) | 250-500 mg 2x/gün → maksimum 2-4 g/gün | IIHTT (2014) hafif görme alanı defekti olan IIH’de etkinliği kanıtlamıştır16). Baş ağrısı üzerinde tutarlı etkisi yoktur. Japonya’da sigorta kapsamı dışındadır |
| Topiramat (ikinci basamak) | Bireysel ayarlama | KİBAS düşürücü + kilo verme etkisi. Migren benzeri baş ağrılarında da faydalıdır. Teratojenik → gebelikte kontrendikedir |
| Furosemid | Yardımcı kullanım | ACZ intoleransında alternatif |
| Metilprednizolon IV | 1 g/gün x 3 gün | Sadece fulminan IIH’de geçici önlem. Kuzey Amerika’da kullanılan bir uygulamadır |
ACZ’nin başlıca yan etkileri: parestezi (ellerde/ayaklarda uyuşma), tat bozukluğu (metalik tat), gastrointestinal semptomlar (bulantı, kusma, ishal), yorgunluk, böbrek taşı. Kronik kompanse metabolik asidoz, hafif hipokalemi.
| Cerrahi yöntem | Görme iyileşme oranı | Baş ağrısı iyileşme oranı | Başlıca komplikasyonlar |
|---|---|---|---|
| Optik sinir kılıfı fenestrasyonu (ONSF) | %59 | %44 | Komplikasyon %10-15 (CRAO/CRVO’ya bağlı %1-2 görme kaybı dahil). 1 yılda %34, 3 yılda %45 nüks oranı1) |
| BOS şantı (LPS/VPS) | %54 | %80 | Şant yetmezliği %43-50, enfeksiyon, yer değiştirme1) |
| Dura venöz sinüs stentlemesi (VSS) | %78 | %82-83 | Ameliyat sonrası 6 ay antiplatelet tedavi zorunludur. Tekrar ameliyat oranı %10-181) |
| Obezite cerrahisi | — | — | IIHWT RCT’de 2 yıl boyunca sürekli BKB düşüşü ve kilo kaybı15) |
VSS (Venöz Sinüs Stenti) Endikasyonu: Transvers sinüs darlığı + basınç gradiyenti >8 mmHg doğrulandığında. ONSF, BKB’yi düşürmez. Tek taraflı ONSF’nin karşı tarafa yetersiz etkisi olabilir. Lomber-peritoneal (LP) şant, IIH’de birincil cerrahi müdahale olarak sıklıkla tercih edilir.
IIH hastalarının %2-3’ü. Semptom başlangıcından itibaren 4 hafta içinde hızlı görme kaybı ile karakterizedir. Hastanede yatış ve agresif medikal/cerrahi tedavi prensiptir.
Ortalama BOS açılış basıncı 54.1 cmH2O (aralık 29-70) 6) ile son derece yüksektir. Thambisetty ve ark. 16 vakalık serisinde 6), agresif tedaviye rağmen %50’si yasal körlüğe ulaştı ve tüm vakalarda kalıcı görme alanı defekti ve optik atrofi kaldı. HVF başlangıç MD’si -7 dB’nin altında ise görme iyileşmesi zordur. 1) Yüksek başlangıç pRNFL, daha kötü uzun dönem görme prognozu ile ilişkilidir. 1)
Sadece asetazolamid maksimum 4 g/gün ile FIH iyileşmesi bildirilmiştir (36 yaşında erkek, BMI 47.3, BOS OP 45 cmH2O → 4 ayda papilödem kayboldu, 6 ayda bilateral 20/20 görme) 8). FIH ve malign hipertansiyon birlikteliğinde tanı gecikmesi ortalama 3.2 ay olur ve nihai görme 20/400 ile ışık hissi arasında son derece kötü prognozlu olabilir 7).
Gebelikte IIH prevalansı 16/100.000’dir. Vakaların %61’i ilk trimesterde ortaya çıkar 9). Gebelik, IIH için etiyolojik bir faktör olarak kabul edilmez. Görsel prognoz gebe olmayanlarla benzerdir ve genellikle yüksek riskli gebelik olarak değerlendirilmez.
Prognoz: IIH nüks oranı %9-282). Kötü prognoz faktörleri: kilo alımı, papilödem şiddeti, bazal baş ağrısı şiddeti2).
Asetazolamid, IIH için birinci basamak ilaç olarak etkinliği kanıtlanmıştır, ancak serebral ven trombozuna bağlı vakalarda durumu kötüleştirebileceğinden kontrendikedir. Kriptokok menenjitinde de kontrendikedir. Öncelikle neden belirlenmeli ve tedavi altta yatan nedene göre seçilmelidir. Japonya’da sigorta kapsamında olmadığı da unutulmamalıdır.
FDA Kategori C’de sınıflandırılmasına rağmen, sistematik derleme konjenital anomalilerle nedensel ilişkiyi reddetmektedir9). İlk trimesterde bile yüksek doz (≥1 g/gün) kullanımında anomali riskinde artış gözlenmemiştir. Mutlaka kadın doğum uzmanı ile konsültasyon halinde kullanılmalı ve genellikle gebeliğin 20. haftasından sonrasıyla sınırlıdır.
FIH, IIH’nin bir alt tipidir ve semptom başlangıcından itibaren 4 hafta içinde hızlı ve ciddi görme kaybı ile karakterizedir. IIH hastalarının %2-3’ünde görülür. Normal IIH nispeten yavaş ilerlerken, FIH birkaç gün içinde görme kaybına yol açar ve acil müdahale olmaksızın geri dönüşümsüz körlüğe neden olabilir6).
Optik sinir çevresindeki subaraknoid boşlukta artan basınç, optik siniri sıkıştırarak aksonal akışın durmasına ve papilödeme neden olur. Spesifik yol aşağıdaki gibidir:
ICP artışı → optik sinir çevresindeki subaraknoid boşluk basıncında artış → optik sinir sıkışması → anterograd aksonal taşımada durma → sinir ödemi (papilödem). Basıncın devamı → sinir içi iskemi → akson kaybı → optik atrofi → görme bozukluğu. Atrofi evresinde ölü sinir lifleri şişmez, bu nedenle ICP yüksekliği devam etse bile papilödem kaybolabilir (atrofik son dönem).
BOS boşaltım bozukluğu hipotezi
Araknoid granülasyonlar ve lenfatik yollarda BOS boşaltımında gecikme ICP artışına neden olur. Minosiklin, araknoid granülasyonlardaki cAMP sinyalini bozarak BOS emilimini azaltır13).
Venöz sinüs basıncı artışı hipotezi
IIH hastalarının %90’ından fazlasında bilateral transvers sinüs darlığı görülür2). Obezite → intraabdominal basınç artışı → intratorasik basınç artışı → serebral venöz dönüş bozukluğu → ICP artışı zinciri. VSS’nin etkinliği bu hipotezi destekler.
Metabolik ve hormonal anormallik hipotezi
Androjen düzensizliğinin rolü öne sürülmektedir2). Aşırı leptin → koroid pleksus aşırı aktivasyonu → aşırı BOS üretimi. GLP-1 reseptörü koroid pleksusta bulunur ve GLP-1RA’nın sıçan modelinde BOS üretimini azalttığı gösterilmiştir.
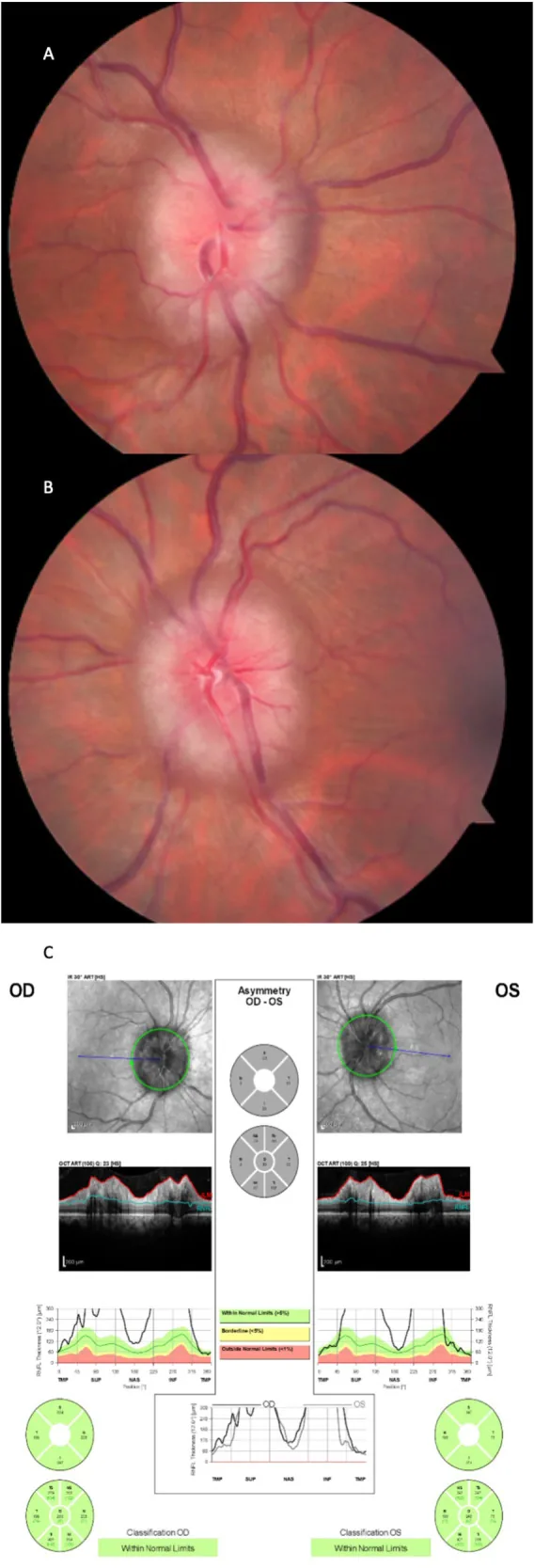
Obezite cerrahisi ile bölgesel kilo yönetimi müdahalesini karşılaştıran randomize kontrollü çalışmada, obezite cerrahisi grubu iki yıl boyunca sürekli ICP düşüşü ve kilo kaybı gösterdi15). Beş yıl sonraki maliyet etkinlik de diyet tedavisine göre üstündü. ICP düşüş miktarı kilo kaybı miktarı ile koreleydi.
Eksenatid gibi GLP-1RA’lar IIH tedavisi için yeni adaylar olarak dikkat çekmektedir. Na⁺/K⁺-ATPaz aktivitesini azaltarak koroid pleksusta BOS sekresyonunu azaltırlar. İnsanlarda uygulamadan 2.5 saat sonra ICP’de 5.7±2.9 cmH₂O düşüş (P=0.048) bildirilmiştir. Kilo kaybını teşvik edici etki ve doğrudan ICP düşürücü etki olmak üzere çift mekanizma beklenmektedir. Ancak tedavi kesildikten sonra kilo geri alımı ve buna bağlı IIH gelişme riskine dikkat edilmelidir.
Transvers sinüs stentlemenin güvenli ve etkili olduğuna dair raporlar birikmektedir4, 5). İngiltere’de VSS’yi ventriküloperitoneal şant (VPS) ile karşılaştıran randomize kontrollü bir çalışma devam etmektedir. VSS ile görme iyileşme oranı %78, baş ağrısı iyileşme oranı %82-83 (meta-analiz). Tekrar cerrahi oranı %10-18 aralığındadır.
11β-HSD1 (11β-hidroksisteroid dehidrogenaz tip 1) inhibitörleri, IIH için yeni tedavi hedefleri olarak araştırılmaktadır1).
Zamansal kriter olan ‘dört hafta içinde’ yerine ‘görme tehdit edici’ temelli bir tanım öneren tartışmalar bulunmaktadır1). Zamansal kriter, hızlı ilerlemeye rağmen tanıdan kaçan vakaların olabileceği anlamına gelir.
Geleneksel risk profiline uymayan hastalarda papilödem bildirilmiştir 1). Obez olmayan ve kadın olmayan bireylerde IIH, MIS-C (çocuklarda multisistem inflamatuar sendrom) ile ilişkili ve AstraZeneca aşısı sonrası VITT gibi.
ABD içinde eyaletler arasında anlamlı farklılıklar tespit edilmiştir (Moran I=0.20, P=0.03) 3). Teksas ve Oklahoma gibi yerlerde yüksek obezite oranına karşın düşük IIH görülmesi gibi bir uyumsuzluk da gözlenmiş olup nedeni bilinmemektedir.
Bonelli L, Menon V, Arnold AC, Mollan SP. Managing idiopathic intracranial hypertension in the eye clinic. Eye. 2024;38:2472-2481.
Toshniwal SS, Kinkar J, Chadha Y, et al. Navigating the enigma: a comprehensive review of idiopathic intracranial hypertension. Cureus. 2024;16(3):e56256.
Fraz MA, Kim BM, Chen JJ, et al. Nationwide prevalence and geographic variation of idiopathic intracranial hypertension among women in the United States. Ophthalmology. 2025;132:476-483.
Ghorbani M, Griessenauer CJ, Wipplinger C, et al. Intracranial hypertension and papilledema secondary to an unruptured arteriovenous malformation: review of the literature. Neuroradiol J. 2025;38(4):387-393.
Waser B, Wood HM, Mews P, Lalloo S. Transverse sinus stenting for treatment of papilloedema secondary to a large brain herniation into a dural venous sinus with associated tectal plate lesion: case report and literature review. Interv Neuroradiol. 2021;27(6):756-762.
Thambisetty M, Lavin PJ, Newman NJ, Biousse V. Fulminant idiopathic intracranial hypertension. Neurology. 2007;68(3):229-232.
Aldhahwani B, Shah SM, Jiang H, Lam BL. Severe visual loss from concurrent fulminant idiopathic intracranial hypertension and malignant arterial hypertension: prompt suspicion matters. Am J Ophthalmol Case Reports. 2024;36:102201.
Srivastava O, Micieli JA. Resolution of fulminant idiopathic intracranial hypertension treated with acetazolamide. Case Rep Neurol. 2022;14:432-436.
Palermo M, Trevisi G, D’Arrigo S, Sturiale CL. Idiopathic intracranial hypertension in pregnancy: a systematic review on clinical course, treatments, delivery and maternal-fetal outcome. Eur J Neurol. 2025;32:e70186.
Alves S, Sousa N, Cardoso L, Alves J. Multidisciplinary management of idiopathic intracranial hypertension in pregnancy: case series and narrative review. Braz J Anesthesiol. 2022;72(6):790-794.
Regev T, Fried-Regev N, Leeman S, et al. Transverse venous sinus stenting for fulminant idiopathic intracranial hypertension during pregnancy: a report of two cases and literature review. Quant Imaging Med Surg. 2025;15(5):4796-4815.
Selvaraj J, Veeranki V, Kommaraju SY, et al. Abortion and fulminant idiopathic intracranial hypertension. Cureus. 2021;13(2):e13501.
Paramo R, Leishangthem L. Optic atrophy secondary to minocycline-induced idiopathic intracranial hypertension. BMJ Case Rep. 2023;16:e252731.
Mollan SP, Davies B, Silver NC, et al. Idiopathic intracranial hypertension: consensus guidelines on management. J Neurol Neurosurg Psychiatry. 2018;89(10):1088-1100.
Mollan SP, Mitchell JL, Ottridge RS, et al. Effectiveness of bariatric surgery vs community weight management intervention for the treatment of idiopathic intracranial hypertension: a randomized clinical trial. JAMA Neurol. 2021;78:678-686.
Wall M, McDermott MP, Kieburtz KD, et al. Effect of acetazolamide on visual function in patients with idiopathic intracranial hypertension and mild visual loss: the idiopathic intracranial hypertension treatment trial. JAMA. 2014;311:1641-1651.
Pasricha SV, Bhayana R, Wu PE. Supine headache and papilledema: a case and review of cerebral venous sinus thrombosis. Clin Case Rep. 2023;11:e07329.
Fisayo A, Bruce BB, Newman NJ, Biousse V. Overdiagnosis of idiopathic intracranial hypertension. Neurology. 2016;86:341-350.