مرحله ۰ تا ۱
مرحله ۰ (طبیعی): مرزهای بینی، فوقانی و تحتانی تار. لایه فیبرهای عصبی شعاعی.
مرحله ۱ (بسیار اولیه): تار شدن مرز بینی دیسک. بدون برجستگی مرز. هاله خاکستری ظریف. چینهای کوروئید متحدالمرکز و شعاعی.

پاپیادم تورم دیسک بینایی دوطرفه ناشی از افزایش فشار داخل جمجمه (ICP) است. اصطلاح «papilledema (choked disc)» منحصراً برای افزایش ICP استفاده میشود و تورم دیسک به دلایل دیگر «ادم دیسک بینایی (optic disc edema)» نامیده میشود. افزایش فشار در فضای زیرعنکبوتیه اطراف عصب بینایی باعث فشردگی عصب و توقف جریان آکسوپلاسمی میشود که منجر به تورم دیسک میگردد.
بروز سالانه IIH 1.15 در 100,000 نفر است (دادههای ایالات متحده 1997-2016، زنان 1.97 در مقابل مردان 0.36) 2) و بیشترین میزان در سنین 18-44 سال (2.47 در 100,000) است. شیوع در زنان 18-55 ساله ایالات متحده 3.44 در 10,000 نفر (95% CI 2.61-5.39) است 3). از نظر نژادی، میزان بروز در سیاهپوستان 2.05 > سفیدپوستان 1.04 > اسپانیاییتبارها 0.67 > آسیاییها و جزایر اقیانوس آرام 0.16 (در 100,000) است 2) و تقریباً با شیوع چاقی همبستگی جغرافیایی دارد (Moran I=0.20, P=0.03) 3).
ICP طبیعی در بزرگسالان <250 mmH2O و در کودکان <280 mmH2O است. IIH حاد (FIH) در 2 تا 3٪ از کل بیماران IIH رخ میدهد و با کاهش سریع بینایی در عرض 4 هفته از شروع علائم، یک اورژانس است. 1)
پاپیادم (papilledema) اصطلاحی است که منحصراً به افزایش فشار داخل جمجمه (ICP) اشاره دارد و تورم دیسک بینایی ناشی از علل دیگر (مانند نوریت بینایی، ایسکمی، ضایعات نفوذی) «ادم دیسک بینایی (optic disc edema)» نامیده میشود. تمایز این اصطلاحات برای شناسایی علت و انتخاب درمان مناسب اهمیت دارد.
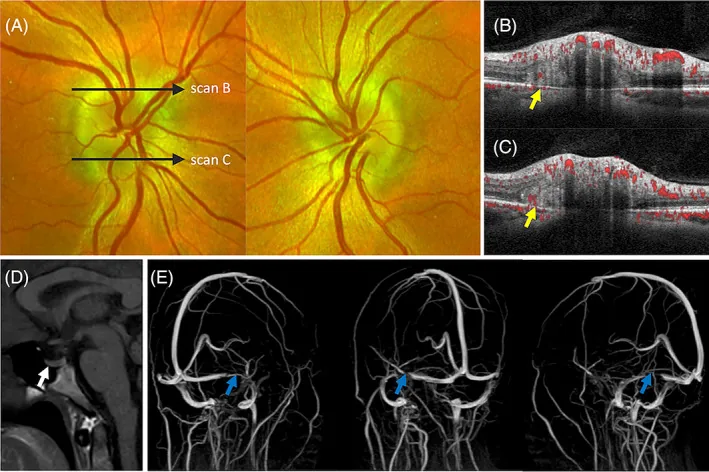
پاپیادم حاد در مراحل اولیه اغلب بدون علامت است و عملکرد بینایی مرکزی (بهترین دید اصلاح شده، دید رنگی) معمولاً حفظ میشود.
در کودکان، افزایش فشار داخل جمجمه اغلب با استرابیسم همگرا ناشی از فلج دوطرفه عصب ابدوسنس تشخیص داده میشود.
یافتههای افتالموسکوپیک در پاپیلادم حاد:
یافتههای اضافی در پاپیلادم مزمن: رنگ پریدگی دیسک بینایی، گلیوز، عروق شانت اپتو-سیلیاری، و اجسام رفراکتیو. در مرحله مزمن، فیبرهای عصبی مرده متورم نمیشوند، بنابراین حتی با ادامه افزایش فشار داخل جمجمه، ادم ممکن است ناپدید شود (مرحله نهایی آتروفیک).
در صورت قرمزی دوطرفه دیسک بینایی با دید خوب، حتماً باید پاپیلادم احتقانی را در تشخیص افتراقی در نظر گرفت. در پاپیلادم احتقانی، بینایی تا مراحل پایانی تقریباً طبیعی است.
شدت ادم دیسک با مقیاس فریزن (مرحله ۰ تا ۵) ارزیابی میشود و به عنوان شاخص پیشآگهی بینایی استفاده میشود.
مرحله ۰ تا ۱
مرحله ۰ (طبیعی): مرزهای بینی، فوقانی و تحتانی تار. لایه فیبرهای عصبی شعاعی.
مرحله ۱ (بسیار اولیه): تار شدن مرز بینی دیسک. بدون برجستگی مرز. هاله خاکستری ظریف. چینهای کوروئید متحدالمرکز و شعاعی.
مرحله ۲ تا ۳
مرحله 2 (اولیه): تار شدن تمام مرزها. برآمدگی مرز بینی. هاله کامل اطراف پاپی.
مرحله 3 (متوسط): افزایش قطر پاپی. تار شدن بخشهایی از عروق اصلی. امتدادهای انگشتمانند در لبه خارجی هاله.
مرحله 4 تا 5
مرحله 4 (قابل توجه): برآمدگی کل پاپی. تار شدن کامل بخشهای اصلی عروق روی پاپی.
مرحله 5 (شدید): برآمدگی گنبدیشکل. هاله باریک با لبه صاف. ناپدید شدن فرورفتگی فیزیولوژیک.
TVO یک علامت مشخصه ادم پاپی است، اما به خودی خود نشانه مستقیم از دست دادن بینایی نیست. با این حال، اگر افزایش فشار داخل جمجمه برای مدت طولانی ادامه یابد، میتواند از نقص شدید میدان بینایی محیطی به کاهش بینایی مرکزی پیشرفت کند. اگر TVO مکرر رخ دهد، مراجعه سریع به متخصص برای بررسی علت مهم است.
سرعت تشکیل ادم پاپی به سرعت افزایش فشار داخل جمجمه بستگی دارد. در افزایش آهسته ICP، طی چند هفته ظاهر میشود و در افزایش ناگهانی، ممکن است طی چند ساعت تا یک روز ظاهر شود.
در موارد IIH، کاهش وزن ۵ تا ۱۰ درصدی باعث بهبود علائم ICP و ادم پاپی میشود. برای نرمالسازی ICP (بهبودی) کاهش وزن ۲۴ درصدی لازم است (تحلیل per protocol IIHWT)15) و در صورت دشواری دستیابی تنها با اصلاح سبک زندگی، جراحی چاقی نیز گزینهای است. مدیریت وزن تنها بخشی از درمان محافظهکارانه است و بسته به شدت ادم پاپی و وجود اختلال بینایی، ممکن است ترکیب با دارودرمانی یا درمان جراحی لازم باشد.
ارزیابی به ترتیب: تأیید ادم پاپی دوطرفه با افتالموسکوپ → آنژیوگرافی فلورسئین → OCT → CT/MRI + MRV با کنتراست → پونکسیون کمری (LP). ابتدا فشار خون برای رد فشار خون بدخیم اندازهگیری میشود و تصویربرداری فوری (CT → MRI + MRV با کنتراست) برای ارزیابی ضایعات فضاگیر و ترومبوز سینوس وریدی انجام میشود. پس از تأیید عدم خطر فتق مغزی، LP انجام میشود.
MRI + MRV با کنتراست بهترین است و در IIH ارزیابی تنگی/انسداد سینوس وریدی ضروری است. علائم ICP بالا شامل موارد زیر است:
| معیار | شرح |
|---|---|
| 1. ادم پاپی | ادم پاپی دوطرفه وجود دارد |
| 2. معاینه عصبی | به جز ناهنجاری اعصاب مغزی، طبیعی |
| 3. تصویربرداری عصبی | پارانشیم مغز طبیعی، بدون گشادشدگی بطنی، بدون توده، بدون اثر کنتراست غیرطبیعی |
| 4. ترکیب CSF | طبیعی |
| 5. فشار اولیه CSF | بزرگسالان ≥250 mmH2O، کودکان ≥280 mmH2O |
تشخیص مشکوک: ادم پاپی دوطرفه + معیارهای 1 تا 4 را دارد اما فشار CSF کمتر از حد معیار است. 25-30 cmH2O به عنوان منطقه خاکستری توصیه به ارزیابی مجدد میشود.
گزارش شده است که 17.8% از تشخیصهای IIH نادرست یا عجولانه و 13.0% اشتباه بودهاند 18). شایعترین علت تشخیص اشتباه، عدم انجام MRV (42.4%) در بیماران غیرمعمول (مردان، BMI طبیعی، کودکان) است که منجر به نادیده گرفتن CVST میشود.
ادم کاذب پاپی میتواند ناشی از دوربینی شدید، دروزن، دیسک مایل، رشتههای عصبی میلیندار، هامارتوم و غیره باشد. یافتههای زیر به نفع ادم کاذب پاپی هستند:
فهرست تشخیصهای افتراقی: دروزن نهفته، دیسک مایل، پاپیلوپاتی دیابتی، پاپیلوپاتی فشارخونی، اسکلریت خلفی، پرینوریت، یووئیت (سارکوئیدوز، VKH)، نوریت اپتیک، افتالموپاتی تیروئیدی، CRVO، NAION، نوروپاتی نفوذی اپتیک، مننژیوم غلاف عصب اپتیک.
گزارش شده است که 10% از بیماران مبتلا به ادم پاپی دارای کمخونی فقر آهن قابل درمان هستند و غربالگری توصیه میشود.
در پاپیادم احتقانی (ادم پاپی ناشی از افزایش ICP)، بینایی ممکن است در مراحل اولیه طبیعی باقی بماند. این به این دلیل است که اگرچه افزایش ICP جریان آکسوپلاسمی در سر عصب اپتیک را مختل میکند، اما تأثیر بر عملکرد بینایی آوران در مراحل اولیه خفیف است. در مقابل، نوریت اپتیک معمولاً با کاهش حاد بینایی همراه است و این تفاوت میتواند به تشخیص افتراقی کمک کند.
سه هدف درمان عبارتند از: ① درمان علت زمینهای، ② حفظ عملکرد بینایی، و ③ تسکین علائم (مانند سردرد).
اگر فشار داخل جمجمه زودتر کاهش یابد، ادم پاپی به سرعت جذب شده و اختلال عملکرد بینایی باقی نمیماند. در صورت تأخیر در درمان و بروز اختلال عملکرد بینایی، این اختلال غیرقابل برگشت خواهد بود.
| دارو | دوز | توضیحات |
|---|---|---|
| استازولامید (خط اول) | ۲۵۰-۵۰۰ میلیگرم دو بار در روز → حداکثر ۲-۴ گرم در روز | IIHTT (2014) اثربخشی را در IIH با اختلال میدان بینایی خفیف نشان داد16). اثر ثابتی بر سردرد ندارد. در ژاپن تحت پوشش بیمه نیست |
| توپیرامات (خط دوم) | تنظیم فردی | کاهش ICP + اثر کاهش وزن. همچنین برای سردردهای میگرنی مفید است. تراتوژنیک → در بارداری منع مصرف دارد |
| فروزماید | استفاده کمکی | جایگزین در صورت عدم تحمل ACZ |
| متیلپردنیزولون وریدی | ۱ گرم در روز به مدت ۳ روز | فقط در IIH برقآسا به عنوان اقدام موقت. در آمریکای شمالی استفاده میشود |
عوارض جانبی اصلی ACZ: پارستزی (بیحسی اندامها)، اختلال چشایی (طعم فلزی)، علائم گوارشی (تهوع، استفراغ، اسهال)، خستگی، سنگ کلیه. اسیدوز متابولیک مزمن جبرانشده و هیپوکالمی خفیف.
| روش جراحی | نرخ بهبود بینایی | نرخ بهبود سردرد | عوارض اصلی |
|---|---|---|---|
| فنرتره غلاف عصب بینایی (ONSF) | 59% | 44% | عوارض 10-15% (شامل 1-2% از دست دادن بینایی به دلیل CRAO/CRVO). میزان عود مجدد 34% در یک سال و 45% در سه سال1) |
| شنت مایع مغزی-نخاعی (LPS/VPS) | 54% | 80% | نارسایی شنت 43-50%، عفونت، جابجایی1) |
| استنت گذاری سینوس وریدی سختشامه (VSS) | 78% | 82-83% | درمان ضد پلاکتی به مدت 6 ماه پس از جراحی ضروری است. میزان جراحی مجدد 10-18%1) |
| جراحی چاقی | — | — | در کارآزمایی IIHWT، کاهش ICP و کاهش وزن به مدت 2 سال پایدار بود15) |
اندیکاسیون VSS (استنت سینوس وریدی دورال): در صورت تأیید تنگی سینوس عرضی و گرادیان فشار > 8 میلیمتر جیوه. ONSF فشار داخل جمجمه را کاهش نمیدهد. ONSF یک طرفه ممکن است اثر کافی بر طرف مقابل نداشته باشد. شنت کمری-صفاقی (LP) اغلب به عنوان مداخله جراحی اولیه برای IIH انتخاب میشود.
۲ تا ۳٪ از بیماران IIH. با کاهش سریع بینایی در عرض ۴ هفته از شروع علائم مشخص میشود. بستری در بیمارستان و درمان طبی و جراحی تهاجمی اصولی است.
میانگین فشار باز شدن CSF 54.1 سانتیمتر آب (محدوده ۲۹-۷۰) 6) بسیار بالا است. در سری ۱۶ موردی Thambisetty و همکاران 6)، با وجود درمان تهاجمی، ۵۰٪ به نابینایی قانونی رسیدند و در همه موارد نقص میدان بینایی باقیمانده و آتروفی عصب بینایی وجود داشت. اگر MD پایه HVF کمتر از ۷- دسیبل باشد، بهبود بینایی دشوار است. 1) pRNFL اولیه بالاتر با پیشآگهی طولانیمدت بینایی بدتر همراه است. 1)
گزارشهایی از بهبود FIH با استازولامید به تنهایی با دوز حداکثر ۴ گرم در روز وجود دارد (مرد ۳۶ ساله، BMI 47.3، CSF OP 45 سانتیمتر آب → ناپدید شدن ادم پاپی در ۴ ماه، بهبود بینایی ۲۰/۲۰ دوطرفه در ۶ ماه) 8). در صورت ترکیب FIH با فشار خون بدخیم، تأخیر تشخیص به طور متوسط ۳.۲ ماه رخ میدهد و پیشآگهی نهایی بینایی بسیار ضعیف (۲۰/۴۰۰ تا درک نور) خواهد بود 7).
شیوع IIH در بارداری ۱۶ در ۱۰۰٬۰۰۰ است. ۶۱٪ موارد در سهماهه اول رخ میدهد 9). بارداری به خودی خود یک عامل اتیولوژیک برای IIH در نظر گرفته نمیشود. پیشآگهی بینایی مشابه با غیربارداری است و معمولاً بارداری پرخطر محسوب نمیشود.
پیشآگهی: میزان عود IIH 9 تا 28 درصد است2). عوامل پیشآگهی بد: افزایش وزن، شدت ادم پاپی، و شدت سردرد پایه2).
استازولامید به عنوان داروی خط اول برای IIH اثربخشی ثابت شدهای دارد، اما در موارد ناشی از ترومبوز وریدهای مغزی ممکن است وضعیت را بدتر کند، بنابراین منع مصرف دارد. همچنین در مننژیت کریپتوکوکی منع مصرف دارد. ابتدا باید علت مشخص شود و درمان بر اساس علت زمینهای انتخاب شود. توجه داشته باشید که در ژاپن تحت پوشش بیمه نیست.
این دارو در رده C FDA قرار دارد، اما مرور سیستماتیک ارتباط علی با ناهنجاریهای مادرزادی را رد کرده است9). حتی در سه ماهه اول با دوز بالا (≥1 گرم در روز) افزایش خطر ناهنجاری مشاهده نشد. حتماً با مشورت متخصص زنان و زایمان استفاده شود و معمولاً به بعد از هفته 20 بارداری محدود میشود.
FIH زیرگروهی از IIH است که با شروع سریع و کاهش شدید بینایی در عرض 4 هفته از شروع علائم مشخص میشود. در 2 تا 3 درصد از بیماران IIH رخ میدهد. در حالی که IIH معمولی نسبتاً آهسته پیشرفت میکند، FIH در عرض چند روز بینایی را بدتر کرده و بدون مداخله فوری میتواند به نابینایی غیرقابل برگشت منجر شود6).
افزایش فشار در فضای زیرعنکبوتیه اطراف عصب بینایی باعث فشردگی عصب بینایی و توقف جریان آکسونی میشود که منجر به ادم پاپی میگردد. مسیر دقیق به شرح زیر است:
افزایش ICP → افزایش فشار فضای زیرعنکبوتیه اطراف عصب بینایی → تنگ شدن عصب بینایی → توقف انتقال آکسونی پیشرونده → ادم عصبی (ادم پاپی). تداوم فشار → ایسکمی درون عصبی → از بین رفتن آکسونها → آتروفی عصب بینایی → اختلال بینایی. در مرحله آتروفی، فیبرهای عصبی مرده متورم نمیشوند، بنابراین حتی با ادامه افزایش ICP، ادم پاپی ممکن است ناپدید شود (مرحله نهایی آتروفیک).
فرضیه اختلال در تخلیه CSF
تأخیر در تخلیه CSF از طریق گرانولهای عنکبوتیه و مسیرهای لنفاوی منجر به افزایش ICP میشود. مینوسیکلین با اختلال در سیگنال cAMP گرانولهای عنکبوتیه، جذب CSF را کاهش میدهد13).
فرضیه افزایش فشار سینوس وریدی
بیش از 90٪ بیماران IIH تنگی دوطرفه سینوس عرضی دارند2). زنجیره: چاقی → افزایش فشار داخل شکمی → افزایش فشار داخل قفسه سینه → اختلال در بازگشت وریدی مغز → افزایش ICP. اثربخشی VSS از این فرضیه حمایت میکند.
فرضیه ناهنجاری متابولیک و هورمونی
نقش اختلال تنظیم آندروژن مطرح است2). لپتین اضافی → فعال شدن بیش از حد شبکه کوروئید → تولید بیش از حد CSF. گیرنده GLP-1 در شبکه کوروئید وجود دارد و GLP-1RA تولید CSF را در مدل موش کاهش میدهد.
در یک کارآزمایی تصادفیسازی شده که جراحی چاقی را با مداخله مدیریت وزن محلی مقایسه کرد، گروه جراحی چاقی به مدت دو سال کاهش پایدار ICP و وزن را نشان دادند15). هزینهاثربخشی پس از پنج سال نیز نسبت به رژیم غذایی برتر بود. میزان کاهش ICP با میزان کاهش وزن همبستگی داشت.
آگونیستهای GLP-1 مانند اگزناتید به عنوان کاندیدهای جدید برای درمان IIH مورد توجه قرار گرفتهاند. آنها ترشح CSF را در شبکه کوروئید از طریق کاهش فعالیت Na⁺/K⁺-ATPase کاهش میدهند. گزارش شده است که در انسان، 2.5 ساعت پس از تجویز، ICP به میزان 5.7 ± 2.9 سانتیمتر آب کاهش یافته است (P=0.048). مکانیسم دوگانه کاهش وزن و کاهش مستقیم ICP مورد انتظار است. با این حال، باید به خطر بازگشت وزن پس از قطع درمان و متعاقباً بروز IIH توجه کرد.
گزارشهای فزایندهای از ایمنی و اثربخشی استنتگذاری سینوس عرضی وجود دارد4, 5). یک کارآزمایی تصادفیسازی شده در بریتانیا در حال انجام است که VSS را با شنت بطنی-صفاقی (VPS) مقایسه میکند. نرخ بهبود بینایی با VSS 78% و بهبود سردرد 82-83% (متاآنالیز) است. محدوده نرخ جراحی مجدد 10-18% است.
مهارکنندههای 11β-HSD1 (11β-هیدروکسی استروئید دهیدروژناز نوع 1) به عنوان اهداف درمانی جدید برای IIH در دست تحقیق هستند1).
بحثهایی برای تعریف FIH بر اساس «تهدیدکننده بینایی» به جای معیار زمانی «ظرف چهار هفته» وجود دارد1). معیار زمانی ممکن است مواردی را که با وجود پیشرفت سریع از تشخیص جا میمانند، نادیده بگیرد.
ادم پاپی در بیمارانی که با پروفایل خطر معمول مطابقت ندارند گزارش شده است 1). مانند IIH در افراد غیرچاق و غیرزن، مرتبط با MIS-C (سندرم التهابی چندسیستمی کودکان)، و VITT پس از واکسن آسترازنکا.
تفاوتهای معنیداری بین ایالتهای ایالات متحده مشاهده شده است (Moran I=0.20، P=0.03) 3). در تگزاس و اوکلاهاما، ناهماهنگی بین نرخ بالای چاقی و شیوع پایین IIH نیز مشاهده شده که علت آن ناشناخته است.
Bonelli L, Menon V, Arnold AC, Mollan SP. Managing idiopathic intracranial hypertension in the eye clinic. Eye. 2024;38:2472-2481.
Toshniwal SS, Kinkar J, Chadha Y, et al. Navigating the enigma: a comprehensive review of idiopathic intracranial hypertension. Cureus. 2024;16(3):e56256.
Fraz MA, Kim BM, Chen JJ, et al. Nationwide prevalence and geographic variation of idiopathic intracranial hypertension among women in the United States. Ophthalmology. 2025;132:476-483.
Ghorbani M, Griessenauer CJ, Wipplinger C, et al. Intracranial hypertension and papilledema secondary to an unruptured arteriovenous malformation: review of the literature. Neuroradiol J. 2025;38(4):387-393.
Waser B, Wood HM, Mews P, Lalloo S. Transverse sinus stenting for treatment of papilloedema secondary to a large brain herniation into a dural venous sinus with associated tectal plate lesion: case report and literature review. Interv Neuroradiol. 2021;27(6):756-762.
Thambisetty M, Lavin PJ, Newman NJ, Biousse V. Fulminant idiopathic intracranial hypertension. Neurology. 2007;68(3):229-232.
Aldhahwani B, Shah SM, Jiang H, Lam BL. Severe visual loss from concurrent fulminant idiopathic intracranial hypertension and malignant arterial hypertension: prompt suspicion matters. Am J Ophthalmol Case Reports. 2024;36:102201.
Srivastava O, Micieli JA. Resolution of fulminant idiopathic intracranial hypertension treated with acetazolamide. Case Rep Neurol. 2022;14:432-436.
Palermo M, Trevisi G, D’Arrigo S, Sturiale CL. Idiopathic intracranial hypertension in pregnancy: a systematic review on clinical course, treatments, delivery and maternal-fetal outcome. Eur J Neurol. 2025;32:e70186.
Alves S, Sousa N, Cardoso L, Alves J. Multidisciplinary management of idiopathic intracranial hypertension in pregnancy: case series and narrative review. Braz J Anesthesiol. 2022;72(6):790-794.
Regev T, Fried-Regev N, Leeman S, et al. Transverse venous sinus stenting for fulminant idiopathic intracranial hypertension during pregnancy: a report of two cases and literature review. Quant Imaging Med Surg. 2025;15(5):4796-4815.
Selvaraj J, Veeranki V, Kommaraju SY, et al. Abortion and fulminant idiopathic intracranial hypertension. Cureus. 2021;13(2):e13501.
Paramo R, Leishangthem L. Optic atrophy secondary to minocycline-induced idiopathic intracranial hypertension. BMJ Case Rep. 2023;16:e252731.
Mollan SP, Davies B, Silver NC, et al. Idiopathic intracranial hypertension: consensus guidelines on management. J Neurol Neurosurg Psychiatry. 2018;89(10):1088-1100.
Mollan SP, Mitchell JL, Ottridge RS, et al. Effectiveness of bariatric surgery vs community weight management intervention for the treatment of idiopathic intracranial hypertension: a randomized clinical trial. JAMA Neurol. 2021;78:678-686.
Wall M, McDermott MP, Kieburtz KD, et al. Effect of acetazolamide on visual function in patients with idiopathic intracranial hypertension and mild visual loss: the idiopathic intracranial hypertension treatment trial. JAMA. 2014;311:1641-1651.
Pasricha SV, Bhayana R, Wu PE. Supine headache and papilledema: a case and review of cerebral venous sinus thrombosis. Clin Case Rep. 2023;11:e07329.
Fisayo A, Bruce BB, Newman NJ, Biousse V. Overdiagnosis of idiopathic intracranial hypertension. Neurology. 2016;86:341-350.