0-1期
**0期(正常):**鼻侧、上侧、下侧边界模糊。放射状神经纤维层。
**1期(极早期):**视乳头鼻侧边界模糊。边界无隆起。微妙的灰色晕轮。同心圆状或放射状脉络膜皱襞。

视乳头水肿是由于颅内压(ICP)增高引起的双侧视乳头肿胀。“papilledema(choked disc)”一词仅限于ICP增高时使用,其他原因引起的视乳头肿胀称为“视神经乳头水肿(optic disc edema)”。视神经周围蛛网膜下腔压力升高,压迫视神经,导致轴浆流停滞,从而引起视乳头水肿。
IIH的年发病率为1.15/10万(美国1997-2016年数据,女性1.97 vs 男性0.36)2),1844岁最高(2.47/10万)。美国1855岁女性的患病率为3.44/10,000(95%CI 2.61~5.39)3)。按种族划分,发病率(/10万)依次为黑人2.05 > 白人1.04 > 西班牙裔0.67 > 亚裔/太平洋岛民0.16 2),与肥胖患病率在地理上大致一致(Moran I=0.20,P=0.03)3)。
正常ICP成人<250 mmH2O,儿童<280 mmH2O。暴发性IIH(FIH)占所有IIH患者的2~3%,是一种以症状出现4周内快速视力损害为特征的急症。1)
视乳头水肿(papilledema)是仅限于颅内压增高时的术语,其他原因(如视神经炎、缺血、浸润性病变等)引起的视盘肿胀则称为“视盘水肿(optic disc edema)”。这种术语区分对于确定病因和选择适当治疗至关重要。
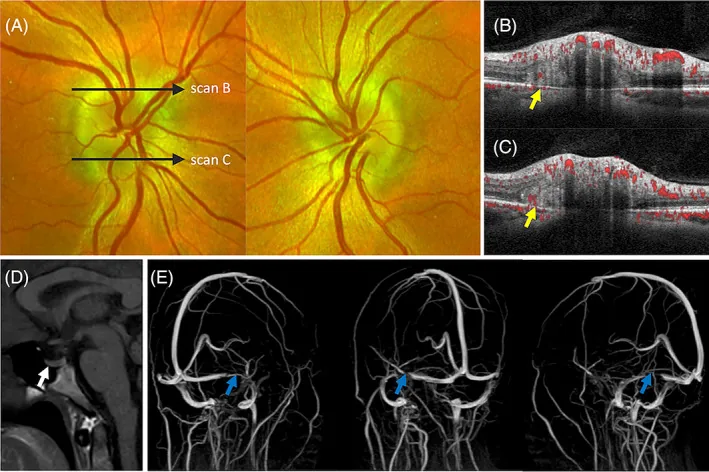
急性视乳头水肿早期通常无症状,中心视觉功能(最佳矫正视力、色觉)通常保留。
在儿童中,颅内压增高常因双侧外展神经麻痹引起的内斜视而被发现。
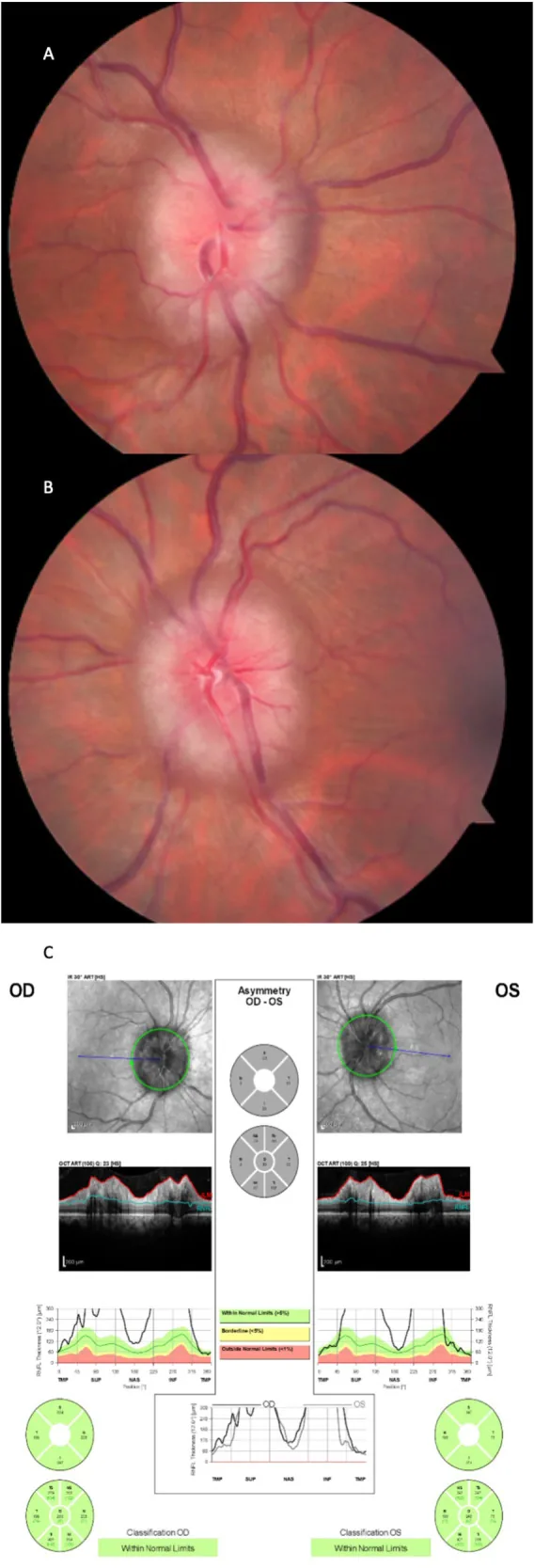
急性视乳头水肿的眼底表现:
**慢性视乳头水肿的附加表现:**视乳头苍白,胶质增生,视睫状分流血管,屈光体。慢性期,死亡的神经纤维不再肿胀,因此即使颅内压持续升高,水肿也可能消失(萎缩性终末期)。
双眼视乳头发红且视力良好时,必须鉴别淤血乳头。淤血乳头除非到末期,否则视力接近正常。
视乳头水肿的严重程度采用Frisén分级(0-5期)评估,并作为视功能预后的指标。
0-1期
**0期(正常):**鼻侧、上侧、下侧边界模糊。放射状神经纤维层。
**1期(极早期):**视乳头鼻侧边界模糊。边界无隆起。微妙的灰色晕轮。同心圆状或放射状脉络膜皱襞。
2-3期
2期(早期):所有边界模糊。鼻侧边界隆起。完全性视乳头周围晕轮。
3期(中度):视乳头直径增大。部分主要血管节段模糊。晕轮外缘有指状延伸。
4~5期
4期(显著):整个视乳头隆起。视乳头上的主要血管节段完全模糊。
5期(重度):穹顶状突出。晕轮狭窄,边界光滑。生理凹陷消失。
TVO是视乳头水肿的特征性症状,但其本身并非视力丧失的直接预兆。然而,如果颅内压增高长期持续,可能从严重的周边视野缺损进展为中心视力下降。如果TVO频繁出现,应及时就医查明原因。
视乳头水肿的形成速度取决于颅内压升高的速度。缓慢的ICP升高可能需要数周出现,而急剧升高可能在数小时至一天内出现。
对于IIH,体重减轻5-10%可改善ICP症状和视乳头水肿。ICP正常化(缓解)需要体重减少24%(IIHWT的符合方案分析)15)。如果仅通过生活方式改善难以实现,肥胖外科手术也是一种选择。体重管理仅是保守治疗的一部分,根据视乳头水肿程度和视功能损害情况,可能需要与药物治疗或手术治疗联合。
按以下顺序评估:检眼镜确认双眼视乳头水肿→荧光素眼底血管造影→OCT→CT/MRI+增强MRV→腰椎穿刺(LP)。首先测量血压以排除恶性高血压,然后进行紧急影像学检查(CT→MRI+增强MRV)评估占位病变和静脉窦血栓。确认无脑疝风险后进行LP。
MRI+增强MRV是最佳选择;IIH必须评估静脉窦狭窄/闭塞。评估以下高ICP征象:
| 标准 | 内容 |
|---|---|
| 1. 视乳头水肿 | 存在双侧视乳头水肿 |
| 2. 神经系统检查 | 除脑神经异常外正常 |
| 3. 神经影像学 | 脑实质正常、无脑室扩大、无占位、无异常强化 |
| 4. 脑脊液成分 | 正常 |
| 5. 脑脊液初压 | 成人≥250 mmH2O,儿童≥280 mmH2O |
疑似诊断:双侧视乳头水肿存在 + 满足标准1-4但脑脊液压力低于标准。25-30 cmH2O为灰色地带,建议重新评估。
据报道,17.8%的IIH诊断不准确或过早,13.0%为误诊18)。非典型患者(男性、正常BMI、儿童)中未进行MRV(42.4%)是最常见的误诊原因,导致CVST漏诊最多。
假性视乳头水肿可由高度远视、玻璃膜疣、倾斜视盘、有髓神经纤维、错构瘤等引起。以下表现提示假性视乳头水肿。
鉴别诊断列表:埋藏性玻璃膜疣、倾斜视盘、糖尿病性视乳头病变、高血压性视乳头病变、后巩膜炎、视神经周围炎、葡萄膜炎(结节病、VKH)、视神经炎、甲状腺眼病、CRVO、NAION、浸润性视神经病变、视神经鞘脑膜瘤。
据报道,10%的视乳头水肿患者存在可治疗的缺铁性贫血,建议进行筛查。
在淤血乳头(ICP升高引起的视乳头水肿)中,早期视力可能保持正常。这是因为尽管ICP升高导致视神经乳头轴浆流停滞,但对传入性视功能的影响尚轻微。相反,视神经炎常引起急性视力下降,这一差异可作为鉴别的线索。
治疗的三个目标是:①治疗根本原因,②保护视功能,③缓解症状(如头痛)。
如果早期降低颅内压,视乳头水肿会迅速吸收,不留视功能障碍。如果治疗延迟,出现视功能障碍则不可逆。
| 药物 | 剂量 | 备注 |
|---|---|---|
| 乙酰唑胺(一线用药) | 250–500 mg,每日2次 → 最大2–4 g/日 | IIHTT(2014)证明对轻度视野缺损的IIH有效16)。对头痛无一致效果。日本未纳入医保。 |
| 托吡酯(二线用药) | 个体化调整 | 降低颅内压并促进减重。对偏头痛样头痛也有用。有致畸性 → 孕妇禁用。 |
| 呋塞米 | 辅助使用 | 不耐受乙酰唑胺时的替代药物。 |
| 甲泼尼龙静脉注射 | 1 g/日,连用3天 | 仅用于暴发性IIH的临时措施。北美有使用惯例。 |
乙酰唑胺的主要副作用:感觉异常(手脚麻木)、味觉障碍(金属味)、消化道症状(恶心、呕吐、腹泻)、乏力、肾结石。慢性代偿性代谢性酸中毒、轻度低钾血症。
| 术式 | 视力改善率 | 头痛改善率 | 主要并发症 |
|---|---|---|---|
| 视神经鞘开窗术(ONSF) | 59% | 44% | 并发症10 |
| 脑脊液分流术(LPS/VPS) | 54% | 80% | 分流失败43~50%,感染,移位1) |
| 硬脑膜静脉窦支架植入术(VSS) | 78% | 82~83% | 术后需抗血小板治疗6个月。再次手术率10~18%1) |
| 减重手术 | — | — | IIHWT随机对照试验显示2年内持续降低颅内压和减轻体重15) |
VSS(硬脑膜静脉窦支架)的适应证:确认横窦狭窄且压力梯度 >8 mmHg。ONSF不能降低ICP。单侧ONSF可能对侧效果不佳。腰椎腹腔(LP)分流术常被选为IIH的一线外科干预。
占IIH患者的2%~3%。特征为症状出现后4周内快速视力下降。原则上需住院治疗,并积极进行内科和外科治疗。
CSF开放压平均为54.1 cmH2O(范围29~70)6),极高。Thambisetty等16例系列研究6)显示,尽管积极治疗,50%仍达到法定盲,所有患者均残留视野缺损和视神经萎缩。若HVF基线MD低于-7 dB,视力恢复困难。1) 初始pRNFL越高,长期视力预后越差。1)
有报道单用乙酰唑胺最大4 g/天治愈FIH(36岁男性,BMI 47.3,CSF OP 45 cmH2O→4个月后视乳头水肿消失,6个月后双眼视力恢复至20/20)8)。当FIH合并恶性高血压时,诊断延迟平均3.2个月,最终视力可能极差(20/400至光感)7)。
妊娠期IIH患病率为16/10万。61%的病例发生在妊娠早期9)。妊娠本身不被视为IIH的病因因素。视觉预后与非妊娠期相当,通常不被视为高危妊娠。
预后:IIH复发率9~28%2)。预后不良因素:体重增加、视乳头水肿严重程度、基线头痛程度2)。
乙酰唑胺是IIH的一线治疗药物,疗效确切,但若病因为脑静脉血栓,则可能加重病情,因此禁忌使用。隐球菌性脑膜炎也禁忌使用。首先必须明确病因,并根据根本原因选择治疗方法。还需注意,该药在日本不属于医保范围。
虽然属于FDA分类C类,但系统性综述未发现其与先天畸形有因果关系9)。即使在孕早期大剂量使用(≥1克/天),也未观察到畸形风险增加。必须在产科医生协商下使用,且多数情况下仅限于妊娠20周后使用。
暴发性IIH(FIH)是IIH的一种亚型,其特点是在症状出现后4周内迅速出现严重视力损害。约2~3%的IIH患者会发生。普通IIH进展相对缓慢,而FIH可在数天内视力恶化,若不及时干预,可能导致不可逆性失明6)。
视神经周围蛛网膜下腔压力升高,压迫视神经,导致轴浆流停滞,从而引起视乳头水肿。具体途径如下。
颅内压升高→视神经周围蛛网膜下腔压力升高→视神经受压→顺行性轴浆运输停滞→神经水肿(视乳头水肿)。压力持续→神经内缺血→轴突消失→视神经萎缩→视力障碍。萎缩期死亡的神经纤维不再肿胀,因此即使颅内压持续升高,视乳头水肿也可能消失(萎缩终末期)。
脑脊液排出障碍假说
蛛网膜颗粒和淋巴通路中脑脊液排出延迟导致颅内压升高。米诺环素扰乱蛛网膜颗粒的cAMP信号,降低脑脊液吸收13)。
静脉窦压力升高假说
超过90%的IIH患者存在双侧横窦狭窄2)。链条:肥胖→腹腔内压升高→胸腔内压升高→脑静脉回流障碍→颅内压升高。静脉窦支架术的有效性支持这一假说。
代谢和激素异常假说
雄激素调节异常被认为参与其中2)。瘦素过量→脉络丛过度激活→脑脊液过度产生。GLP-1受体存在于脉络丛,大鼠模型显示GLP-1受体激动剂可减少脑脊液产生。
在一项比较减重手术与社区体重管理干预的随机对照试验中,减重手术组在2年内持续降低颅内压并减轻体重15)。5年后的成本效益也优于饮食疗法。颅内压降低量与减重幅度相关。
艾塞那肽等GLP-1受体激动剂作为IIH的新候选治疗药物备受关注。它们通过降低Na⁺/K⁺-ATP酶活性减少脉络丛的脑脊液分泌。有报告称,在人类中给药2.5小时后颅内压降低5.7±2.9 cmH₂O(P=0.048)。预期具有促进减重和直接降低颅内压的双重机制。但需注意停药后体重反弹导致IIH发病的风险。
关于横窦支架植入安全性和有效性的报告不断积累4, 5)。英国正在进行一项比较VSS与脑室腹腔分流术的随机对照试验。VSS的视力改善率为78%,头痛改善率为82-83%(荟萃分析)。再次手术率为10-18%。
11β-HSD1(11β-羟基类固醇脱氢酶1型)抑制剂作为IIH的新型治疗靶点正在研究中1)。
有讨论提出基于“视力威胁性”而非“4周内”的时间标准来定义1)。时间标准可能会漏诊快速进展的病例。
已有报告指出,在不符合传统风险特征的患者中出现视乳头水肿1)。例如:非肥胖、非女性个体的IIH;与MIS-C(儿童多系统炎症综合征)相关的病例;以及阿斯利康疫苗后的VITT等。
美国境内已确认存在显著的州际差异(Moran I = 0.20,P = 0.03)3)。在德克萨斯州、俄克拉荷马州等地,观察到肥胖率高但IIH发病率低的不一致现象,其原因尚不清楚。
Bonelli L, Menon V, Arnold AC, Mollan SP. Managing idiopathic intracranial hypertension in the eye clinic. Eye. 2024;38:2472-2481.
Toshniwal SS, Kinkar J, Chadha Y, et al. Navigating the enigma: a comprehensive review of idiopathic intracranial hypertension. Cureus. 2024;16(3):e56256.
Fraz MA, Kim BM, Chen JJ, et al. Nationwide prevalence and geographic variation of idiopathic intracranial hypertension among women in the United States. Ophthalmology. 2025;132:476-483.
Ghorbani M, Griessenauer CJ, Wipplinger C, et al. Intracranial hypertension and papilledema secondary to an unruptured arteriovenous malformation: review of the literature. Neuroradiol J. 2025;38(4):387-393.
Waser B, Wood HM, Mews P, Lalloo S. Transverse sinus stenting for treatment of papilloedema secondary to a large brain herniation into a dural venous sinus with associated tectal plate lesion: case report and literature review. Interv Neuroradiol. 2021;27(6):756-762.
Thambisetty M, Lavin PJ, Newman NJ, Biousse V. Fulminant idiopathic intracranial hypertension. Neurology. 2007;68(3):229-232.
Aldhahwani B, Shah SM, Jiang H, Lam BL. Severe visual loss from concurrent fulminant idiopathic intracranial hypertension and malignant arterial hypertension: prompt suspicion matters. Am J Ophthalmol Case Reports. 2024;36:102201.
Srivastava O, Micieli JA. Resolution of fulminant idiopathic intracranial hypertension treated with acetazolamide. Case Rep Neurol. 2022;14:432-436.
Palermo M, Trevisi G, D’Arrigo S, Sturiale CL. Idiopathic intracranial hypertension in pregnancy: a systematic review on clinical course, treatments, delivery and maternal-fetal outcome. Eur J Neurol. 2025;32:e70186.
Alves S, Sousa N, Cardoso L, Alves J. Multidisciplinary management of idiopathic intracranial hypertension in pregnancy: case series and narrative review. Braz J Anesthesiol. 2022;72(6):790-794.
Regev T, Fried-Regev N, Leeman S, et al. Transverse venous sinus stenting for fulminant idiopathic intracranial hypertension during pregnancy: a report of two cases and literature review. Quant Imaging Med Surg. 2025;15(5):4796-4815.
Selvaraj J, Veeranki V, Kommaraju SY, et al. Abortion and fulminant idiopathic intracranial hypertension. Cureus. 2021;13(2):e13501.
Paramo R, Leishangthem L. Optic atrophy secondary to minocycline-induced idiopathic intracranial hypertension. BMJ Case Rep. 2023;16:e252731.
Mollan SP, Davies B, Silver NC, et al. Idiopathic intracranial hypertension: consensus guidelines on management. J Neurol Neurosurg Psychiatry. 2018;89(10):1088-1100.
Mollan SP, Mitchell JL, Ottridge RS, et al. Effectiveness of bariatric surgery vs community weight management intervention for the treatment of idiopathic intracranial hypertension: a randomized clinical trial. JAMA Neurol. 2021;78:678-686.
Wall M, McDermott MP, Kieburtz KD, et al. Effect of acetazolamide on visual function in patients with idiopathic intracranial hypertension and mild visual loss: the idiopathic intracranial hypertension treatment trial. JAMA. 2014;311:1641-1651.
Pasricha SV, Bhayana R, Wu PE. Supine headache and papilledema: a case and review of cerebral venous sinus thrombosis. Clin Case Rep. 2023;11:e07329.
Fisayo A, Bruce BB, Newman NJ, Biousse V. Overdiagnosis of idiopathic intracranial hypertension. Neurology. 2016;86:341-350.