非缺血型

视网膜中央静脉阻塞
一目了然的要点
Section titled “一目了然的要点”1. 什么是视网膜中央静脉阻塞?
Section titled “1. 什么是视网膜中央静脉阻塞?”视网膜中央静脉阻塞(CRVO)是一种在视神经内筛板水平发生视网膜中央静脉阻塞的疾病。阻塞导致静脉压升高,引起视网膜内血液淤滞、缺血和渗出,四个象限均出现火焰状出血、视盘水肿和黄斑水肿。
视网膜静脉阻塞总体上是仅次于糖尿病视网膜病变的第二常见视网膜血管疾病9, 10)。截至2015年,全球患病率约为0.77%,估计30-89岁患者约2800万人10)。CRVO在40岁以上人群中的患病率约为0.2%,是视网膜分支静脉阻塞(BRVO)的六分之一到七分之一10)。好发于60-70岁,40岁以下相对罕见9, 10)。
CRVO大致分为灌注型(非缺血型)和非灌注型(缺血型)。非缺血型约占所有CRVO的75-80%。此外,还有半侧视网膜中央静脉阻塞(hemi-CRVO),仅累及上方或下方两个象限,临床病程与CRVO相似9, 10)。Hemi-CRVO是由于筛板水平两条独立的半侧中央静脉之一阻塞所致,与BRVO不同,通常看不到动静脉交叉。约90%累及上方或下方半视野10)。与CRVO一样,需注意新生血管性青光眼的高风险10)。
CRVO的重要并发症是黄斑水肿和新生血管。黄斑水肿可发生在非缺血型和缺血型中,是视力下降的主要原因。新生血管(虹膜新生血管、视网膜新生血管)主要发生在缺血型,约25%的CRVO患者出现虹膜新生血管,可能导致新生血管性青光眼而失明10)。有报道称,CRVO患者的心血管事件和全因死亡率高于一般人群10),从全身管理的角度来看,与内科的协作非常重要。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”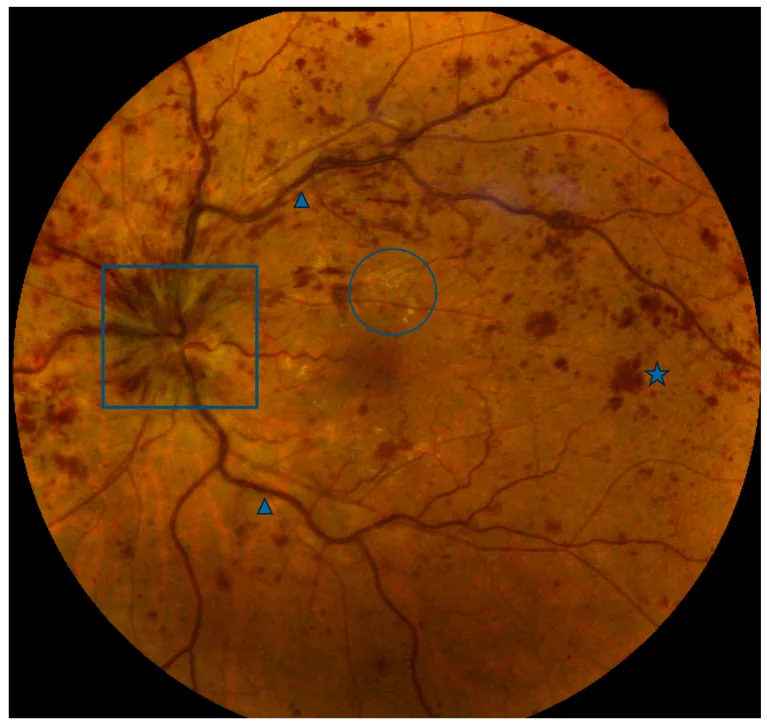
CRVO的症状因阻塞类型而异。
- 非缺血型:有时无自觉症状而被偶然发现,但多数病例因黄斑水肿出现视力下降。急性发作时可能仅为轻度视物模糊。
- 缺血型:表现为突然且严重的视力障碍,常出现低于20/200的严重视力下降。合并玻璃体积血时可导致急剧视力丧失。合并新生血管性青光眼时出现眼痛和头痛。
- 两者均以无痛性为特征。
临床所见(医生检查确认的所见)
Section titled “临床所见(医生检查确认的所见)”CRVO的典型眼底所见如下:
- 四个象限的火炬状出血:与BRVO的扇形分布不同,累及所有象限是鉴别诊断上的重要特征。
- 视网膜静脉扩张迂曲:反映阻塞导致的静脉内压升高。
- 视乳头水肿:常伴有视乳头周围水肿。
- 黄斑水肿:视力下降的主要原因,OCT定量评估必不可少。
- 软性渗出(棉絮斑):反映缺血的体征,在缺血型中明显可见。
- 硬性渗出:长期病例中可在黄斑周围观察到。
根据特征性视网膜出血,诊断本身并不困难,但为了区分非缺血型和缺血型、确定治疗适应症和预后评估,除眼底检查外的详细检查也很重要。随着病程进展,急性期出血被吸收,软性渗出也消退。长期来看,视乳头周围和视网膜静脉之间可能形成侧支循环。黄斑水肿可能自行消退,但如果持续存在,会导致视网膜色素上皮萎缩,视力预后恶化。
非缺血型和缺血型的鉴别要点如下表所示。据报道,约三分之一的非缺血型病例在病程中转变为缺血型,其中4个月内转变率为15%,3年内为34%10)。
| 特征 | 非缺血型 | 缺血型 |
|---|---|---|
| 视力 | 20/200及以上 | 低于20/200 |
| RAPD | 轻度/阴性 | 明显(约90%阳性) |
| FA无灌注区 | <10个视盘面积 | ≥10个视盘面积(CVOS标准) |
| ERG | 正常至轻度降低 | b/a比值和b波振幅降低 |
| 预后 | 相对良好 | 不良(NVG高风险) |
缺血型
PAMM(paracentral acute middle maculopathy)
Section titled “PAMM(paracentral acute middle maculopathy)”CRVO的OCT B扫描中,旁中心凹的内核层可见带状高反射,称为PAMM(paracentral acute middle maculopathy)。这是由于静脉灌注障碍导致供应视网膜深层毛细血管丛的末梢小动脉循环障碍所致。视网膜浅层的en face图像中高反射不明显,但视网膜深层的en face图像中,与混浊视网膜一致的高反射区域清晰可见。PAMM反映了中间毛细血管丛的缺血,作为评估CRVO视网膜缺血程度的辅助指标受到关注。
Matsuo T等人(2025)报告了一例71岁男性双侧CRVO病例1)。右眼CRVO在发病4个月后进展为眼压35mmHg的新生血管性青光眼,最终光感丧失。左眼CRVO通过抗VEGF治疗和保守治疗维持了视力。心脏手术后右心功能不全被认为是双侧发病的诱因。
3. 原因与风险因素
Section titled “3. 原因与风险因素”CRVO的病理生理可用Virchow三联征(血管损伤、血流淤滞、高凝状态)解释。在筛板后方,视网膜中央动脉和视网膜中央静脉共享同一外膜,动脉硬化性变化导致动脉壁增厚硬化,压迫相邻静脉,引起血管内皮损伤、血栓形成和闭塞。
主要风险因素如下表所示。
| 风险因素 | 频率/关联 |
|---|---|
| 年龄增长 | 最重要:超过90%的患者年龄在55岁以上 |
| 高血压 | 50岁以上患者中高达73%合并高血压9, 10) |
| 高脂血症 | 主要危险因素7) |
| 糖尿病 | 独立危险因素9, 10) |
| 青光眼/高眼压 | 独立危险因素9, 10) |
荟萃分析显示,48%的RVO归因于高血压,20%归因于高脂血症,5%归因于糖尿病10)。
其他重要的危险因素如下所示。
- 低HDL胆固醇血症:低HDL-C已被报道为RVO的独立危险因素,需注意常规血脂筛查中容易忽略这一点10)。
- 系统性自身免疫性疾病:SLE患者的CRVO发生率是对照组的3.5倍9, 10)。
- 心血管风险:RVO患者的心血管事件和全因死亡率升高。与内科协作非常重要9, 10)。
- PDE5抑制剂(如西地那非):FDA报告已收集82例RVO,推测其机制为全身血压下降时诱发视网膜静脉怒张2)。
- COVID-19感染:机制被认为是细胞因子风暴导致的血管内皮损伤和凝血功能亢进3, 4)。
- COVID-19疫苗:提出了VITT(疫苗诱导的血栓性血小板减少症)机制,ChAdOx1(阿斯利康)接种后血栓发生率为1.13/10万剂次5, 6)。
- MTHFR基因突变:高同型半胱氨酸血症导致凝血功能亢进3, 4)。
- 右心功能不全:静脉引流障碍导致静脉压升高,可能诱发双侧CRVO1)。
- 睡眠呼吸暂停综合征和颈动脉闭塞性疾病:已被报道为CRVO的危险因素10)。
- 对侧眼风险:单眼发生CRVO后,对侧眼同样发生CRVO的风险为每年1%10)。
- 抑郁症:有报道称抑郁症患者RVO风险升高10)。
50岁以下发病时强烈建议进行全身检查。据报道,58%的病例发现了非传统危险因素(如凝血异常、自身免疫性疾病等)9, 10)。即使50岁以上,也务必检查高血压、糖尿病、血脂异常的管理状况,并建议与内科主治医生共享信息。
40岁以下发病虽然罕见,但可能发生。凝血异常、MTHFR基因突变、COVID-19感染、疫苗后VITT、PDE5抑制剂等可能成为病因2, 3, 4, 5, 6)。50岁以下建议进行凝血系统筛查(蛋白C/S、抗凝血酶III等)和自身抗体检查(抗磷脂抗体、抗核抗体等)9, 10)。在年轻CRVO中,与视乳头血管炎的鉴别也很重要,后者可能需要全身性类固醇治疗。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”诊断结合病史、视力和眼底检查结果。四个象限的火焰状出血和静脉扩张迂曲的特征性眼底表现使诊断本身并不困难,但缺血型/非缺血型的分类和治疗适应症的判断需要以下检查。
- 病史采集:视力下降的经过、用药史(抗凝药、PDE5抑制剂)、既往史(高血压、糖尿病、血液疾病、睡眠呼吸暂停)9, 10)。
- 视力检查:缺血型初诊时视力常低于20/200。
- RAPD检查:非缺血型通常阴性,但缺血型约90%阳性,对鉴别缺血型/非缺血型非常有用。也是新生血管发生风险的重要预测因子9, 10)。
- 裂隙灯和眼底检查:评估四个象限的出血、视盘水肿和黄斑水肿。散瞳前检查虹膜新生血管。
- 眼压和房角镜检查:缺血型每月一次房角镜检查,持续6个月,检查虹膜和房角新生血管9)。约1/3的非缺血型会转为缺血型,因此应始终观察房角。
主要检查方法
Section titled “主要检查方法”以下显示各项检查的作用。
| 检查 | 目的 |
|---|---|
| FA(荧光眼底造影) | 评估缺血范围(CVOS标准)9, 10) |
| OCT(光学相干断层扫描) | 黄斑水肿的定量评估和PAMM检测9, 10) |
| OCTA(光学相干断层扫描血管成像) | 无创检测毛细血管无灌注区9) |
| ERG(视网膜电图) | 缺血型的鉴别(b/a比值降低) |
| 视野检查 | 缺血型的大中心暗点 |
- FA(荧光素眼底血管造影):根据CVOS标准(毛细血管无灌注区≥10个视盘面积)对缺血型的定义至关重要9, 10)。但在急性期,大量视网膜出血可能遮挡荧光,导致无灌注区判断困难。因此,出血吸收数周后可能需要复查。广角FA正在提高周边缺血评估的准确性,并可能有助于预测非缺血型向缺血型转化的风险9, 10)。FA也有助于区分侧支血管(荧光素造影晚期无渗漏)和新生血管(早期和晚期均有渗漏)18)。
- OCT(光学相干断层扫描):对黄斑水肿的定量评估非常有用,也用于监测治疗效果9, 10)。在CRVO中,中心凹旁内核层可能出现PAMM表现(高反射带),反映末梢小动脉循环障碍。
- OCTA(光学相干断层扫描血管成像):无需造影剂即可检测毛细血管无灌注区9)。也可评估FAZ(中心凹无血管区)面积扩大,但成像范围有限是挑战。
- ERG(视网膜电图):缺血型表现为b/a比值降低、b波振幅下降、闪烁反应降低,有助于鉴别缺血型和非缺血型。
- 视野检查:缺血型显示大中心暗点。
由于全身性血管危险因素参与CRVO的发病,需进行以下全身检查。
- 所有患者均推荐的检查:
- 血压测量
- 血液检查:全血细胞计数(CBC)、红细胞沉降率(ESR)、空腹血糖和糖化血红蛋白(HbA1c)、总胆固醇、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、甘油三酯
- 肾功能(血尿素氮、肌酐)
- C反应蛋白(CRP)(排除炎症性疾病)
- 50岁以下患者额外推荐的检查9, 10):
- 凝血功能筛查:蛋白C活性、蛋白S活性、抗凝血酶III活性、同型半胱氨酸、凝血因子V Leiden突变
- 自身抗体:抗磷脂抗体(狼疮抗凝物、抗心磷脂抗体)、抗核抗体
- 必要时考虑咨询血液科或风湿免疫科
- 视乳头血管炎:在年轻发病的CRVO中,鉴别诊断很重要。伴有视乳头血管炎的CRVO可能需要全身性类固醇治疗。
- 血液疾病:如果双眼发生CRVO,可能伴有血液疾病如红细胞增多症、白血病或骨髓增殖性疾病,需要进一步检查。
- 糖尿病视网膜病变:当出现弥漫性视网膜出血时需要鉴别。CRVO的特点是单眼急性发作,四个象限均匀出血,而糖尿病视网膜病变是双眼慢性病程,新生血管分布模式不同。
- 眼缺血综合征:由颈动脉闭塞性疾病引起的慢性眼缺血可能呈现类似CRVO的眼底表现。CRVO的出血更急性且大量,而眼缺血综合征的出血为中等程度,且早期出现低眼压和虹膜新生血管。
5. 标准治疗方法
Section titled “5. 标准治疗方法”CRVO的治疗包括两大支柱:黄斑水肿的治疗和新生血管的治疗。
抗VEGF治疗(一线选择)
Section titled “抗VEGF治疗(一线选择)”玻璃体内注射抗VEGF药物是CRVO相关黄斑水肿的一线治疗9, 10)。多项大规模RCT已证实其有效性。与BRVO相比,注射次数更多,尤其是缺血型,完全治愈的病例很少,但这是目前最有望改善视力的治疗方法。
雷珠单抗
CRUISE试验:0.5mg组在6个月后平均改善+14.9个字母。47.7%的患者改善≥15个字母(假注射组改善0.8个字母,16.9%改善≥15个字母)12)。
剂量:每月玻璃体内注射0.5mg/0.05mL。
保险覆盖:适用于“视网膜静脉阻塞引起的黄斑水肿”。
阿柏西普
COPERNICUS试验:2mg组56%的患者改善≥15个字母(假注射组12%)13)。
GALILEO试验:同样证实了优于假注射组14)。
剂量:每月玻璃体内注射2mg/0.05mL。
保险覆盖:适用于“视网膜静脉阻塞引起的黄斑水肿”。
法瑞西单抗
COMINO试验(CRVO/半侧CRVO,n=729):基线BCVA 50.5个字母,CST 711.6μm。6mg组在24周时平均改善+16.9个字母。56.6%的患者改善≥15个字母。达到对阿柏西普的非劣效性11)。
CST变化:24周时CST减少,法瑞西单抗组-461.6μm vs 阿柏西普组-448.8μm。黄斑渗漏消失率:法瑞西单抗44.4% vs 阿柏西普30.0%11)。
安全性:眼内炎症(IOI)发生率:法瑞西单抗2.2% vs 阿柏西普1.1%。严重IOI:法瑞西单抗组2例葡萄膜炎,阿柏西普组1例非感染性眼内炎11)。
机制:是一种双特异性抗体,除抗VEGF-A作用外,还具有抗Ang-2作用。
其他抗VEGF药物及主要临床试验结果如下所示。
- 贝伐珠单抗:玻璃体内注射1.25mg/0.05mL为超说明书使用4, 9)。
- LEAVO试验(100周,CRVO 463例):阿柏西普组改善+15.1个字母,雷珠单抗组+12.5个字母,贝伐珠单抗组+9.8个字母。阿柏西普显示非劣效于雷珠单抗,但与贝伐珠单抗的比较未得出结论16)。阿柏西普组52%、雷珠单抗组47%、贝伐珠单抗组45%达到15个字母以上的视力改善。
- SCORE2试验(CRVO/半侧CRVO 362例):贝伐珠单抗与阿柏西普在6个月时(主要终点)视力相当17)。6个月时反应不佳的病例接受了地塞米松植入物的补救治疗。24个月时,两组视力均呈从12个月开始下降的趋势。
- 治疗持续时间:约56-75%的CRVO患者需要持续抗VEGF治疗超过5年10)。长期定期随访和持续治疗至关重要,中断治疗有视力下降的风险。
- 给药方案:从每月注射开始,广泛采用治疗-延长方案,在OCT确认黄斑水肿改善的同时延长注射间隔。法瑞西单抗正在研究延长至最多16周间隔11)。
在抗VEGF无效或不适用时选择。
- 曲安奈德玻璃体内注射(TAIV):SCORE研究中,标准治疗(光凝)组7%、TAIV 1mg组27%、4mg组26%在12个月后视力改善15个字母以上。但超过60%的病例黄斑水肿复发,需要追加注射。4mg组眼压升高和白内障进展显著,因此如使用,推荐1mg10)。
- 地塞米松缓释植入物(Ozurdex 0.7mg):GENEVA试验(CRVO/BRVO 1267例)中,视力改善从第30天开始,第90天达到峰值,但6个月时效果消失15)。1年时16%出现眼压≥25mmHg。与抗VEGF相比,白内障和眼压升高的风险更高。
- 迟发性眼内炎:DEX植入物后也有迟发性眼内炎的报道,异物感、充血、视力下降需要紧急处理8)。
全视网膜光凝(PRP)
Section titled “全视网膜光凝(PRP)”PRP(全视网膜光凝)用于处理缺血型CRVO的新生血管9)。PRP没有改善视力的效果,但通过使新生血管消退和抑制其进展,可预防新生血管性青光眼的发生。
- 非缺血型:不会发生新生血管,因此不适用PRP。不推荐进行预防性PRP。
- 缺血型:约30%的缺血型CRVO会发生新生血管,因此可能需要PRP。目前VEGF抑制剂可在一定程度上控制新生血管,因此认为在发现新生血管后再进行PRP也不迟。但在高度缺血或老年患者中,可能会考虑早期进行PRP。
- CVOS研究结果:中央静脉阻塞研究(CVOS)探讨了格栅样光凝治疗CRVO黄斑水肿,但未证明有视力改善效果。因此,不推荐对黄斑水肿进行格栅样光凝。仅在确认虹膜或房角新生血管时,才推荐进行密集的全视网膜光凝9, 10)。联合抗VEGF药物可能有助于完成全视网膜光凝10)。
在VEGF抑制剂获批后,玻璃体手术不作为首选治疗。尚未针对CRVO黄斑水肿进行大规模临床试验,证据尚未确立。过去曾进行的放射状视神经乳头切开术(radial optic neurotomy)基于通过筛板减压降低静脉压的理论依据,但由于可能导致视野缺损、出血等严重并发症,目前已不再进行。
对于合并玻璃体积血的病例,可在清除积血的同时进行PRP。合并牵拉性玻璃体黄斑综合征(黄斑前膜、玻璃体黄斑牵拉)时,玻璃体手术可能有助于改善黄斑水肿。
- 疫苗相关CRVO:有报道显示类固醇冲击疗法(甲泼尼龙1g×3天)有效,中心凹厚度从823μm改善至166μm,视力从2/60恢复至6/96)。
- 抗凝治疗:可能恶化视力预后,不推荐使用4)。
为评估治疗效果和早期发现并发症,按以下时间表进行随访。
- 非缺血型:发病后4-6周重新评估,之后根据黄斑水肿状态每1-3个月随访一次。每次进行OCT定量评估黄斑水肿和视力检查。
- 缺血型:发病后6个月内必须每月就诊一次9)。散瞳前检查虹膜新生血管,并通过房角镜检查监测房角新生血管。即使停止抗VEGF治疗后,新生血管出现风险仍然存在,因此需要继续包括房角检查在内的随访。
- 非缺血型向缺血型转化的监测:约1/3的非缺血型在病程中转化为缺血型,因此应始终进行房角观察。RAPD变化、视力急剧下降、出血加重等是提示转化为缺血型的表现。
- 抗VEGF治疗期间:每次注射后1个月通过OCT评估黄斑水肿,如有复发则再次注射。如果稳定,逐渐延长注射间隔(treat-and-extend方案)。
- 全身管理:与内科协作定期监测血压、血糖和血脂。CRVO伴有对侧眼发病风险(每年1%),因此双眼定期检查很重要10)。
在CRUISE研究中,每月注射6次,确认了显著的视力改善12)。实际治疗中,从每月注射开始,在通过OCT确认黄斑水肿改善的同时延长间隔。据报道,约56-75%的CRVO病例需要持续治疗超过5年10),因此长期定期就诊至关重要。法瑞西单抗采用treat-and-extend方案,可延长至最大16周间隔11)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”闭塞的形成机制
Section titled “闭塞的形成机制”在筛板后方,视网膜中央动脉和视网膜中央静脉共享同一外膜(结缔组织鞘)。动脉硬化导致的动脉壁增厚和硬化压迫相邻静脉,导致血管内皮损伤→血栓形成→闭塞9, 10)。在BRVO中,闭塞主要发生在动静脉交叉处,而CRVO的特征是筛板附近的闭塞,但血栓形成的机制本身被认为与BRVO相似。
Virchow三联征(血管损伤、血流淤滞、高凝状态)均参与其中。BRVO中,动静脉交叉处的压迫是闭塞的主要原因,而CRVO中,动静脉在筛板这一狭窄解剖空间共享外膜的独特结构是闭塞发生的基础。
VEGF、黄斑水肿与新生血管的关系
Section titled “VEGF、黄斑水肿与新生血管的关系”静脉闭塞→静脉压升高→血浆成分渗漏→视网膜水肿和出血。视网膜缺血→缺氧→VEGF(血管内皮生长因子)过度产生→黄斑水肿加重和新生血管形成(虹膜新生血管、视网膜新生血管)发生9, 10)。
在所有视网膜血管疾病中,RVO的Ang-2(血管生成素-2)水平最高。Ang-2与Ang-1竞争结合Tie2,抑制Ang-1/Tie2信号介导的血管稳定11)。这为同时靶向VEGF-A和Ang-2的法瑞西单抗的作用机制提供了依据。
这一机制是抗VEGF治疗和抗Ang-2治疗的理论基础。在缺血型CRVO中,VEGF的产生量显著高于非缺血型,涉及虹膜、房角和视网膜的新生血管形成迅速进展。VEGF抑制剂不仅能改善黄斑水肿,还能使新生血管消退;但药效减弱时会复发,因此需要持续给药。
PAMM(旁中心急性中层黄斑病变)
Section titled “PAMM(旁中心急性中层黄斑病变)”在CRVO中,静脉灌注障碍导致外周小动脉水平的循环障碍。OCT B扫描显示为旁中心凹内核层带状高反射(PAMM表现)。在浅层en face图像上不明显,但在深层en face图像上,与白色混浊视网膜对应的高反射区域清晰可见。
特殊病因的机制
Section titled “特殊病因的机制”- COVID-19相关:细胞因子风暴引起的血管内皮损伤、促血栓状态以及直接感染血管内皮细胞共同导致高凝状态3)。
- VITT(疫苗后血栓性血小板减少症):形成针对血小板第4因子(PF4)的自身抗体,激活血小板并形成血栓5)。
- PDE5抑制剂:在全身血压降低的情况下,诱发视网膜静脉扩张和血流速度减慢,增加静脉血栓风险2)。
- 右心功能不全:右心系统静脉回流障碍导致眼静脉压升高,可能诱发双侧CRVO1)。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”COVID-19、疫苗与视网膜静脉阻塞
Section titled “COVID-19、疫苗与视网膜静脉阻塞”关于COVID-19感染后视网膜静脉阻塞风险的报告正在积累。
RiaziEsfahani H等人(2024)报告了一例有COVID-19病史的年轻患者的半侧CRVO病例3)。提示感染后数月内RVO风险可能持续存在。
在一项对20例疫苗接种后RVO的回顾中,7例为40岁以下年轻患者6)。ChAdOx1(阿斯利康)疫苗接种后血栓发生率为1.13/10万剂次,提出了通过VITT机制导致高凝状态的观点5, 6)。
PDE5抑制剂与视网膜静脉阻塞
Section titled “PDE5抑制剂与视网膜静脉阻塞”Torkashvand A等人(2023年)报告了一例服用西地那非后同时发生CRVO和视网膜中央动脉阻塞的病例2)。OCTA记录到血管密度降低,PDE5抑制剂对视网膜循环的影响受到关注。
广角FA和OCTA的进展
Section titled “广角FA和OCTA的进展”广角成像技术的进步使周边缺血范围的评估更加精确9, 10)。广角FA能够检测到传统标准FA难以评估的周边视网膜无灌注区,有望提高从非缺血型向缺血型转变的风险预测精度。OCTA无需造影剂即可定量评估FAZ面积扩大和毛细血管密度降低,在RVO患者随访中的有用性已有报道。然而,目前由于拍摄范围的限制,尚不能完全替代FA9)。
人工智能(AI)诊断辅助
Section titled “人工智能(AI)诊断辅助”利用深度学习算法从彩色眼底照片中自动检测RVO的研究正在进行,并报告了良好的识别能力10)。未来有望应用于筛查和远程医疗。
生物类似药的开发
Section titled “生物类似药的开发”2021年至2024年,FDA批准了两种雷珠单抗生物类似药(ranibizumab-nuna [Byooviz]、ranibizumab-eqrn [Cimerli])和四种阿柏西普生物类似药(aflibercept-jbvf [Yesafili]、aflibercept-yszy [Opuviz]、aflibercept-mrbb [Ahzantive]、aflibercept-ayyh [Pavblu])用于RVO伴黄斑水肿的适应症10)。生物类似药的普及有望改善治疗可及性并降低医疗成本。
COMINO 72周数据展望
Section titled “COMINO 72周数据展望”在法瑞西单抗的COMINO试验中,第24周后(第2部分:24-72周),所有患者转为法瑞西单抗6mg T&E给药(最长间隔16周)。72周时的持久性和长期安全性数据预计将在未来公布,有望为RVO治疗中延长给药间隔的可能性提供重要结果11)。
双侧CRVO与全身疾病的协作
Section titled “双侧CRVO与全身疾病的协作”有报告以双侧CRVO为契机发现右心功能不全的病例,显示了与心脏外科、心血管内科跨学科协作的重要性1)。
8. 参考文献
Section titled “8. 参考文献”- Matsuo T, et al. Sequential bilateral central retinal vein occlusion with differential long-term outcomes following cardiac surgery. Cureus. 2025;17(12):e100045.
- Torkashvand A, et al. Central retinal vein and artery occlusion associated with sildenafil. J Med Case Rep. 2023;17:399.
- RiaziEsfahani H, et al. Hemicentral retinal vein occlusion in a patient with COVID-19 history. J Med Case Rep. 2024;18:50.
- Staropoli PC, et al. Central retinal vein occlusion associated with COVID-19 and MTHFR mutation in a 15-year-old male. Am J Ophthalmol Case Rep. 2022;26:101522.
- Sonawane NJ, et al. Central retinal vein occlusion post-COVID-19 vaccination. Indian J Ophthalmol. 2022;70:308-9.
- Dutta Majumder P, et al. Retinal venous occlusion following COVID-19 vaccination: third dose and review. Indian J Ophthalmol. 2022;70:2191-4.
- Zhao J, et al. Chylous aqueous humor caused by hyperlipidemia. Medicine. 2023;102:e34972.
- Tripathi AN, et al. Atypical delayed-onset endophthalmitis following intravitreal dexamethasone implant. Rom J Ophthalmol. 2024;68(4):343-8.
- Flaxel CJ, et al. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2020;127:P288-P320.
- Flaxel CJ, et al. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024;131:P288-P332.
- Tadayoni R, et al. Efficacy and Safety of Faricimab for Macular Edema due to Retinal Vein Occlusion: 24-Week Results from the BALATON and COMINO Trials. Ophthalmology. 2024.
- Campochiaro PA, et al. Ranibizumab for macular edema following central retinal vein occlusion: six-month primary end point results of a phase III study (CRUISE). Ophthalmology. 2010;117(6):1124-1133.e1. doi:10.1016/j.ophtha.2010.02.022. PMID:20381871.
- Boyer D, et al. Vascular endothelial growth factor Trap-Eye for macular edema secondary to central retinal vein occlusion: six-month results of the phase 3 COPERNICUS study. Ophthalmology. 2012;119(5):1024-1032. doi:10.1016/j.ophtha.2012.01.042. PMID:22440275.
- Holz FG, et al. VEGF Trap-Eye for macular oedema secondary to central retinal vein occlusion: 6-month results of the phase III GALILEO study. Br J Ophthalmol. 2013;97(3):278-284. doi:10.1136/bjophthalmol-2012-301504. PMID:23298885.
- Haller JA, et al. Randomized, sham-controlled trial of dexamethasone intravitreal implant in patients with macular edema due to retinal vein occlusion (GENEVA). Ophthalmology. 2010;117(6):1134-1146.e3. doi:10.1016/j.ophtha.2010.03.032. PMID:20417567.
- Hykin P, et al. Clinical effectiveness of intravitreal therapy with ranibizumab vs aflibercept vs bevacizumab for macular edema secondary to central retinal vein occlusion (LEAVO). JAMA Ophthalmol. 2019;137(11):1256-1264. doi:10.1001/jamaophthalmol.2019.3305. PMID:31465100; PMCID:PMC6865295.
- Scott IU, et al. Effect of bevacizumab vs aflibercept on visual acuity among patients with macular edema due to central retinal vein occlusion: the SCORE2 randomized clinical trial. JAMA. 2017;317(20):2072-2087. doi:10.1001/jama.2017.4568. PMID:28492910; PMCID:PMC5710547.
- 日本眼科学会. 眼底血管造影実施基準(改訂版). 日眼会誌. 2011;115(9):675-681.
