青光眼前期至开角期
虹膜红变:瞳孔缘出现微细的新生血管簇。正常血管在虹膜实质内呈放射状走行,而新生血管在虹膜表面呈不规则、迂曲的图案。
房角新生血管:可见越过巩膜突延伸至小梁网上的树枝状细血管。眼压正常至轻度升高。
纤维血管膜:覆盖小梁网增殖,导致继发性开角型青光眼。

新生血管性青光眼(NVG)是一种以眼前房角纤维血管组织增生为特征的重症继发性青光眼。视网膜缺血是主要原因,导致VEGF(血管内皮生长因子)增加,虹膜和房角形成新生血管。纤维血管组织的形成和收缩导致周边虹膜前粘连(PAS),最终引起不可逆的房角关闭。
自20世纪上半叶开始,就有关于视网膜缺血伴虹膜红变的报道,1960年代以后“新生血管性青光眼”这一术语得以确立。在此之前,曾使用出血性青光眼、充血性青光眼、血栓性青光眼等多种名称,但现在统一为NVG。
最常见的原发病是增殖性糖尿病视网膜病变(PDR)和视网膜静脉阻塞(RVO),约占所有病例的三分之二。其他原因包括视网膜脱离、视网膜动脉阻塞和眼缺血综合征(OIS)1)。一项大型回顾性研究(129只眼)显示,原发病的分布为:增殖性糖尿病视网膜病变53%、视网膜静脉阻塞29%、视网膜脱离7%、视网膜动脉阻塞6%、眼缺血综合征2%2)。
病理核心是VEGF介导的前段新生血管形成。Wakabayashi等人对41例继发于缺血性视网膜疾病的虹膜新生血管和新生血管性青光眼连续病例进行了玻璃体内注射贝伐珠单抗,几乎所有病例在给药后48小时内观察到虹膜新生血管消退12)。这种快速的新生血管消退证实了VEGF在前段新生血管形成中的主要作用。
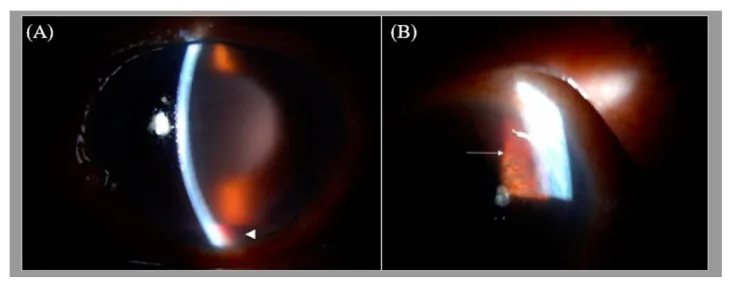
眼压轻度升高时无症状。随着眼压升高,出现视物模糊、虹视、眼痛。如果病情急剧恶化,可能伴有类似急性闭角型青光眼发作的剧烈眼痛、头痛、恶心、呕吐。另一方面,如果糖尿病视网膜病变或视网膜静脉阻塞等原发病导致的视力下降先于眼压升高,则对眼压升高的自觉症状可能不明显。当眼压极度升高时,会发生大疱性角膜病变,患者可能因异物感和眼痛就诊。
本病的分期广泛采用Shields的四期分类。各期的临床所见如下。
青光眼前期至开角期
虹膜红变:瞳孔缘出现微细的新生血管簇。正常血管在虹膜实质内呈放射状走行,而新生血管在虹膜表面呈不规则、迂曲的图案。
房角新生血管:可见越过巩膜突延伸至小梁网上的树枝状细血管。眼压正常至轻度升高。
纤维血管膜:覆盖小梁网增殖,导致继发性开角型青光眼。
闭角期至绝对期
葡萄膜外翻:纤维血管膜收缩导致虹膜后方的色素层向前表面翻转。虹膜表面变得平滑。
周边虹膜前粘连进展:虹膜被帐篷状拉向小梁网,导致粘连性房角关闭。眼压显著升高。
绝对期青光眼:视功能恢复极为困难。高眼压引起的眼痛成为主要症状。
一项针对129只眼的回顾性研究显示,新生血管性青光眼诊断时,25%为开放房角,30%为部分关闭,45%为完全关闭2)。完全关闭眼的视力更差(中位数20/4375),眼压更高(中位数59 mmHg)2)。仅凭临床所见无法准确预测房角状态,因此所有病例均需进行房角镜检查2)。
| 原发疾病 | 频率 |
|---|---|
| 增殖性糖尿病视网膜病变 | 53%2) |
| 视网膜静脉阻塞 | 29%2) |
| 视网膜脱离 | 7%2) |
| 视网膜动脉阻塞 | 6%2) |
| 眼缺血综合征 | 2%2) |
在视网膜静脉阻塞中,缺血型CRVO约在3个月内易发生虹膜红变,常被称为“100天青光眼”(90-day glaucoma)。在增殖性糖尿病视网膜病变中,长期视网膜无灌注区的积累促进VEGF产生,前段新生血管倾向于缓慢进展。眼缺血综合征由于存在颈内动脉闭塞或狭窄,需要通过颈动脉超声和头部MRA等进行辅助诊断。
Temkar等人(2023)报告了一例30岁男性因外伤性颈内动脉海绵窦瘘(CCF)伴视网膜动静脉复合闭塞而发展为NVG的病例4)。静脉淤滞和动脉功能不全导致的严重视网膜缺血是NVG发病的机制。
Zakaria等人(2023)报告了一例睫状视网膜动脉保留型CRAO患者在2周内发展为NVG的病例3)。CRAO中18.2%发生新生血管化,平均在8.5周出现3)。
Fliney等人(2021)报告了一例20岁男性以NVG为首发表现的脉络膜恶性黑色素瘤病例7)。肿瘤产生的VEGF和FGF是NVG的原因。约2%的脉络膜黑色素瘤出现眼压升高,其中大部分为NVG7)。
增殖性糖尿病视网膜病变是NVG最常见的病因,约占所有NVG的53%2)。但并非所有糖尿病患者都会发展为NVG,血糖控制和通过视网膜光凝管理视网膜缺血对预防发病至关重要。在无灌注区变得广泛之前进行全视网膜光凝是抑制前段新生血管发生的关键。
早期发现虹膜红变是诊断的关键。由于散瞳药会引起血管收缩,使新生血管不易观察,因此在未散瞳状态下进行裂隙灯显微镜检查和房角镜检查非常重要10)。在高倍镜下观察瞳孔缘,不要漏诊早期虹膜红变至关重要。
房角镜检查中,可见新生血管越过巩膜突延伸到小梁网上。有时由于全周周边虹膜前粘连,房角内可能无法直接看到新生血管,但如果存在虹膜红变,应考虑本病并开始治疗。在糖尿病视网膜病变或视网膜静脉阻塞的随访中,需要定期在未散瞳状态下观察瞳孔缘,以检测微小的新生血管。
需要与表现为虹膜红变的疾病进行鉴别。Fuchs虹膜异色性虹膜睫状体炎可在虹膜表面出现异常血管,但通常不伴有房角关闭,且通常不出现纤维血管膜收缩引起的葡萄膜外翻。ICE综合征(虹膜角膜内皮综合征)通常为单眼,伴有角膜内皮异常,并呈现虹膜实质萎缩、虹膜孔形成、瞳孔偏位等特征性表现,因此可以区分。与炎症性继发性青光眼的鉴别可参考前房细胞和角膜后沉着物的有无。
治疗策略是改善视网膜缺血和控制眼压并行10)。仅处理一方面无法使病情稳定,需要根据病期将两者结合。
全视网膜光凝术(PRP)
抗VEGF药物
开角期:通过玻璃体内注射VEGF抑制剂使新生血管消退后,再进行PRP
快速消退:Wakabayashi等人的41例连续病例中,IVB给药后48小时内虹膜新生血管消退12)
术前给药:术前联合使用抗VEGF药物可减少术中及术后并发症10)14)(证据等级2B)
抗VEGF药物的玻璃体内注射(intravitreal bevacizumab: IVB)是新生血管性青光眼药物治疗的核心。一项关于贝伐珠单抗玻璃体内注射的随机对照试验报告,与对照组相比,IVB单药治疗NVG显著促进了眼压下降和新生血管消退13)。新生血管抑制期一般为3至6周,在此期间完成PRP是理想的。在日本,贝伐珠单抗玻璃体内注射属于超说明书用药,因此必须经过各医疗机构的伦理委员会批准。
按照原发性开角型青光眼进行药物治疗10)。抑制房水生成的β受体阻滞剂和碳酸酐酶抑制剂理论上有效性较高。前列腺素类似物和α2肾上腺素能受体激动剂也可联合使用。口服碳酸酐酶抑制剂应在确认无肾功能障碍后进行。高渗剂的静脉输注旨在暂时降低眼压,但效果持续时间短,肾功能减退患者有急性肾衰竭风险,需谨慎。硫酸阿托品滴眼液和皮质类固醇滴眼液可能对消炎和缓解疼痛有效10)。
副交感神经受体激动剂毛果芸香碱(缩瞳药)通常无效,并可能因破坏血-房水屏障而导致病情恶化,因此不推荐使用10)11)。
根据病期的治疗选择指南如下。
在IVB使用之前,小梁切除术术中及术后常伴有大量前房出血,常导致滤过功能不全。术前进行IVB可减少围手术期前房出血,眼压控制在21 mmHg以下的成功率约为60%。预后不良因素包括年龄小于50岁和有玻璃体手术史。特别是在年轻患者中,周边虹膜前粘连快速进展的闭角期病例,术后效果往往不佳。近年来微创玻璃体手术的普及减少了结膜瘢痕,也有助于提高小梁切除术的疗效。
视网膜缺血导致供氧不足时,视网膜细胞释放VEGF、IL-6等血管生成因子。正常情况下,VEGF水平与抗血管生成因子色素上皮衍生因子(PEDF)保持平衡。当这种平衡向VEGF优势倾斜时,内皮细胞的活化、增殖和迁移得到促进,导致眼前段新生血管形成。已知房水中VEGF浓度在NVG眼中比健康眼高出数十倍以上,与眼前段新生血管的发生直接相关。
新生血管性青光眼的新生血管壁薄,缺乏肌层,紧密连接缺失,通透性增高。这些新生血管伴有由肌成纤维细胞增殖形成的纤维血管膜。最初,纤维血管膜覆盖小梁网,增加房水流出阻力,表现为继发性开角型青光眼。随后,膜的收缩导致虹膜表面变平、葡萄膜外翻和周边虹膜前粘连形成,最终导致房角不可逆关闭1)。
初期,纤维血管膜覆盖小梁网,形成继发性开角型青光眼1)11)。随后,膜收缩导致周边虹膜前粘连,转变为粘连性闭角型青光眼。在有晶状体眼中,房角关闭更容易进展2),一旦到达此阶段,常规滤过手术单独难以实现长期眼压控制。只要基础视网膜缺血持续存在,新生血管和纤维血管膜收缩就会继续进展,因此通过PRP或抗VEGF疗法抑制缺血状态是治疗的根本。
Wang等人(2024)对129只NVG眼进行了研究,探讨诊断时房角状态的预测因素2)。完全关闭眼的视力和眼压均更严重,但仅凭临床特征无法准确预测房角状态。急诊就诊的病例中完全关闭的频率更高,有PRP或玻璃体手术史的眼也倾向于更多房角关闭2)。
Soman等人(2022)报告了一例由COVID-19相关视网膜病变引起的快速发作NVG病例5)。一名50岁男性在感染COVID-19三周后出现双眼视网膜血管病变,右眼在两周内进展为NVG。其机制被认为是血栓前状态相关的视网膜血管损伤。通过抗青光眼药物和PRP,新生血管完全消退,眼压恢复正常5)。
ALKhamees等人(2023)报告了一名患有Pierson综合征(LAMB2突变)的11岁女孩,出现自发性前房积血、玻璃体积血和新生血管性青光眼8)。观察到继发于视网膜缺血的虹膜和房角新生血管,最终需要睫状体光凝术,但眼球仍进展为眼球痨8)。