视网膜中央动脉阻塞(CRAO)是由于视网膜 中央动脉突然阻塞,导致无痛性急剧严重视力 下降的眼科急症 。
动脉阻塞后约100分钟视网膜 开始发生不可逆变化,因此需要尽早处理。
CRAO大致分为非动脉炎性(90%以上)和动脉炎性两种。有永久性、一过性和睫状视网膜 动脉开放型三种亚型。
CRAO与脑卒中具有相同的危险因素,15-20%的CRAO患者在30天内发生脑卒中。
所有50岁及以上的患者必须排除巨细胞动脉炎 ;若怀疑,应在确诊前开始使用类固醇 。
不经治疗,视力 恢复的可能性仅约18%,视力 预后不良,常降至指数或更差。
急性期治疗包括亚硝酸异戊酯吸入、静脉注射醋甲唑胺、尿激酶给药、眼球按摩和前房穿刺 。发病24小时内应积极治疗。
早期给予PGE₁(前列腺素E₁)可能改善视力 (研究阶段)。
视网膜动脉阻塞 是由于视网膜动脉阻塞 导致视网膜 缺血和坏死,引起严重视功能障碍的疾病。动脉阻塞后约100分钟视网膜 开始发生不可逆变化,因此即使治疗,视力 预后也常不良。根据阻塞部位分为以下三型。
CRAO
视网膜中央动脉阻塞(CRAO) :视网膜中央动脉阻塞。是最严重的类型,视力 常降至手动或光感。
发病率 :每年每10万人中1例,每1万门诊患者中1例8) 。
BRAO
视网膜 分支动脉阻塞视力 预后因阻塞部位而异。
特点 :80%最终能维持矫正视力 0.5以上。如果黄斑部 未受损,视力 不会下降。
睫状视网膜动脉阻塞
睫状视网膜动脉阻塞 :睫状视网膜 动脉的阻塞。它是短后睫状动脉的分支,存在于约32%的眼睛中。供应视乳头黄斑 束附近的视网膜 。
特点 :可能合并CRAO发生,也可能单独发生。
CRAO进一步分为非动脉炎性和动脉炎性。非动脉炎性CRAO占所有病例的90%以上,有以下三种亚型:
持续性非动脉炎性CRAO :由动脉粥样硬化引起的血栓形成或栓塞所致。约占所有CRAO病例的三分之二。视力 通常低于0.1,樱桃红斑 是典型表现。一过性非动脉炎性CRAO :类似于TIA(短暂性脑缺血发作),持续数分钟至数小时。最常见原因是游走性栓塞,视力 预后最好。伴有睫状视网膜 动脉开放的非动脉炎性CRAO :由于睫状视网膜 动脉维持了中心凹 循环,中心视力 可能得以保留。
动脉炎性CRAO 继发于巨细胞动脉炎 (GCA),约占CRAO患者的4%。在四种类型中预后最差,视力 丧失几乎不可逆。更可能发生在70岁及以上的患者,常伴有头痛、头皮压痛、下颌跛行、全身乏力、体重减轻等GCA相关症状。对于所有50岁及以上的CRAO患者,最重要的是排除动脉炎性CRAO,需快速检测ESR和CRP ,必要时进行颞动脉活检。如果高度怀疑GCA,应立即开始全身类固醇 治疗,无需等待确诊8) 。治疗延迟会增加对侧眼失明的风险。
CRAO的发病率估计为每年每10万人约1例,或每1万名门诊患者中1例。平均发病年龄在60岁出头,发病率随年龄增长而增加8) 。男性多见,通常单眼发病,但1-2%为双眼发病。双眼发病时应怀疑巨细胞动脉炎 8) 。日本的发病率低于西方国家,属于相对罕见的疾病,但早期处理对视力 预后至关重要,是一种高度紧急的疾病。
视网膜 是胚胎期从脑分化而来的组织,被视为中枢神经系统的一部分。它与脑卒中的关系密切;2013年,AHA/ASA(美国心脏协会/美国卒中协会)修订了脑卒中的定义,明确将视网膜 缺血列为CNS(中枢神经系统)梗死的一种类型8) 。15-20%的CRAO患者在30天内发生脑卒中,作为“眼卒中”,建议在卒中中心进行紧急全身评估8) 。
Q
CRAO与脑卒中有关吗?
A
CRAO与脑卒中共享相同的危险因素(动脉硬化、心房颤动、栓塞等),发病后30天内脑卒中风险高达15-20%8) 。AHA/ASA将视网膜 缺血定义为CNS梗死,CRAO发病后必须与神经科和心血管科协作进行紧急全身评估。
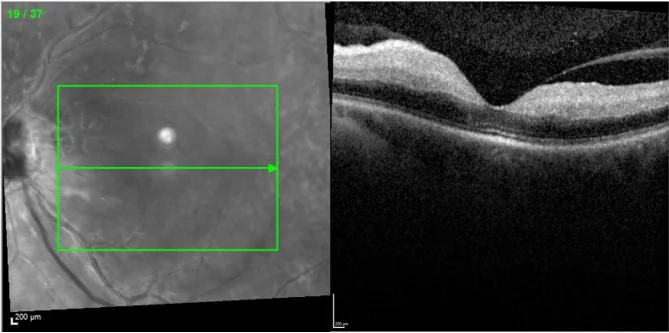
视网膜中央动脉阻塞的OCT图像。黄斑区内视网膜弥漫性高反射和增厚。 Louie E, et al. Paracentral acute middle maculopathy presenting as a sign of impending central retinal artery occlusion: a case report. BMC Ophthalmol. 2023. Figure 3. PM
CI D: PMC10262410. License: CC BY.
红外线眼底像和黄斑部 OCT 断层像。OCT 显示内视网膜 弥漫性高反射和增厚,是急性视网膜 缺血的表现,适用于视网膜中央动脉阻塞的文章。
突然发作的无痛性重度视力 下降是最大特征。
急剧视力 下降 :数秒至数分钟内完成,视力 常降至手动或光感。由于无痛,患者不易意识到紧急性。一过性视力 障碍前驱 :部分患者在CRAO发生前反复出现一过性视力 障碍(一过性黑蒙 )。这是脑卒中前驱症状(TIA)的重要表现。睫状视网膜 动脉保留时的视力 保持 :在睫状视网膜 动脉供应中心凹 的个体(约占全部眼睛的32%,CRAO病例的约1/3)中,CRAO时该动脉不受阻塞影响,因此中心视力 可能得以保留。
CRAO患者可能在发病前反复出现一过性视力 障碍。这称为一过性黑蒙 (amaurosis fugax),是脑卒中前驱症状(TIA)的重要警告信号。视力 消失数分钟后自然恢复,但常常是主要发作的前兆。
有报道一例6岁女童的COVID-19相关CRAO,表现为突然双眼视力 丧失,表明(尽管罕见)儿童也可能发病1) 。
急性期呈现特征性所见,但随时间推移而变化。发病后2小时内的超急性期,眼底所见可能正常或仅黄斑部 轻微混浊。
樱桃红斑 (cherry-red spot)视网膜 呈乳白色混浊。中心凹 仅由视网膜 外层构成,由脉络膜 营养,因此不发生混浊,与周围白浊对比呈红色。眼动脉阻塞(OAO )时,脉络膜 循环也受损,因此缺乏樱桃红斑 8) 。动脉变细、白线化 :闭塞的视网膜 动脉显著变细,呈白线化,血管内可能无血液。串珠状血流(beading)和分节状血流(fragmentation) :闭塞动脉中可见微小血柱缓慢流动的特征性表现。箱车现象(boxcar segmentation) :动脉或静脉内血液被分割成节段状。提示急性期严重缺血8) 。
OCT 视网膜 内层(从神经纤维层到内颗粒层)高反射和增厚。与通常的视网膜 水肿不同,这反映了缺血引起的细胞内水肿(细胞肿胀)。旁中心凹 急性中层黄斑 病变(PAMM )是OCT 检测到的视网膜 中层高反射带,在急性期具有特征性8) 。一过性非动脉炎性CRAO中,视网膜 内层增厚轻微,内层高反射可见。数周后视网膜 和脉络膜 变薄,发病4-6周后视网膜 混浊消失,但不仅内层,外层也发生逆行性萎缩,层结构难以辨认。荧光眼底造影(FA ) :臂-视网膜 循环时间延长至30秒以上(通常约12秒),视网膜 血管充盈显著延迟。可见血管壁不规则、明显的荧光素 渗漏和视网膜 内循环时间延迟。有助于确定闭塞部位,并评估睫状视网膜 动脉的存在和灌注范围。视网膜电图 (ERG )脉络膜 营养而存活,a波正常,但双极细胞和Müller细胞受损导致b波减弱或消失,呈负波型ERG 。这是CRAO的特征性表现,从电生理学上证实了内层为主的缺血。OCTA (光相干断层扫描血管成像)视网膜 毛细血管的灌注缺损 。急性期灌注缺损 模式可能成为长期预后的预测因子,已有研究。
在一例COVID-19相关CRAO的6岁女童中,发病5个月后RNFL (视网膜神经纤维层 )变薄仍持续存在1) 。慢性期OCT 显示视网膜 变薄,不仅内层,外层也发生逆行性萎缩,层结构难以辨认。
Q
为什么会出现樱桃红斑?
A
在CRAO中,整个视网膜 内层因缺血性细胞内水肿而呈乳白色混浊。然而,中心凹 仅由视网膜 外层构成,并从脉络膜 毛细血管获得营养,因此不发生混浊。与周围白浊对比,脉络膜 的红色浮现出来,这就是樱桃红斑 的机制。详细的血管解剖请参见“病理生理学”一节 。
CRAO的主要原因是栓塞,约占所有病例的95%8) 。原因分布因年龄和基础疾病而异。
年龄组 主要原因 应检查的病变 50岁及以上 动脉硬化性栓塞/血栓 颈动脉狭窄、心房颤动、高血压 50岁以下 凝血异常、PFO、血管炎 反常栓塞、自身免疫性疾病
动脉硬化性栓塞 :多见于患有高血压、动脉硬化、糖尿病等全身性疾病的老年人。颈内动脉粥样硬化或心脏疾病形成的心腔内血栓成为栓子。胆固醇栓子(Hollenhorst斑块)或钙化栓子从颈动脉或主动脉弓脱落,在视网膜 中央动脉管腔最狭窄处(视神经 硬膜鞘穿通部)引起闭塞。卵圆孔未闭(PFO) :50岁以下CRAO患者的重要病因。通过静脉系统血栓经PFO进入动脉系统的反常栓塞机制引起。经食管超声心动图(TEE)诊断率高达85.7%,而经胸超声心动图(TTE)仅为14.3% 3) 。巨细胞动脉炎 (GCA)RP 、CBC筛查 8) 。透明质酸(HA)注射 :因美容目的面部皮下注射HA后发生视网膜动脉阻塞 (RAO )的病例正在增加 8) 。机制考虑为逆行栓塞,即使少量HA(0.08 mL)也可导致阻塞 2) 。血管炎、感染、外伤、血管痉挛 :虽不常见,但可能成为病因。血管痉挛与偏头痛 或可卡因使用等相关。年轻患者的特殊原因 :在50岁以下年轻患者中,血液凝固系统异常(如抗磷脂抗体综合征、血栓形成倾向)、心脏病、先天异常和视网膜血管炎 比动脉粥样硬化更常见。年轻CRAO患者需积极进行经食管超声心动图和凝血功能检查以寻找栓子来源。COVID-19 :可通过高凝状态和血管内皮损伤导致血栓形成而引起CRAO,儿童中也有发病报道 1) 。
可改变的风险因素包括吸烟、高血压、高BMI、血脂异常、糖尿病、凝血异常和心脏病(包括心房颤动)8) 。约60%的CRAO患者至少有一个未诊断的血管危险因素,其中血脂异常最常见。低HDL胆固醇也被报道为独立危险因素 8) 。
全身性风险因素列举如下。
高血压 :最重要的可改变风险因素血脂异常 :CRAO患者中最常见的未诊断危险因素糖尿病 :与视网膜 微血管病变的复合风险。有报道糖尿病患者一只眼发生BRAO 后,对侧眼发生CRAO的病例 4) 吸烟 :动脉粥样硬化促进因素心房颤动 :心源性栓塞的主要风险高BMI和阻塞性睡眠呼吸暂停 :与动脉粥样硬化相关的因素美容填充剂注射 :一种呈增加趋势的医源性风险因素8)
控制高血压、糖尿病和血脂异常对视网膜动脉阻塞 的一级预防有效。
戒烟是抑制动脉硬化进展最重要的生活方式改善。
面部美容用透明质酸注射是有视力 丧失风险的操作。接受治疗前请充分了解风险。
如果出现突然的视力 下降,即使没有疼痛也应立即就诊眼科。该疾病被视为“眼部卒中”。
CRAO通常可通过眼底所见诊断,但必须进行全身评估以查找病因。CRAO的管理分为三个阶段:第一,急性期的血流恢复;第二,亚急性期的继发性并发症预防;第三,未来血管缺血事件的全身控制和预防。
裂隙灯 显微镜和眼底检查 樱桃红斑 、视网膜 混浊、动脉变细和盒样现象。可视化栓子,评估睫状视网膜 动脉的存在,并评估闭塞范围。光学相干断层扫描 (OCT )视网膜 内层的高反射和增厚。有助于检测旁中心凹 急性中层黄斑 病变(PAMM )8) 。慢性期会残留视网膜 内层变薄和萎缩。荧光素眼底血管造影 (FA )视网膜 动脉的充盈延迟或充盈缺损 ,并确定闭塞部位。臂-视网膜 循环时间延长(≥30秒)是特征性表现。视网膜电图 (ERG )ERG (a波正常,b波减弱)是CRAO的特征,反映内层为主的缺血。
各项检查获得的主要所见如下所示。
检查方法 主要所见 OCT 急性期:内层高反射、增厚 → 慢性期:内层变薄 FA 充盈延迟,臂-视网膜 循环时间≥30秒 ERG a波正常,b波减弱(负波型ERG )
急性CRAO需立即转诊至卒中中心进行紧急全身评估8) 。症状性RAO 患者的卒中风险在发病前2周至发病后1个月最高8) 。
颈动脉超声/MRA :查找动脉粥样硬化病变和栓塞来源。症状性颈动脉狭窄(50-99%)时,颈动脉内膜剥脱术的预后优于内科治疗8) 。心电图/动态心电图 :检测心房颤动。超声心动图(经胸:TTE) :评估心脏瓣膜病和心内血栓。50岁以下年轻CRAO患者中,TTE的诊断率仅为14.3%,85.7%需要TEE3) 。经食管超声心动图(TEE) :在怀疑PFO的病例中进行。TTE容易漏诊3) 。血液检查 :血常规、凝血功能(PT、APTT、D-二聚体)、ESR、CRP (排除巨细胞动脉炎 )。50岁及以上新发CRAO患者必须检测ESR和CRP 以鉴别巨细胞动脉炎 8) 。TOAST分型 :采用与脑梗死相同的病因分类框架(大动脉粥样硬化性栓塞、心源性栓塞、小血管闭塞、其他明确病因、不明原因)5) 。
排除动脉炎性CRAO :所有50岁及以上患者必须进行。检查有无头痛、头皮压痛和下颌跛行,并迅速测量ESR和CRP 。血小板计数升高也是GCA的辅助指标。若高度怀疑,在颞动脉活检确诊前即开始使用类固醇 8) 。与睫状视网膜 动脉开放型CRAO的区分 :根据中心视力 是否保留来判断。眼底可见樱桃红斑 周围有典型的CRAO混浊,但乳头黄斑 束附近未受累。一过性CRAO与BRAO 的鉴别 :根据症状持续时间(一过性在数分钟至数小时内自行恢复)和闭塞范围(BRAO 局限于扇形视野缺损 )来区分。眼动脉闭塞症(OAO ) :视网膜 循环和脉络膜 循环均受损,缺乏樱桃红斑 是与CRAO的不同之处8) 。FA 检查也可确认脉络膜 充盈延迟。无症状性视网膜 栓塞 :在49岁及以上的一般人群中约1.4%可见8) 。目前没有证据支持对无症状性视网膜 栓塞进行紧急卒中评估8) 。
Q
50岁及以上CRAO患者最重要的鉴别诊断是什么?
A
排除巨细胞动脉炎 (GCA)引起的动脉炎性CRAO最为重要。GCA相关CRAO约占所有CRAO的4%,预后最差。若怀疑GCA,应立即开始全身类固醇 治疗,无需等待确诊(颞动脉活检)8) 。未经治疗,存在对侧眼失明的风险。
CRAO是眼科急症 ,为改善视力 预后,超急性期的迅速处理至关重要。发病后立即治疗最为理想,发病1天内的病例应积极治疗。
动脉闭塞后约100分钟开始出现严重的视网膜 损伤。治疗在发病后立即进行最为理想,约4小时内是急性期治疗的目标时间6) 。从发病到就诊的时间越长,预后越差,但发病1天内的病例仍应积极治疗。对于早期出现视力 障碍的BRAO ,采用与CRAO相同的治疗策略。
Zokri MF等人(2024)在急性RAO 病例系列中强调,治疗开始时间是决定视力 预后的最重要因素6) 。因就诊延迟而失去治疗干预机会的病例不在少数。
根据症状采用以下治疗方法。
血管扩张药
亚硝酸异戊酯 :将0.25 mL/瓶的安瓿压碎,吸附于覆盖物上,经鼻孔吸入(注意血压下降;医保外用药)。
硝酸异山梨酯舌下含服 :促进血管扩张。
卡波金吸入 :吸入95%氧气+5%二氧化碳混合气体。促进血流增加,但伴有全身血压下降的风险。
己酮可可碱 :改善末梢循环的药物。通过改善红细胞变形能力促进视网膜 血流。
药物治疗
醋唑磺胺注射液 :500 mg 每日一次静脉注射(医保外用药)。作为碳酸酐酶抑制剂 ,降低眼压 并促进视网膜 动脉扩张。
尿激酶 :初始每日剂量6万~24万单位,之后逐渐减量,约给药7天。注意脑出血和全身出血。
奥巴蒙片 :5 μg×6片,分3次饭后服用。作为前列腺素E₁衍生物,旨在改善末梢血流。
操作与全身管理
眼球按摩 :降低眼压 ,将栓子推向末梢。是可立即实施的操作。
前房穿刺 房水 ,使眼压 急剧下降,相对提高动脉灌注压。
星状神经节阻滞 :有时为改善眼部血流而实施。
但是,保守治疗(眼球按摩、前房穿刺 、卡波金吸入)尚未被证明有显著疗效8) 。这些操作仅在发病超早期理论上具有意义,但尚无确凿证据表明其能改善预后优于自然病程。
急性CRAO应紧急转诊至卒中中心,并按照“眼卒中方案”进行评估和治疗8) 。在卒中中心,CRAO被视为与脑梗死同等的紧急疾病,正在建立统一管理tPA给药适应症判断、全身血管评估和二级预防的体系。
根据症状酌情使用以下药物。
亚硝酸异戊酯 :将0.25 mL/瓶碾碎,吸附于敷料上经鼻孔吸入(注意血压下降,超说明书用药)Diamox注射液 :500 mg 每日一次静脉注射。作为碳酸酐酶抑制剂 ,降低眼压 并促进视网膜 动脉扩张(超说明书用药)尿激酶静脉注射 :初始日剂量6万~24万单位,之后逐渐减量,约给药7天。需注意脑出血及全身出血倾向。Opalmon片(利马前列素α-环糊精) :5 μg×6片,分3次饭后服用。作为前列腺素E₁衍生物,旨在改善末梢血流。
静脉tPA给药 :适用于发病4.5小时内的适应症患者。荟萃分析显示,发病4.5小时内静脉给予tPA可能与改善预后相关8) 。需与卒中中心协作判断。动脉内溶栓治疗 :部分机构实施选择性眼动脉内尿激酶灌注。
有报告称,动脉内给予尿激酶30万单位后,视力 从20/2000戏剧性改善至20/33.34) 。
CRAO自然病程的视力 恢复率约为18%,但早期溶栓治疗可将其提高至约40%。然而,EAGLE试验(RCT)显示,动脉内(IA)tPA与保守治疗相比在视力 改善方面无显著差异,并指出了颅内出血(ICH)的安全性问题7) 。目前,CRAO的动脉内和静脉内纤溶治疗证据尚不充分8) 。
若怀疑动脉炎性CRAO,应立即开始全身性类固醇 治疗,无需等待确诊。治疗延迟有对侧眼失明的风险8) 。
一些小型回顾性研究提示有轻微效果,但Cochrane综述认为证据不确定8) 。
CRAO后的亚急性期,再灌注不全导致的慢性视网膜 缺血可能引起眼部新生血管 。新生血管 的患病率据报道为2.5%~31.6%,观察到新生血管 的平均时间为8.5周。据报道,18%的CRAO患者出现虹膜新生血管 ,发病后约4个月内定期眼科检查很重要。如果出现虹膜 或视网膜 新生血管 ,则适用全视网膜光凝 (PRP )8) 。
CRAO患者全身缺血性事件的风险增加,长期并发症预防需要与内科医生、卒中专家和心脏病专家合作。约60%的CRAO患者至少有一个未诊断的血管危险因素,以CRAO发病为契机进行全身检查是二级预防的第一步。
抗血小板治疗 :如果怀疑动脉粥样硬化性栓塞源,基本治疗是口服阿司匹林。CRAO的抗血小板治疗与轻度卒中的指南相同,如无禁忌则推荐使用5) 。抗凝治疗 :如果存在心源性栓塞源如心房颤动,则选择抗凝药物。心源性栓塞和动脉粥样硬化性栓塞的复发预防策略不同,因此需要基于病因检查进行治疗选择。颈动脉内膜剥脱术 :如果发现症状性颈动脉狭窄(50%~99%),颈动脉内膜剥脱术比内科治疗有更好的预后8) 。PFO封堵术 :在年轻CRAO患者中,如果认为PFO是原因,可考虑经皮PFO封堵术3) 。危险因素管理 :严格控制高血压、糖尿病和血脂异常,并彻底进行戒烟指导。也推荐饮食疗法和定期运动。他汀类药物治疗的心血管风险降低效果也有报道8) 。
CRAO的视力 预后不良,通常降至指数或更差。不经治疗,视力 恢复的可能性仅约18%。初诊时61%的患者视力 为20/400或更差8) 。发病后46周视网膜 混浊消失,视网膜 颜色恢复正常,但除非早期治疗有效,否则视功能不会恢复。发病后410周可能引起新生血管性青光眼 。
另一方面,在保留睫状视网膜 动脉的CRAO中,睫状视网膜 动脉的灌注区域得以保留,因此中心视力 可能得以维持。在短暂性CRAO中,闭塞自然解除,因此视力 预后最好。在BRAO 中,80%的患者最终维持矫正视力 0.5以上,但如果黄斑部 分支闭塞,则视力 预后不良。
CRAO后还需注意再灌注不全相关的并发症。虹膜新生血管 发生于约18%的CRAO患者,发病后4~10周可能进展为新生血管性青光眼 。如果出现新生血管 ,应迅速进行全视网膜光凝 (PRP )8) 。
动脉闭塞后约100分钟开始出现不可逆变化。需要尽早处理。
吸入亚硝酸异戊酯有血压下降的风险,需在血压监测下使用。属于医保外用药。
静脉注射醋唑磺胺也属于医保外使用。
尿激酶有脑出血和全身出血的风险,需要谨慎管理给药。
tPA疗法尚未确立为CRAO的标准治疗,并伴有ICH等严重并发症风险。
在GCA相关的CRAO中,需要毫不犹豫地开始使用类固醇 。即使活检未确诊,也应优先治疗。
新生血管 并发症好发于发病后4至10周,因此应持续进行约4个月的定期眼底和眼压 检查。
Q
发病后几小时内就诊才有治疗可能?
A
视网膜 不可逆损伤在闭塞后约100分钟开始。发病1天内应积极治疗,治疗越早预后越好。静脉注射tPA的适应症为发病4.5小时内8) 。无论如何,作为“眼部卒中”,应紧急前往卒中中心就诊。
眼动脉(颈内动脉的第一分支)分出的视网膜 中央动脉从视盘进入视网膜 ,为视网膜 内2/3(从神经纤维层到内颗粒层)提供氧气和营养。视网膜 外层的感光细胞 接受脉络膜 血管的营养,因此CRAO中外层相对保留。
睫状视网膜 动脉是短后睫状动脉的分支,存在于约32%的眼睛中,供应视乳头黄斑 束附近的视网膜 。由于睫状视网膜 动脉在眼动脉移行为视网膜 中央动脉之前分出,因此不受CRAO闭塞的影响。因此,如果该动脉保留,中心凹 视力 可能得以保持。
樱桃红斑 的发生机制如下。CRAO导致视网膜 动脉供血的视网膜 内层因急性缺血而发生细胞肿胀(细胞内水肿)和缺血性坏死,以后极部为中心呈现乳白色混浊。这种混浊的机制与普通视网膜 水肿(细胞外水肿)不同。普通视网膜 水肿因细胞外液体积聚在OCT 上表现为低反射,而CRAO因缺血性细胞内水肿(细胞肿胀)导致视网膜 内层呈高反射。OCT 显示视网膜 内层高亮且增厚。
中心凹 仅由视网膜 外层构成,由脉络膜 供血,因此不发生混浊。中心凹 几乎缺少内层(神经节细胞层、内丛状层、内颗粒层),仅存在外层(感光细胞 层)。因此,在周围乳白色混浊中,正常的红色调(脉络膜 毛细血管的颜色)浮现出来。这就是樱桃红斑 的成因。
在眼动脉闭塞症(OAO )中,眼动脉主干闭塞,视网膜 循环和脉络膜 循环均受损。由于脉络膜 缺血,樱桃红斑 不会出现8) 。
CRAO最常见的原因是血栓栓塞,闭塞发生在视网膜 中央动脉管腔最狭窄的部分(穿过视神经 硬膜鞘的部位)。栓子来源于颈动脉或心脏的斑块。
心源性/主动脉源性栓塞 :胆固醇栓子(Hollenhorst斑块)、钙化栓子、血小板纤维蛋白血栓从颈动脉斑块或主动脉弓脱落,阻塞视网膜 中央动脉。反常栓塞(经PFO) :静脉系统的血栓通过卵圆孔未闭(PFO)进入动脉系统,阻塞视网膜 动脉。有病例报告显示臂-视网膜 循环时间延长至约25秒,约为正常的两倍5) 。有研究表明,不经TEE检查可能漏诊PFO3) 。逆行性栓塞(HA注射后) :注入面动脉的透明质酸(HA)逆行到达眼动脉和视网膜 动脉的机制。仅0.08 mL的HA也可能引起闭塞2) 。
视网膜神经节细胞 对缺血极为脆弱,血流中断后数分钟内即开始出现功能障碍。不可逆损伤大约在100至105分钟后发生8) 。这是本病紧急性的依据。
根据缺血时间过程的组织变化如下。
超急性期(~2小时) :眼底所见基本正常,或仅黄斑部 轻微混浊。OCT 上视网膜 内层的高反射已开始出现。急性期(2小时至数天) :以后极部为中心的视网膜 呈乳白色混浊,樱桃红斑 清晰化。动脉显著变细,可见串珠状血流。OCT 显示视网膜 内层明显增厚和高亮。亚急性期(1-6周) :视网膜 混浊逐渐消退,4-6周后恢复为正常视网膜 色调。但除非早期治疗有效,否则视功能不会恢复。此期可能出现虹膜 和视网膜 新生血管 。慢性期(6周后) :OCT 显示视网膜 变薄,不仅内层,外层也出现逆行性萎缩。视盘苍白加重。即使闭塞血管最终再通,视力 通常也无法恢复。
有报道称,在慢性高血压状态下,发生不可逆变化的时间可延长至最长240分钟6) 。
在一例COVID-19相关CRAO的6岁女童中,使用了低分子肝素(LMWH)100 mg/kg和甲泼尼龙30 mg/kg,发病5个月后随访时RNFL 变薄持续存在1) 。
Sano等人(2025)在德岛红十字医院回顾性研究了发病24小时内CRAO患者早期使用PGE₁的效果9) 。PGE₁组(n=4)将阿普司特阿尔法地塞40 μg溶于250 mL生理盐水中,以125 mL/h的速度静脉输注,每日两次(80 μg/日),持续5天,随后口服利马前列素阿尔法地塞10 μg,每日三次(30 μg/日),持续至少1个月。与传统治疗组(n=6)相比,PGE₁组1个月时的最佳矫正视力 (BCVA)显著更好。PGE₁组基线最大视网膜 厚度(MRT)与1个月时的BCVA呈负相关。两组均未观察到不良事件9) 。
PGE₁除了血管扩张作用外,还具有通过减轻氧化应激 和炎症来发挥神经保护作用。样本量较小,需要前瞻性随机对照试验,但在现有治疗尚无确切疗效的情况下,这一发现值得关注。
将CRAO视为脑卒中的等同疾病,由脑卒中中心与眼科合作进行急性期评估和治疗的“眼卒中方案”正在推广中8) 。该方案有望提高tPA给药率,并促进脑卒中的早期发现和二级预防。
选择性眼动脉内注入尿激酶/tPA在一些机构进行,但随机对照试验的证据有限。EAGLE试验显示,IA tPA与保守治疗相比在视力 改善方面无显著差异,并指出了ICH(颅内出血)的安全性问题7) 。
在一例CRAO病例中,动脉内给予30万单位尿激酶使视力 从20/2000戏剧性地改善至20/33.34) 。然而,IA tPA存在血管夹层和颅内出血的风险7) ,病例积累和适应症标准的建立是未来的挑战。
这是一种非侵入性治疗方法,通过模拟主动脉内球囊反搏,在舒张期压迫下肢以增加眼灌注压。
有报道一例HA注射后RAO 合并PFO的40岁女性患者接受ECP 治疗,视力 从CF 30 cm改善至20/1332) 。然而,ECP 在RAO 中的证据仅限于病例报告和小规模研究。
当年轻CRAO患者确定PFO为病因时,可考虑经皮PFO封堵术预防反常栓塞。
Wieder MS 等人(2021年)在7例合并PFO的CRAO文献综述中得出结论,推荐适当的抗凝/抗血小板治疗或PFO封堵3) 。然而,尚无专门针对CRAO的PFO封堵随机试验。
PGE₁疗法
日本报告 :在CRAO中,PGE₁(前列地尔80 μg/日静脉注射5天,随后口服利马前列素30 μg/日)在1个月时显著改善BCVA9) 。
机制 :血管扩张+神经保护(减少氧化应激 和炎症)。无不良事件。
tPA的现状
EAGLE试验 :IA tPA与保守治疗相比无视力 改善益处,且存在ICH风险7) 。
IV tPA :在发病4.5小时内可能改善结局(荟萃分析),但RCT证据不足8) 。
Abbati G, Battini R, Bartalena L, et al. Central retinal artery occlusion in a 6-year-old girl with COVID-19. BMC Pediatrics. 2023;23:462.
Si M, Ma S, Lin H, et al. Retinal artery occlusion after hyaluronic acid rhinoplasty with patent foramen ovale: a case report. J Int Med Res. 2023;51:1-9.
Wieder MS , Barreto GNS, Barreto MNS, et al. Central retinal artery occlusion and patent foramen ovale. Arq Bras Oftalmol. 2021;84:494-498.
Li Z, Li M, Zhao Y, et al. Intra-arterial thrombolysis for bilateral sequential retinal artery occlusion in a diabetic patient: a case report and literature review. BMC Ophthalmology. 2025;25:331.
Zhu L, Gu X, Cai D, et al. Central retinal artery occlusion combined with internal carotid artery dysplasia and patent foramen ovale: a case report and literature review. Eur J Med Res. 2021;26:55.
Zokri MF, Othman O. A case series of retinal artery occlusion: when time is of the essence. Cureus. 2024;16(5):e60520.
Dalzotto K, Richards P, Boulter TD, Kay M, Mititelu M. Complications of intra-arterial tPA for iatrogenic branch retinal artery occlusion: a case report through multimodal imaging and literature review. Medicina. 2021;57(9):963.
American Academy of Ophthalmology Retina/Vitreous Panel. Retinal and Ophthalmic Artery Occlusions Preferred Practice Pattern. AAO ; 2024.
Sano H, Yanai R, Kondo H, Mitamura Y. Early prostaglandin E₁ treatment improves visual outcomes in central retinal artery occlusion: a retrospective study. Front Med (Lausanne). 2025.