CRAO
網膜中心動脈閉塞症(Central Retinal Artery Occlusion):網膜中心動脈の閉塞。最重症型であり、視力は眼前手動弁〜光覚弁にまで低下することが多い。
発生率:年間10万人に1人、外来患者1万人に1人8)。

網膜動脈閉塞症は、網膜動脈の閉塞による網膜の虚血と壊死によって重篤な視機能障害をきたす疾患である。動脈閉塞から約100分で不可逆性の変化が網膜に始まるため、治療をしても視力転帰は不良であることが多い。閉塞部位により以下の3型に分類される。
CRAO
網膜中心動脈閉塞症(Central Retinal Artery Occlusion):網膜中心動脈の閉塞。最重症型であり、視力は眼前手動弁〜光覚弁にまで低下することが多い。
発生率:年間10万人に1人、外来患者1万人に1人8)。
BRAO
網膜動脈分枝閉塞症(Branch Retinal Artery Occlusion):分枝の閉塞。視力予後は閉塞部位により大きく異なる。
特徴:80%は最終的に矯正視力0.5以上を維持する。黄斑部が障害されなければ視力は低下しない。
毛様網膜動脈閉塞症
毛様網膜動脈閉塞症(Cilioretinal Artery Occlusion):毛様動脈の閉塞。短後毛様動脈の分枝であり、全眼の約32%に存在する。乳頭黄斑束付近の網膜を栄養する。
特徴:CRAOに合併する場合と単独で生じる場合がある。
CRAOはさらに非動脈炎性と動脈炎性に分類される。非動脈炎性CRAOは全症例の90%以上を占め、以下の3亜型がある。
動脈炎性CRAOは巨細胞性動脈炎(GCA)に続発し、CRAO患者の約4%を占める。4型のなかで最も予後が不良であり、視力喪失はほぼ不可逆的である。70歳以上の患者で発生する可能性が高く、頭痛・頭皮圧痛・顎跛行・全身倦怠感・体重減少などのGCA関連症状を伴うことが多い。50歳以上のすべてのCRAO患者において動脈炎性CRAOを除外することが最も重要とされ、ESR・CRPの迅速測定と必要に応じた側頭動脈生検を行う。GCAが強く疑われる場合は確定診断を待たずにステロイドの全身投与を直ちに開始する8)。治療の遅延は対側眼失明のリスクを高める。
CRAOの発生率は年間10万人あたり約1人、外来患者1万人あたり1人と推定される。平均発症年齢は60代前半であり、発症率は年齢とともに増加する8)。男性に多く、片眼に発症することが多いが、1〜2%は両眼に発症する。両眼発症の場合は巨細胞性動脈炎を疑う必要がある8)。わが国での発症率は欧米に比較し低く、ややまれな疾患といえるが、ごく早期の対応が視力予後を左右する緊急性の高い疾患である。
網膜は胎生期に脳から分化した組織であり、中枢神経系の一部とみなされる。脳卒中との関係は密接であり、2013年にAHA/ASA(米国心臓協会/脳卒中協会)は脳卒中の定義を改訂し、網膜虚血をCNS(中枢神経系)梗塞の一型として明示的に位置づけた8)。CRAO患者の15〜20%が30日以内に脳卒中を発症するとされ、「Eye stroke(眼の脳卒中)」として脳卒中センターによる緊急全身評価が推奨されている8)。
CRAOは脳卒中と同一の危険因子(動脈硬化、心房細動、塞栓など)を共有し、発症後30日以内の脳卒中リスクが15〜20%と高い8)。AHA/ASAは網膜虚血をCNS梗塞と定義しており、CRAO発症後は神経科・循環器科と連携した緊急全身評価が不可欠である。
突然発症する無痛性の高度視力低下が最大の特徴である。
CRAOでは発症前から一過性の視力障害を繰り返している場合がある。これは一過性黒内障(amaurosis fugax)と呼ばれ、脳卒中の前駆症状(TIA)として重要な警告サインである。数分間の視力消失後に自然回復するが、本発作の前兆であることが少なくない。
6歳女児のCOVID-19関連CRAOでは、突然の両眼視力喪失をきたした症例が報告されており、小児での発症も(まれながら)起こりうる1)。
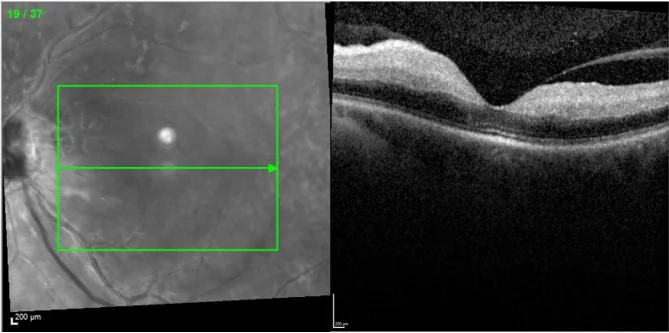
急性期に特徴的な所見を呈するが、時間経過とともに変化する。発症後2時間以内の超急性期では眼底所見は正常か、黄斑部がわずかに混濁しているに過ぎない。
COVID-19関連CRAOの6歳女児例では、発症5か月後もRNFL(網膜神経線維層)菲薄化が持続していた1)。慢性期のOCTでは網膜が菲薄化し、内層のみならず外層まで逆行性萎縮をきたして層構造が確認困難となる。
CRAOでは網膜内層全体が虚血性細胞内浮腫により乳白色に混濁する。しかし中心窩は網膜外層のみで構成され、脈絡膜毛細血管から栄養を受けるため混濁しない。周囲の白濁との対比で脈絡膜の赤色が浮かび上がって見えるのが桜実紅斑の機序である。詳細な血管解剖は「病態生理学」の項を参照。
CRAOの主な原因は塞栓であり、全症例の約95%を占める8)。年齢や基礎疾患によって原因分布が異なる。
| 年齢層 | 主な原因 | 検索すべき病態 |
|---|---|---|
| 50歳以上 | 動脈硬化性塞栓・血栓 | 頸動脈狭窄・心房細動・高血圧 |
| 50歳未満 | 凝固異常・PFO・血管炎 | 奇異性塞栓・自己免疫疾患 |
修正可能なリスク因子として、喫煙・高血圧・高BMI・脂質異常症・糖尿病・凝固異常・心疾患(心房細動を含む)が挙げられる8)。CRAO患者の約60%は少なくとも1つの未診断の血管危険因子を有しており、脂質異常症が最も多い。HDLコレステロール低値も独立したリスク因子として報告されている8)。
全身的なリスク因子を以下に列挙する。
CRAOは眼底所見で診断できることが多いが、原因検索のための全身評価が不可欠である。CRAOの管理は3段階に分類される。第一に急性期の血流回復、第二に亜急性期の二次合併症予防、第三に今後の血管虚血イベントの全身制御と予防である。
各検査で得られる主な所見を以下に示す。
| 検査法 | 主な所見 |
|---|---|
| OCT | 急性期:内層高反射・肥厚→慢性期:内層菲薄化 |
| FA | 充盈遅延、腕網膜循環時間30秒以上 |
| ERG | a波正常・b波減弱(陰性型ERG) |
急性期のCRAOは脳卒中センターへ即時紹介し、緊急全身評価を行う8)。症候性RAO患者の脳卒中リスクは発症前2週間〜発症後1か月が最も高い8)。
巨細胞性動脈炎(GCA)による動脈炎性CRAOの除外が最重要である。GCA関連CRAOはCRAO全体の約4%を占め、予後が最も不良である。GCAが疑われたら確定診断(側頭動脈生検)を待たずに全身ステロイド投与を即座に開始する8)。未治療では対側眼失明のリスクがある。
CRAOは眼科的緊急疾患であり、視力予後改善のためには超急性期の迅速な対応が不可欠である。発症直後の治療が好ましく、発症から1日以内の症例であれば積極的に治療を行うべきとされる。
動脈閉塞から約100分で重篤な網膜障害が生じ始める。治療は発症直後が最も好ましく、約4時間以内が急性期治療の目安とされる6)。発症から受診までの時間が長いほど予後は不良となるが、発症1日以内であれば積極的に治療を行うべきとされる。BRAOでも発症早期で視力障害があるものはCRAOと同様の治療方針をとる。
Zokri MFら(2024)は急性RAOの症例シリーズにおいて、治療開始までの時間が視力転帰を決定する最も重要な因子であることを強調した6)。受診の遅れにより治療介入の機会が失われる症例が少なくない。
以下の治療法が症状に応じて用いられる。
血管拡張薬
亜硝酸アミル:0.25 mL/バイアルを破砕し、被覆に吸収させて鼻孔から吸入(血圧低下に注意・保険適用外)。
硝酸イソソルビド舌下:血管拡張を促す。
カーボゲン吸入:95%酸素+5%CO₂混合ガスの吸入。血流増加を促すが全身血圧低下のリスクを伴う。
ペントキシフィリン:末梢循環改善薬。赤血球変形能の改善を介して網膜血流を促進する。
薬物療法
ダイアモックス注:500 mg 1日1回静脈注射(保険適用外)。炭酸脱水酵素阻害薬として眼圧を低下させ網膜動脈拡張を促す。
ウロキナーゼ:初期1日量6万〜24万単位、以後は漸減し約7日間投与。脳出血・全身出血に注意。
オバルモン錠:5 μg×6錠 分3 食後。プロスタグランジンE₁誘導体として末梢血流改善を目的とする。
処置・全身管理
眼球マッサージ:眼圧を低下させ塞栓を末梢へ移動させる。即時施行可能な処置である。
前房穿刺:前房水を穿刺吸引して眼圧を急降下させ、動脈灌流圧を相対的に高める。
星状神経節ブロック:眼血流の改善を目的に施行される場合がある。
ただし、保存的治療(眼球マッサージ・前房穿刺・カーボゲン吸入)は有意な効果が証明されていない8)。これらの処置は発症超早期にのみ理論的に意義があるが、自然経過より予後を改善するという確実なエビデンスは得られていない。
急性CRAOは脳卒中センターへ緊急紹介し、「Eye strokeプロトコル」に従って評価・治療を行うことが推奨されている8)。脳卒中センターではCRAOを脳梗塞と同等の緊急疾患として扱い、tPA投与の適応判断・全身血管評価・二次予防を一元的に管理する体制が整備されつつある。
症状に応じて以下を適宜用いる。
動脈内ウロキナーゼ30万単位投与により視力が20/2000から20/33.3へ劇的に改善された症例が報告されている4)。
CRAOの自然経過での視力回復率は約18%であるが、発症早期の血栓溶解療法により40%前後まで上昇するとされる。一方、EAGLE試験(RCT)では動脈内(IA)tPAは保存的治療と比較して視力改善に有意差がなく、頭蓋内出血(ICH)の安全性懸念が指摘された7)。現時点ではCRAOに対する動脈内・静脈内の線溶療法のエビデンスは不十分とされている8)。
動脈炎性CRAOが疑われる場合は、確定診断を待たずにステロイドの全身投与を即座に開始する。治療の遅れは対側眼失明のリスクがある8)。
一部の小規模後方視的研究で軽度の効果が示唆されているが、Cochraneレビューではエビデンスは不確実と結論されている8)。
CRAO後の亜急性期では、再灌流不全による慢性網膜虚血が眼の血管新生を引き起こす可能性がある。新生血管の有病率は2.5〜31.6%と報告され、新生血管が観察されるまでの平均期間は8.5週間である。CRAOの18%に虹彩新生血管が生じるとの報告もあり、発症後4か月程度は定期的な眼科検査が重要である。虹彩・網膜新生血管が生じた場合は汎網膜光凝固(PRP)が適応となる8)。
CRAO患者は全身の虚血性イベントのリスクが増加しており、長期の合併症予防には内科医・脳卒中専門医・循環器専門医との連携が重要である。CRAO患者の約60%は少なくとも1つの未診断の血管危険因子を有しており、CRAO発症を契機に全身検索を行うことが二次予防の第一歩となる。
CRAOの視力転帰は不良であり、指数弁以下になることが多い。治療しないで視機能が回復する可能性は約18%にとどまる。初診時20/400以下が61%に認められる8)。発症4〜6週後に網膜混濁は消失して健常網膜の色調に回復するが、早期治療が有効でない限り視機能は回復しない。発症4〜10週後には血管新生緑内障を引き起こすこともある。
一方、毛様網膜動脈が温存されたCRAOでは毛様網膜動脈の灌流域が保存されるため中心視力が維持される可能性がある。一過性CRAOでは閉塞が自然解除されるため視覚的予後は最も良好である。BRAOでは80%が最終的に矯正視力0.5以上を維持するが、黄斑部への分枝が閉塞した場合は視力予後が不良となる。
CRAO後には再灌流不全に伴う合併症にも注意が必要である。虹彩新生血管はCRAOの約18%に生じ、発症4〜10週後に血管新生緑内障に進展することがある。新生血管が生じた場合は汎網膜光凝固(PRP)を速やかに施行する8)。
網膜の不可逆的損傷は閉塞後約100分から始まる。発症1日以内であれば積極的に治療を行うべきとされるが、治療開始が早いほど予後は良好である。tPA静脈内投与の適応は発症4.5時間以内とされている8)。いずれにしても「眼の脳卒中」として、脳卒中センターへの緊急受診が基本である。
眼動脈(内頸動脈の第一枝)から分岐した網膜中心動脈は、視神経乳頭から網膜内に入り、網膜内層2/3(神経線維層〜内顆粒層)に酸素・栄養を供給する。網膜外層にある視細胞は脈絡膜血管からの栄養を受けるため、CRAOでは外層は比較的保たれる。
短後毛様動脈の分枝である毛様網膜動脈(cilioretinal artery)は全眼の約32%に存在し、乳頭黄斑束付近の網膜を栄養する。毛様網膜動脈は眼動脈が網膜中心動脈に移行する前に分岐するため、CRAOでも閉塞の影響を受けない。そのため、この動脈が温存されていれば中心窩の視力が保たれる可能性がある。
桜実紅斑の発生機序は以下のとおりである。CRAOにより網膜動脈が栄養している網膜内層が急性虚血により細胞膨化(細胞内浮腫)・虚血壊死に陥り、後極部を中心に乳白色に混濁する。この混濁は通常の網膜浮腫(細胞外浮腫)とは機序が異なる。通常の網膜浮腫では細胞外の水分貯留によりOCT上網膜は低反射となるが、CRAOでは虚血性の細胞内浮腫(細胞膨化)により網膜内層は高反射を呈する。OCTでは網膜内層が高輝度かつ肥厚した像として描出される。
中心窩は網膜外層のみで構成され、脈絡膜により栄養されているため混濁を生じない。中心窩では内層(神経節細胞層・内網状層・内顆粒層)がほぼ欠如しており、外層(視細胞層)のみが存在する。そのため、周囲の乳白色混濁の中に正常の赤い色調(脈絡膜毛細血管の色)が浮かび上がって見える。これが桜実紅斑の成因である。
眼動脈閉塞症(OAO)では眼動脈本幹が閉塞するため、網膜循環と脈絡膜循環の双方が障害される。脈絡膜虚血により桜実紅斑は出現しない8)。
CRAOの最も一般的な原因は血栓塞栓症であり、網膜中心動脈の内腔が最も狭くなる部分(視神経の硬膜鞘を貫通する部分)で閉塞が発生する。塞栓は頸動脈または心臓のプラークに由来する。
網膜神経節細胞は虚血に対して極めて脆弱であり、血流途絶から数分以内に機能障害が始まる。不可逆的損傷は約100〜105分から生じるとされる8)。これが本疾患の緊急性の根拠である。
虚血の時間経過に応じた組織変化は以下のとおりである。
慢性高血圧の状態では不可逆変化が生じるまでの時間が最大240分に延長するとの報告がある6)。
COVID-19関連CRAOの6歳女児例では、低分子ヘパリン(LMWH)100 mg/kgとメチルプレドニゾロン30 mg/kgが使用され、発症5か月後のフォローアップ時にRNFL菲薄化が持続していた1)。
Sanoら(2025)は徳島赤十字病院において、発症24時間以内のCRAO患者を対象にPGE₁の早期投与効果を後方視的に検討した9)。PGE₁群(n=4)にはアルプロスタジルアルファデクス40 μgを250 mL生理食塩水に溶解し、125 mL/hで1日2回(80 μg/日)5日間静注した。その後リマプロストアルファデクス10 μgを1日3回(30 μg/日)1か月以上経口投与した。従来治療群(n=6)と比較して、1か月時点の最良矯正視力(BCVA)はPGE₁群が有意に良好であった。PGE₁群ではベースラインの最大網膜厚(MRT)が1か月後のBCVAと負の相関を示した。有害事象は両群ともに観察されなかった9)。
PGE₁は血管拡張作用に加え、酸化ストレスと炎症の軽減による神経保護作用を持つとされる。サンプルサイズが小さく前方視的RCTが必要であるが、既存治療の確実な有効性が示されていない状況において注目される知見である。
CRAOを脳卒中の同等疾患と捉え、脳卒中センターが眼科と連携して急性期評価・治療を行う「Eye strokeプロトコル」の普及が進んでいる8)。このプロトコルにより、tPA投与率の向上や脳卒中の早期発見・二次予防が期待される。
選択的眼動脈内へのウロキナーゼ/tPA注入は一部施設で実施されているが、ランダム化比較試験のエビデンスは限定的である。EAGLE試験ではIA tPAは保存的治療と比較して視力改善に有意差がなく、ICH(頭蓋内出血)の安全性懸念が指摘された7)。
CRAOの症例では動脈内ウロキナーゼ30万単位投与により20/2000から20/33.3への劇的な視力改善が得られた4)。一方でIA tPAには血管解離や頭蓋内出血のリスクがあり7)、症例蓄積と適応基準の確立が今後の課題である。
大動脈内バルーンパンピングを体外から模倣し、拡張期に下肢を圧迫することで眼灌流圧を高める非侵襲的治療法である。
HA注射後RAO症例で、PFOを合併した40歳女性にECPが施行され、視力がCF 30 cmから20/133に改善した症例が報告されている2)。ただしECPのRAOに対するエビデンスは症例報告・小規模研究にとどまる。
若年CRAOでPFOが原因と同定された場合、経皮的PFO閉鎖術による奇異性塞栓の予防が検討される。
Wieder MSら(2021)は7例のPFO合併CRAO文献レビューにおいて、適切な抗凝固・抗血小板療法またはPFO閉鎖が推奨されると結論した3)。ただしCRAOに特化したPFO閉鎖のランダム化試験は行われていない。
PGE₁療法
日本発の報告:CRAOに対しPGE₁(アルプロスタジル80 μg/日×5日間静注→リマプロスト30 μg/日経口)で1か月後BCVAが有意に改善9)。
機序:血管拡張+神経保護(酸化ストレス・炎症軽減)。有害事象なし。
tPAの現状
EAGLE試験:IA tPAは保存的治療と比較して視力改善効果なく、ICHリスクあり7)。
IV tPA:発症4.5時間以内で転帰改善の可能性(メタ解析)だが、RCTエビデンス不十分8)。