CRAO
انسداد شریان مرکزی شبکیه (Central Retinal Artery Occlusion): انسداد شریان مرکزی شبکیه. شدیدترین نوع است و بینایی اغلب به حرکت دست یا حس نور کاهش مییابد.
بروز: ۱ نفر در ۱۰۰٬۰۰۰ نفر در سال، ۱ نفر در ۱۰٬۰۰۰ بیمار سرپایی8).

انسداد شریان شبکیه بیماری است که به دلیل انسداد شریان شبکیه، ایسکمی و نکروز شبکیه ایجاد کرده و منجر به اختلال شدید عملکرد بینایی میشود. از آنجایی که تغییرات غیرقابل برگشت شبکیه تقریباً ۱۰۰ دقیقه پس از انسداد شریان شروع میشود، حتی با درمان نیز نتیجه بینایی اغلب ضعیف است. بر اساس محل انسداد به سه نوع زیر تقسیم میشود:
CRAO
انسداد شریان مرکزی شبکیه (Central Retinal Artery Occlusion): انسداد شریان مرکزی شبکیه. شدیدترین نوع است و بینایی اغلب به حرکت دست یا حس نور کاهش مییابد.
بروز: ۱ نفر در ۱۰۰٬۰۰۰ نفر در سال، ۱ نفر در ۱۰٬۰۰۰ بیمار سرپایی8).
BRAO
انسداد شریان شبکیه (Branch Retinal Artery Occlusion): انسداد شاخه. پیشآگهی بینایی بسته به محل انسداد بسیار متفاوت است.
ویژگی: 80٪ در نهایت حدت بینایی اصلاحشده 0.5 یا بالاتر را حفظ میکنند. اگر ماکولا آسیب نبیند، بینایی کاهش نمییابد.
انسداد شریان سیلیورتینال
انسداد شریان سیلیورتینال (Cilioretinal Artery Occlusion): انسداد شریان مژگانی. این شاخه از شریان مژگانی کوتاه خلفی است و در حدود 32٪ از چشمها وجود دارد. ناحیه نزدیک باند پاپیلوماکولار شبکیه را تغذیه میکند.
ویژگی: ممکن است همراه با CRAO یا به تنهایی رخ دهد.
CRAO بیشتر به دو نوع غیرآرتریتی و آرتریتی تقسیم میشود. CRAO غیرآرتریتی بیش از 90٪ موارد را تشکیل میدهد و دارای سه زیرگروه زیر است:
CRAO آرتریتی ثانویه به آرتریت سلول ژانت (GCA) است و حدود 4٪ از بیماران CRAO را تشکیل میدهد. بدترین پیشآگهی را در بین چهار نوع دارد و از دست دادن بینایی تقریباً غیرقابل برگشت است. احتمال بروز در بیماران بالای 70 سال بیشتر است و اغلب با علائم مرتبط با GCA مانند سردرد، حساسیت پوست سر، لنگش فک، خستگی عمومی و کاهش وزن همراه است. در تمام بیماران CRAO بالای 50 سال، رد CRAO آرتریتی مهمترین اقدام است و باید ESR و CRP سریعاً اندازهگیری شود و در صورت لزوم بیوپسی شریان تمپورال انجام شود. در صورت شک قوی به GCA، درمان سیستمیک با استروئید بلافاصله بدون انتظار برای تشخیص قطعی شروع میشود 8). تأخیر در درمان خطر نابینایی چشم مقابل را افزایش میدهد.
بروز CRAO حدود 1 نفر در هر 100,000 نفر در سال و 1 نفر در هر 10,000 بیمار سرپایی تخمین زده میشود. میانگین سن شروع حدود 60 سالگی است و بروز با افزایش سن افزایش مییابد 8). در مردان شایعتر است و معمولاً یک چشم را درگیر میکند، اما 1-2٪ موارد دوطرفه هستند. در موارد دوطرفه باید به آرتریت سلول ژانت مشکوک شد 8). بروز در ژاپن نسبت به کشورهای غربی کمتر است و میتوان آن را یک بیماری نسبتاً نادر دانست، اما یک بیماری اورژانسی است که پاسخ بسیار زودهنگام پیشآگهی بینایی را تعیین میکند.
شبکیه در دوره جنینی از مغز تمایز مییابد و بخشی از سیستم عصبی مرکزی محسوب میشود. ارتباط نزدیکی با سکته مغزی دارد؛ در سال ۲۰۱۳، AHA/ASA (انجمن قلب آمریکا/انجمن سکته مغزی) تعریف سکته مغزی را بازبینی کرده و ایسکمی شبکیه را بهعنوان نوعی از انفارکتوس CNS (سیستم عصبی مرکزی) بهصراحت طبقهبندی کرد8). ۱۵ تا ۲۰٪ از بیماران CRAO در عرض ۳۰ روز دچار سکته مغزی میشوند و بهعنوان «سکته چشمی» ارزیابی فوری سیستمیک توسط مرکز سکته مغزی توصیه میشود8).
CRAO عوامل خطر مشترکی با سکته مغزی (آترواسکلروز، فیبریلاسیون دهلیزی، آمبولی و غیره) دارد و خطر سکته مغزی در ۳۰ روز پس از شروع ۱۵ تا ۲۰٪ است8). AHA/ASA ایسکمی شبکیه را بهعنوان انفارکتوس CNS تعریف کرده است؛ پس از شروع CRAO، ارزیابی فوری سیستمیک با همکاری متخصصان مغز و اعصاب و قلب ضروری است.
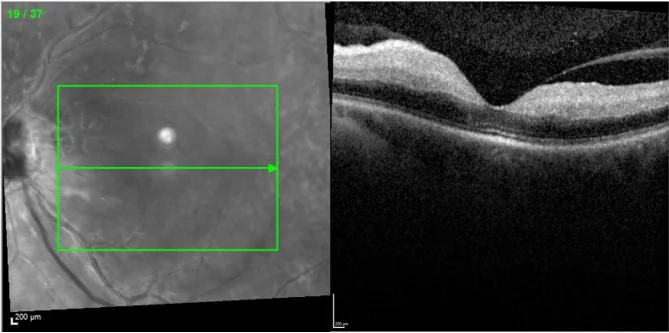
کاهش شدید و ناگهانی بینایی بدون درد، مشخصه اصلی است.
در CRAO، ممکن است قبل از شروع، دورههای مکرر اختلال بینایی گذرا وجود داشته باشد. این حالت آموروزیس فوگاکس نامیده میشود و بهعنوان علامت هشداردهنده مهم سکته مغزی (TIA) است. بینایی پس از چند دقیقه از دست رفتن بهطور خودبهخود بازمیگردد، اما اغلب پیشدرآمد حمله اصلی است.
در یک دختر ۶ ساله مبتلا به CRAO مرتبط با COVID-19، از دست دادن ناگهانی بینایی دوطرفه گزارش شده است که نشان میدهد (هرچند نادر) بروز در کودکان نیز ممکن است1).
در مرحله حاد، یافتههای مشخصی وجود دارد که با گذشت زمان تغییر میکند. در مرحله فوقحاد (در عرض ۲ ساعت پس از شروع)، یافتههای فوندوس طبیعی است یا فقط کدورت خفیف ماکولا دیده میشود.
در یک مورد دختر ۶ ساله مبتلا به CRAO مرتبط با COVID-19، نازک شدن لایه فیبرهای عصبی شبکیه (RNFL) حتی ۵ ماه پس از شروع نیز ادامه داشت1). در OCT مرحله مزمن، شبکیه نازک میشود و آتروفی رتروگراد نه تنها لایههای داخلی بلکه خارجی را نیز درگیر کرده و تشخیص ساختار لایهای دشوار میشود.
در CRAO، کل لایه داخلی شبکیه به دلیل ادم سلولی ایسکمیک به رنگ سفید شیری در میآید. با این حال، فووئا فقط از لایه خارجی شبکیه تشکیل شده و از مویرگهای کوروئید تغذیه میکند، بنابراین کدر نمیشود. در مقابل سفیدی اطراف، رنگ قرمز کوروئید نمایان میشود که مکانیسم لکه قرمز گیلاسی است. برای آناتومی عروقی دقیق، به بخش «پاتوفیزیولوژی» مراجعه کنید.
علت اصلی CRAO آمبولی است که حدود 95٪ موارد را تشکیل میدهد8). توزیع علل بر اساس سن و بیماری زمینهای متفاوت است.
| گروه سنی | علت اصلی | بیماریهای قابل بررسی |
|---|---|---|
| 50 سال و بالاتر | آمبولی و ترومبوز آترواسکلروتیک | تنگی کاروتید، فیبریلاسیون دهلیزی، فشار خون بالا |
| زیر 50 سال | اختلال انعقادی، PFO، واسکولیت | آمبولی متناقض، بیماری خودایمنی |
عوامل خطر قابل اصلاح شامل سیگار کشیدن، فشار خون بالا، BMI بالا، دیسلیپیدمی، دیابت، اختلالات انعقادی و بیماریهای قلبی (از جمله فیبریلاسیون دهلیزی) هستند 8). حدود ۶۰٪ از بیماران CRAO حداقل یک عامل خطر عروقی تشخیصدادهنشده دارند که شایعترین آن دیسلیپیدمی است. کلسترول HDL پایین نیز به عنوان یک عامل خطر مستقل گزارش شده است 8).
عوامل خطر سیستمیک در زیر فهرست شدهاند.
CRAO اغلب با یافتههای فوندوس قابل تشخیص است، اما ارزیابی سیستمیک برای یافتن علت ضروری است. مدیریت CRAO به سه مرحله تقسیم میشود: اول، بازیابی جریان خون در مرحله حاد؛ دوم، پیشگیری از عوارض ثانویه در مرحله تحت حاد؛ و سوم، کنترل و پیشگیری سیستمیک از رویدادهای ایسکمیک عروقی آینده.
یافتههای اصلی به دست آمده از هر آزمایش در زیر نشان داده شده است.
| روش آزمایش | یافتههای اصلی |
|---|---|
| OCT | فاز حاد: هایپررفلکتیویته و ضخیمشدن لایه داخلی → فاز مزمن: نازکشدن لایه داخلی |
| FA | تأخیر در پرشدگی، زمان گردش بازو-شبکیه بیش از ۳۰ ثانیه |
| ERG | موج a طبیعی، موج b کاهشیافته (ERG نوع منفی) |
در فاز حاد CRAO، بیمار باید فوراً به مرکز سکته مغزی ارجاع داده شود و ارزیابی سیستمیک اورژانسی انجام شود8). خطر سکته مغزی در بیماران RAO علامتدار در دو هفته قبل تا یک ماه پس از شروع علائم بالاترین است8).
رد CRAO آرتریتی ناشی از آرتریت سلول ژانت (GCA) مهمترین است. CRAO مرتبط با GCA حدود 4% از کل CRAOها را تشکیل میدهد و بدترین پیشآگهی را دارد. در صورت شک به GCA، تجویز سیستمیک استروئید بلافاصله و بدون انتظار برای تشخیص قطعی (بیوپسی شریان تمپورال) آغاز میشود8). در صورت عدم درمان، خطر نابینایی چشم مقابل وجود دارد.
CRAO یک اورژانس چشمی است و برای بهبود پیشآگهی بینایی، اقدام سریع در مرحله فوقحاد ضروری است. درمان بلافاصله پس از شروع علائم مطلوب است و در مواردی که کمتر از یک روز از شروع گذشته باشد، باید درمان فعال انجام شود.
حدود 100 دقیقه پس از انسداد شریان، آسیب شدید شبکیه آغاز میشود. درمان بلافاصله پس از شروع بهترین است و حدود 4 ساعت به عنوان معیار درمان حاد در نظر گرفته میشود6). هرچه زمان از شروع تا مراجعه طولانیتر باشد، پیشآگهی بدتر است، اما در مواردی که کمتر از یک روز گذشته باشد، باید درمان فعال انجام شود. در BRAO نیز اگر در مراحل اولیه و با اختلال بینایی باشد، همان رویکرد درمانی CRAO اتخاذ میشود.
Zokri MF و همکاران (2024) در یک سری موارد RAO حاد تأکید کردند که زمان شروع درمان مهمترین عامل تعیینکننده نتیجه بینایی است6). تأخیر در مراجعه باعث از دست رفتن فرصت مداخله درمانی در بسیاری از موارد میشود.
روشهای درمانی زیر با توجه به علائم استفاده میشوند.
داروهای گشادکننده عروق
آمیل نیتریت: یک ویال 0.25 میلیلیتری را خرد کرده، روی پوشش جذب کرده و از طریق بینی استنشاق کنید (مراقب افت فشار خون باشید - خارج از پوشش بیمه).
ایزوسورباید دینیترات زیرزبانی: باعث گشاد شدن عروق میشود.
استنشاق کربوژن: استنشاق مخلوط 95% اکسیژن و 5% CO₂. جریان خون را افزایش میدهد اما با خطر افت فشار خون سیستمیک همراه است.
پنتوکسی فیلین: داروی بهبود دهنده گردش خون محیطی. با بهبود قابلیت تغییر شکل گلبولهای قرمز، جریان خون شبکیه را افزایش میدهد.
دارودرمانی
تزریق دیاموکس: 500 میلیگرم یک بار در روز به صورت وریدی (خارج از پوشش بیمه). به عنوان مهارکننده کربنیک انیدراز، فشار داخل چشم را کاهش داده و باعث گشاد شدن شریان شبکیه میشود.
اوروکیناز: دوز اولیه 60,000 تا 240,000 واحد در روز، سپس به تدریج کاهش یافته و حدود 7 روز تجویز میشود. مراقب خونریزی مغزی و خونریزی سیستمیک باشید.
قرص اووارمون: 5 میکروگرم × 6 قرص، سه بار در روز بعد از غذا. به عنوان مشتق پروستاگلاندین E₁ برای بهبود جریان خون محیطی استفاده میشود.
اقدامات و مدیریت سیستمیک
ماساژ کره چشم: فشار داخل چشم را کاهش داده و آمبولی را به سمت محیط حرکت میدهد. این یک اقدام قابل انجام فوری است.
پاراسنتز اتاق قدامی: با سوزن زدن و آسپیراسیون مایع اتاق قدامی، فشار داخل چشم به سرعت کاهش یافته و فشار پرفیوژن شریانی به طور نسبی افزایش مییابد.
بلوک گانگلیون ستارهای: ممکن است برای بهبود جریان خون چشم انجام شود.
با این حال، درمانهای محافظهکارانه (ماساژ کره چشم، پاراسنتز اتاق قدامی، استنشاق کربوژن) اثربخشی قابل توجهی اثبات نشده است8). این اقدامات تنها در مراحل بسیار اولیه شروع بیماری از نظر تئوری مفید هستند، اما شواهد قطعی مبنی بر بهبود پیشآگهی نسبت به سیر طبیعی بیماری وجود ندارد.
در انسداد حاد شریان مرکزی شبکیه (CRAO)، ارجاع فوری به مرکز سکته مغزی و ارزیابی و درمان مطابق با «پروتکل سکته چشمی» توصیه میشود8). در مرکز سکته مغزی، CRAO به عنوان یک اورژانس مشابه سکته مغزی ایسکمیک درمان میشود و سیستمهایی برای ارزیابی اندیکاسیون تجویز tPA، ارزیابی عروق سیستمیک و پیشگیری ثانویه به صورت یکپارچه در حال توسعه است.
بسته به علائم، موارد زیر بهطور مناسب استفاده میشود.
موردی گزارش شده است که در آن تجویز 300,000 واحد اوروکیناز داخل شریانی منجر به بهبود چشمگیر بینایی از 20/2000 به 20/33.3 شده است4).
میزان بهبود خودبهخودی بینایی در CRAO حدود 18٪ است، اما با ترومبولیز زودهنگام به حدود 40٪ افزایش مییابد. با این حال، در مطالعه EAGLE (RCT)، tPA داخل شریانی (IA) تفاوت معنیداری در بهبود بینایی در مقایسه با درمان محافظهکارانه نشان نداد و نگرانیهای ایمنی در مورد خونریزی داخل جمجمه (ICH) مطرح شد7). در حال حاضر، شواهد برای ترومبولیز داخل شریانی و وریدی در CRAO ناکافی در نظر گرفته میشود8).
در صورت مشکوک بودن به CRAO آرتریتی، تجویز سیستمیک استروئیدها باید بلافاصله و بدون انتظار برای تشخیص قطعی آغاز شود. تأخیر در درمان خطر نابینایی چشم مقابل را به همراه دارد8).
برخی مطالعات گذشتهنگر کوچک اثرات خفیفی را نشان دادهاند، اما مرور کاکرین نتیجه گرفته است که شواهد نامطمئن است8).
در مرحله تحت حاد پس از CRAO، ایسکمی مزمن شبکیه به دلیل نارسایی پرفیوژن مجدد میتواند منجر به نئوواسکولاریزاسیون چشم شود. شیوع نئوواسکولاریزاسیون 2.5 تا 31.6٪ گزارش شده است و میانگین زمان مشاهده نئوواسکولاریزاسیون 8.5 هفته است. همچنین گزارش شده است که 18٪ موارد CRAO منجر به نئوواسکولاریزاسیون عنبیه میشود و معاینات منظم چشم تا حدود 4 ماه پس از شروع علائم مهم است. در صورت بروز نئوواسکولاریزاسیون عنبیه یا شبکیه، فتوکوآگولاسیون پانرتینال (PRP) اندیکاسیون دارد 8).
بیماران CRAO در معرض افزایش خطر رویدادهای ایسکمیک سیستمیک هستند و همکاری با پزشکان داخلی، متخصصان سکته مغزی و متخصصان قلب برای پیشگیری طولانی مدت از عوارض مهم است. حدود 60٪ از بیماران CRAO حداقل یک عامل خطر عروقی تشخیص داده نشده دارند و شروع CRAO فرصتی برای جستجوی سیستمیک و اولین گام در پیشگیری ثانویه است.
پیشآگهی بینایی در CRAO ضعیف است و اغلب به شمارش انگشت یا کمتر میرسد. احتمال بهبود عملکرد بینایی بدون درمان تنها حدود 18٪ است. در 61٪ موارد، حدت بینایی در اولین ویزیت 20/400 یا کمتر است 8). کدورت شبکیه 4-6 هفته پس از شروع ناپدید میشود و رنگ شبکیه به حالت عادی بازمیگردد، اما عملکرد بینایی بهبود نمییابد مگر اینکه درمان زودهنگام مؤثر باشد. 4-10 هفته پس از شروع، ممکن است گلوکوم نئوواسکولار ایجاد شود.
از سوی دیگر، در CRAO با حفظ شریان مژگانی شبکیه، ناحیه پرفیوژن شریان مژگانی شبکیه حفظ میشود و بنابراین ممکن است دید مرکزی حفظ شود. در CRAO گذرا، به دلیل رفع خودبهخودی انسداد، پیشآگهی بینایی بهترین است. در BRAO، 80٪ موارد در نهایت حدت بینایی اصلاحشده 0.5 یا بالاتر را حفظ میکنند، اما اگر شاخه منتهی به ماکولا مسدود شود، پیشآگهی بینایی ضعیف است.
پس از CRAO، باید به عوارض ناشی از نارسایی پرفیوژن مجدد نیز توجه کرد. نئوواسکولاریزاسیون عنبیه در حدود 18٪ موارد CRAO رخ میدهد و ممکن است 4-10 هفته پس از شروع به گلوکوم نئوواسکولار تبدیل شود. در صورت بروز نئوواسکولاریزاسیون، فتوکوآگولاسیون پانرتینال (PRP) باید سریعاً انجام شود 8).
آسیب غیرقابل برگشت شبکیه حدود ۱۰۰ دقیقه پس از انسداد آغاز میشود. اگر بیمار در عرض ۱ روز مراجعه کند، درمان تهاجمی توصیه میشود، اما هرچه درمان زودتر شروع شود، پیشآگهی بهتر است. اندیکاسیون تزریق وریدی tPA در عرض ۴.۵ ساعت از شروع علائم است8). در هر صورت، به عنوان «سکته مغزی چشم»، مراجعه اورژانسی به مرکز سکته مغزی اساسی است.
شریان مرکزی شبکیه که از شریان چشمی (اولین شاخه شریان کاروتید داخلی) منشعب میشود، از دیسک بینایی وارد شبکیه شده و دو سوم داخلی شبکیه (از لایه فیبرهای عصبی تا لایه گرانولار داخلی) را با اکسیژن و مواد مغذی تأمین میکند. سلولهای گیرنده نور در لایه خارجی شبکیه از عروق کوروئید تغذیه میکنند، بنابراین در CRAO لایه خارجی نسبتاً حفظ میشود.
شریان سیلیورتینال که شاخهای از شریان مژگانی خلفی کوتاه است، در حدود ۳۲٪ از چشمها وجود دارد و ناحیه نزدیک باندل پاپیلوماکولار را تغذیه میکند. از آنجا که شریان سیلیورتینال قبل از تبدیل شریان چشمی به شریان مرکزی شبکیه منشعب میشود، در CRAO تحت تأثیر انسداد قرار نمیگیرد. بنابراین، اگر این شریان حفظ شود، احتمال حفظ بینایی فووئال وجود دارد.
مکانیسم ایجاد لکه قرمز گیلاسی به شرح زیر است. در CRAO، لایه داخلی شبکیه که توسط شریان مرکزی شبکیه تغذیه میشود، به دلیل ایسکمی حاد دچار تورم سلولی (ادم داخل سلولی) و نکروز ایسکمیک میشود و بهویژه در قطب خلفی به رنگ سفید شیری در میآید. این کدورت با ادم معمولی شبکیه (ادم خارج سلولی) متفاوت است. در ادم معمولی شبکیه، به دلیل تجمع مایع خارج سلولی، شبکیه در OCT هیپواکو میشود، اما در CRAO، به دلیل ادم داخل سلولی ایسکمیک (تورم سلولی)، لایه داخلی شبکیه هایپرارفلاکتیو میشود. در OCT، لایه داخلی شبکیه به صورت ضخیم و با شدت بالا دیده میشود.
فووآ فقط از لایه خارجی شبکیه تشکیل شده و توسط مشیمیه تغذیه میشود، بنابراین دچار کدورت نمیشود. در فووآ، لایه داخلی (لایه سلولهای گانگلیونی، لایه شبکهای داخلی، لایه دانهدار داخلی) تقریباً وجود ندارد و فقط لایه خارجی (لایه فوتورسپتورها) وجود دارد. بنابراین، در میان کدورت سفید شیری اطراف، رنگ قرمز طبیعی (رنگ مویرگهای مشیمیه) نمایان میشود. این علت ایجاد لکه قرمز گیلاسی است.
در انسداد شریان چشمی (OAO)، تنه اصلی شریان چشمی مسدود میشود، بنابراین هر دو گردش خون شبکیه و مشیمیه مختل میشوند. به دلیل ایسکمی مشیمیه، لکه قرمز گیلاسی ظاهر نمیشود 8).
شایعترین علت CRAO ترومبوآمبولی است و انسداد در باریکترین قسمت لومن شریان مرکزی شبکیه (محل عبور از غلاف دورال عصب بینایی) رخ میدهد. آمبولی از پلاکهای کاروتید یا قلب منشأ میگیرد.
سلولهای گانگلیونی شبکیه در برابر ایسکمی بسیار آسیبپذیر هستند و اختلال عملکرد در عرض چند دقیقه پس از قطع جریان خون آغاز میشود. آسیب غیرقابل برگشت از حدود 100 تا 105 دقیقه شروع میشود 8). این مبنای فوریت این بیماری است.
تغییرات بافتی با توجه به زمان ایسکمی به شرح زیر است:
گزارش شده است که در شرایط فشار خون مزمن، زمان تا بروز تغییرات غیرقابل برگشت میتواند تا 240 دقیقه افزایش یابد6).
در یک مورد CRAO مرتبط با COVID-19 در یک دختر 6 ساله، از هپارین با وزن مولکولی پایین (LMWH) با دوز 100 میلیگرم/کیلوگرم و متیلپردنیزولون با دوز 30 میلیگرم/کیلوگرم استفاده شد و در پیگیری 5 ماه پس از شروع، نازک شدن RNFL ادامه داشت1).
Sano و همکاران (2025) در بیمارستان صلیب سرخ توکوشیما، اثر تجویز زودهنگام PGE₁ را در بیماران CRAO که در عرض 24 ساعت از شروع علائم مراجعه کرده بودند، به صورت گذشتهنگر بررسی کردند9). در گروه PGE₁ (n=4)، آلپروستادیل آلفادکس 40 میکروگرم در 250 میلیلیتر نرمال سالین حل شده و با سرعت 125 میلیلیتر/ساعت دو بار در روز (80 میکروگرم/روز) به مدت 5 روز به صورت وریدی تزریق شد. سپس لیماپروست آلفادکس 10 میکروگرم سه بار در روز (30 میکروگرم/روز) به مدت بیش از یک ماه خوراکی تجویز شد. در مقایسه با گروه درمان معمول (n=6)، بهترین corrected visual acuity (BCVA) در یک ماه در گروه PGE₁ به طور معنیداری بهتر بود. در گروه PGE₁، حداکثر ضخامت شبکیه (MRT) در ابتدا با BCVA در یک ماه همبستگی منفی نشان داد. هیچ عارضه جانبی در هیچ یک از گروهها مشاهده نشد9).
PGE₁ علاوه بر اثر گشادکنندگی عروق، دارای اثر محافظت عصبی از طریق کاهش استرس اکسیداتیو و التهاب است. اگرچه حجم نمونه کوچک است و نیاز به RCT آیندهنگر وجود دارد، اما این یافته در شرایطی که اثربخشی قطعی درمانهای موجود نشان داده نشده است، قابل توجه است.
CRAO به عنوان معادل سکته مغزی در نظر گرفته میشود و گسترش پروتکل «Eye stroke» که در آن مرکز سکته مغزی با همکاری چشمپزشکی ارزیابی و درمان حاد را انجام میدهد، در حال پیشرفت است8). این پروتکل انتظار میرود که نرخ تجویز tPA را افزایش داده و به تشخیص زودهنگام سکته مغزی و پیشگیری ثانویه کمک کند.
تزریق اوروکیناز/tPA به داخل شریان چشمی انتخابی در برخی مراکز انجام میشود، اما شواهد حاصل از کارآزماییهای تصادفیشده محدود است. در کارآزمایی EAGLE، IA tPA در مقایسه با درمان محافظهکارانه تفاوت معنیداری در بهبود بینایی نداشت و نگرانیهای ایمنی در مورد خونریزی داخل جمجمه (ICH) مطرح شد7).
در موارد CRAO، تزریق 300,000 واحد اوروکیناز داخل شریانی منجر به بهبود چشمگیر بینایی از 20/2000 به 20/33.3 شد4). از سوی دیگر، IA tPA با خطر تشریح عروق و خونریزی داخل جمجمه همراه است7) و تجمیع موارد و تعیین معیارهای مناسب برای استفاده از آن، چالشهای آینده است.
این یک روش درمانی غیرتهاجمی است که با تقلید از بالون پمپ داخل آئورت، با فشردن پاها در مرحله دیاستول، فشار پرفیوژن چشمی را افزایش میدهد.
در یک مورد RAO پس از تزریق اسید هیالورونیک، ECP در زن 40 سالهای که PFO نیز داشت انجام شد و بینایی از CF 30 cm به 20/133 بهبود یافت2). با این حال، شواهد ECP برای RAO محدود به گزارش موارد و مطالعات کوچک است.
در CRAO جوانان که PFO به عنوان علت شناسایی میشود، بستن از راه پوست PFO برای پیشگیری از آمبولی پارادوکسیکال بررسی میشود.
Wieder MS و همکاران (2021) در مرور 7 مورد CRAO همراه با PFO نتیجه گرفتند که درمان مناسب ضد انعقاد/ضد پلاکت یا بستن PFO توصیه میشود3). با این حال، کارآزمایی تصادفیشده اختصاصی برای بستن PFO در CRAO انجام نشده است.
درمان با PGE₁
گزارش از ژاپن: در CRAO، PGE₁ (آلپروستادیل 80 میکروگرم/روز به مدت 5 روز وریدی، سپس لیماپروست 30 میکروگرم/روز خوراکی) پس از یک ماه بهبود معنیداری در BCVA نشان داد9).
مکانیسم: گشادکننده عروق + محافظت عصبی (کاهش استرس اکسیداتیو و التهاب). بدون عارضه جانبی.
وضعیت tPA
کارآزمایی EAGLE: IA tPA در مقایسه با درمان محافظهکارانه تأثیری در بهبود بینایی نداشت و خطر ICH داشت7).
IV tPA: احتمال بهبود پیامد در عرض 4.5 ساعت از شروع (متاآنالیز) اما شواهد RCT کافی نیست8).