مرحله 1 تا 2
مرحله 1: فقط گشادشدگی مویرگهای شبکیه بدون ترشح دیده میشود.
مرحله 2A: علاوه بر گشاد شدن مویرگها، ترشحات خارج از حفره مرکزی (فووآ) مشاهده میشود.
مرحله 2B: ترشحات به حفره مرکزی (فووآ) رسیده است. کاهش بینایی آشکار میشود.

بیماری کوتس (Coats disease) یک بیماری عروقی ایدیوپاتیک شبکیه است که اولین بار در سال ۱۹۰۸ توسط جورج کوتس گزارش شد. ویژگی اصلی آن اتساع غیرطبیعی مویرگهای شبکیه (تلانژکتازی) و تجمع ترشحات داخل و زیر شبکیه از دیواره عروق است.
این بیماری به صورت پراکنده و غیرارثی رخ میدهد و با بیماریهای سیستمیک یا سابقه خانوادگی مرتبط نیست 1). میزان بروز آن نادر و حدود ۰.۰۹ در ۱۰۰٬۰۰۰ نفر است 2). حدود ۷۵٪ بیماران مرد، ۹۵٪ موارد یکطرفه هستند و بیشتر در سنین زیر ۲۰ سال (میانگین حدود ۵ سال) رخ میدهد.
شروع در بزرگسالی بسیار نادر است اما تصویر بالینی متفاوتی نسبت به نوع کودکان دارد. موارد بزرگسالی خفیفتر، پیشرفت آهستهتر و پاسخ به درمان بهتری دارند 3). در یک گزارش، از ۴۸ چشم بزرگسال، تنها ۲۱٪ دچار جداشدگی اگزوداتیو شبکیه شدند که در مقایسه با ۸۱٪ در کودکان به طور معنیداری کمتر بود 3).
نوع خفیف آن آنوریسمهای میلیاری لبر (Leber’s miliary aneurysms) نیز نامیده میشود و بخشی از طیف بیماری کوتس را تشکیل میدهد. همچنین تلانژکتازی ایدیوپاتیک ماکولار نوع ۱ نیز بخشی از همین طیف در نظر گرفته میشود.
موارد شروع در سن بالای ۳۵ سال گزارش شده است و به عنوان بیماری کوتس بزرگسالی شناخته میشود 3). در مقایسه با نوع کودکان، پیشرفت ضایعات آهستهتر، فراوانی جداشدگی اگزوداتیو شبکیه کمتر و پاسخ به درمان معمولاً بهتر است. با این حال، بروز آن نادر است و در صورت مشاهده یافتههای مشابه در بزرگسالان، افتراق از سایر بیماریها مهم است.
در صورت بروز در دوران نوزادی یا کودکی، کودک به ندرت از علائم شکایت میکند.
در موارد بروز در بزرگسالی، بینایی نسبتاً حفظ میشود و گاهی به طور تصادفی در معاینات کشف میشود3).
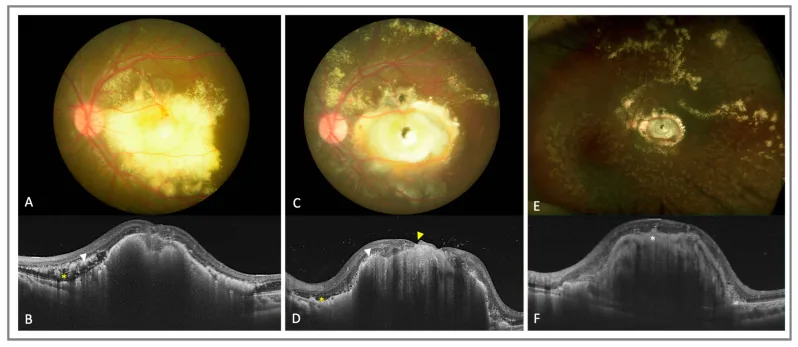
ویژگیهای یافتههای فوندوس شامل عروق شبکیه با اتساع غیرطبیعی متمرکز در محیط و تجمع ترشحات زرد-سفید زیرشبکیه و داخل شبکیه است. در آنژیوگرافی فلورسئین، انسداد عروق شبکیه محیطی، گشادشدگی مویرگها، آنوریسم مویرگی و عروق جدید به عنوان یافتههای مشخص دیده میشود. با پیشرفت، جداشدگی شبکیه اگزوداتیو رخ میدهد و در نهایت به جداشدگی کامل میرسد. در سونوگرافی، CT و MRI، مایع زیرشبکیه به طور یکنواخت در همه جا دیده میشود که این نکته یک تفاوت تصویربرداری مهم با رتینوبلاستوما است که تصویری ناهمگن با کلسیفیکاسیون نشان میدهد.
در مراحل晚期، عوارض بخش قدامی مانند روبئوز عنبیه و گلوکوم نئوواسکولار ایجاد میشود. سوراخ ماکولا یک عارضه نادر است و تنها حدود 7 مورد در ادبیات گزارش شده است4). ندول فیبری یک عامل پیشآگهی بد بینایی است و در OCTA، عروق جدید نوع 3 (SVC→DVC→کمپلکس بدون عروق) در داخل ندول تأیید شده است5).
طبقهبندی شیلدز مراحل بیماری کوتس را به 5 مرحله زیر تقسیم میکند. برای انتخاب روش درمان و تخمین پیشآگهی استفاده میشود.
مرحله 1 تا 2
مرحله 1: فقط گشادشدگی مویرگهای شبکیه بدون ترشح دیده میشود.
مرحله 2A: علاوه بر گشاد شدن مویرگها، ترشحات خارج از حفره مرکزی (فووآ) مشاهده میشود.
مرحله 2B: ترشحات به حفره مرکزی (فووآ) رسیده است. کاهش بینایی آشکار میشود.
مرحله 3
مرحله 3A1: همراه با جداشدگی نسبی شبکیه در خارج از حفره مرکزی.
مرحله 3A2: همراه با جداشدگی نسبی شبکیه شامل حفره مرکزی. پیشآگهی بینایی ضعیف است.
مرحله 3B: جداشدگی کامل شبکیه رخ داده است. نیاز به مداخله فوری دارد.
مراحل 4 تا 5
مرحله 4: جداشدگی کامل شبکیه همراه با گلوکوم ثانویه، مرحله قبل از پایان. ممکن است با درد همراه باشد.
مرحله 5: مرحله پایانی. منجر به فتیزیس بولبی (آتروفی) شده است. برداشتن چشم (انوکلئاسیون) در نظر گرفته میشود.
بیماریهای متعددی با مردمک سفید تظاهر میکنند و بیماری کوتس تنها یکی از آنهاست. مهمترین تشخیص افتراقی رتینوبلاستوما (Rb) است که به دلیل ارتباط مستقیم با بقای بیمار نیاز به ارزیابی فوری دارد. سایر موارد شامل رتینوپاتی نارسی، سندرم عروق جنینی پایدار (PHPV) و اندوفتالمیت است. برای جزئیات به بخش «تشخیص و روشهای آزمایش» مراجعه کنید.
علت بیماری کوتس ناشناخته است و ارتباطی با بیماریهای سیستمیک یا سابقه خانوادگی یافت نشده است. گزارشهایی از زمینه ژنتیکی شامل ناپایداری کروموزومهای 3 و 13، ارتباط با ژن NDP (مرتبط با بیماری نوری) و ژن CRB1 وجود دارد، اما اثبات نشده است.
به عنوان نقطه شروع پاتوفیزیولوژی، اختلال در سد خونی-شبکیه داخلی (iBRB) نقش اصلی را ایفا میکند1). کاهش سلولهای پریسیت (سلولهای حمایتکننده اندوتلیال عروق) باعث ضعیف شدن دیواره عروق و تشکیل مویرگهای گشاد شده غیرطبیعی و آنوریسم میشود1). نشت و تجمع اجزای پلاسما در دیواره عروق و لایههای شبکیه باعث ضخیم شدن دیواره عروق و تشدید ترشحات میشود که یک چرخه معیوب ایجاد میکند2).
همچنین نشان داده شده است که محیط با VEGF بالا باعث گشاد شدن مویرگهای محیطی میشود2)، که این مکانیسم مبنای نظری درمان ضد VEGF است.
برای تشخیص، ترکیبی از چندین آزمایش به کار میرود و مهمترین اولویت، افتراق قطعی از رتینوبلاستوما (Rb) است.
در معاینه فوندوس با مردمک گشاد شده، شبکه عروقی غیرطبیعی و پرپیچوخم در ناحیه محیطی و ترشحات زرد-سفید زیرشبکیه مشاهده میشود. اگر ترشحات به ناحیه ماکولا برسند، ظاهری شبیه به اگزوداهای سخت (hard exudates) پیدا میکنند.
یکی از مهمترین آزمایشها در تشخیص بیماری کوتس است. گشاد شدن قابل توجه مویرگها، آنوریسمهای مویرگی، آناستوموز شریانی-وریدی و نشت فلورسین به شکل «لامپهای روشن» (light bulbs) از یافتههای مشخصه هستند. این آزمایش برای تعیین وسعت عروق غیرطبیعی و تصمیمگیری در مورد محل لیزر درمانی ضروری است.
برای تأیید عدم وجود توده جامد انجام میشود. رتینوبلاستوما اغلب در B-mode اکوهای پرنور (کلسیفیکاسیون) در داخل توده جامد نشان میدهد، اما در بیماری کوتس توده جامد تشکیل نمیشود.
برای ارزیابی وجود یا عدم وجود کلسیفیکاسیون انجام میشود. رتینوبلاستوما با درصد بالایی همراه با کلسیفیکاسیون است، در حالی که بیماری کوتس کلسیفیکاسیون ایجاد نمیکند. این یافته یک مبنای مهم برای افتراق است.
تفاوتهای اصلی بین بیماری کوتس و رتینوبلاستوما در زیر نشان داده شده است.
| ویژگی | بیماری کوتس | رتینوبلاستوما |
|---|---|---|
| سن شایع | حدود ۵ سالگی | ۱ تا ۲ سالگی |
| تفاوت جنسیتی | ۷۵٪ مرد | ندارد |
| درگیری دوطرفه | حدود ۵٪ | حدود ۴۰٪ |
| کلسیفیکاسیون | ندارد | دارد (با شیوع بالا) |
| توده جامد | ندارد | دارد |
| سونوگرافی | تجمع مایع زیر شبکیه | توده جامد، کلسیفیکاسیون داخلی، سایه خلفی |
| MRI | مایع زیر شبکیه همگن است | ناهمگن (سیگنال توده) |
سایر تشخیصهای افتراقی شامل همانژیوم شبکیه، بیماری فون هیپل-لینداو، هیپرپلازی زجاجیه اولیه (PHPV)، ویترئورتینوپاتی اگزوداتیو خانوادگی (FEVR)، توکسوکاریازیس، تومور واسوپرولیفراتیو، بیماری ایلز و غیره است.
هدف درمان مسدود کردن عروق غیرطبیعی و توقف تولید ترشحات است. رویکرد مرحلهای بر اساس مرحله بیماری اتخاذ میشود.
این درمان خط اول است. عروق غیرطبیعی و آنوریسمهای مویرگی که در آنژیوگرافی فلورسئین (FA) تأیید شدهاند، مستقیماً منعقد میشوند و همچنین نواحی بدون پرفیوژن اطراف نیز تحت فوتوکوآگولاسیون قرار میگیرند. در کودکان، این عمل تحت بیهوشی عمومی انجام میشود. اغلب به جلسات متعدد نیاز است و پس از درمان نیز ارزیابی مجدد منظم با FA و انعقاد اضافی تکرار میشود.
این گزینه بعدی برای ضایعات ناحیه قدامی محیطی یا نواحی است که فوتوکوآگولاسیون در آنها دشوار است. گاهی همراه با فوتوکوآگولاسیون استفاده میشود.
انعقاد لیزری
موارد مصرف: عروق غیرطبیعی و ضایعات ترشحی در مراحل 1 تا 3A.
روش: تحت هدایت FA، نواحی گشادشدگی مویرگی و نواحی بدون پرفیوژن مستقیماً منعقد میشوند. در کودکان تحت بیهوشی عمومی انجام میشود.
ویژگیها: قابل انجام مکرر. ارزیابی مجدد منظم با FA پس از درمان و انعقاد اضافی، مدیریت استاندارد است.
انجماد
موارد مصرف: ضایعات محیطی قدامی که فوتوکوآگولاسیون در آنها دشوار است، و به عنوان کمک در موارد شدید مرحله 3B و پایینتر.
روش: پروب انجماد از طریق صلبیه اعمال میشود تا عروق غیرطبیعی منعقد و مسدود شوند.
ویژگیها: مزیت آن قابلیت انجام در محیطهای کدر و در دورترین نواحی محیطی است.
جراحی زجاجیه و شبکیه
موارد مصرف: مرحله 3B (جداشدگی کامل شبکیه) و بالاتر، موارد عدم پاسخ به انجماد.
روش: تخلیه مایع زیرشبکیه از طریق خارجی یا ویترکتومی و جااندازی شبکیه از داخل 8). در موارد شدید، ممکن است تخلیه مایع زیرشبکیه همراه با بستن حلقهای (اسکلرال باکل) انجام شود.
ویژگیها: گزارش شده است که در موارد همراه با سوراخ ماکولا، روش فلپ غشای محدودکننده داخلی (ILM) مؤثر است 4).
استفاده از داروهای ضد VEGF در بیماری کوتس هنوز به اجماع نرسیده است و به عنوان درمان استاندارد در نظر گرفته نمیشود، بلکه به عنوان درمان کمکی در کنار فتوکوآگولاسیون قرار میگیرد.
در یک مورد از بیماری کوتس بزرگسالان، ترکیبی از تزریق داخل زجاجیهای ranibizumab 0.5 میلیگرم و لیزر فتوکوآگولاسیون انجام شد و بهترین دید اصلاح شده از شمارش انگشتان به 20/60 بهبود یافت 3).
در یک گزارش از کودکان، تزریق داخل زجاجیهای bevacizumab 1.25 میلیگرم، تریامسینولون زیر تانون و لیزر به صورت ترکیبی هر 6 هفته تحت بیهوشی عمومی انجام شد. اشاره شده است که پس از درمان ممکن است تشدید ترشحات متناقض (رتینوپاتی اگزوداتیو متناقض) رخ دهد 2).
همچنین گزارش شده است که brolucizumab در موارد مقاوم به bevacizumab مؤثر بوده است 2). احتمال دارد درمان ضد VEGF از تشکیل ندول فیبروزی جلوگیری کند 5).
در موارد چشم نابینا و دردناک (مرحله 4 تا 5) که رد رتینوبلاستوما دشوار است، انوکلئاسیون انتخاب میشود.
در بیماری کوتس، مواردی از عود و جداشدگی مجدد در طی چند سال دیده میشود و همچنین موارد دوطرفه با زمان شروع متفاوت وجود دارد. حتی پس از اتمام درمان، ارزیابی مجدد دورهای با آنژیوگرافی فلورسئین ضروری است و در صورت مشاهده ضایعات جدید، باید فتوکوآگولاسیون یا کرایوتراپی اضافی انجام شود.
در حال حاضر، در مورد استفاده از داروهای ضد VEGF برای بیماری کوتس اجماعی وجود ندارد و این داروها به عنوان درمان استاندارد محسوب نمیشوند. اگرچه گزارشهایی از استفاده کمکی همراه با لیزر فوتوکوآگولاسیون در حال افزایش است، اما ارزیابی اثربخشی و ایمنی نیاز به تحقیقات بیشتری دارد.
مرکز مکانیسم بروز بیماری کوتس، اختلال در سد خونی-شبکیه داخلی (inner blood-retinal barrier; iBRB) است1).
iBRB از سلولهای اندوتلیال مویرگهای شبکیه و سلولهای پریسیت که از آنها حمایت میکنند، تشکیل شده است. در بیماری کوتس، تعداد پریسیتها به طور قابل توجهی کاهش مییابد که منجر به کاهش عملکرد حمایتی عروق اندوتلیال میشود1). همچنین با رنگآمیزی ایمنی و میکروسکوپ الکترونی تأیید شده است که تعداد خود سلولهای اندوتلیال نیز کاهش مییابد1).
اختلال در سد خونی-شبکیه داخلی باعث نشت و تجمع اجزای پلاسما (عمدتاً لیپوپروتئینها و کلسترول) در دیواره عروق، داخل شبکیه و زیر شبکیه میشود1). لیپیدهای تجمعیافته باعث نفوذ ماکروفاژهای حاوی لیپید (سلولهای کفآلود) و واکنش ایمنی گرانولوماتوز شده و آسیب بافتی را تشدید میکنند1).
محیط با VEGF بالا باعث گشاد شدن بیشتر مویرگهای محیطی و پیشرفت ضایعه میشود2). مشاهدات OCTA در ندولهای فیبروتیک ماکولار ضایعات پیشرفته، وجود عروق نوزاد نوع 3 (به ترتیب تشکیل SVC → DVC → کمپلکس عروقی) را تأیید کرده است5) و درک فرآیند تشکیل عروق نوزاد در حال پیشرفت است.
مکانیسم ایجاد سوراخ ماکولا این است که لیزر محیطی باعث کوتاه شدن شبکیه و ایجاد کشش مماسی میشود که منجر به سوراخ در ناحیه ماکولا میگردد4).
OCTA امکان ارزیابی غیرتهاجمی ساختار عروق ریز داخل ندولهای فیبروتیک را فراهم کرده است.
Ong و همکاران (2021) با استفاده از OCTA ساختار عروق داخل ندول ماکولا را به طور دقیق تحلیل کردند و وجود عروق نوزاد نوع 3 را که به ترتیب SVC → DVC → کمپلکس عروقی تشکیل میشوند، آشکار ساختند5). این یافته برای درک مکانیسم تشکیل ندول و به عنوان هدف درمان ضد VEGF مهم است.
پدیدهای گزارش شده است که در آن پس از شروع درمان ضد VEGF، ترشحات به طور متناقضی افزایش مییابد و نیاز به کشف مکانیسم و ایجاد روش مدیریت وجود دارد.
Kalavar و همکاران (2022) یک مورد بیماری کوتس در کودک را گزارش کردند که پس از شروع درمان، افزایش موقت ترشحات و تشکیل ستاره ماکولا (macular star formation) رخ داد2). استفاده از برولوسیزوماب در موارد مقاوم به بواسیزوماب مؤثر بوده و به عنوان یک گزینه درمانی جدید مورد توجه قرار گرفته است2).
Nawrocka و همکاران (2023) یک مورد از جراحی ویترکتومی با استفاده از روش فلپ معکوس غشای محدود کننده داخلی (inverted ILM flap) را برای سوراخ ماکولا همراه با بیماری کوتس گزارش کردند4). بسته شدن سوراخ ماکولا 18 ماه پس از جراحی تأیید شد و بهترین دید اصلاح شده 20/40 بود. سوراخ ماکولا مرتبط با بیماری کوتس یک عارضه نادر است که تنها حدود 7 مورد در PubMed گزارش شده است4).
Shields و همکاران (2019) 351 چشم از موارد بیماری کوتس را در یک دوره 45 ساله تحلیل کردند و بهبود نتایج درمان را در طول دههها نشان دادند9). Dalvin و همکاران (2019) همان گروه را بر اساس رده سنی تحلیل کردند و نشان دادند که موارد شروع در دوران کودکی نسبت به موارد شروع در بزرگسالی تمایل به شدت بیشتر و پیشآگهی بینایی بدتری دارند10).
بیماری کوتس با شروع در بزرگسالی یک مفهوم بیماری است که قبلاً کمتر شناخته شده بود و تعداد گزارشها در حال افزایش است3). تفاوتهای بالینی با نوع کودکان (خفیفتر، پیشرفت آهسته، پاسخ خوب به درمان) در حال روشن شدن است و ایجاد پروتکل درمانی مناسب برای بزرگسالان یک چالش است.