第1~2期
第1期:僅見視網膜毛細血管擴張,不伴滲出。
Stage 2A:除毛細血管擴張外,在中心凹外可見滲出物。
Stage 2B:滲出物延伸至中心凹。視力下降變得明顯。

Coats病是1908年由George Coats報告的特發性視網膜血管疾病。其本質是視網膜毛細血管異常擴張(毛細血管擴張症)以及血管壁向視網膜內和視網膜下滲出物積聚。
該病為散發性、非遺傳性,與全身疾病或家族史無關1)。發病率約為每10萬人0.09例,十分罕見2)。約75%的患者為男性,95%為單眼發病,好發於20歲以下(平均約5歲)。
成人發病非常罕見,但呈現與兒童型不同的臨床特徵。成人發病病例比兒童型症狀輕、進展緩慢,治療反應也良好3)。某報告顯示,48隻成人發病眼中僅21%發生滲出性視網膜剝離,顯著低於兒童發病的81%3)。
輕型也稱為Leber粟粒狀血管瘤病,構成Coats病譜系的一部分。第1型特發性黃斑毛細血管擴張症也被認為屬於同一疾病譜系。
已有35歲以上發病的病例報告,被認定為成人發病型Coats病3)。與兒童型相比,病變進展緩慢,滲出性視網膜剝離的發生頻率低,治療反應通常良好。但發病本身罕見,在成人中發現類似表現時,與其他疾病的鑑別很重要。
嬰幼兒期發病時,患兒本身很少主訴症狀。
成人發病病例視力相對保持較好,有時在體檢中偶然發現3)。
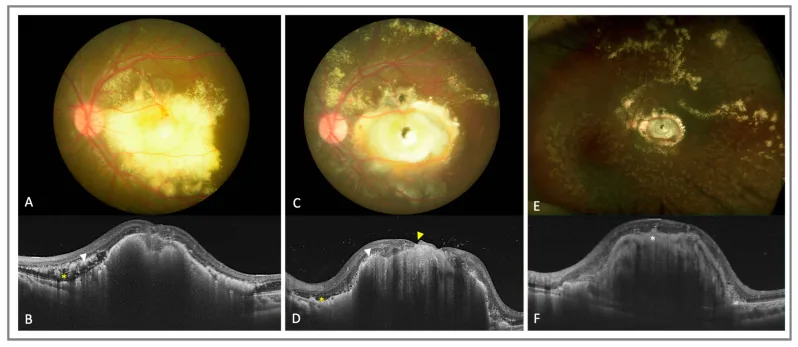
眼底所見特徵為集中於周邊部的異常擴張視網膜血管,以及黃白色視網膜下和視網膜內滲出物的蓄積。螢光眼底造影顯示周邊部視網膜血管閉塞、毛細血管擴張、毛細血管瘤、新生血管等特徵性表現。病情進展可導致滲出性視網膜剝離,最終發展為全剝離。超音波檢查、CT、MRI顯示視網膜下液均勻分佈,這一點與伴有鈣化的不均勻影像的視網膜母細胞瘤是重要的影像學鑑別點。
後期可出現虹膜紅變和新生血管性青光眼等眼前節併發症。黃斑裂孔是罕見併發症,文獻中僅報告約7例4)。纖維性結節是視力預後不良的因素,OCTA顯示結節記憶體在3型新生血管(SVC→DVC→無血管複合體)5)。
Shields分類將Coats病的病程分為以下5期。用於選擇治療方案和預後評估。
第1~2期
第1期:僅見視網膜毛細血管擴張,不伴滲出。
Stage 2A:除毛細血管擴張外,在中心凹外可見滲出物。
Stage 2B:滲出物延伸至中心凹。視力下降變得明顯。
Stage 3
Stage 3A1:伴有中心凹外的次全視網膜剝離。
Stage 3A2:伴有累及中心凹的次全視網膜剝離。視力預後不良。
Stage 3B:發生全視網膜剝離。需要緊急介入。
Stage 4~5
Stage 4:全視網膜剝離合併續發性青光眼,為終末期前階段。可能伴有疼痛。
Stage 5:終末期。眼球癆(萎縮)。可考慮眼球摘除。
多種疾病可表現為白瞳孔,Coats病只是其中之一。最重要的鑑別診斷是視網膜母細胞瘤(Rb),因其直接關係到生命預後,需要緊急評估。其他鑑別診斷包括早產兒視網膜病變、永存原始玻璃體增生症(PHPV)、眼內炎等。詳見「診斷與檢查方法」一節。
Coats病的發病原因不明,未發現與全身性疾病或家族史有關。有報告提示遺傳背景,如第3、13號染色體不穩定,以及與NDP基因(Norrie病相關)、CRB1基因的關聯,但尚未確立。
作為病理的起點,內血-視網膜屏障(iBRB)的破壞被認為扮演核心角色1)。周細胞(支持血管內皮的細胞)減少導致血管壁脆弱,形成異常擴張的毛細血管和動脈瘤1)。血漿成分滲漏並積聚在血管壁內和視網膜層內,導致血管壁增厚,進一步加重滲出,形成惡性循環2)。
高VEGF環境也被認為促進周邊毛細血管擴張2),這一機制構成了抗VEGF治療的理論基礎。
診斷需結合多種檢查,其中最重要的是與視網膜母細胞瘤(Rb)的鑑別。
散瞳下眼底檢查可見周邊部迂曲的異常血管網和黃白色視網膜下滲出物。滲出物累及黃斑部時呈硬性白斑樣外觀。
這是診斷Coats病最重要的檢查之一。特徵性表現包括微血管顯著擴張、微血管瘤、動靜脈吻合以及「燈泡樣」螢光滲漏。對於確定異常血管範圍和雷射光凝部位至關重要。
確認無實體腫塊。Rb在B模式中常顯示實體腫塊內高回音(鈣化),而Coats病不形成實體腫塊。
評估有無鈣化。Rb常伴有鈣化,而Coats病不發生鈣化。此發現是鑑別診斷的重要依據。
Coats病與視網膜母細胞瘤的主要鑑別點如下所示。
| 項目 | Coats病 | 視網膜母細胞瘤 |
|---|---|---|
| 好發年齡 | 5歲左右 | 1~2歲 |
| 性別差異 | 男性75% | 無 |
| 雙眼性 | 約5% | 約40% |
| 鈣化 | 無 | 有(高機率) |
| 實性腫塊 | 無 | 有 |
| 超音波 | 視網膜下液體積聚 | 實性腫塊、內部鈣化、後方陰影 |
| MRI | 視網膜下液均質 | 不均質(腫塊訊號) |
其他鑑別診斷包括視網膜血管瘤、von Hippel-Lindau病、持續性增生性原始玻璃體(PHPV)、家族性滲出性玻璃體視網膜病變(FEVR)、弓蟲症、血管增生性腫瘤、Eales病等。
治療目標是阻塞異常血管,停止滲出物的產生。根據疾病分期採取逐步治療策略。
這是第一線治療。透過FA確認的異常擴張血管和微動脈瘤直接進行光凝固,同時對周圍無灌流區域也進行光凝固。在兒童中,需在全身麻醉下進行。通常需要多次療程,治療後需定期透過FA重新評估並重複追加凝固。
這是用於前部周邊病變或光凝固困難部位的後續選擇。有時會與光凝固合併使用。
雷射光凝固
適應症:第1至3A期的異常血管和滲出性病變。
方法:在FA引導下直接凝固毛細血管擴張區域和無灌流區。兒童在全身麻醉下進行。
特點:可重複進行。治療後定期FA再評估和追加凝固是標準管理。
冷凍凝固
適應症:光凝固困難的前部周邊病變,以及第3B期以下重症病例的輔助治療。
方法:經鞏膜應用冷凍探頭,凝固並閉塞異常血管。
特點:在混濁介質或最周邊部也可施行。
玻璃體視網膜手術
適應症:第3B期(全視網膜剝離)及以上,冷凍凝固無效的病例。
方法:透過外部引流或玻璃體手術引流視網膜下液,並進行內部視網膜復位8)。重症病例可合併視網膜下液引流和鞏膜扣帶術。
特點:對於合併黃斑裂孔的病例,有報告指出內界膜(ILM)翻轉術有效4)。
抗VEGF藥物用於Coats病尚未達成共識,不是標準治療,而是作為與光凝聯合使用的輔助治療。
有報告稱,一例成人發病的Coats病患者接受了ranibizumab 0.5mg玻璃體內注射聯合雷射光凝治療,最終矯正視力從指數提高到20/603)。
在一例兒童病例中,每6週在全身麻醉下進行bevacizumab 1.25mg玻璃體內注射、sub-Tenon triamcinolone和雷射聯合治療,有報告指出治療後可能出現矛盾性滲出性視網膜病變2)。
也有報告稱brolucizumab對bevacizumab抗藥病例有效2)。抗VEGF治療可能有助於預防纖維結節形成5)。
對於疼痛性失明眼(Stage 4~5)且難以排除視網膜母細胞瘤時,選擇眼球摘除。
Coats病中,有些病例在數年內復發或再次剝離,也有雙眼發病時間不同的病例。治療完成後也需要定期進行螢光眼底造影重新評估,如果發現新病變,需要追加光凝或冷凍治療。
目前,關於抗VEGF藥物用於Coats病尚未達成共識,不被視為標準治療。雖然作為雷射光凝輔助聯合療法的報告正在累積,但其有效性與安全性評估仍需進一步研究。
Coats病的核心發病機轉是內血-視網膜屏障(inner blood-retinal barrier; iBRB)的破壞1)。
iBRB由視網膜微血管內皮細胞與支持它們的周細胞構成。在Coats病中,周細胞數量顯著減少,導致血管內皮支持功能下降1)。免疫染色和電子顯微鏡觀察已證實內皮細胞本身的數量也減少1)。
內皮BRB的破壞導致血漿成分(主要是脂蛋白和膽固醇)滲漏並積聚在血管壁內、視網膜內和視網膜下1)。積聚的脂質引發含脂巨噬細胞(泡沫細胞)的浸潤和肉芽腫性免疫反應,加劇組織損傷1)。
高VEGF環境促進周邊微血管進一步擴張,參與病變進展2)。OCTA觀察顯示,在晚期病變的黃斑纖維結節內存在第3型新生血管(按SVC→DVC→無血管複合體的順序形成)5),對新生血管形成過程的認識正在深入。
黃斑裂孔形成的機轉被認為是周邊雷射光凝導致視網膜縮短,產生切線方向牽引,從而在黃斑部造成穿孔4)。
OCTA使得非侵入性評估纖維結節內的微血管結構成為可能。
Ong等人(2021)利用OCTA詳細分析了黃斑結節內的血管結構,揭示了按SVC→DVC→無血管複合體順序形成的第3型新生血管的存在5)。這一發現對於闡明結節形成機轉以及作為抗VEGF治療的標靶具有重要意義。
有報告指出在抗VEGF治療開始後出現矛盾性滲出惡化現象,需要闡明機制並建立管理方法。
Kalavar等人(2022)報告了一例兒童Coats病在治療開始後出現一過性滲出惡化和黃斑星芒狀滲出的病例2)。對於bevacizumab抵抗的病例,使用brolucizumab有效,作為新的治療選擇受到關注2)。
Nawrocka等人(2023)報告了一例對Coats病合併黃斑裂孔採用內界膜翻轉瓣法進行玻璃體手術的病例4)。術後18個月確認黃斑裂孔閉合,最終矯正視力為20/40。Coats病相關黃斑裂孔在PubMed上僅報告約7例,是一種罕見的併發症4)。
Shields等人(2019)分析了351眼、45年的Coats病病例,顯示不同年代的治療效果有所改善9)。Dalvin等人(2019)按年齡類別分析了同一隊列,顯示兒童發病病例比成人發病病例病變更易加重,視力預後更差10)。
成人發病Coats病是傳統上被低估的疾病概念,報告數量正在增加3)。與兒童型的臨床差異(輕症、緩慢進展、治療反應良好)正在整理中,建立成人適當的治療方案成為課題。