ระยะ 1-2
ระยะ 1: มีเพียงการขยายของเส้นเลือดฝอยจอตา โดยไม่มีสารคัดหลั่ง
ระยะ 2A: มีการขยายตัวของเส้นเลือดฝอยร่วมกับมีสารคัดหลั่งนอกบริเวณรอยบุ๋มจอตา (fovea)
ระยะ 2B: สารคัดหลั่งลามไปถึงรอยบุ๋มจอตา การมองเห็นลดลงอย่างชัดเจน

โรคคอตส์ (Coats disease) เป็นโรคหลอดเลือดจอตาที่ไม่ทราบสาเหตุ รายงานครั้งแรกโดย George Coats ในปี ค.ศ. 1908 มีลักษณะสำคัญคือการขยายตัวผิดปกติของหลอดเลือดฝอยจอตา (telangiectasia) และการสะสมของสารคัดหลั่งในและใต้จอตาจากผนังหลอดเลือด
โรคนี้เกิดเป็นประปรายและไม่ถ่ายทอดทางพันธุกรรม ไม่เกี่ยวข้องกับโรคทางระบบหรือประวัติครอบครัว 1) อุบัติการณ์พบน้อย ประมาณ 0.09 ต่อ 100,000 คน 2) ประมาณ 75% ของผู้ป่วยเป็นเพศชาย 95% เป็นตาเดียว และมักเกิดในผู้ที่มีอายุต่ำกว่า 20 ปี (เฉลี่ยประมาณ 5 ปี)
การเริ่มป่วยในผู้ใหญ่พบน้อยมาก แต่มีลักษณะทางคลินิกแตกต่างจากในเด็ก กรณีที่เริ่มป่วยในผู้ใหญ่จะรุนแรงน้อยกว่า ดำเนินโรคช้า และตอบสนองต่อการรักษาได้ดี 3) ในรายงานหนึ่ง พบว่ามีจอตาลอกแบบมีน้ำใต้จอตาเพียง 21% จาก 48 ตาในผู้ใหญ่ ซึ่งต่ำกว่าอย่างมีนัยสำคัญเมื่อเทียบกับ 81% ในเด็ก 3)
ชนิดที่ไม่รุนแรงเรียกว่า หลอดเลือดโป่งพองแบบลูกเดือยของเลเบอร์ (Leber’s miliary aneurysms) ซึ่งเป็นส่วนหนึ่งของสเปกตรัมโรคคอตส์ ภาวะหลอดเลือดฝอยจอตาผิดปกติชนิดที่ 1 ที่ไม่ทราบสาเหตุก็ถือว่าอยู่ในสเปกตรัมเดียวกัน
มีรายงานกรณีที่เริ่มป่วยหลังอายุ 35 ปี และได้รับการยอมรับว่าเป็นโรคคอตส์ที่เริ่มในผู้ใหญ่ 3) เมื่อเทียบกับชนิดในเด็ก การดำเนินโรคช้ากว่า ความถี่ของจอตาลอกแบบมีน้ำใต้จอตาน้อยกว่า และมักตอบสนองต่อการรักษาได้ดี อย่างไรก็ตาม การเกิดโรคเองนั้นพบได้น้อย และเมื่อพบลักษณะคล้ายกันในผู้ใหญ่ จำเป็นต้องแยกจากโรคอื่น
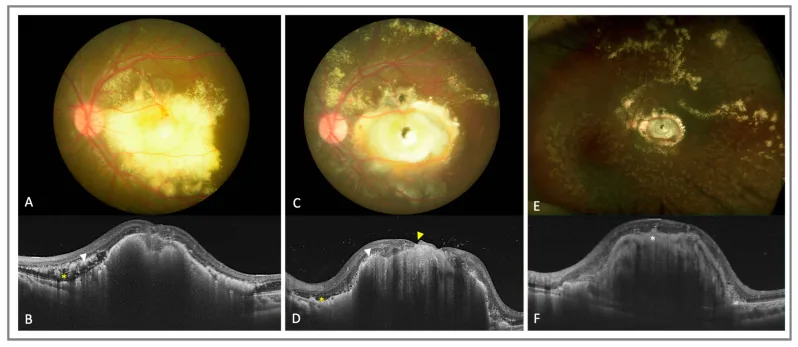
เมื่อเกิดในวัยทารกหรือเด็กเล็ก ผู้ป่วยเด็กมักไม่บ่นอาการ
ในกรณีที่เกิดในผู้ใหญ่ สายตาค่อนข้างดี และบางครั้งพบโดยบังเอิญจากการตรวจสุขภาพ 3)
ลักษณะเด่นของจอตาคือ หลอดเลือดจอตาที่ขยายผิดปกติกระจุกตัวบริเวณรอบนอก และการสะสมของสารคัดหลั่งสีเหลืองขาวใต้จอตาและในจอตา ในการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน ลักษณะเฉพาะ ได้แก่ การอุดตันของหลอดเลือดจอตาส่วนปลาย การขยายของเส้นเลือดฝอย หลอดเลือดโป่งพองขนาดเล็ก และเส้นเลือดใหม่ เมื่อดำเนินโรค จะเกิดจอตาลอกแบบมีน้ำใต้จอตา และในที่สุดนำไปสู่การลอกทั้งหมด ในการตรวจอัลตราซาวนด์ CT และ MRI ของเหลวใต้จอตาจะเห็นเป็นเนื้อเดียวกันทั่วทุกส่วน ซึ่งเป็นจุดแยกทางภาพที่สำคัญจาก retinoblastoma ที่มีลักษณะไม่เป็นเนื้อเดียวกันร่วมกับการกลายเป็นปูน
ในระยะปลาย เกิดภาวะแทรกซ้อนของส่วนหน้าดวงตา เช่น rubeosis iridis และต้อหินชนิดเส้นเลือดใหม่ รูที่จุดรับภาพเป็นภาวะแทรกซ้อนที่พบได้ยาก มีรายงานเพียงประมาณ 7 รายในวรรณกรรม 4) ก้อน fibrous เป็นปัจจัยพยากรณ์โรคทางสายตาที่ไม่ดี และในการตรวจ OCTA ยืนยันว่ามีเส้นเลือดใหม่ชนิดที่ 3 (SVC→DVC→complex avascular) ภายในก้อน 5)
การจำแนกตาม Shields แบ่งระยะของโรค Coats ออกเป็น 5 ระยะดังนี้ ใช้ในการเลือกแผนการรักษาและประเมินพยากรณ์โรค
ระยะ 1-2
ระยะ 1: มีเพียงการขยายของเส้นเลือดฝอยจอตา โดยไม่มีสารคัดหลั่ง
ระยะ 2A: มีการขยายตัวของเส้นเลือดฝอยร่วมกับมีสารคัดหลั่งนอกบริเวณรอยบุ๋มจอตา (fovea)
ระยะ 2B: สารคัดหลั่งลามไปถึงรอยบุ๋มจอตา การมองเห็นลดลงอย่างชัดเจน
ระยะ 3
ระยะ 3A1: จอตาลอกบางส่วนนอกบริเวณรอยบุ๋ม
ระยะ 3A2: จอตาลอกบางส่วนรวมถึงรอยบุ๋ม การพยากรณ์การมองเห็นไม่ดี
ระยะ 3B: จอตาลอกทั้งหมด จำเป็นต้องได้รับการรักษาอย่างเร่งด่วน
ระยะ 4–5
ระยะ 4: จอตาลอกทั้งหมดร่วมกับต้อหินทุติยภูมิ อาจมีอาการปวด
ระยะ 5: ระยะสุดท้าย ลูกตาฝ่อ (phthisis bulbi) พิจารณาเอาลูกตาออก
มีหลายโรคที่ทำให้เกิดรูม่านตาขาว และโรค Coats เป็นเพียงหนึ่งในนั้น การวินิจฉัยแยกโรคที่สำคัญที่สุดคือเรติโนบลาสโตมา (Rb) ซึ่งต้องประเมินอย่างเร่งด่วนเนื่องจากเกี่ยวข้องกับการพยากรณ์ชีวิต โรคอื่นๆ ได้แก่ จอประสาทตาในทารกคลอดก่อนกำหนด กลุ่มอาการหลอดเลือดเลี้ยงลูกตาคงอยู่ (PHPV) และเยื่อบุตาอักเสบ ดูรายละเอียดในหัวข้อ การวินิจฉัยและวิธีการตรวจ
ไม่ทราบสาเหตุของโรค Coats และไม่มีความสัมพันธ์กับโรคทางระบบหรือประวัติครอบครัว มีรายงานที่บ่งชี้ความสัมพันธ์กับความไม่เสถียรของโครโมโซมคู่ที่ 3 และ 13, ยีน NDP (โรค Norrie) และยีน CRB1 แต่ยังไม่เป็นที่ยืนยัน
การทำลายสิ่งกีดขวางเลือด-จอตาชั้นใน (iBRB) เชื่อว่ามีบทบาทสำคัญในการเกิดโรค 1) การลดลงของเพอริไซต์ (เซลล์ที่รองรับเยื่อบุผนังหลอดเลือด) ทำให้ผนังหลอดเลือดอ่อนแอลง นำไปสู่การเกิดเส้นเลือดฝอยขยายผิดปกติและโป่งพอง 1) ส่วนประกอบของพลาสมารั่วและสะสมในผนังหลอดเลือดและชั้นจอตา ทำให้ผนังหนาตัวและเกิดการรั่วซึมมากขึ้น เกิดเป็นวงจรอุบาทว์ 2)
สภาพแวดล้อมที่มี VEGF สูงยังถูกเสนอว่าส่งเสริมการขยายตัวของเส้นเลือดฝอยส่วนปลาย 2) ซึ่งเป็นเหตุผลทางทฤษฎีสำหรับการรักษาด้วยยาต้าน VEGF
การวินิจฉัยต้องใช้การตรวจหลายวิธีร่วมกัน โดยเฉพาะการแยกโรคจากเรติโนบลาสโตมา (Rb) อย่างแน่ชัดเป็นสิ่งที่สำคัญที่สุด
การตรวจอวัยวะภายในลูกตาภายใต้การขยายม่านตาเผยให้เห็นเครือข่ายหลอดเลือดผิดปกติที่คดเคี้ยวในบริเวณรอบนอกและสารคัดหลั่งใต้จอประสาทตาสีเหลืองขาว หากสารคัดหลั่งลามไปถึงจุดรับภาพ จะมีลักษณะคล้ายแผ่นแข็ง
นี่คือหนึ่งในการตรวจที่สำคัญที่สุดในการวินิจฉัยโรคคาทส์ ลักษณะเฉพาะ ได้แก่ การขยายตัวของเส้นเลือดฝอยอย่างเด่นชัด หลอดเลือดโป่งพองขนาดเล็ก การเชื่อมต่อระหว่างหลอดเลือดแดงและดำ และการรั่วของฟลูออเรสซีนรูปหลอดไฟ จำเป็นอย่างยิ่งในการกำหนดขอบเขตของหลอดเลือดผิดปกติและตำแหน่งจี้ด้วยเลเซอร์
ยืนยันว่าไม่มีก้อนเนื้อแข็ง Rb มักแสดงสัญญาณสะท้อนความเข้มสูง (การกลายเป็นหินปูน) ภายในก้อนเนื้อแข็งในโหมด B ในขณะที่โรคคาทส์ไม่ก่อให้เกิดก้อนเนื้อแข็ง
ประเมินว่ามีการกลายเป็นหินปูนหรือไม่ Rb มักมีการกลายเป็นหินปูนในอัตราสูง ในขณะที่โรคคาทส์ไม่ทำให้เกิดการกลายเป็นหินปูน ผลการตรวจนี้เป็นพื้นฐานสำคัญในการแยกโรค
ต่อไปนี้คือข้อแตกต่างหลักระหว่างโรคคาทส์และเรติโนบลาสโตมา
| รายการ | โรคคาทส์ | เรติโนบลาสโตมา |
|---|---|---|
| อายุที่พบบ่อย | ประมาณ 5 ปี | 1-2 ปี |
| เพศ | ชาย 75% | ไม่มี |
| เป็นสองตา | ประมาณ 5% | ประมาณ 40% |
| การกลายเป็นหินปูน | ไม่มี | มี (อัตราสูง) |
| ก้อนเนื้อแข็ง | ไม่มี | มี |
| อัลตราซาวนด์ | การสะสมของของเหลวใต้จอประสาทตา | ก้อนเนื้อแข็ง, การกลายเป็นปูนภายใน, เงาด้านหลัง |
| MRI | ของเหลวใต้จอประสาทตาเป็นเนื้อเดียวกัน | ไม่เป็นเนื้อเดียวกัน (สัญญาณก้อน) |
โรคอื่นๆ ที่ต้องแยกวินิจฉัย ได้แก่: หลอดเลือดแดงจอประสาทตาผิดปกติ, โรค von Hippel-Lindau, ภาวะ Persistent Hyperplastic Primary Vitreous (PHPV), โรค Familial Exudative Vitreoretinopathy (FEVR), โรค Toxocara, เนื้องอกหลอดเลือดขยายตัว, โรค Eales
เป้าหมายของการรักษาคือการอุดหลอดเลือดที่ผิดปกติและหยุดการผลิตสารคัดหลั่ง โดยใช้วิธีการแบบเป็นขั้นตอนตามระยะของโรค
เป็นการรักษาทางเลือกแรก หลอดเลือดที่ขยายผิดปกติและโป่งพองของเส้นเลือดฝอยที่ยืนยันโดย FA จะถูกจี้แข็งโดยตรง และยังทำการจี้ด้วยแสงในบริเวณที่ไม่มีการไหลเวียนรอบนอก ในเด็ก จะทำภายใต้การดมยาสลบ มักต้องทำหลายครั้ง และจะมีการประเมินซ้ำด้วย FA เป็นระยะและการจี้เพิ่มเติมหลังการรักษา
เป็นทางเลือกถัดไปที่ใช้สำหรับรอยโรคบริเวณส่วนรอบนอกด้านหน้าหรือตำแหน่งที่ยากต่อการจี้ด้วยแสง บางครั้งใช้ร่วมกับการจี้ด้วยแสง
การจี้ด้วยเลเซอร์
ข้อบ่งชี้: หลอดเลือดผิดปกติและรอยโรคที่มีสารคัดหลั่งในระยะที่ 1 ถึง 3A
วิธีการ: จี้บริเวณที่มีเส้นเลือดฝอยขยายและบริเวณที่ไม่มีการไหลเวียนโดยตรงภายใต้การนำของ FA ในเด็ก ทำภายใต้การดมยาสลบ
ลักษณะเด่น: สามารถทำซ้ำได้ การประเมินซ้ำด้วย FA เป็นระยะและการจี้เพิ่มเติมหลังการรักษาเป็นการจัดการมาตรฐาน
การจี้เย็น
ข้อบ่งชี้: รอยโรคส่วนรอบนอกด้านหน้าที่จี้ด้วยแสงได้ยาก ช่วยเหลือในกรณีรุนแรงจนถึงระยะ 3B
วิธีการ: ใช้หัววัดเย็นผ่านตาขาวเพื่อจี้และอุดหลอดเลือดผิดปกติ
ลักษณะเด่น: สามารถทำได้ในสื่อขุ่นหรือในส่วนที่อยู่รอบนอกที่สุด
การผ่าตัดวุ้นตาและจอตา
ข้อบ่งชี้: ระยะ 3B (จอตาลอกทั้งหมด) ขึ้นไป กรณีที่ไม่ตอบสนองต่อการจี้เย็น
วิธีการ: ระบายของเหลวใต้จอตาผ่านการระบายภายนอกหรือการผ่าตัดวุ้นตา และการจัดจอตาให้เข้าที่จากภายใน 8) ในกรณีรุนแรง อาจระบายของเหลวใต้จอตาร่วมกับการรัดตาขาว (scleral buckle)
ลักษณะเด่น: เทคนิคการพลิกเยื่อหุ้มขอบใน (ILM) มีรายงานว่ามีประสิทธิภาพในกรณีที่มีรูที่จุดรับภาพ 4)
การใช้ยาต้าน VEGF สำหรับโรคคอตส์ยังไม่มีฉันทามติที่ชัดเจน และถือเป็นการรักษาเสริมร่วมกับการจี้ด้วยแสง ไม่ใช่การรักษามาตรฐาน
มีรายงานผู้ป่วยโรคคอตส์ในผู้ใหญ่ 1 รายที่ได้รับการรักษาด้วยการฉีด ranibizumab 0.5 มก. เข้าแก้วตาเลนส์ร่วมกับการจี้ด้วยเลเซอร์ และค่าสายตาที่แก้ไขแล้วดีขึ้นจากนับนิ้วเป็น 20/60 3)
ในรายงานผู้ป่วยเด็กที่ได้รับการรักษาด้วยการฉีด bevacizumab 1.25 มก. เข้าแก้วตาเลนส์, triamcinolone ใต้ Tenon และเลเซอร์ภายใต้การดมยาสลบทุก 6 สัปดาห์ พบว่าอาจเกิดภาวะน้ำรั่วที่รุนแรงขึ้นอย่างขัดแย้งหลังการรักษา 2)
มีรายงานว่า brolucizumab มีประสิทธิภาพในกรณีที่ดื้อต่อ bevacizumab 2) มีข้อเสนอแนะว่าการรักษาด้วยยาต้าน VEGF อาจช่วยป้องกันการเกิดก้อนเนื้อเยื่อพังผืด 5)
ในกรณีตาบอดที่เจ็บปวด (ระยะ 4-5) และยากที่จะแยกโรคเรติโนบลาสโตมา การควักลูกตาเป็นทางเลือก
ในโรคคอตส์ มีผู้ป่วยที่เกิดอาการกำเริบหรือจอประสาทตาลอกซ้ำในช่วงหลายปี และยังมีกรณีที่เป็นทั้งสองตาโดยมีเวลาเริ่มต้นต่างกัน หลังจากเสร็จสิ้นการรักษา จำเป็นต้องประเมินซ้ำเป็นระยะด้วยการตรวจฟลูออเรสซีนแองจิโอกราฟี และหากพบรอยโรคใหม่ ควรทำการจี้ด้วยแสงหรือจี้ด้วยความเย็นเพิ่มเติม
ในปัจจุบัน ยังไม่มีฉันทามติเกี่ยวกับการใช้ยาต้าน VEGF สำหรับโรค Coats และยังไม่ถือว่าเป็นการรักษามาตรฐาน รายงานเกี่ยวกับการใช้เป็นยาเสริมร่วมกับการจี้ด้วยเลเซอร์กำลังสะสมมากขึ้น แต่การประเมินประสิทธิภาพและความปลอดภัยจำเป็นต้องมีการวิจัยเพิ่มเติม
ศูนย์กลางของกลไกการเกิดโรค Coats คือ การสลายของสิ่งกีดขวางเลือด-จอประสาทตาชั้นใน (inner blood-retinal barrier; iBRB) 1)
iBRB ประกอบด้วยเซลล์บุผนังหลอดเลือดฝอยจอประสาทตาและเพอริไซต์ที่ค้ำจุน ในโรค Coats จำนวนเพอริไซต์ลดลงอย่างมีนัยสำคัญ ซึ่งทำให้การทำงานสนับสนุนเซลล์บุผนังหลอดเลือดลดลง 1) จำนวนเซลล์บุผนังหลอดเลือดเองก็ลดลงเช่นกัน ซึ่งยืนยันโดยการย้อมอิมมูโนและกล้องจุลทรรศน์อิเล็กตรอน 1)
การสลายของ BRB ชั้นบุผนังหลอดเลือดทำให้ส่วนประกอบของพลาสมา (โดยเฉพาะไลโปโปรตีน คอเลสเตอรอล) รั่วและสะสมในผนังหลอดเลือด ภายในจอประสาทตา และใต้จอประสาทตา 1) ไขมันที่สะสมกระตุ้นการแทรกซึมของ มาโครฟาจที่มีไขมัน (เซลล์โฟม) และการตอบสนองทางภูมิคุ้มกันแบบแกรนูโลมา ทำให้เนื้อเยื่อเสียหายรุนแรงขึ้น 1)
สภาพแวดล้อมที่มี VEGF สูงส่งเสริมการขยายตัวของหลอดเลือดฝอยส่วนปลายมากขึ้น และมีส่วนร่วมในการดำเนินของรอยโรค 2) การสังเกตด้วย OCTA ยืนยันการมีอยู่ของเส้นเลือดใหม่ชนิดที่ 3 (เกิดขึ้นตามลำดับ SVC → DVC → คอมเพล็กซ์ไร้หลอดเลือด) ภายในปุ่มเส้นใยที่จอประสาทตาในรอยโรคระยะลุกลาม 5) และความเข้าใจเกี่ยวกับกระบวนการสร้างเส้นเลือดใหม่กำลังก้าวหน้า
ในฐานะกลไกการเกิดรูที่จอประสาทตา เชื่อว่าการหดสั้นของจอประสาทตาจากการจี้ด้วยเลเซอร์ส่วนปลายทำให้เกิดแรงดึงในแนวสัมผัส นำไปสู่การทะลุที่จอประสาทตาส่วนกลาง 4)
OCTA ทำให้สามารถประเมินโครงสร้างหลอดเลือดขนาดเล็กภายในปุ่มเส้นใยได้โดยไม่ต้องผ่าตัด
Ong และคณะ (2021) วิเคราะห์โครงสร้างหลอดเลือดภายในปุ่มจอประสาทตาอย่างละเอียดโดยใช้ OCTA และเปิดเผยการมีอยู่ของเส้นเลือดใหม่ชนิดที่ 3 ซึ่งเกิดขึ้นตามลำดับ SVC → DVC → คอมเพล็กซ์ไร้หลอดเลือด 5) การค้นพบนี้มีความสำคัญต่อการทำความเข้าใจกลไกการเกิดปุ่มและเป็นเป้าหมายสำหรับการรักษาด้วยยาต้าน VEGF
มีรายงานปรากฏการณ์ที่การขับ渗出แย่ลงอย่างขัดแย้งหลังจากเริ่มการรักษาด้วย anti-VEGF และจำเป็นต้องมีการอธิบายกลไกและการกำหนดแนวทางการจัดการ
Kalavar และคณะ (2022) รายงานผู้ป่วยเด็กโรค Coats ที่มีการขับ渗出แย่ลงชั่วคราวและการเกิด macular star formation หลังจากเริ่มการรักษา2) การใช้ brolucizumab ในกรณีที่ดื้อต่อ bevacizumab พบว่ามีประสิทธิภาพ จึงเป็นทางเลือกการรักษาใหม่ที่น่าสนใจ2)
Nawrocka และคณะ (2023) รายงานผู้ป่วยหนึ่งรายที่มีรูที่จอประสาทตาร่วมกับโรค Coats ซึ่งได้รับการรักษาด้วยการผ่าตัดน้ำวุ้นตาโดยใช้เทคนิค inverted ILM flap4) การปิดของรูที่จอประสาทตาได้รับการยืนยัน 18 เดือนหลังการผ่าตัด และค่าสายตาที่แก้ไขแล้วสุดท้ายคือ 20/40 รูที่จอประสาทตาที่เกี่ยวข้องกับโรค Coats เป็นภาวะแทรกซ้อนที่พบได้ยาก โดยมีรายงานเพียงประมาณ 7 รายใน PubMed4)
Shields และคณะ (2019) วิเคราะห์ผู้ป่วยโรค Coats จำนวน 351 ตาเป็นเวลา 45 ปี และแสดงให้เห็นถึงการปรับปรุงผลการรักษาตามช่วงเวลา9) Dalvin และคณะ (2019) วิเคราะห์กลุ่มประชากรเดียวกันตามหมวดอายุ และแสดงให้เห็นว่าผู้ป่วยที่เริ่มในวัยเด็กมีแนวโน้มที่จะรุนแรงกว่าและมีการพยากรณ์โรคทางสายตาที่แย่กว่าเมื่อเทียบกับผู้ป่วยที่เริ่มในวัยผู้ใหญ่10)
โรค Coats ที่เริ่มในวัยผู้ใหญ่เป็นแนวคิดโรคที่ก่อนหน้านี้ไม่ได้รับการยอมรับอย่างเพียงพอ และจำนวนรายงานกำลังเพิ่มขึ้น3) ความแตกต่างทางคลินิกจากชนิดในเด็ก (อาการน้อยกว่า ดำเนินโรคช้า ตอบสนองต่อการรักษาดี) กำลังถูกจัดระบบ และการกำหนดแนวทางการรักษาที่เหมาะสมในผู้ใหญ่ยังคงเป็นความท้าทาย