หลอดเลือดแดงจอตาขยายใหญ่แบบโป่งพองที่ได้มา (RAM ) คือการขยายเฉพาะที่แบบถุงหรือกระสวยในหลอดเลือดแดงจอตาภายในกิ่งที่สาม มักเกิดที่จุดแยกหรือจุดตัดหลอดเลือดแดง-ดำ
พบบ่อยในหญิงสูงอายุที่อายุมากกว่า 60 ปี โดยผู้ป่วย 70-78% เป็นผู้หญิง9)
ความดันโลหิตสูงเป็นปัจจัยเสี่ยงที่สำคัญที่สุด พบร่วมในผู้ป่วย 51-75%9)
หากเลือดออกหรือสารน้ำรั่วไม่ถึงจอประสาทตา ส่วนกลาง จะไม่มีอาการและตรวจพบได้ยาก หากถึงจอประสาทตา ส่วนกลาง จะทำให้การมองเห็น ลดลงและภาพบิดเบี้ยว
เลือดออกหลายชั้น (ใต้จอตา, ในจอตา, ในน้ำวุ้นตา ) เป็นลักษณะเฉพาะของ RAM
มีแนวโน้มที่จะหายได้เอง แต่ระดับความบกพร่องทางการมองเห็น และการฟื้นตัวแตกต่างกันไปตามระดับของสารน้ำรั่วหรือเลือดออกที่จอประสาทตา ส่วนกลางที่คงอยู่
การถ่ายภาพหลายรูปแบบร่วมกันของ FA , IA, OCT และ OCTA เป็นกุญแจสำคัญในการวินิจฉัย3)
การรักษาจะเลือกตามขั้นตอนตามชนิดและความรุนแรงของโรค รวมถึงการจี้ด้วยเลเซอร์ การรักษาด้วยยาต้าน VEGF และการผ่าตัดน้ำวุ้นตา
หลอดเลือดแดงจอตาขยายใหญ่แบบโป่งพองที่ได้มา (Retinal Arterial Macroaneurysm; RAM ) คือการขยายเฉพาะที่แบบถุงหรือกระสวยในหลอดเลือดแดงจอตาภายในกิ่งที่สาม มักสังเกตเห็นยื่นออกมาจากจุดแยกของหลอดเลือดแดงจอตาหรือจุดตัดหลอดเลือดแดง-ดำ สารน้ำรั่วหรือเลือดออกจาก RAM ทำให้เกิดการเปลี่ยนแปลงทางสัณฐานวิทยาและความบกพร่องทางการทำงาน รายงานครั้งแรกโดย Robertson ในปี 1973
ขนาดโดยทั่วไปคือ 100-250 ไมโครเมตร1, 3) ประมาณ 50% เกิดที่หลอดเลือดแดงขมับด้านบน 45% ที่หลอดเลือดแดงขมับด้านล่าง และพบน้อยที่ด้านจมูก3) พบบ่อยที่ด้านขมับแต่ก็เกิดที่ด้านจมูกได้ มักเป็นข้างเดียวและตำแหน่งเดียว แต่ก็มีกรณีสองตาและหลายตำแหน่ง พบบ่อยในผู้สูงอายุที่มีประวัติความดันโลหิตสูงและหลอดเลือดแดงแข็ง
RAM ที่เกิดขึ้นบนหัวประสาทตาคิดเป็น 3.7-8% ของทั้งหมด ซึ่งเป็นภาวะที่พบได้ยาก7, 10) เป็นที่ทราบกันว่า RAM มีแนวโน้มที่จะหายได้เอง ซึ่งส่งผลต่อการตัดสินใจในการรักษา
Q
หลอดเลือดแดงจอตาขยายใหญ่แบบโป่งพองที่ได้มาพบได้ยากเพียงใด?
A
โรคที่พบได้ค่อนข้างน้อย แต่โอกาสพบเพิ่มขึ้นตามอายุที่มากขึ้น โป่งพองของหลอดเลือดแดงจอประสาทตา บนจานประสาทตา พบได้น้อยยิ่งขึ้น โดยรายงานว่าอยู่ที่ 3.7-8% ของทั้งหมด 7, 10) ในชนิดเลือดออก หากเลือดออกหรือสารน้ำรั่วกระจายไปถึงจุดรับภาพ จะทำให้สูญเสียการมองเห็น อย่างรุนแรง ดังนั้นการวินิจฉัยและการจัดการตั้งแต่เนิ่นๆ จึงมีความสำคัญ
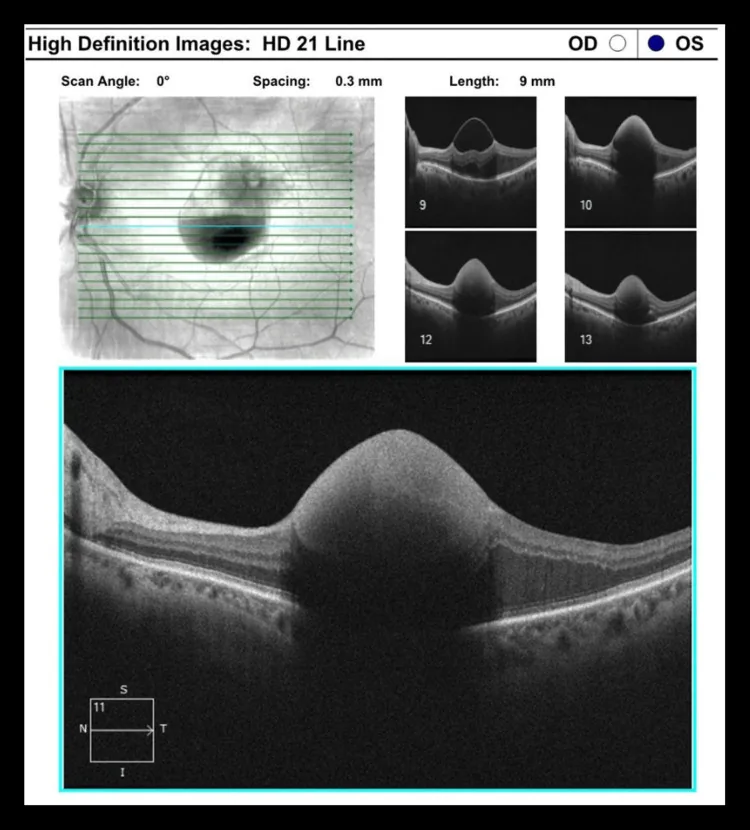
ภาพ OCT ของโป่งพองของหลอดเลือดแดงจอประสาทตาที่ได้มา Jemelian A, et al. Outcomes of Combined Therapy With Focal Laser and Intravitreal Bevacizumab for Retinal Arterial Macroaneurysm: A Case Series. Cureus. 2025. Figure 2. PM
CI D: PMC12034429. License: CC BY.
ภาพตัดขวาง OCT สอดคล้องกับรอยโรคสะท้อนแสงสูงรูปโดมที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
เมื่อสารน้ำรั่วหรือเลือดออกกระจายถึงจุดรับภาพ จะเกิดการมองเห็น ลดลงและภาพบิดเบี้ยว หากไม่มีเลือดออกหรือสารน้ำรั่ว อาจไม่มีอาการที่ผู้ป่วยรับรู้ได้และตรวจพบได้ยาก
เมื่อเลือดออกหรือสารน้ำรั่วกระจายถึงจุดรับภาพ จะเกิดอาการดังต่อไปนี้:
การมองเห็น ลดลงการมองเห็น ลดลงเนื่องจากเลือดออกหรือสารน้ำรั่วที่จุดรับภาพ อาจเป็นแบบค่อยเป็นค่อยไปหรือเฉียบพลันภาพบิดเบี้ยว (เมตามอร์ฟอปเซีย)จุดบอดกลาง ความบกพร่องของลานสายตา จากความเสียหายต่อรอยบุ๋มจอตา การมองเห็น ลดลงอย่างเฉียบพลันวุ้นตา
โป่งพองของหลอดเลือดแดงจอประสาทตา แบ่งทางคลินิกเป็น 3 ชนิดดังต่อไปนี้ 3, 9)
ชนิด อาการหลัก ผลการตรวจที่จำเพาะ ชนิดไม่มีอาการ ไม่มี พบโดยบังเอิญ ชนิดเลือดออก การมองเห็น ลดลงเฉียบพลันเลือดออกหลายชั้น ชนิดมีสารขับออก การมองเห็น ลดลงช้าๆไขมันแข็งสีขาวและบวมน้ำ
เลือดออกที่มีลักษณะเฉพาะของ RAM คือเลือดออกหลายชั้น ซึ่งเกี่ยวข้องกับหลายชั้น เช่น ใต้จอประสาทตา ภายในจอประสาทตา ใต้เยื่อจำกัดชั้นใน (ILM ) หน้าก่อนจอประสาทตา และแก้วตา 9) รูปแบบเลือดออกหลายชั้นนี้เป็นหนึ่งในลักษณะเด่นของ RAM
ในการตรวจอวัยวะรับภาพ RAM จะมีสีแดงตามแนวหลอดเลือดแดงจอประสาทตา หากมีไฟบรินร่วมด้วยจะกลายเป็นสีขาว และหากเกิดพังผืดจะเป็นสีเทาขาว ในบางกรณีอาจไม่สามารถระบุโป่งพองได้เนื่องจากเลือดออกหรือสารขับออก ในชนิดมีสารขับออก จะพบไขมันแข็งสีขาวเป็นวง (จอประสาทตา อักเสบแบบวงแหวน) จอประสาทตา บวมน้ำ และจอประสาทตาลอก แบบมีน้ำใต้จอประสาทตา และอาจมีไขมันแข็งสีขาวเป็นวงรอบโป่งพอง (จอประสาทตา อักเสบแบบวงแหวน)
ภาวะแทรกซ้อนของ RAM ได้แก่ การเกิดรูที่จุดรับภาพหลังการแตก 7) และการอุดตันของแขนงหลอดเลือดแดงจอประสาทตา 10) RAM ที่หัวประสาทตามีแนวโน้มทำให้เกิดเลือดออกในแก้วตาตั้งแต่แรกเริ่ม และต้องได้รับการดูแลเป็นพิเศษ 10)
Q
เลือดออกหลายชั้นเป็นลักษณะเฉพาะของ RAM หรือไม่?
A
เลือดออกหลายชั้น (เลือดออกที่เกี่ยวข้องกับหลายชั้น เช่น ใต้จอประสาทตา ภายในจอประสาทตา และแก้วตา) เป็นลักษณะเด่นของ RAM และเป็นเบาะแสสำคัญในการวินิจฉัย 9) ในทางกลับกัน เมื่อเลือดออกเป็นบริเวณกว้าง ตัวโป่งพองเองอาจมองเห็นได้ยาก ดังนั้นการประเมินเสริมด้วย IA, OCT และ OCTA จึงจำเป็นสำหรับการวินิจฉัย 3)
ปัจจัยเสี่ยงหลายประการที่ส่งเสริมการอ่อนแอของผนังหลอดเลือดมีส่วนเกี่ยวข้องในการเกิด RAM พบได้บ่อยในผู้สูงอายุที่มีประวัติความดันโลหิตสูงและหลอดเลือดแดงแข็ง เชื่อว่าการสูญเสียชั้นกล้ามเนื้อของผนังหลอดเลือดและการเกิดพังผืดคอลลาเจนในชั้นกลางทำให้ความยืดหยุ่นลดลงและเกิดการขยายตัวเนื่องจากแรงดันในรูหลอดเลือด 1, 9)
ปัจจัยเสี่ยงหลัก
ความดันโลหิตสูง : ปัจจัยเสี่ยงที่ใหญ่ที่สุด พบร่วมในผู้ป่วย 51–75% ความดันโลหิตสูงอย่างต่อเนื่องส่งเสริมการเสื่อมแบบไฮยาลินและหลอดเลือดแดงแข็งของผนังหลอดเลือด 9)
หลอดเลือดแดงแข็ง : ผนังหลอดเลือดอ่อนแอลงเนื่องจากการเสื่อมแบบไฮยาลินและการเกิดคอลลาเจน ความเสียหายของผนังหลอดเลือดระยะยาวเป็นพื้นฐานของการขยายตัว 1, 9)
อายุที่มากขึ้น : มักเกิดในผู้ที่มีอายุมากกว่า 60 ปี การอ่อนแอของผนังหลอดเลือดตามอายุเป็นปัจจัยพื้นหลัง
เพศหญิง : ผู้หญิงคิดเป็น 70–78% ของผู้ป่วย กลไกโดยละเอียดของความแตกต่างทางเพศไม่เป็นที่ทราบ 9)
ปัจจัยเสี่ยงอื่นๆ
ภาวะไขมันในเลือดผิดปกติ : เร่งการดำเนินของหลอดเลือดแดงแข็งและทำให้ความเสียหายของผนังหลอดเลือดแย่ลง 1, 3)
โรคหัวใจและหลอดเลือด : มีรายงานความสัมพันธ์กับโรคหลอดเลือดหัวใจและโป่งพองของเอออร์ตา RAM อาจเกิดขึ้นเป็นส่วนหนึ่งของโรคหลอดเลือดทั่วร่างกาย 9)
กลุ่มอาการลินช์ : มีการเสนอความเป็นไปได้ของความซับซ้อนของเครือข่ายหลอดเลือดเนื่องจากการกลายพันธุ์ของยีนซ่อมแซมดีเอ็นเอ นี่เป็นรายงานแรกที่เกี่ยวข้องกับ RAM 1)
การทำวัลซัลวา : การเปลี่ยนแปลงความดันโลหิตอย่างฉับพลันสามารถกระตุ้นให้ RAM แตกได้ มีรายงานการทำงานหนัก การไอ และการเบ่งขณะถ่ายอุจจาระเป็นตัวกระตุ้น 9)
มาตรการป้องกันที่สำคัญที่สุดสำหรับโป่งพองของหลอดเลือดแดงจอประสาทตา ที่ได้มาคือการควบคุมความดันโลหิตสูงอย่างเคร่งครัด โปรดวัดความดันโลหิตอย่างสม่ำเสมอและดูแลทางการแพทย์อย่างต่อเนื่อง การรักษาภาวะไขมันในเลือดผิดปกติและการเลิกบุหรี่ก็มีประโยชน์ต่อการปกป้องหลอดเลือด หากการมองเห็น ลดลงอย่างกะทันหันหรือมีความผิดปกติของลานสายตา ให้ไปพบจักษุแพทย์ทันที
การถ่ายภาพหลายรูปแบบเป็นสิ่งจำเป็นสำหรับการวินิจฉัย RAM ที่แม่นยำ 3) โดยเฉพาะอย่างยิ่งในกรณีที่มีเลือดออกมาก การระบุตัวโป่งพองเองอาจทำได้ยากด้วยการตรวจฟลูออเรสซีน แองจิโอกราฟีเพียงอย่างเดียว จึงจำเป็นต้องรวมการตรวจหลายอย่างเข้าด้วยกัน
การวินิจฉัยแยกโรคที่สำคัญที่สุดคือจอประสาทตา เสื่อมตามอายุ รองลงมาคือหลอดเลือดดำจอประสาทตาสาขาอุดตัน (BRVO ) จอประสาทตาเสื่อมจากเบาหวาน และโรค Coats การตรวจดูจอตา การทำฟลูออเรสซีน แองจิโอกราฟี (FA ) และอินโดไซยานีนกรีนแองจิโอกราฟี (IA) เพื่อยืนยันรอยโรคคล้ายโป่งพองตามหลอดเลือดแดงจอประสาทตา หาก OCT ไม่พบการยกตัวของเยื่อบุผิวรงควัตถุจอตา (RPE ) โอกาสเป็นจอประสาทตา เสื่อมชนิดเปียกตามอายุมีน้อย
การตรวจ ผลการตรวจหลัก ข้อบ่งชี้/ข้อดี FA การเรืองแสงเกินแบบโป่งพองและการรั่ว วิธีมาตรฐานในการวินิจฉัย IA การเห็นโป่งพองใต้เลือดออก มีประโยชน์โดยเฉพาะในกรณีเลือดออก OCT การสะท้อนสูงแบบกลมและบวมน้ำ การวัดปริมาณโครงสร้างชั้นจอตา
ฟลูออเรสซีน แองจิโอกราฟี (FA )RAM และในระยะปลายจะเห็นการรั่วและการย้อมเนื้อเยื่อ หากการเรืองแสงเกินจากการรั่วของฟลูออเรสซีน หรือการย้อมเนื้อเยื่อรุนแรง แสดงว่าผนังหลอดเลือดของโป่งพองมีการซึมผ่านเพิ่มขึ้นและมีการดำเนินโรค มีประโยชน์ในการประเมินการดำเนินโรค และเป็นวิธีมาตรฐานในการวินิจฉัย
อินโดไซยานีนกรีนแองจิโอกราฟี (IA) : ในกรณีที่มีเลือดออกมาก IA จะดีกว่า FA ในการตรวจหา RAM 3) เนื่องจากการรั่วของสีเขียวจากโป่งพองน้อยกว่าฟลูออเรสซีน การเรืองแสงเกินใน IA จึงบ่งชี้ถึงการดำเนินโรคที่สูงกว่า
การตรวจด้วยเครื่อง Optical Coherence Tomography (OCT ) : แสดงภาพ RAM เป็นโครงสร้างทรงกลมสะท้อนแสงสูงในจอประสาทตา ชั้นใน สามารถยืนยันและวัดปริมาณจอประสาทตา บวมน้ำและจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา และยังมีประโยชน์ในการจำแนกตำแหน่งของเลือดออก (ก่อนจอประสาทตา หรือใต้จอประสาทตา )
การตรวจด้วยเครื่อง Optical Coherence Tomography Angiography (OCTA ) : แสดงสัญญาณการไหลเวียนเลือดแบบไม่รุกราน สามารถมองเห็นช่องทางภายในผนังหลอดเลือดที่เกิดจากการเปลี่ยนแปลงคล้ายการฉีกขาดของผนังหลอดเลือด 8) .
การตรวจด้วยเครื่อง Laser Speckle Flowgraphy (LSFG) : วิธีการประเมินการไหลเวียนเลือดเชิงปริมาณแบบไม่รุกราน ค่า MBR (Mean Blur Rate) สัมพันธ์กับการถดถอยของ RAM และสามารถใช้ติดตามผลการรักษา 5) .
การถ่ายภาพด้วยแสงอินฟราเรดใกล้ (NIR-R) : มีรายงานผู้ป่วยที่ตรวจพบผนังหลอดเลือดหนาตัวแบบ cuff ก่อนเริ่มมีอาการ 3 ปี แสดงถึงศักยภาพในการเป็นเครื่องมือตรวจพบตั้งแต่ระยะแรก 6) .
การตรวจอัลตราซาวนด์แบบ B-mode : ใช้เมื่อมีเลือดออกในน้ำวุ้นตา ทำให้ไม่สามารถมองเห็นจอประสาทตา ได้ 7, 10) ช่วยประเมินรอยโรคภายในลูกตาอย่างคร่าวๆ
แนวทางการรักษา RAM ขึ้นอยู่กับชนิดย่อย ผลกระทบต่อจอประสาทตา ส่วนกลาง และแนวโน้มการหายเอง แม้จะมีแนวโน้มการหายเอง แต่ระดับความผิดปกติทางการมองเห็น และการฟื้นตัวแตกต่างกันไปตามระดับของสารน้ำรั่วหรือเลือดออกที่คงอยู่บริเวณจอประสาทตา ส่วนกลาง
แนวทางการรักษาเป็นขั้นตอน :
มีสารน้ำรั่ว/เลือดออก → ขั้นแรก จ่ายยารับประทาน (carbazochrome)
สารน้ำรั่วไปยังจอประสาทตา ส่วนกลางอย่างต่อเนื่อง ไม่มีแนวโน้มหายเอง → การจี้ด้วยเลเซอร์ (จี้โป่งพองของหลอดเลือด)
เลือดออกใต้จอประสาทตา ถึงจอประสาทตา ส่วนกลาง (ภายใน 2 สัปดาห์หลังเริ่มมีอาการ ยังไม่เป็นก้อน) → การฉีดแก๊สเข้าในน้ำวุ้นตา (ย้ายก้อนเลือด)
เลือดออกก่อนจอประสาทตา (เลือดออกใต้เยื่อ ILM ) ถึงจอประสาทตา ส่วนกลาง → การผ่าตัดน้ำวุ้นตา (ร่วมกับการลอกเยื่อ ILM )
เลือดออกในน้ำวุ้นตา ที่ไม่หาย → การผ่าตัดน้ำวุ้นตา
การรักษาแบบประคับประคอง
การสังเกตอาการ : เนื่องจากมีแนวโน้มหายเอง จึงเหมาะสำหรับกรณีที่ไม่มีอาการหรือไม่เกี่ยวข้องกับจอประสาทตา ส่วนกลาง ติดตามผลด้วยการตรวจจอประสาทตา เป็นระยะ
การรักษาด้วยยา : ใช้ carbazochrome (Adona tablet 30 มก.) 3 เม็ด แบ่งรับประทาน 3 ครั้ง เป็นการรักษาเสริมเพื่อยับยั้งการเพิ่มการซึมผ่านของหลอดเลือดและห้ามเลือด
การจัดการปัจจัยเสี่ยง : การควบคุมความดันโลหิตและไขมันอย่างเคร่งครัดเป็นสิ่งจำเป็นเพื่อป้องกันการกลับเป็นซ้ำและควบคุมโรค
การรักษาแบบรุกราน
การจี้ด้วยเลเซอร์ : มีเป้าหมายเพื่อส่งเสริมการสมานแผลของผนังโป่งพองที่มีการซึมผ่านเพิ่มขึ้นหรือแตก ทำโดยการจี้ผิวของโป่งพองโดยไม่ทำให้หลอดเลือดแดงอุดตัน ไม่จำเป็นต้องยิงซ้ำจนกว่าโป่งพองทั้งหมดจะกลายเป็นสีขาวเทา แนวทาง: ขนาดจุด 300-500 ไมครอน ระยะเวลา 0.2-0.3 วินาที กำลัง 120 มิลลิวัตต์ ภาวะแทรกซ้อนรวมถึงความเสี่ยงต่อการอุดตันของหลอดเลือดแดง
การฉีดยาเข้าแก้วตาเพื่อต้าน VEGF : ใช้สำหรับ RAM ชนิดมีน้ำเหลือง渗出 ไม่ครอบคลุมโดยประกันสุขภาพในญี่ปุ่น 2, 3, 4)
การผ่าตัดน้ำวุ้นตา เยื่อจำกัดชั้นใน และชั้นใยประสาท จะทำการผ่าตัดน้ำวุ้นตา ร่วมกับการลอกเยื่อจำกัดชั้นใน ภาวะเลือดออกในน้ำวุ้นตา ที่ไม่หายก็เป็นข้อบ่งชี้ในการผ่าตัดน้ำวุ้นตา
การจี้ทางอ้อม : เทคนิคการจี้จอประสาทตา รอบๆ โป่งพองเพื่อเบี่ยงการรั่วออกจากจุดรับภาพ มักใช้ร่วมกับการจี้โดยตรง
การรักษาแบบผสมผสานเลเซอร์ร่วมกับยาต้าน VEGF : ในการศึกษา 3 ราย ความหนาจอประสาทตา ส่วนโฟเวียเฉลี่ย (CRT) ลดลง 275.7 ไมครอน และการมองเห็น ดีขึ้น 0.55 logMAR 4)
เลเซอร์ Nd:YAG : ใช้เพื่อระบายเลือดใต้เยื่อจำกัดชั้นใน แนะนำให้ทำเร็ว 9)
การฉีดแก๊สเข้าแก้วตา (การย้ายก้อนเลือด) : ข้อบ่งชี้ภายใน 2 สัปดาห์หลังจากมีเลือดออกใต้จอประสาทตา ที่จุดรับภาพ หากเลือดมีการจัดตัวแล้วจะไม่เหมาะสม ฉีด SF6 หรือ C3F8 0.2-0.8 มล. ผู้ป่วยต้องนอนคว่ำ 1-2 สัปดาห์หลังผ่าตัด การใช้ร่วมกับ tPA อาจเพิ่มประสิทธิภาพในการย้ายก้อนเลือดใต้จุดรับภาพ
เลเซอร์ระดับต่ำกว่าเกณฑ์ 9)
ภาวะแทรกซ้อนของการจี้ด้วยเลเซอร์: การจี้โดยตรงมีความเสี่ยงต่อการอุดตันของหลอดเลือดแดง การดึงรั้งจอประสาทตา และการเพิ่มขึ้นของน้ำเหลือง渗出
RAM ที่เต้นเป็นจังหวะมีความเสี่ยงสูงต่อการแตก การจี้โดยตรงต้องพิจารณาอย่างรอบคอบในตาที่ยังไม่มีการหลุดของน้ำวุ้นตา ส่วนหลัง ต้องระวังความเสี่ยงต่อการฉีกขาดและจอประสาทตา หลุดจากการฉีดแก๊ส
อธิบายให้ผู้ป่วยทราบว่าการรักษาด้วย anti-VEGF ไม่ครอบคลุมโดยประกันในญี่ปุ่น 2)
Q
สามารถหายได้เองหรือไม่?
A
RAM มีแนวโน้มที่จะหายได้เอง และในชนิดไม่มีอาการ หลายกรณีดีขึ้นเพียงแค่สังเกตอาการ อย่างไรก็ตาม หากมีเลือดออกหรือสารน้ำรั่วไปถึงจอประสาทตา ส่วนกลาง จะส่งผลต่อพยากรณ์การมองเห็น ดังนั้นจึงควรพิจารณาการรักษาเชิงรุก การเลือกระหว่างการดำเนินโรคตามธรรมชาติหรือการรักษาขึ้นอยู่กับชนิดของโรค ความรุนแรงของโรค และประวัติผู้ป่วย
แกนหลักของพยาธิสรีรวิทยาของ RAM คือการเสื่อมของผนังหลอดเลือดและความดันในช่องหลอดเลือดที่เพิ่มขึ้น ความอ่อนแอของผนังหลอดเลือดจากความดันโลหิตสูงและหลอดเลือดแดงแข็งเป็นพื้นฐาน ทำให้เกิดการรั่วซึมจากการซึมผ่านของผนังหลอดเลือดแดงที่เพิ่มขึ้น และเลือดออกจากการแตก ส่งผลให้การทำงานของการมองเห็น บกพร่อง
กระบวนการเสื่อมของผนังหลอดเลือด : ความดันโลหิตสูงทำให้เกิดการเสื่อมแบบไฮยาลินและหลอดเลือดแดงแข็ง ทำลายชั้นกล้ามเนื้อของผนังหลอดเลือด และเกิดพังผืดของคอลลาเจนในชั้นกลาง 9) ผลที่ตามมา ความยืดหยุ่นของผนังหลอดเลือดลดลง ความต้านทานต่อความดันในช่องหลอดเลือดหายไป และเกิดการขยายเฉพาะที่ 1, 9)
สมมติฐานของ Gass : หลอดเลือดอุดตันจากคราบไขมันทำลายผนังหลอดเลือด ทำให้เกิดภาวะขาดเลือดเฉพาะที่ ส่งผลให้การแสดงออกของ VEGF เพิ่มขึ้น เป็นผลให้การซึมผ่านที่เพิ่มขึ้นและการขยายตัวของหลอดเลือดถูกเร่ง 2) VEGF ทำให้เกิดการขยายตัวของหลอดเลือดแดงและการซึมผ่านที่เพิ่มขึ้นผ่านการผลิต NO จากเซลล์บุผนังหลอดเลือด และมีส่วนร่วมในพยาธิสรีรวิทยาของ RAM ชนิดมีน้ำรั่ว 3)
การเปลี่ยนแปลงคล้ายการฉีกขาด : ผ่านการสังเกตอย่างละเอียดโดยใช้กล้องตรวจตาปรับแสงได้ (AO SLO), OCT และ OCTA มีรายงานกรณีที่เกิดรอยแตก (crack) ในผนังหลอดเลือดและเกิดช่องทางภายในผนัง 8) จากช่องทางภายในผนังนี้ อาจเกิด RAM ใหม่ในตำแหน่งที่อยู่ติดกัน
กลไกการแตก : การแตกเกิดขึ้นเมื่อความดันในช่องหลอดเลือดเกินขีดจำกัดของผนังหลอดเลือดที่อ่อนแอ 9) ความดันโลหิตที่เพิ่มขึ้นอย่างกะทันหันจากท่าทาง Valsalva (การไอ การทำงานหนัก การเบ่งขณะถ่ายอุจจาระ) อาจเป็นปัจจัยกระตุ้นให้เกิดการแตก 9)
Meng Y และคณะได้ทบทวนวรรณกรรมกรณี RAM แตกที่เกิดจากท่าทาง Valsalva และอภิปรายกลไกการแตกของผนังหลอดเลือดที่อ่อนแอจากความดันหลอดเลือดดำและหลอดเลือดแดงที่เพิ่มขึ้นอย่างรวดเร็วเนื่องจากความดันในช่องท้องที่เพิ่มขึ้นอย่างกะทันหัน 9)
การสลายตัวของสิ่งกีดขวางเลือด-จอประสาทตา : ใน RAM ชนิดมีน้ำรั่ว ความเสียหายต่อสิ่งกีดขวางเลือด-จอประสาทตา เป็นพื้นฐานของจอประสาทตา บวมน้ำและสารแข็ง 15)
ลักษณะของ RAM ที่หัวประสาทตา : หลอดเลือดแดงใกล้จานประสาทตา มีเส้นผ่านศูนย์กลางใหญ่และความเร็วการไหลของเลือดสูง ดังนั้น ความเค้นของผนังจึงมาก ทำให้มีแนวโน้มที่จะมีเลือดออกในน้ำวุ้นตา ตั้งแต่แรก 10)
เนื้อหาต่อไปนี้ส่วนใหญ่เป็นความรู้ในขั้นการวิจัยหรือระดับรายงานผู้ป่วย และไม่ใช่การรักษามาตรฐานที่ใช้กับผู้ป่วยทุกราย เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต สำหรับการรักษาจริง โปรดปรึกษาแพทย์ผู้รักษาของคุณเสมอ
การวิเคราะห์โครงสร้างจุลภาคด้วยกล้องตรวจตาแบบปรับแสงได้ (AO SLO) : การสังเกตอย่างละเอียดด้วย AO SLO ทำให้เห็นภาพการหายไปของการเต้นเป็นจังหวะ กระบวนการเกิดลิ่มเลือด และรอยแตกในผนังหลอดเลือดภายใน RAM 8) ซึ่งเผยให้เห็นภาวะทางพยาธิวิทยาใหม่คือการเปลี่ยนแปลงคล้ายการฉีกขาดของผนังหลอดเลือด ทำให้เข้าใจกลไกการเกิดโรคได้ลึกซึ้งยิ่งขึ้น
การประเมินตามเวลาด้วย Laser Speckle Flowgraphy (LSFG) : มีรายงานว่า Mean Blur Rate (MBR) ลดลงอย่างมีนัยสำคัญจาก 6.8 AU เป็น 1.1 AU เมื่อ RAM ยุบตัว 5) การติดตามการไหลเวียนเลือดแบบไม่รุกรานด้วย LSFG เป็นเครื่องมือที่มีแนวโน้มดีสำหรับการประเมินประสิทธิภาพการรักษาอย่างเป็นกลาง
Hanazaki H และคณะ แสดงให้เห็นว่าการประเมินการไหลเวียนเลือดของตาแบบตามเวลาด้วย LSFG ใน RAM ที่ได้รับการรักษาพบความสัมพันธ์ระหว่างการลดลงของ MBR กับการยุบตัวของ RAM 5)
การตรวจพบตั้งแต่เนิ่นๆ ด้วยการถ่ายภาพสะท้อนแสงอินฟราเรดใกล้ (NIR-R) : มีรายงานกรณีที่ตรวจพบผนังหลอดเลือดหนาตัวเป็นรูปปลอกแขนในภาพ NIR-R สามปีก่อนที่ RAM จะแสดงอาการทางคลินิก 6) สิ่งนี้มีศักยภาพเป็นปัจจัยทำนายในผู้ป่วยความดันโลหิตสูง และคาดว่าจะนำไปประยุกต์ใช้เป็นเครื่องมือคัดกรองตั้งแต่เนิ่นๆ
ประสิทธิภาพของการรักษาแบบผสมผสานเลเซอร์ร่วมกับสารต้าน VEGF : ในชุดการศึกษา 3 ราย การรักษาแบบผสมผสานระหว่างการจี้เลเซอร์แบบโฟกัสและการฉีดเบวาซิซูแมบ เข้าแก้วตา ทำให้ค่า CRT เฉลี่ยลดลง 275.7 ไมครอน และการมองเห็น ดีขึ้น 0.55 logMAR 4) ซึ่งบ่งชี้ถึงฤทธิ์เสริมกันระหว่างการทำให้หลอดเลือดคงที่ด้วยสารต้าน VEGF และการซ่อมแซมผนังด้วยเลเซอร์ จึงจำเป็นต้องมีการทดลองขนาดใหญ่ในอนาคต
เลเซอร์ระดับต่ำกว่าเกณฑ์ จอประสาทตา แบบไม่ถึงตายผ่านโปรตีนฮีทช็อคเชื่อว่าให้ผลเท่าเทียมกันโดยมีภาวะแทรกซ้อนน้อยกว่า 9)
ความสัมพันธ์ระหว่าง Lynch syndrome กับ RAM : มีรายงานครั้งแรกของการเกิด RAM ในผู้ป่วย Lynch syndrome ที่มีการกลายพันธุ์ของยีนซ่อมแซม DNA 1) การกลายพันธุ์ของยีนซ่อมแซม DNA อาจทำให้เครือข่ายหลอดเลือดซับซ้อนขึ้นและเพิ่มการแสดงออกของ VEGF-A ซึ่งมีส่วนทำให้เกิด RAM
ความจำเป็นของแนวทางการรักษา : ด้วยความหลากหลายของวิธีการรักษา จึงจำเป็นต้องมีการกำหนดแนวทางปฏิบัติทางคลินิกตามหลักฐานเชิงประจักษ์ 9)
การสะสมกรณีเลือดออกหลายชั้นและการประเมินภาพแบบไม่รุกราน : ใน RAM ที่แตก มีรายงานกรณีเลือดออกหลายชั้น (ใต้จอประสาทตา ภายในจอประสาทตา แก้วตา) 11) ในกรณีที่มีเลือดออกใต้แก้วตา การพิจารณาข้อบ่งชี้สำหรับเลเซอร์ Nd:YAG หรือการตัดแก้วตาเป็นสิ่งสำคัญ 12) การถ่ายวิดีโอสะท้อนแสงอินฟราเรดใกล้ใช้ประเมินการเต้นเป็นจังหวะของ RAM ในขณะที่ OCTA ใช้ประเมินการไหลเวียนเลือดภายในรอยโรคแบบไม่รุกราน 13, 14)
Q
การรักษาด้วยสารต้าน VEGF มีประสิทธิภาพสำหรับ RAM หรือไม่?
A
รายงานผู้ป่วยและชุดข้อมูลขนาดเล็กได้รายงานประสิทธิภาพของการฉีดยา anti-VEGF เข้าไปในน้ำวุ้นตา ใน RAM ชนิด渗出 2, 3, 4) การรักษาร่วมกับเลเซอร์ให้ผลลัพธ์ที่มีแนวโน้มดี 4) อย่างไรก็ตาม ในญี่ปุ่นยังไม่ครอบคลุมโดยประกัน 2) และยังไม่มีการทดลองแบบสุ่มขนาดใหญ่ จำเป็นต้องปรึกษาแพทย์ผู้ดูแลอย่างเพียงพอก่อนการใช้
Sood S, Friedman S. Retinal Arterial Macroaneurysm in a Patient With Lynch Syndrome. J VitreoRetinal Diseases. 2023;7(3):239-241.
Takamiya M. The Management of Two Cases with Retinal Arterial Macroaneurysm by Anti-Vascular Endothelial Growth Factor. Case Rep Ophthalmol. 2024;15:483-489.
Balas M, Mandell MA, Arjmand P. Juxtafoveal Retinal Arterial Macroaneurysm Diagnosed on Ancillary Imaging. J VitreoRetinal Diseases. 2024;8(5):609-613.
Jemelian A, Enghelberg M. Outcomes of Combined Therapy With Focal Laser and Intravitreal Bevacizumab for Retinal Arterial Macroaneurysm: A Case Series. Cureus. 2025;17(3):e81382.
Hanazaki H, Yokota H, Aso H, et al. Evaluation of ocular blood flow over time in a treated retinal arterial macroaneurysm using laser speckle flowgraphy. Am J Ophthalmol Case Rep. 2021;21:101022.
Zienkiewicz A, Francone A, Cirillo MP, et al. Near-Infrared Reflectance Imaging to Detect an Incipient Retinal Arterial Macroaneurysm. Case Rep Ophthalmol. 2021;12:150-153.
Takahashi S, Nishida K, Sakaguchi H, et al. A Case of Idiopathic Dense Vitreous Hemorrhage: Suspected Rupture of a Large Retinal Arterial Macroaneurysm on the Optic Disc. Case Rep Ophthalmol. 2021;12:634-639.
Ishikura M, Muraoka Y, Kadomoto S, et al. Retinal arterial macroaneurysm rupture caused by dissection-like change in the vessel wall. Am J Ophthalmol Case Rep. 2022;25:101346.
Meng Y, Xu Y, Li L, et al. Retinal arterial macroaneurysm rupture by Valsalva maneuver: a case report and literature review. BMC Ophthalmology. 2022;22:461.
Sasajima H, Zako M, Aoyagi A, et al. Acute Onset of Dense Vitreous Hemorrhage Associated with Retinal Arterial Macroaneurysm on the Optic Disc. Case Rep Ophthalmol. 2022;13:763-769.
Temkar S, Stephen M, Agarwal D, et al. Multilayered retinal bleed in ruptured retinal artery macroaneurysm. BMJ Case Rep. 2023;16:e254669.
Mahjoub A, Zaafrane N, Ben Youssef C, et al. Retinal artery macroaneurysm complicated with subhyaloid hemorrhage: two case reports. Ann Med Surg. 2023;85:1130-1136.
Abdul-Rahman A, Morgan W, Yu DY. Near infra-red reflectance videography in the evaluation of retinal artery macroaneurysm pulsatility. Am J Ophthalmol Case Reports. 2022;27:101664.
Mohd Lokman M, Catherine Bastion ML, Che Hamzah J. Objective assessment of retinal artery macroaneurysm with optical coherence tomography angiography. Cureus. 2022;14(12):e32328.
O’Leary F, Campbell M. The blood-retina barrier in health and disease. FEB S J. 2021;290:878-891.