ภาวะหลอดเลือดดำจอประสาทตาสาขาอุดตัน เป็นโรคหลอดเลือดจอประสาทตา ที่พบบ่อยเป็นอันดับสองรองจากจอประสาทตาเสื่อมจากเบาหวาน โดยมีความชุกประมาณ 2.0% ในผู้ที่มีอายุ 40 ปีขึ้นไป
เกิดจากหลอดเลือดแดงที่แข็งตัวกดทับหลอดเลือดดำบริเวณจุดไขว้ของหลอดเลือดแดงและดำ ทำให้เกิดลิ่มเลือด ตำแหน่งขมับด้านบนพบบ่อยที่สุด (58-66%)
ภาวะจอประสาทตา บวมน้ำ ( macular edema ) พบร่วมในมากกว่าครึ่งหนึ่งของกรณี และเป็นสาเหตุสำคัญที่สุดของการมองเห็น ลดลง
การฉีดยา anti-VEGF เข้าแก้วตาเป็นทางเลือกแรกในการรักษาภาวะจอประสาทตา บวมน้ำ โดยใช้ ranibizumab, aflibercept และ faricimab
แบ่งเป็นชนิดไม่ขาดเลือด (ประมาณ 80%) และชนิดขาดเลือด โดยชนิดขาดเลือดมีความเสี่ยงสูงต่อการเกิดเส้นเลือดใหม่และเลือดออกในน้ำวุ้นตา
ความดันโลหิตสูงเป็นปัจจัยเสี่ยงที่สำคัญที่สุด โดยมีรายงานว่า 48% ของผู้ป่วย RVO เกิดจากความดันโลหิตสูง
มีความเสี่ยงเพิ่มขึ้นของเหตุการณ์โรคหัวใจและหลอดเลือดในผู้ป่วย BRVO ดังนั้นการจัดการทางระบบจึงมีความสำคัญ
โรคหลอดเลือดดำจอประสาทตาสาขาอุดตัน (Branch Retinal Vein Occlusion; BRVO ) เป็นโรคหลอดเลือดที่หลอดเลือดดำอุดตันบริเวณจุดไขว้ของหลอดเลือดแดงและดำในจอประสาทตา ทำให้เกิดเลือดออกในจอประสาทตา จอประสาทตา บวมน้ำ และการไหลเวียนเลือดฝอยไม่เพียงพอในบริเวณที่ได้รับผลกระทบ เป็นชนิดที่พบบ่อยที่สุดของโรคหลอดเลือดดำจอประสาทตาอุดตัน โดยพบบ่อยกว่าหลอดเลือดดำจอประสาทตาส่วนกลางอุดตัน (CRVO ) ประมาณ 5 เท่า 1)
ความชุกทั่วโลกในปี 2015 อยู่ที่ประมาณ 0.77% โดยประมาณการว่ามีผู้ป่วย 28 ล้านคนอายุ 30-89 ปี 1) หากจำกัดเฉพาะอายุ 40 ปีขึ้นไป ความชุกอยู่ที่ประมาณ 2.0% ในญี่ปุ่น การศึกษาฮิยามะรายงานอุบัติการณ์สะสม 9 ปีและปัจจัยเสี่ยง 2) การศึกษา Beaver Dam Eye รายงานอุบัติการณ์สะสม 15 ปีที่ 2.3% สำหรับ RVO ทั้งหมด 1) ความชุกเพิ่มขึ้นอย่างมีนัยสำคัญตามอายุ โดยสูงขึ้นหลังจากอายุ 60 ปี 4) อุบัติการณ์ในเอเชียตะวันออกรายงานว่าเทียบเท่ากับสหรัฐอเมริกา โดยอาจสูงกว่าเล็กน้อยในเกาหลี 12)
ตำแหน่งที่อุดตันบ่อยที่สุดคือขมับด้านบน (58-66%) รองลงมาคือขมับด้านล่าง (22-43%) และจมูก (12.9%) 3) โรคนี้จำแนกตามตำแหน่งและขอบเขตของการอุดตันดังนี้:
การอุดตันของสาขาหลักของหลอดเลือดดำจอประสาทตา : การอุดตันของสาขาที่ 1-3 พื้นที่จอประสาทตา กว้างได้รับความเสียหายการอุดตันของหลอดเลือดดำจอประสาทตา บริเวณจุดรับภาพ : การอุดตันของหลอดเลือดขนาดเล็กที่เลี้ยงจุดรับภาพ ส่งผลโดยตรงต่อการมองเห็น อย่างมากhemiRVO (การอุดตันของหลอดเลือดดำจอประสาทตา ครึ่งซีก) : การอุดตันที่ขั้วประสาทตา ทำให้การระบายของจอประสาทตา ครึ่งหนึ่งบกพร่อง ทางคลินิกดำเนินโรคใกล้เคียงกับ CRVO มากกว่า BRVO 12)
นอกจากนี้ยังจำแนกเป็น 2 ชนิดตามระดับของภาวะขาดเลือด
ชนิดไม่ขาดเลือด : บริเวณที่ไม่มีการไหลเวียนเลือด น้อยกว่า 5 เส้นผ่านศูนย์กลางจานประสาทตา (DD) จากการตรวจฟลูออเรสซีน แองจิโอกราฟี (FA ) คิดเป็นประมาณ 80% ของทั้งหมดชนิดขาดเลือด : บริเวณที่ไม่มีการไหลเวียนเลือด ≥5 DD (≥10 DD ตามเกณฑ์ CVOS) มีความเสี่ยงสูงต่อการสร้างเส้นเลือดใหม่และเลือดออกในน้ำวุ้นตา 15-20% ของชนิดไม่ขาดเลือดจะเปลี่ยนเป็นชนิดขาดเลือดในระหว่างดำเนินโรค 3)
Q
หากเกิดในตาข้างเดียว ตาอีกข้างมีแนวโน้มที่จะเกิดโรคได้ง่ายหรือไม่?
A
ประมาณ 10% ของผู้ป่วย BRVO จะเกิด RVO (BRVO หรือ CRVO ) ในตาอีกข้างภายใน 3 ปี 3) เนื่องจากปัจจัยเสี่ยงทางระบบ เช่น ความดันโลหิตสูงและภาวะไขมันในเลือดผิดปกติมักร่วมด้วย การตรวจอวัยวะภายในตาอีกข้างเป็นประจำและการจัดการความเสี่ยงทางระบบจึงมีความสำคัญ
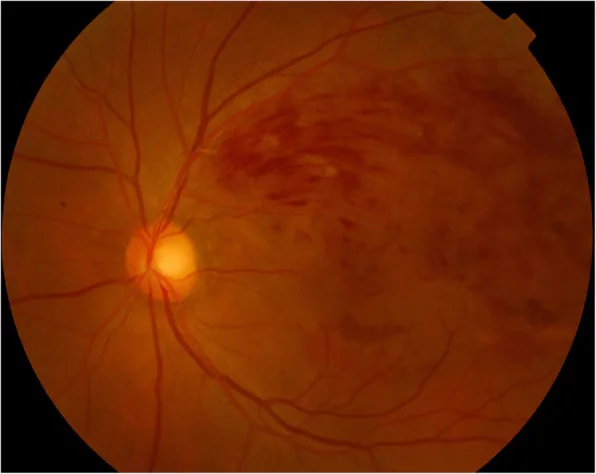
ภาพถ่ายจอประสาทตาของภาวะหลอดเลือดดำจอประสาทตาสาขาอุดตัน พบเลือดออกและจุดขาวในจอประสาทตาส่วนขมับด้านบน Lee JH, et al. Rapid progression of cataract to mature stage after intravitreal dexamethasone implant injection: a case report. BMC Ophthalmol. 2019. Figure 1. PM
CI D: PMC6318997. License: CC BY.
ในภาพถ่าย
จอประสาทตา จะเห็นเลือดออกใน
จอประสาทตา เป็นรูปร่างพัดและรอยโรคสีเหลืองขาวบริเวณขมับด้านบน สามารถยืนยันผลการตรวจที่บ่งชี้ถึงความผิดปกติของการไหลเวียนของหลอดเลือดดำสาขา ซึ่งแสดงภาพทางคลินิกของภาวะ
หลอดเลือดดำจอประสาทตาสาขาอุดตัน อาการแตกต่างกันไปตามตำแหน่งที่อุดตัน
การมองเห็น ลดลงเฉียบพลันแบบไม่เจ็บปวดข้อบกพร่องของลานสายตา : จุดบอดรูปพัดที่สอดคล้องกับบริเวณที่อุดตันภาพบิดเบี้ยว จอประสาทตา บวมน้ำจุดลอย : เกิดขึ้นเมื่อมีเลือดออกในน้ำวุ้นตา ร่วมด้วยไม่มีอาการ : ในกรณีอุดตันบริเวณรอบนอก ผู้ป่วยอาจไม่มีอาการและตรวจพบโดยบังเอิญ
ในระยะเฉียบพลัน จะพบลักษณะเฉพาะของจอประสาทตา ที่สอดคล้องกับบริเวณที่มีการอุดตัน
เลือดออกในจอประสาทตา รูปพัด (ลิ่ม) : การกระจายตัวสอดคล้องกับบริเวณหลอดเลือดดำที่อุดตัน ลักษณะเลือดออกเป็นรูปเปลวไฟ (flame-shaped hemorrhage) เป็นลักษณะเฉพาะเครื่องหมาย Bonnet : เลือดออกที่รวมตัวบริเวณจุดไขว้ของหลอดเลือดแดงและดำ มีประโยชน์ในการระบุตำแหน่งที่อุดตันจุดขาวคล้ายสำลี (CWS) : เนื้อตายของชั้นใยประสาทเนื่องจากการอุดตันของหลอดเลือดแดงเล็กก่อนเส้นเลือดฝอย เป็นตัวบ่งชี้ความผิดปกติของการไหลเวียนระดับจุลภาคในจอประสาทตา เมื่อเพิ่มขึ้น ควรประเมินระดับการขาดเลือดด้วยการตรวจ FA และพิจารณาความจำเป็นในการจี้ด้วยแสง จุดขาวแข็ง : การสะสมของไขมันในระยะเรื้อรังหลอดเลือดดำโป่งพองและคดเคี้ยว : เห็นได้ชัดทางด้านปลายของหลอดเลือดดำที่อุดตันผลการตรวจในระยะเรื้อรัง : การดูดซึมเลือดออก การสร้างทางเดินเลือดเลี้ยงเสริม (หลอดเลือดเชื่อมระหว่างหลอดเลือดดำบนและล่าง) หลอดเลือดโป่งพองขนาดเล็ก
จำเป็นสำหรับการประเมินปริมาณของจอประสาทตา บวมน้ำ
จอประสาทตา บวมน้ำชนิดถุงน้ำ (CME )จอประสาทตา เป็นรูปแบบที่พบบ่อยที่สุดของอาการบวมน้ำจอประสาทตา บวมน้ำไม่สมมาตรในแนวตั้งฉากBRVO แสดงอาการบวมน้ำที่เด่นชัดทางด้านที่อุดตันของเหลวใต้จอประสาทตา (SRF)จอประสาทตา การแตกของเยื่อจำกัดชั้นนอก (ELM) : ตัวบ่งชี้ความเสียหายของเซลล์รับแสง ปัจจัยพยากรณ์โรคทางสายตาที่ไม่ดีการขาดตอนของโซนรูปไข่ (EZ ) : ร่วมกับ ELM เป็นผลการตรวจสำคัญในการทำนายพยากรณ์การทำงานของการมองเห็น จุดสะท้อนแสงสูง ภายในจอประสาทตา
ภาวะแทรกซ้อนที่สำคัญของ BRVO คือ จอประสาทตา บวมน้ำ (macular edema) และการสร้างเส้นเลือดใหม่ (neovascularization)
จอประสาทตา บวมน้ำการมองเห็น ลดลงจาก BRVO เกิดขึ้นประมาณ 30% ของผู้ป่วย BRVO ทั้งหมด12) การสร้างเส้นเลือดใหม่ : เกิดขึ้นที่จานประสาทตา และจอประสาทตา แตกต่างจาก CRVO ซึ่งไม่ค่อยเกิดขึ้นที่ส่วนหน้าของลูกตา เมื่อเกิดการสร้างเส้นเลือดใหม่ มีรายงานว่าประมาณ 60% จะมีเลือดออกในน้ำวุ้นตา เยื่อเหนือจอประสาทตา (epiretinal membrane)BRVO และอาจเกิดร่วมกับจอประสาทตา บวมน้ำ12)
สาเหตุหลักของการมองเห็น ลดลงมีดังนี้:
สาเหตุ ระยะเวลา ความถี่ จอประสาทตา บวมน้ำเฉียบพลันถึงเรื้อรัง พบบ่อยที่สุด จอประสาทตา ขาดเลือดระยะเฉียบพลัน กรณีรุนแรง เลือดออกจากเส้นเลือดใหม่ ระยะเรื้อรัง ประมาณ 30% ของชนิดขาดเลือด
BRVO เกิดขึ้นที่จุดตัดหลอดเลือดแดง-ดำ ซึ่งหลอดเลือดแดงที่แข็งตัวจะกดทับหลอดเลือดดำ ในตำแหน่งนี้ หลอดเลือดแดงและดำถูกหุ้มด้วยเยื่อหุ้มชั้นนอกเดียวกัน (adventitia ร่วม) และการหนาตัวและแข็งตัวของผนังหลอดเลือดแดงจะกดทับหลอดเลือดดำโดยตรง สัดส่วนของหลอดเลือดแดงที่วิ่งอยู่ด้านหน้าหลอดเลือดดำ (ด้านผิว) สูงถึง 97.6-100% การกดทับทำให้รูหลอดเลือดดำตีบแคบ และเกิด Virchow’s triad (ภาวะเลือดแข็งตัวมากเกินไป การไหลเวียนเลือดผิดปกติ การบาดเจ็บของเยื่อบุผนังหลอดเลือด) นำไปสู่การเกิดลิ่มเลือด
จากการวิเคราะห์อภิมาน พบว่า 48% ของกรณี RVO เกิดจากความดันโลหิตสูง 20% จากภาวะไขมันในเลือดผิดปกติ และ 5% จากโรคเบาหวาน5)
ปัจจัยเสี่ยงหลัก
ความดันโลหิตสูง : เป็นปัจจัยเสี่ยงที่สำคัญที่สุด เพิ่มความเสี่ยงของ BRVO ผ่านภาวะหลอดเลือดแดงแข็ง5)
ภาวะไขมันในเลือดผิดปกติ : การวิเคราะห์อภิมานแสดงความสัมพันธ์ที่มีนัยสำคัญกับ BRVO 5) นอกจากนี้ยังมีรายงานว่า HDL คอเลสเตอรอลต่ำเป็นปัจจัยเสี่ยงอิสระของ RVO 12)
โรคเบาหวาน : มีส่วนทำให้เกิดโรคผ่านการบาดเจ็บของเยื่อบุผนังหลอดเลือดและภาวะเลือดแข็งตัวมากเกินไป5)
ต้อหิน ความดันลูกตา สูงทำให้เลือดดำคั่ง เพิ่มความเสี่ยง12)
ปัจจัยเสี่ยงอื่นๆ
อายุที่เพิ่มขึ้น : อุบัติการณ์เพิ่มขึ้นตามการดำเนินของภาวะหลอดเลือดแดงแข็ง
โรคอ้วนและการสูบบุหรี่ : มีส่วนเกี่ยวข้องผ่านการทำลายเยื่อบุผนังหลอดเลือดและการเพิ่มความหนืดของเลือด 5)
ภาวะเลือดแข็งตัวง่าย : แนะนำให้ตรวจคัดกรองในผู้ที่มีอายุต่ำกว่า 50 ปี กรณีเป็นสองตา และกรณีกลับเป็นซ้ำ 6)
ภาวะหยุดหายใจขณะหลับ : การศึกษาแบบกลุ่มใหญ่ในไต้หวันรายงานความสัมพันธ์กับความเสี่ยงในการเกิด RVO 7)
โรคหัวใจและหลอดเลือด : ผู้ป่วย RVO มีความเสี่ยงเพิ่มขึ้นต่อเหตุการณ์ทางหัวใจและหลอดเลือดและอัตราการเสียชีวิตโดยรวม 8) นอกจากนี้ยังมีรายงานความเสี่ยง RVO ที่เพิ่มขึ้นในโรคซึมเศร้า 12)
การควบคุมความดันโลหิตสูง ภาวะไขมันในเลือดผิดปกติ และเบาหวานอย่างเหมาะสมมีความสำคัญต่อการป้องกัน BRVO โปรดวัดความดันโลหิตอย่างสม่ำเสมอและจัดการยา การสูบบุหรี่เพิ่มความเสี่ยงต่อหลอดเลือด ดังนั้นจึงแนะนำให้เลิกสูบบุหรี่ ผู้ป่วยที่มีประวัติ BRVO ควรตรวจตาเป็นประจำเพื่อตรวจหาการเกิดในตาอีกข้างและการกลับเป็นซ้ำตั้งแต่เนิ่นๆ ผู้ป่วย RVO ยังมีความเสี่ยงสูงต่อภาวะกล้ามเนื้อหัวใจตายและโรคหลอดเลือดสมอง ดังนั้นการติดตามผลกับอายุรแพทย์เป็นประจำก็สำคัญเช่นกัน
มีรายงานกรณี BRVO หลังการฉีดวัคซีน mRNA
Sugihara และคณะ (2022) รายงาน BRVO ในชายอายุ 38 ปี 2 วันหลังฉีดวัคซีน BNT162b2 (Pfizer) 9) ค่าความคมชัดของสายตาที่ดีที่สุดที่แก้ไขแล้วดีขึ้นจาก 0.9 เป็น 1.2 หลังฉีดยา aflibercept ขนาด 2 มก. เข้าแก้วตา 2 ครั้ง
Tanaka และคณะ (2022) รายงานผู้หญิง 2 รายอายุ 50 และ 56 ปี 3 วันหลังฉีดวัคซีน mRNA 10) ทั้งสองมีประวัติใช้ยา tamoxifen ซึ่งชี้ให้เห็นถึงความเป็นไปได้ที่ความเสี่ยงลิ่มเลือดอุดตันในหลอดเลือดดำจาก tamoxifen จะซ้อนทับกับภาวะเลือดแข็งตัวง่ายหลังวัคซีน ค่าความคมชัดของสายตาดีขึ้นจาก 20/25 เป็น 20/20 หลังฉีดยา ranibizumab 3 ครั้ง
Girioni และคณะ (2023) รายงาน BRVO ในตาทั้งสองข้างในชายอายุ 50 ปี 24 ชั่วโมงหลังได้รับวัคซีนกระตุ้น mRNA-SARS-CoV-2 และบันทึกว่าเป็นรายงานแรกของ BRVO ในตาทั้งสองข้างหลังฉีดวัคซีน 11) มากกว่า 50% ของ RVO ที่เกี่ยวข้องกับวัคซีนเกิดจากวัคซีน mRNA โดยมีระยะเวลาตั้งแต่ฉีดจนถึงเริ่มมีอาการเฉลี่ย 2 วัน
กลไกที่ตั้งสมมติฐานเกี่ยวข้องกับการส่งเสริมการเกิดลิ่มเลือดและการตอบสนองต่อการอักเสบโดยโปรตีนหนาม 10, 11) แต่อุบัติการณ์พบน้อยมาก และประโยชน์ของการฉีดวัคซีนมีมากกว่าความเสี่ยงอย่างมาก
Q
การอุดตันของหลอดเลือดดำจอประสาทตาสาขาสามารถเกิดขึ้นได้หลังฉีดวัคซีนโควิด-19 หรือไม่?
A
มีรายงาน BRVO หลังฉีดวัคซีน mRNA (Pfizer, Moderna) สะสมมากขึ้น โดยมีระยะเวลาตั้งแต่ฉีดจนถึงเริ่มมีอาการเฉลี่ยประมาณ 2 วัน 11) อุบัติการณ์ต่ำมาก และประโยชน์ของการฉีดวัคซีนมีมากกว่าความเสี่ยงอย่างมาก หากคุณรู้สึกว่าสายตาลดลงอย่างกะทันหันหรือมีข้อบกพร่องของลานสายตาหลังฉีดวัคซีน แนะนำให้ไปพบจักษุแพทย์ทันที
การวินิจฉัย BRVO อาศัยการตรวจพบที่จอประสาทตา เนื่องจากมีเลือดออกในจอประสาทตา ลักษณะเป็นรูปพัดที่สอดคล้องกับบริเวณหลอดเลือดดำที่อุดตัน การวินิจฉัยจึงไม่ยาก อย่างไรก็ตาม เพื่อตัดสินใจในการรักษาและพยากรณ์โรค การตรวจอื่นๆ นอกเหนือจากการตรวจจอประสาทตา ก็มีความสำคัญ
การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : เป็นการตรวจที่จำเป็นเพื่อประเมินการไหลเวียนโลหิต แสดงให้เห็นการเติมช้าในบริเวณที่ได้รับผลกระทบ การขยายของหลอดเลือดดำ และการเพิ่มขึ้นของการซึมผ่านของหลอดเลือด ทันทีหลังจากเริ่มมีอาการ มักจะประเมินบริเวณที่หลอดเลือดฝอยอุดตันได้ยากเนื่องจากเลือดออกในจอประสาทตา ดังนั้นจึงตรวจซ้ำหลังจากเลือดถูกดูดซึม นอกจากนี้ยังมีประโยชน์มากในการแยกแยะระหว่างการไหลเวียนเลือดทางอ้อมและหลอดเลือดใหม่ คำจำกัดความของชนิดขาดเลือดตามเกณฑ์ CVOS คือบริเวณที่หลอดเลือดฝอยไม่มีการไหลเวียนเลือดตั้งแต่ 10 เท่าของเส้นผ่านศูนย์กลางของจานประสาทตา ขึ้นไป 12) การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน มุมกว้าง (wide-field FA ) ช่วยให้ประเมินบริเวณรอบนอกที่ไม่มีการไหลเวียนเลือดได้อย่างครอบคลุม แต่ข้อมูลเกี่ยวกับประโยชน์ทางคลินิกยังมีจำกัด 12) ในยุคของสารต้าน VEGF ความถี่ในการใช้ FA ลดลง แต่ก็ยังคงเป็นการตรวจที่สำคัญOCT จอประสาทตา บวมน้ำ มีประโยชน์ไม่เพียงแต่ในการวินิจฉัย แต่ยังใช้ติดตามผลการรักษา และในการทดลองทางคลินิก การตัดสินใจรักษาโดยอาศัยการวัดค่า OCT กลายเป็นกระแสหลัก 12) การลดลงของความหนาจอประสาทตา ส่วนโฟเวีย (CST) เป็นตัวบ่งชี้ผลการรักษา ควรสังเกตว่าแม้ความหนาจอประสาทตา จะลดลง แต่การมองเห็น อาจไม่ดีขึ้น ดังนั้นความหนาและการมองเห็น จึงไม่สัมพันธ์กันเสมอไป 12) OCTA (การถ่ายภาพหลอดเลือดด้วยแสงแบบคลื่นความถี่ต่ำ)FA Z แต่ยังคงมีปัญหาเรื่องสิ่งแปลกปลอมในภาพและข้อจำกัดของขอบเขตการมองเห็น 12) การตรวจด้วยคลื่นเสียงความถี่สูง : ใช้เพื่อประเมินความสัมพันธ์ระหว่างจอประสาทตา และวุ้นตา ในกรณีที่มีความขุ่นของสื่อกลาง เช่น เลือดออกในวุ้นตา 12)
แนะนำให้ตรวจคัดกรองภาวะเลือดแข็งตัวง่ายในผู้ป่วยอายุต่ำกว่า 50 ปี กรณีเป็นสองตาหรือเป็นซ้ำ 6) มีรายงานว่า 58% ของผู้ป่วย CRVO ที่เริ่มมีอาการก่อนอายุ 50 ปีตรวจพบปัจจัยเสี่ยงที่ไม่ใช่แบบดั้งเดิม การตรวจที่ทำมีดังนี้:
การขาดโปรตีน C และโปรตีน S
กลุ่มอาการแอนไทฟอสโฟไลปิด
ระดับโฮโมซิสเทอีน
การกลายพันธุ์ของแฟกเตอร์ V ไลเดน
การประเมินความดันโลหิตสูง ภาวะไขมันในเลือดผิดปกติ และเบาหวาน ดำเนินการในทุกราย เนื่องจากผู้ป่วย RVO มีความเสี่ยงสูงต่อโรคหัวใจและหลอดเลือดและโรคหลอดเลือดสมอง จึงแนะนำให้ประสานงานกับอายุรแพทย์และแพทย์ปฐมภูมิ 12)
การวินิจฉัยแยกโรคประกอบด้วยโรคดังต่อไปนี้ การแยกโรคทำได้โดยการตรวจอวัยวะรับภาพและการตรวจ FA ในกรณีที่เริ่มมีอาการตั้งแต่อายุน้อย ควรทำงานร่วมกับอายุรศาสตร์เพื่อตรวจสอบโรคพื้นฐาน
โรค จุดที่ใช้แยกโรค จอประสาทตาเสื่อมจากเบาหวาน เป็นทั้งสองข้าง มีเลือดออกแบบจุด และหลอดเลือดฝอยโป่งพองกระจาย จอประสาทตาเสื่อมจากความดันโลหิตสูง เลือดออกไม่จำกัดเฉพาะตามการกระจายของหลอดเลือดดำ จอประสาทตาเสื่อมจากโรคไต สภาพร่างกายโดยรวม การเปลี่ยนแปลงทั้งสองข้าง หลอดเลือดฝอยขยายรอบรอยบุ๋มจอตา การเปลี่ยนแปลงจำกัดเฉพาะบริเวณจุดรับภาพ จอประสาทตาเสื่อมจากรังสี ประวัติการได้รับรังสี
การรักษา BRVO แบ่งเป็นการรักษาอาการบวมน้ำที่จุดรับภาพและการรักษาหลอดเลือดใหม่ที่ผิดปกติ
การฉีดยา Anti-VEGF เข้าแก้วตาเป็นการรักษาแนวแรกสำหรับจอประสาทตา บวมน้ำจาก BRVO 12) ประสิทธิภาพได้รับการยืนยันจากการทดลองแบบสุ่มขนาดใหญ่หลายฉบับ และแนะนำให้ใช้เป็นการรักษาเริ่มต้นเนื่องจากมีอัตราส่วนความเสี่ยงต่อประโยชน์ที่ดี
การรักษาด้วย Anti-VEGF
Ranibizumab (การทดลอง BRAVO) : 0.5 มก. เดือนละครั้งนาน 6 เดือน ทำให้การมองเห็น ดีขึ้นเฉลี่ย +18.3 ตัวอักษร และ 61.1% มีการดีขึ้น ≥15 ตัวอักษร 13) การมองเห็น คงที่หลังจาก 12 เดือน (การทดลอง HORIZON: -0.7 ตัวอักษร) และการดีขึ้นคงอยู่นาน 48 เดือน (การศึกษา RETAIN: เฉลี่ย 53 เดือน ฉีด 14.8 ครั้ง จอประสาทตา บวมน้ำหายไปใน 50% ของกรณีหลังจาก ≥6 เดือนโดยไม่ต้องฉีดซ้ำ)
Aflibercept (การทดลอง VIBRANT) : 2 มก. เดือนละครั้ง ทำให้ 52.7% มีการดีขึ้น ≥15 ตัวอักษรที่สัปดาห์ที่ 24 แสดงความเหนือกว่ากลุ่มเลเซอร์กริด (26.7%) 14)
Faricimab (การทดลอง BALATON) : 6 มก. เดือนละครั้ง แสดงการดีขึ้น +16.9 ตัวอักษรที่สัปดาห์ที่ 24 โดยไม่ด้อยกว่ากลุ่ม aflibercept (+17.5 ตัวอักษร) 56.1% เทียบกับ 60.4% ดีขึ้น ≥15 ตัวอักษร อุบัติการณ์ IOI ในการทดลอง BALATON คือ 0.4% สำหรับ faricimab เทียบกับ 0% สำหรับ aflibercept 15)
Bevacizumab : ไม่ครอบคลุมโดยประกัน แต่มีประวัติการใช้ทางคลินิก ในการทดลอง SCORE2 เทียบเท่ากับ aflibercept ในด้านการมองเห็น ที่ 6 เดือนสำหรับ CRVO /HRVO 21) การทดลอง LEAVO 100 สัปดาห์รายงาน RBZ +12.5 ตัวอักษร AFL +15.1 ตัวอักษร BEV +9.8 ตัวอักษร 12)
การรักษาด้วยสเตียรอยด์
การปลูกถ่าย Dexamethasone (การทดลอง GENEVA) : ครั้งเดียว 0.7 มก. ทำให้ 41% ดีขึ้น ≥15 ตัวอักษร (ที่ 6 เดือน) 18) ผลสูงสุดที่ 90 วันและหายไปที่ 6 เดือน มีความเสี่ยงต่อต้อกระจก และความดันลูกตา สูง (≥25 มม.ปรอทใน 16%) การทดลอง COBALT: ฉีดซ้ำทุก 4 เดือนทำให้ดีขึ้น 15.3 ตัวอักษรหลังจาก 12 เดือน โดยประมาณ 70% ของผลสูงสุดเกิดขึ้น 1 สัปดาห์หลังฉีดครั้งแรก 19)
Triamcinolone (การทดลอง SCORE) : 1 มก. และ 4 มก. เปรียบเทียบกับเลเซอร์กริด การมองเห็น ดีขึ้นหลังจาก 12 เดือนเท่ากันในทุกกลุ่ม (ประมาณ 1/3 ดีขึ้น ≥15 ตัวอักษร) โดยไม่มีความเหนือกว่าของ triamcinolone ในกลุ่ม 4 มก. อุบัติการณ์ต้อกระจก สูงกว่าอย่างมีนัยสำคัญ และ triamcinolone เหมาะสำหรับผู้ป่วย BRVO บางรายเท่านั้น
ข้อบ่งใช้ : ใช้ในกรณีที่ดื้อต่อยา Anti-VEGF หรือเพื่อยืดระยะเวลาการฉีด
นอกจากการให้ยาคงที่เดือนละครั้ง (ระยะโหลด) ยังมีสูตรอื่นๆ สำหรับการให้ยา Anti-VEGF
PRN (pro re nata; ให้เมื่อจำเป็น) : การให้ซ้ำขึ้นอยู่กับผล OCT และการมองเห็น Treat-and-extend (T&E) : วิธีการขยายระยะห่างระหว่างการให้ยาเป็นรายบุคคล มีรายงานว่าผลระยะสั้นของ T&E เทียบเท่ากับ PRN ในการเปรียบเทียบ T&E กับการให้รายเดือนในการทดลอง SCORE2 พบว่า T&E ให้ผลการมองเห็น เทียบเท่าโดยฉีดน้อยกว่า 1-2 ครั้ง แต่ช่วงความเชื่อมั่นกว้าง ต้องตีความอย่างระมัดระวัง 16) ผลลัพธ์ 24 เดือนของการทดลอง BRI GHTER แสดงว่าไม่มีความแตกต่างของผลการมองเห็น ระหว่าง ranibizumab เพียงอย่างเดียวกับ ranibizumab ร่วมกับเลเซอร์ และไม่มีประโยชน์จากการเพิ่มเลเซอร์ 17) ข้อมูล 4 ปีของ RETAIN ก็ไม่พบผลของการเพิ่มเลเซอร์เช่นกัน 12)
ผู้ป่วย BRVO ประมาณครึ่งหนึ่งต้องการการรักษาด้วย anti-VEGF อย่างต่อเนื่องนานกว่า 5 ปี ตามรายงาน 12)
Grid laser (BVOS 1984) : ทำในผู้ป่วยที่มีการมองเห็นที่แก้ไขแล้ว ≤ 0.5 ที่ 3-18 เดือนหลังเริ่มมีอาการ ในกลุ่มรักษา 63% มีการมองเห็น ดีขึ้น ≥2 แถว สูงกว่า 37% ในกลุ่มไม่รักษา 20) ที่ติดตาม 3 ปี การมองเห็น สุดท้าย 20/40 หรือดีกว่าใน 34% และ 20/200 หรือแย่กว่าใน 23% อย่างไรก็ตาม grid laser อาจทำให้เกิดจุดบอดสัมบูรณ์ และไม่ใช่ทางเลือกแรกในยุค anti-VEGFScatter laser (การจี้แบบกระจาย) : ทำในชนิดขาดเลือด การจี้บริเวณที่หลอดเลือดฝอยอุดตันใน FA สามารถลดอุบัติการณ์ของเส้นเลือดใหม่จากประมาณ 40% เหลือประมาณ 20% ใน BRVO ชนิดขาดเลือดที่มีเส้นเลือดใหม่ที่จานประสาทตา (NVD) หรือเส้นเลือดใหม่ที่จอตา (NVE) แนะนำให้ทำ sectoral PRP 12)
พิจารณาในกรณีต่อไปนี้:
เลือดออกในน้ำวุ้นตา : เมื่อมีเลือดออกซ้ำจากเส้นเลือดใหม่และไม่คาดว่าจะดูดซึมเองจอตาลอกแบบดึงรั้งจากการเจริญของเยื่อพังผืดและเส้นเลือด : ข้อบ่งชี้การผ่าตัดเร่งด่วนจอประสาทตา บวมที่ดื้อต่อการรักษาวุ้นตา หลุดจากจอตาส่วนหลังเทียมเพื่อลดแรงดึงของน้ำวุ้นตา และกำจัดไซโตไคน์ที่ก่อการอักเสบ มีรายงานการร่วมกับการลอกเยื่อหุ้มลิมิตติงอินเทอร์นาหรือการผ่าตัดเปิดปลอกหลอดเลือดแดง/ดำ (A/V sheathotomy) อย่างไรก็ตาม ในตาที่ไม่มีน้ำวุ้นตา ผลของยายับยั้ง VEGF ลดลง ดังนั้นควรพิจารณาข้อบ่งชี้การผ่าตัดอย่างระมัดระวัง
ตามการศึกษา BVOS แม้ไม่ได้รับการรักษา 37% มีการมองเห็น ดีขึ้นเอง ≥2 แถว ในขณะที่ 23% มีการมองเห็น สุดท้าย 20/200 หรือแย่กว่า และ 34% บรรลุ 20/40 หรือดีกว่า 20) ที่ติดตาม 3 ปี พบการมองเห็น ดีขึ้นเฉลี่ย 2.3 แถว การสร้างวงจรเลือดเลี้ยงข้างช่วยปรับปรุงการระบายเลือดดำและลดอาการบวมและขาดเลือด 12) เนื่องจากการดำเนินโรคตามธรรมชาติมีความหลากหลายมาก การประเมินปริมาณจอประสาทตา บวมด้วย OCT จึงมีความสำคัญต่อการตัดสินใจรักษา
การฉีดยา anti-VEGF เข้าแก้วตา มีความเสี่ยง เช่น เยื่อบุตาอักเสบ ความดันลูกตา สูง และเลนส์ตาเสียหาย ควรปฏิบัติตามนัดหมาย และไปพบแพทย์ทันทีหากมีการเปลี่ยนแปลงการมองเห็น หรือปวดตา
การปลูกถ่ายเดกซาเมทาโซนมีความเสี่ยงต่อการเกิดต้อหินจากสเตียรอยด์ และการลุกลามของต้อกระจก ดังนั้นควรระวังในผู้ป่วยที่มีประวัติต้อหิน
อาการบวมน้ำที่จอประสาทตา ส่วนกลางอาจกลับมาเป็นซ้ำหากหยุดการรักษา หลีกเลี่ยงการหยุดการรักษาโดยไม่ปรึกษาแพทย์
การควบคุมความดันโลหิต ไขมัน และน้ำตาลในเลือดทั่วร่างกายเป็นส่วนหนึ่งของการรักษา ควรประสานงานกับอายุรแพทย์เพื่อการจัดการอย่างต่อเนื่อง
Q
การฉีด anti-VEGF ต้องทำต่อเนื่องนานเท่าใด?
A
การศึกษา RETAIN รายงานว่าต้องใช้เวลาเฉลี่ย 53 เดือน และฉีด 14.8 ครั้ง และประมาณครึ่งหนึ่งของผู้ป่วย BRVO ยังคงรักษาต่อเนื่องนานกว่า 5 ปี 12) การปรับขนาดยามักทำแบบ PRN (ตามความจำเป็น) หรือ T&E (รักษาและยืดระยะ) ขึ้นอยู่กับการตอบสนอง ดูรายละเอียดในหัวข้อ «การรักษามาตรฐาน»
Q
สามารถหายได้เองหรือไม่?
A
จากการศึกษา BVOS แม้ไม่ได้รับการรักษา 37% ของผู้ป่วยมีการมองเห็น ดีขึ้นเอง 2 แถวขึ้นไป แต่ 23% มีค่าการมองเห็น สุดท้ายที่ 20/200 หรือแย่กว่า 20) การสร้างเส้นเลือดเลี้ยงข้างเคียงอาจช่วยลดอาการบวมน้ำ แต่การดำเนินโรคตามธรรมชาติคาดเดาได้ยาก และแนะนำให้รักษาหากอาการบวมน้ำที่จอประสาทตา ส่วนกลางยังคงอยู่
กลไกการเกิด BRVO เป็นแบบหลายปัจจัย เกี่ยวข้องกับลักษณะทางกายวิภาคของจุดตัดหลอดเลือดแดง-ดำ และปัจจัยเสี่ยงทางหลอดเลือดทั่วร่างกาย
ที่จุดตัดหลอดเลือดแดง-ดำ หลอดเลือดแดงและดำถูกหุ้มด้วยเยื่อหุ้มชั้นนอกร่วมกัน ภาวะหลอดเลือดแดงแข็งทำให้ผนังหลอดเลือดแดงหนาและแข็งขึ้น กดทับหลอดเลือดดำจากภายนอก ทำให้รูของหลอดเลือดดำแคบลง การศึกษา OCT ยืนยันการผิดรูปของรูหลอดเลือดดำ (แคบลง ไม่ใช่แบน) ที่จุดตัด การตีบแคบนี้ทำให้เกิดการไหลแบบปั่นป่วน นำไปสู่ความเสียหายของเยื่อบุผนังหลอดเลือดเรื้อรัง การปรับโครงสร้างของชั้นใน และการเกิดลิ่มเลือด
การอุดตันของหลอดเลือดดำทำให้ความดันเลือดไหลกลับเพิ่มขึ้น เกิดการไหลเวียนเลือดชะงักและจอประสาทตา ขาดเลือด ในเวลาเดียวกัน การรั่วจากเส้นเลือดฝอยบริเวณรอยบุ๋มจอตา เนื่องจากความดันเลือดไหลกลับที่เพิ่มขึ้นและการซึมผ่านของผนังหลอดเลือดที่เพิ่มขึ้น ทำให้เกิดอาการบวมน้ำที่จอประสาทตา ส่วนกลาง
ในน้ำวุ้นตา ของผู้ป่วย BRVO มีรายงานการเพิ่มขึ้นของไซโตไคน์ดังต่อไปนี้
VEGF : ตัวกลางหลักที่ทำให้การซึมผ่านของหลอดเลือดเพิ่มขึ้นและการเกิดจอประสาทตา บวมน้ำ มีบทบาทสำคัญในฐานะปัจจัยที่เกี่ยวข้องกับภาวะขาดออกซิเจนที่ปล่อยออกมาจากจอประสาทตา ขาดเลือดAngiopoietin-2 (Ang-2) : มีระดับสูงที่สุดในบรรดาโรคจอประสาทตา ในผู้ป่วย RVO 15) Ang-2 ยับยั้งการจับของ Angiopoietin-1 กับตัวรับ Tie2 อย่างแข่งขัน ทำให้ขัดขวางการคงตัวของหลอดเลือด การทำงานร่วมกันของ VEGF และ Ang-2 ทำให้หลอดเลือดไม่คงตัวมากขึ้น ส่งเสริมการรั่วของหลอดเลือด การอักเสบ และการสร้างเส้นเลือดใหม่ ด้วยการยับยั้ง Ang-2/VEGF แบบคู่โดย faricimab คาดว่าจะทำให้หลอดเลือดจอประสาทตา คงตัวได้ยาวนานกว่าเมื่อเทียบกับการยับยั้ง VEGF เพียงอย่างเดียวIL-6, IL-8 : เกี่ยวข้องกับการขยายสัญญาณการอักเสบMCP -1 (Monocyte Chemoattractant Protein-1)
สำหรับกลไกของ BRVO ที่เกี่ยวข้องกับวัคซีน มีสมมติฐานว่าโปรตีนหนาม (spike protein) ส่งเสริมการเกิดลิ่มเลือดและการตอบสนองต่อการอักเสบ 10, 11) มีทฤษฎีว่าโปรตีนหนามทำลายเซลล์บุผนังหลอดเลือดโดยตรงและส่งเสริมการปล่อยปัจจัยฟอนวิลเลอแบรนด์
Faricimab เป็นแอนติบอดีแบบคู่ที่ยับยั้ง Ang-2 และ VEGF-A พร้อมกัน และในปี 2024 กระบอกฉีดยาที่บรรจุไว้ล่วงหน้าสำหรับข้อบ่งชี้ RVO ได้รับการอนุมัติจาก FDA 12) ในส่วนที่ 1 ของการทดลอง BALATON/COMINO (ขนาดยาคงที่เดือนละครั้งเป็นเวลา 24 สัปดาห์) แสดงประสิทธิภาพเทียบเท่ากับ aflibercept ในการปรับปรุงการมองเห็น และการลด CST 15)
ในการทดลอง BALATON การเปรียบเทียบ faricimab 6 มก. และ aflibercept 2 มก. เป็นเวลา 24 สัปดาห์ พบว่าการลด CST เท่ากัน (-311.4 μm เทียบกับ -304.4 μm) ที่น่าสังเกตคือ อัตราการหายไปของการรั่วของจอประสาทตา จากการตรวจ FA สูงกว่าอย่างมีนัยสำคัญในกลุ่ม faricimab (33.6% เทียบกับ 21.0%, P=0.0023) 15) ในการทดลอง COMINO ก็เช่นกัน 44.4% เทียบกับ 30.0% สูงกว่าในกลุ่ม faricimab ซึ่งบ่งชี้ถึงผลการคงตัวของหลอดเลือดจากการยับยั้ง Ang-2
ในส่วนที่ 2 (สัปดาห์ที่ 24-72) กำลังศึกษาการขยายช่วงเวลาการให้ยาออกไปถึง 16 สัปดาห์ด้วยสูตร T&E ที่ปรับเปลี่ยน 15) กำลังรอข้อมูลเกี่ยวกับความทนทานในระยะยาวและช่วงเวลาการให้ยา
ไบโอซิมิลาร์ ของยาต้าน VEGF ได้รับการอนุมัติจาก FDA อย่างต่อเนื่อง และคาดว่าจะช่วยเพิ่มการเข้าถึงการรักษา12)
Ranibizumab biosimilar : ranibizumab-nuna (Byooviz, ได้รับอนุมัติจาก FDA ปี 2021) และ ranibizumab-eqrn (Cimerli, ได้รับอนุมัติจาก FDA ปี 2022) ได้รับการอนุมัติสำหรับข้อบ่งชี้ภาวะจอประสาทตา บวมน้ำจาก RVO Aflibercept biosimilar : 4 ผลิตภัณฑ์ได้รับการอนุมัติจาก FDA ในปี 2024 (aflibercept-jbvf [Yesafili], aflibercept-yszy [Opuviz], aflibercept-mrbb [Ahzantive], aflibercept-ayyh [Pavblu]) ความเท่าเทียมกับผลิตภัณฑ์อ้างอิงได้รับการยืนยันแล้ว แต่ข้อมูลทางคลินิกระยะยาวยังมีจำกัด
รายงานผู้ป่วย RVO หลังการฉีดวัคซีนกำลังสะสมทั่วโลก
Girioni และคณะ (2023) รายงานผู้ป่วย BRVO ตาทั้งสองข้างรายแรกหลังจากได้รับวัคซีนกระตุ้น mRNA-SARS-CoV-211) มากกว่า 50% ของ RVO ที่เกี่ยวข้องกับวัคซีนเกิดจากวัคซีน mRNA โดยมีระยะเวลามัธยฐานจนกระทั่งเกิดอาการ 2 วัน มีการเสนอว่าการทำลายเซลล์บุผนังหลอดเลือดโดยตรงและปฏิกิริยาส่งเสริมการแข็งตัวของเลือดจากโปรตีนหนามอาจเกี่ยวข้องกับพยาธิกำเนิด
Song P, Xu Y, Zha M, et al. Global epidemiology of retinal vein occlusion: a systematic review and meta-analysis of prevalence, incidence, and risk factors. J Glob Health. 2019;9:010427.
Arakawa S, Yasuda M, Nagata M, et al. Nine-year incidence and risk factors for retinal vein occlusion in a general Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2011;52:5905-9.
Jaulim A, Ahmed B, Khanam T, Chatziralli IP. Branch retinal vein occlusion: epidemiology, pathogenesis, risk factors, clinical features, diagnosis, and complications: an update of the literature. Retina. 2013;33:901-10.
Rogers S, McIntosh RL, Cheung N, et al. The prevalence of retinal vein occlusion: pooled data from population studies from the United States, Europe, Asia, and Australia. Ophthalmology. 2010;117:313-9.
O’Mahoney PR, Wong DT, Ray JG. Retinal vein occlusion and traditional risk factors for atherosclerosis. Arch Ophthalmol. 2008;126:692-9.
Rothman AL, Thomas AS, Khan K, Fekrat S. Central retinal vein occlusion in young individuals: a comparison of risk factors and clinical outcomes. Retina. 2019;39:2205-16.
Chou KT, Huang CC, Tsai DC, et al. Sleep apnea and risk of retinal vein occlusion: a nationwide population-based study of Taiwanese. Am J Ophthalmol. 2012;154:200-5.
Wu CY, Riangwiwat T, Limpruttidham N, et al. Association of retinal vein occlusion with cardiovascular events and mortality: a systematic review and meta-analysis. Retina. 2019;39:1635-45.
Sugihara K, et al. Branch retinal vein occlusion after mRNA-based COVID-19 vaccine. Case Rep Ophthalmol. 2022;13:28-32.
Tanaka H, et al. Branch retinal vein occlusion post SARS-CoV-2 vaccination. Taiwan J Ophthalmol. 2022;12:202-5.
Girioni M, et al. Bilateral BRVO after mRNA-SARS-CoV-2 booster dose vaccination. J Clin Med. 2023;12:1325.
Flaxel CJ, Adelman RA, Bailey ST, et al. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024;131:P1-P48.
Campochiaro PA, Heier JS, Feiner L, et al. Ranibizumab for macular edema following branch retinal vein occlusion: six-month primary end point results of a phase III study (BRAVO). Ophthalmology. 2010;117:1102-12.
Clark WL, Boyer DS, Heier JS, et al. Intravitreal aflibercept for macular edema following branch retinal vein occlusion: 52-week results of the VIBRANT study. Ophthalmology. 2016;123:330-6.
Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131:950-60.
Scott IU, VanVeldhuisen PC, Ip MS , et al. Comparison of monthly vs treat-and-extend regimens for individuals with macular edema who respond well to anti-VEGF treatment: secondary outcomes of the SCORE2 randomized clinical trial. JAMA Ophthalmol. 2020;38:190-9.
Tadayoni R, Waldstein SM, Boscia F, et al. Sustained benefits of ranibizumab with or without laser in branch retinal vein occlusion: 24-month results of the BRI GHTER study. Ophthalmology. 2017;124:1778-87.
Haller JA, Bandello F, Belfort R Jr, et al. Randomized, sham-controlled trial of dexamethasone intravitreal implant in patients with macular edema due to retinal vein occlusion (GENEVA). Ophthalmology. 2010;117:1134-46.
Augustin AJ, Offermann I, Grisanti S, et al. Dexamethasone intravitreal implant for early treatment and retreatment of macular edema related to branch retinal vein occlusion: the COBALT study. Ophthalmology. 2020;127:1420-31.
Branch Vein Occlusion Study Group. Argon laser photocoagulation for macular edema in branch vein occlusion. Am J Ophthalmol. 1984;98:271-82.
Scott IU, VanVeldhuisen PC, Ip MS , et al. Effect of bevacizumab vs aflibercept on visual acuity among patients with macular edema due to central retinal vein occlusion: the SCORE2 randomized clinical trial. JAMA. 2017;317(20):2072-2087. doi:10.1001/jama.2017.4568. PMID:28492910; PMCI D:PMC5710547.