ภาวะหลอดเลือดดำจอตาส่วนกลางอุดตัน (CRVO ) เป็นโรคหลอดเลือดจอตาที่พบบ่อยเป็นอันดับสองรองจากจอตาเสื่อมจากเบาหวาน โดยมีความชุกประมาณ 0.2% ในผู้ที่มีอายุมากกว่า 40 ปี
เกิดการอุดตันของหลอดเลือดดำจอตาส่วนกลางที่ระดับ lamina cribrosa ทำให้เกิดเลือดออกแบบ flame-shaped และจอประสาทตา บวมในทั้งสี่ quadrant
แบ่งเป็นชนิดไม่ขาดเลือด (ประมาณ 75-80%) และชนิดขาดเลือด โดยชนิดขาดเลือดจะเกิด rubeosis iridis ใน 45-80% และมากกว่าครึ่งหนึ่งจะเกิดต้อหิน ชนิด neovascular หากไม่ได้รับการรักษา
เนื่องจากประมาณหนึ่งในสามของชนิดไม่ขาดเลือดจะเปลี่ยนเป็นชนิดขาดเลือดในระหว่างการดำเนินโรค การตรวจมุมช่องหน้าตาอย่างสม่ำเสมอจึงจำเป็น
การรักษาอันดับแรกสำหรับจอประสาทตา บวมคือการฉีดยา anti-VEGF เข้าแก้วตา และการทดลองขนาดใหญ่ เช่น CRUISE, COPERNICUS และ COMINO (COMINO : CRVO /hemi-CRVO n=729) ยืนยันประสิทธิภาพ
Relative afferent pupillary defect (RAPD ) ให้ผลบวกในประมาณ 90% ของชนิดขาดเลือด มีประโยชน์ในการแยกชนิดขาดเลือดและไม่ขาดเลือด
ความดันโลหิตสูง เบาหวาน ไขมันในเลือดสูง และต้อหิน เป็นปัจจัยเสี่ยงหลัก หากเกิดก่อนอายุ 50 ปี จำเป็นต้องตรวจหาความผิดปกติทั่วร่างกาย เช่น ความผิดปกติของการแข็งตัวของเลือด
ภาวะหลอดเลือดดำจอตาส่วนกลางอุดตัน (CRVO ) เป็นโรคที่หลอดเลือดดำจอตาส่วนกลางอุดตันที่ระดับ lamina cribrosa ภายในเส้นประสาทตา การอุดตันทำให้ความดันในหลอดเลือดดำเพิ่มขึ้น ส่งผลให้เลือดคั่ง ขาดเลือด และมีการรั่วซึมในจอตา ทำให้เกิดเลือดออกแบบ flame-shaped จานประสาทตา บวม และจอประสาทตา บวมในทั้งสี่ quadrant
ภาวะหลอดเลือดดำจอตาอุดตันโดยรวมเป็นโรคหลอดเลือดจอตาที่พบบ่อยเป็นอันดับสองรองจากจอตาเสื่อมจากเบาหวาน 9, 10) ความชุกทั่วโลกในปี 2015 ประมาณ 0.77% โดยมีผู้ป่วยประมาณ 28 ล้านคนอายุ 30-89 ปี 10) ความชุกของ CRVO ในผู้ที่มีอายุมากกว่า 40 ปีรายงานประมาณ 0.2% ซึ่งน้อยกว่า BRVO 6-7 เท่า 10) พบได้บ่อยที่สุดในทศวรรษที่ 60-70 และค่อนข้างพบน้อยก่อนอายุ 40 ปี 9, 10)
CRVO แบ่งเป็นชนิดมีเลือดเลี้ยง (ไม่ขาดเลือด) และชนิดไม่มีเลือดเลี้ยง (ขาดเลือด) ชนิดไม่ขาดเลือดคิดเป็นประมาณ 75-80% ของ CRVO ทั้งหมด นอกจากนี้ยังมี ภาวะหลอดเลือดดำจอตาครึ่งส่วนกลางอุดตัน (hemi-CRVO ) ซึ่งมีผลเฉพาะสอง quadrant บนหรือล่าง โดยมีแนวทางทางคลินิกคล้าย CRVO 9, 10) Hemi-CRVO เกิดจากการอุดตันของหนึ่งในสองหลอดเลือดดำครึ่งส่วนกลางอิสระที่ระดับ lamina cribrosa และมักไม่เห็นจุดไขว้ของหลอดเลือดแดง-ดำเหมือนใน BRVO ประมาณ 90% มีผลต่อ hemifield บนหรือล่าง 10) ความเสี่ยงของต้อหิน ชนิด neovascular สูงเช่นเดียวกับ CRVO 10)
ภาวะแทรกซ้อนที่สำคัญของ CRVO คือ macular edema และ neovascularization Macular edema เกิดขึ้นได้ทั้งชนิด non-ischemic และ ischemic และเป็นสาเหตุหลักของการมองเห็น ลดลง Neovascularization (iris neovascularization และ retinal neovascularization) เกิดในชนิด ischemic เป็นหลัก ประมาณ 25% ของ CRVO มี iris neovascularization ซึ่งอาจทำให้ตาบอดจาก neovascular glaucoma 10) มีรายงานว่าผู้ป่วย CRVO มีความเสี่ยงต่อเหตุการณ์หัวใจและหลอดเลือดและอัตราการเสียชีวิตจากทุกสาเหตุสูงกว่าประชากรทั่วไป 10) ดังนั้นการทำงานร่วมกับอายุรแพทย์จึงมีความสำคัญในการดูแลรักษาทั้งระบบ
Q
Central retinal vein occlusion กับ branch retinal vein occlusion ต่างกันอย่างไร?
A
CRVO คือการอุดตันของหลอดเลือดดำหลักภายในเส้นประสาทตา ทำให้เกิดเลือดออกทั่วเรตินา (4 quadrant) BRVO คือการอุดตันของหลอดเลือดดำสาขาในเรตินาที่จุดไขว้ของหลอดเลือดแดงและดำ ความเสียหายจำกัดอยู่ที่ 1-2 quadrant BRVO พบได้บ่อยกว่า CRVO 6-7 เท่า 10) CRVO มีความเสี่ยงต่อ neovascular glaucoma สูงกว่า BRVO และมักต้องฉีด anti-VEGF มากกว่า
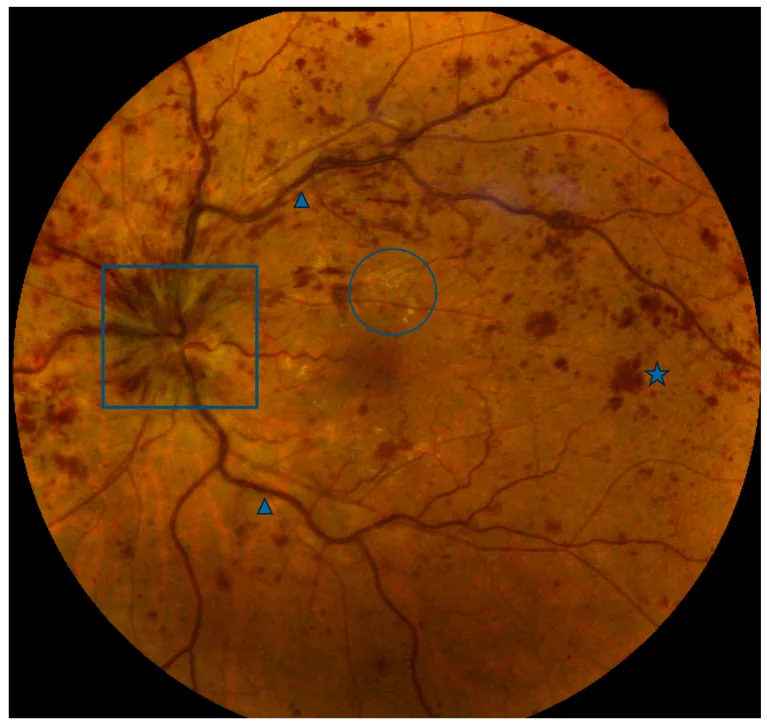
ภาพถ่ายจอประสาทตาของ central retinal vein occlusion แสดงเลือดออกในจอประสาทตากว้าง หลอดเลือดดำขยาย และ papilledema Colcombe J, et al. Retinal Findings and Cardiovascular Risk: Prognostic Conditions, Novel Biomarkers, and Emerging Image Analysis Techniques. J Pers Med. 2023. Figure 1. PM
CI D: PMC10672409. License: CC BY.
ภาพแสดงเลือดออกในจอประสาทตา หลายจุดทั่ว fundus ร่วมกับหลอดเลือดดำขยายและคดเคี้ยว นอกจากนี้ยังมีอาการบวมของ optic disc และจุดขาวรอบ macula ซึ่งเป็นลักษณะทางคลินิกที่พบบ่อยของ central retinal vein occlusion
อาการของ CRVO แตกต่างกันไปตามชนิดของการอุดตัน
ชนิด non-ischemic : อาจไม่มีอาการและพบโดยบังเอิญ แต่หลายรายมีสายตาลดลงจาก macular edema อาจมีอาการตามัวเล็กน้อยแบบเฉียบพลันชนิด ischemic : สูญเสียการมองเห็น อย่างกะทันหันและรุนแรง มักมีสายตาแย่กว่า 20/200 หากมีเลือดออกในน้ำวุ้นตา จะทำให้สูญเสียการมองเห็น เฉียบพลัน หากมี neovascular glaucoma จะมีอาการปวดตา และปวดศีรษะทั้งหมด ไม่เจ็บปวด
ลักษณะ fundus ที่พบบ่อยใน CRVO มีดังนี้:
เลือดออกรูป flame ใน 4 quadrant : ต่างจากการกระจายแบบ sectoral ของ BRVO เลือดออกกระจายไปทุก quadrant ซึ่งสำคัญในการวินิจฉัยแยกโรคหลอดเลือดดำจอประสาทตา ขยายและคดเคี้ยว : สะท้อนถึงความดันในหลอดเลือดดำที่เพิ่มขึ้นจากการอุดตันPapilledema (บวมของหัวประสาทตา) : มักมีอาการบวมรอบหัวประสาทตาร่วมด้วยMacular edema (จอประสาทตา บวม) : เป็นสาเหตุหลักของการมองเห็น ลดลง การประเมินเชิงปริมาณด้วย OCT เป็นสิ่งจำเป็นSoft exudates (จุดขาวนุ่ม) : สะท้อนภาวะขาดเลือด พบได้ชัดเจนในชนิดขาดเลือดHard exudates (จุดขาวแข็ง) : อาจพบรอบจอประสาทตา ในกรณีที่เป็นเรื้อรัง
การวินิจฉัยไม่ยากเนื่องจากมีเลือดออกในจอประสาทตา ที่มีลักษณะเฉพาะ แต่การตรวจเพิ่มเติมนอกเหนือจากการตรวจอวัยวะภายในตาเป็นสิ่งสำคัญในการจำแนกชนิด (ไม่ขาดเลือด vs ขาดเลือด) การบ่งชี้การรักษา และการพยากรณ์โรค เมื่อเวลาผ่านไป เลือดออกเฉียบพลันจะถูกดูดซึมและจุดขาวนุ่มจะหายไป ในระยะยาว อาจมีการพัฒนาของหลอดเลือดเลี้ยงข้างเคียงรอบหัวประสาทตาหรือระหว่างหลอดเลือดดำจอประสาทตา จอประสาทตา บวมอาจหายได้เอง แต่ถ้าคงอยู่นานอาจทำให้เยื่อบุรับแสงฝ่อและทำให้การพยากรณ์โรคทางสายตาแย่ลง
ตารางด้านล่างแสดงประเด็นสำคัญในการแยกชนิดไม่ขาดเลือดและชนิดขาดเลือด มีรายงานว่าประมาณหนึ่งในสามของชนิดไม่ขาดเลือดเปลี่ยนเป็นชนิดขาดเลือดในระหว่างการติดตาม โดยการเปลี่ยนเกิดขึ้น 15% ภายใน 4 เดือน และ 34% ภายใน 3 ปี 10)
ลักษณะ ชนิดไม่ขาดเลือด ชนิดขาดเลือด การมองเห็น 20/200 หรือดีกว่า น้อยกว่า 20/200 RAPD เล็กน้อย/ลบ ชัดเจน (บวกประมาณ 90%) บริเวณที่ไม่มีการไหลเวียนเลือด จาก FA <10 เท่าของพื้นที่จานประสาทตา ≥10 เท่าของพื้นที่จานประสาทตา (เกณฑ์ CVOS) ERG ปกติถึงลดลงเล็กน้อย อัตราส่วน b/a และแอมพลิจูดคลื่น b ลดลง การพยากรณ์โรค ค่อนข้างดี ไม่ดี (เสี่ยงสูงต่อ NVG )
ชนิดที่ไม่ขาดเลือด
ความถี่ : คิดเป็นประมาณ 75-80% ของ CRVO ทั้งหมด
เลือดออก : เลือดออกเป็นรูปเปลวไฟใน 4 จตุภาค (ค่อนข้างตื้น)
บวมน้ำ : ร่วมกับบวมน้ำที่จานประสาทตา และบวมน้ำที่จุดรับภาพ
เส้นเลือดใหม่ : โดยปกติไม่เกิดขึ้น บางรายอาจดีขึ้นเอง
การมองเห็น การมองเห็น ลดลง
ชนิดขาดเลือด
คำจำกัดความ : บริเวณที่ไม่มีการไหลเวียนของเลือดในเส้นเลือดฝอยขนาด ≥10 เท่าของพื้นที่จานประสาทตา ในการตรวจฟลูออเรสซีน แองจิโอกราฟี (เกณฑ์ CVOS) 9, 10) .
RAPD รูม่านตา ชนิด Relative Afferent Pupillary Defect (RAPD ) เป็นบวกในประมาณ 90% ของผู้ป่วย
Rubeosis : เกิดเส้นเลือดใหม่ที่ม่านตา (rubeosis iridis) ใน 45-80% ของผู้ป่วย
NVG ต้อหิน ชนิดเส้นเลือดใหม่ (neovascular glaucoma) เกิดขึ้นในมากกว่าครึ่งหนึ่งของผู้ป่วยที่ไม่ได้รับการรักษา
การเปลี่ยนชนิด : ประมาณหนึ่งในสามของชนิดไม่ขาดเลือดจะเปลี่ยนเป็นชนิดขาดเลือด (15% ภายใน 4 เดือน, 34% ภายใน 3 ปี)
ในการตรวจ OCT B-scan ของ CRVO บางครั้งพบแถบสะท้อนแสงสูง (hyperreflective band) ในชั้นนิวเคลียสชั้นใน (inner nuclear layer) บริเวณพาราฟอฟีเวีย (parafovea) ซึ่งเรียกว่า PAMM (paracentral acute middle maculopathy) สาเหตุเกิดจากความผิดปกติของการไหลเวียนในหลอดเลือดแดงเล็กส่วนปลายที่เลี้ยงข่ายเลือดฝอยชั้นลึกของจอประสาทตา เนื่องจากการไหลเวียนเลือดดำบกพร่อง ในภาพ en-face ของชั้นจอประสาทตา ชั้นตื้น บริเวณสะท้อนแสงสูงไม่ชัดเจน แต่ในภาพ en-face ของชั้นจอประสาทตา ชั้นลึก จะเห็นบริเวณสะท้อนแสงสูงที่สอดคล้องกับจอประสาทตา ขุ่นขาวได้ชัดเจน PAMM สะท้อนถึงภาวะขาดเลือดของข่ายเลือดฝอยชั้นกลาง (intermediate capillary plexus) และถือเป็นตัวบ่งชี้เสริมในการประเมินระดับการขาดเลือดของจอประสาทตา ใน CRVO
Matsuo T และคณะ (2025) รายงานผู้ป่วย CRVO ทั้งสองข้างในชายอายุ 71 ปี 1) CRVO ตาขวาดำเนินไปเป็นต้อหิน ชนิดเส้นเลือดใหม่ที่มีความดันลูกตา 35 mmHg หลังจากเริ่มมีอาการ 4 เดือน และในที่สุดสูญเสียการรับรู้แสง CRVO ตาซ้ายยังคงรักษาการมองเห็น ได้ด้วยการรักษาด้วย anti-VEGF และการรักษาแบบประคับประคอง ภาวะหัวใจห้องล่างขวาล้มเหลวหลังการผ่าตัดหัวใจถูกพิจารณาว่าเป็นปัจจัยกระตุ้นให้เกิดอาการทั้งสองข้าง
Q
หากได้รับการวินิจฉัยว่าเป็นโรคหลอดเลือดดำจอประสาทตาส่วนกลางอุดตัน ฉันต้องมาพบแพทย์บ่อยแค่ไหน?
A
ชนิดไม่ขาดเลือดจะได้รับการประเมินซ้ำหลังจากเริ่มมีอาการ 4-6 สัปดาห์ ชนิดขาดเลือดมีความเสี่ยงสูงต่อการเกิดต้อหิน ชนิดเส้นเลือดใหม่ ดังนั้นจึงจำเป็นต้องมาตรวจทุกเดือนและตรวจมุมลูกตา (gonioscopy) เป็นเวลา 6 เดือน 9) เนื่องจากประมาณหนึ่งในสามของชนิดไม่ขาดเลือดจะเปลี่ยนเป็นชนิดขาดเลือด จึงควรสังเกตมุมลูกตาอยู่เสมอ ในระหว่างการรักษาด้วย anti-VEGF แนะนำให้ตรวจ OCT เกือบทุกเดือนเพื่อประเมินอาการบวมน้ำที่จอประสาทตา ส่วนกลาง
พยาธิสรีรวิทยาของ CRVO อธิบายได้ด้วยสามปัจจัยของ Virchow (การบาดเจ็บของหลอดเลือด, การไหลเวียนเลือดชะงักงัน, ภาวะเลือดแข็งตัวมากเกินไป) ด้านหลังของ lamina cribrosa หลอดเลือดแดงจอประสาทตา ส่วนกลางและหลอดเลือดดำจอประสาทตา ส่วนกลางมีชั้น adventitia ร่วมกัน และเมื่อการเปลี่ยนแปลงจากภาวะหลอดเลือดแดงแข็งทำให้ผนังหลอดเลือดแดงหนาและแข็งขึ้น จะกดทับหลอดเลือดดำที่อยู่ติดกัน ทำให้เกิดการบาดเจ็บของเยื่อบุผนังหลอดเลือด นำไปสู่การเกิดลิ่มเลือดและการอุดตัน
ปัจจัยเสี่ยงหลักแสดงในตารางด้านล่าง
ปัจจัยเสี่ยง ความถี่/ความสัมพันธ์ อายุที่มากขึ้น สำคัญที่สุด: >90% มีอายุมากกว่า 55 ปี ความดันโลหิตสูง ผู้ป่วยอายุมากกว่า 50 ปีสูงถึง 73% มีภาวะนี้ 9, 10) ภาวะไขมันในเลือดสูง ปัจจัยเสี่ยงหลัก 7) เบาหวาน ปัจจัยเสี่ยงอิสระ 9, 10) ต้อหิน / ความดันลูกตา สูงปัจจัยเสี่ยงอิสระ 9, 10)
ในการวิเคราะห์อภิมาน พบว่า 48% ของกรณี RVO เกิดจากความดันโลหิตสูง 20% จากภาวะไขมันในเลือดสูง และ 5% จากเบาหวาน 10) .
ปัจจัยเสี่ยงสำคัญอื่นๆ แสดงไว้ด้านล่าง
ภาวะคอเลสเตอรอล HDL ต่ำ : HDL-C ต่ำถูกรายงานว่าเป็นปัจจัยเสี่ยงอิสระของ RVO และควรสังเกตว่ามักถูกมองข้ามในการตรวจคัดกรองไขมันตามปกติ 10) .โรคภูมิต้านตนเองทั่วร่างกาย : อุบัติการณ์ของ CRVO ในผู้ป่วย SLE สูงกว่ากลุ่มควบคุม 3.5 เท่า 9, 10) .ความเสี่ยงต่อโรคหัวใจและหลอดเลือด : ผู้ป่วย RVO มีความเสี่ยงเพิ่มขึ้นต่อเหตุการณ์หัวใจและหลอดเลือดและการเสียชีวิตจากทุกสาเหตุ การทำงานร่วมกับอายุรกรรมเป็นสิ่งสำคัญ 9, 10) .ยับยั้ง PDE5 (เช่น ซิลเดนาฟิล) : มีรายงาน RVO 82 รายต่อ FDA โดยคาดว่ากลไกคือการขยายตัวของหลอดเลือดดำจอประสาทตา ที่เกิดจากความดันโลหิตต่ำทั่วร่างกาย 2) .การติดเชื้อ COVID-19 : กลไกคือความเสียหายของเยื่อบุผนังหลอดเลือดและการแข็งตัวของเลือดมากเกินไปจากพายุไซโตไคน์ 3, 4) .วัคซีน COVID-19 : มีการเสนอกลไก VITT (ภาวะเกล็ดเลือดต่ำจากการเกิดลิ่มเลือด ที่เกิดจากวัคซีน) โดยอัตราการเกิดลิ่มเลือดหลังฉีดวัคซีน ChAdOx1 (AstraZeneca) คือ 1.13 ต่อ 100,000 โดส 5, 6) .การกลายพันธุ์ของยีน MTHFR : การแข็งตัวของเลือดมากเกินไปจากภาวะโฮโมซิสเทอีนในเลือดสูง 3, 4) .ความผิดปกติของหัวใจห้องขวา : ความดันหลอดเลือดดำที่เพิ่มขึ้นจากการระบายเลือดดำบกพร่องสามารถกระตุ้นให้เกิด CRVO ทั้งสองข้าง 1) .ภาวะหยุดหายใจขณะหลับและโรคหลอดเลือดแดงคาโรติดอุดตัน : มีรายงานว่าเป็นปัจจัยเสี่ยงของ CRVO 10) .ความเสี่ยงของตาข้างตรงข้าม : หากเกิด CRVO ในตาข้างเดียว ความเสี่ยงที่จะเกิด CRVO ในตาอีกข้างคือ 1% ต่อปี 10) .ภาวะซึมเศร้า : มีรายงานว่าผู้ป่วยซึมเศร้ามีความเสี่ยง RVO เพิ่มขึ้น 10) .
ในผู้ป่วยอายุต่ำกว่า 50 ปี แนะนำให้ตรวจร่างกายอย่างละเอียด มีรายงานว่า 58% ของผู้ป่วยมีปัจจัยเสี่ยงที่ไม่ใช่แบบดั้งเดิม (เช่น ความผิดปกติของการแข็งตัวของเลือด โรคภูมิต้านตนเอง) 9, 10) แม้ในผู้ป่วยอายุมากกว่า 50 ปี ควรตรวจสอบการควบคุมความดันโลหิตสูง เบาหวาน และไขมันในเลือดผิดปกติ และแนะนำให้แบ่งปันข้อมูลกับอายุรแพทย์ที่ดูแล
Q
คนหนุ่มสาวสามารถเป็นโรคหลอดเลือดดำจอประสาทตาส่วนกลางอุดตันได้หรือไม่?
A
พบได้น้อยในผู้ที่มีอายุต่ำกว่า 40 ปี แต่ก็เป็นไปได้ สาเหตุอาจรวมถึงความผิดปกติของการแข็งตัวของเลือด การกลายพันธุ์ของยีน MTHFR การติดเชื้อ COVID-19 ภาวะลิ่มเลือดอุดตันหลังวัคซีน ยายับยั้ง PDE5 2, 3, 4, 5, 6) ในผู้ที่มีอายุต่ำกว่า 50 ปี แนะนำให้ตรวจคัดกรองการแข็งตัวของเลือด (โปรตีน C/S, แอนติทรอมบิน III ฯลฯ) และการตรวจหาแอนติบอดีตนเอง (แอนติฟอสโฟลิปิด, แอนตินิวเคลียร์ ฯลฯ) 9, 10) ใน CRVO ในวัยรุ่น สิ่งสำคัญคือต้องแยกความแตกต่างจาก papilitis ชนิดหลอดเลือด ซึ่งต้องรักษาด้วยสเตียรอยด์ ชนิดทั่วร่างกาย
การวินิจฉัยอาศัยประวัติ การมองเห็น และผลการตรวจอวัยวะรับภาพ การวินิจฉัยนั้นไม่ยากเนื่องจากมีเลือดออกเป็นรูปเปลวไฟในสี่จตุภาคและการขยายและคดเคี้ยวของหลอดเลือดดำ แต่การจำแนกชนิดขาดเลือด/ไม่ขาดเลือดและการตัดสินใจในการรักษาจำเป็นต้องมีการตรวจดังต่อไปนี้
การซักประวัติ : ประวัติการมองเห็น ลดลง ยาที่ใช้ (ยาต้านการแข็งตัวของเลือด, ยายับยั้ง PDE5), ประวัติโรคประจำตัว (ความดันโลหิตสูง, เบาหวาน, โรคเลือด, ภาวะหยุดหายใจขณะหลับ) 9, 10) การตรวจวัดการมองเห็น : ในชนิดขาดเลือด มักพบการมองเห็น ต่ำกว่า 20/200 ในการตรวจครั้งแรกการตรวจ RAPD : ในชนิดไม่ขาดเลือดมักให้ผลลบ แต่ในชนิดขาดเลือดให้ผลบวกประมาณ 90% จึงมีประโยชน์มากในการแยกชนิดทั้งสอง นอกจากนี้ยังสำคัญเป็นตัวทำนายความเสี่ยงของการเกิดเส้นเลือดใหม่ 9, 10) การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด และอวัยวะรับภาพจานประสาทตา , บวมของจุดรับภาพ ตรวจดูว่ามีเส้นเลือดใหม่ที่ม่านตา ก่อนขยายม่านตา การวัดความดันลูกตา และการตรวจมุมตา ม่านตา และมุมตา 9) เนื่องจากประมาณ 1 ใน 3 ของชนิดไม่ขาดเลือดเปลี่ยนเป็นชนิดขาดเลือด จึงควรสังเกตมุมตาอยู่เสมอ
ด้านล่างนี้คือบทบาทของการตรวจแต่ละอย่าง
การตรวจ วัตถุประสงค์ การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) ประเมินบริเวณขาดเลือด (เกณฑ์ CVOS) 9, 10) OCT (เครื่องตรวจชั้นตาด้วยแสง)การประเมินปริมาณจอประสาทตา บวมและการตรวจหา PAMM 9, 10) OCTA (การถ่ายภาพหลอดเลือดด้วยแสง)การตรวจหาบริเวณที่เส้นเลือดฝอยไม่มีการไหลเวียนโดยไม่ต้องใช้สารทึบแสง9) ERG (การตรวจคลื่นไฟฟ้าจอประสาทตา )การแยกชนิดขาดเลือด (อัตราส่วน b/a ลดลง) การตรวจลานสายตา จุดบอดกลาง ขนาดใหญ่ในชนิดขาดเลือด
การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : จำเป็นสำหรับการนิยามชนิดขาดเลือดตามเกณฑ์ CVOS (บริเวณที่เส้นเลือดฝอยไม่มีการไหลเวียน ≥ 10 เท่าของพื้นที่จานประสาทตา )9, 10) อย่างไรก็ตาม ในระยะเฉียบพลัน เลือดออกในจอประสาทตา จำนวนมากอาจบดบังการเรืองแสง ทำให้การประเมินบริเวณที่ไม่มีการไหลเวียนทำได้ยาก ดังนั้น อาจต้องตรวจซ้ำหลังจากเลือดออกถูกดูดซึมไปหลายสัปดาห์ FA มุมกว้างช่วยเพิ่มความแม่นยำในการประเมินภาวะขาดเลือดส่วนปลาย และมีรายงานว่ามีประโยชน์ในการทำนายความเสี่ยงของการเปลี่ยนจากชนิดไม่ขาดเลือดเป็นชนิดขาดเลือด9, 10) FA ยังมีประโยชน์ในการแยกความแตกต่างระหว่างการไหลเวียนเลือดทางอ้อม (ไม่มีการรั่วในระยะท้ายของฟลูออเรสซีน ) และเส้นเลือดใหม่ (มีการรั่วทั้งในระยะต้นและระยะท้าย)18) OCT (เครื่องตรวจชั้นตาด้วยแสง)จอประสาทตา บวม และใช้ในการติดตามผลการรักษา9, 10) ใน CRVO อาจพบสัญญาณ PAMM (แถบสะท้อนแสงสูง) ในชั้นนิวเคลียสชั้นในบริเวณพาราฟอฟเวีย ซึ่งสะท้อนถึงความผิดปกติของการไหลเวียนในหลอดเลือดแดงส่วนปลายOCTA (การถ่ายภาพหลอดเลือดด้วยแสง)9) นอกจากนี้ยังสามารถประเมินการขยายตัวของบริเวณไร้หลอดเลือดที่ฟอฟเวีย (FA Z) ได้ แต่ข้อจำกัดของขอบเขตการสแกนเป็นความท้าทายERG (การตรวจคลื่นไฟฟ้าจอประสาทตา )การตรวจลานสายตา จุดบอดกลาง ขนาดใหญ่
เนื่องจากปัจจัยเสี่ยงทางหลอดเลือดทั่วร่างกายมีส่วนเกี่ยวข้องกับการเกิด CRVO จึงทำการตรวจร่างกายทั่วร่างกายดังต่อไปนี้
การตรวจที่แนะนำสำหรับผู้ป่วยทุกราย :
วัดความดันโลหิต
การตรวจเลือด: CBC (การนับเม็ดเลือดสมบูรณ์), ESR (อัตราการตกตะกอนของเม็ดเลือดแดง), น้ำตาลในเลือดขณะอดอาหารและ HbA1c, คอเลสเตอรอลรวม, HDL-C, LDL-C และไตรกลีเซอไรด์
การทำงานของไต (BUN และ Cr)
CRP (เพื่อแยกโรคอักเสบ)
การตรวจเพิ่มเติมที่แนะนำสำหรับผู้ป่วยอายุต่ำกว่า 50 ปี9, 10) :
การคัดกรองระบบการแข็งตัวของเลือด: กิจกรรมโปรตีน C, กิจกรรมโปรตีน S, กิจกรรมแอนติทรอมบิน III, โฮโมซิสเทอีน, การกลายพันธุ์แฟกเตอร์ V Leiden
แอนติบอดีตนเอง: แอนติบอดีต่อฟอสโฟลิปิด (ลูปัสแอนติโคแอกกูแลนต์, แอนติคาร์ดิโอไลปินแอนติบอดี), แอนติบอดีต่อนิวเคลียส
พิจารณาปรึกษาแพทย์เฉพาะทางด้านโลหิตวิทยาหรือโรคข้อและรูมาติสซั่มหากจำเป็น
ปุ่มประสาทตาอักเสบ (Papillitis) : การแยกโรคมีความสำคัญใน CRVO ที่เกิดในวัยหนุ่มสาว CRVO ที่เกี่ยวข้องกับปุ่มประสาทตาอักเสบอาจต้องได้รับการรักษาด้วยสเตียรอยด์ ทั่วร่างกายโรคทางโลหิตวิทยา : หาก CRVO เกิดขึ้นในตาทั้งสองข้าง อาจเกี่ยวข้องกับโรคทางโลหิตวิทยา เช่น ภาวะเม็ดเลือดแดงมาก, มะเร็งเม็ดเลือดขาว หรือโรคไมอีโลโปรลิเฟอเรทีฟ จึงจำเป็นต้องตรวจสอบอย่างละเอียดจอประสาทตาเสื่อมจากเบาหวาน จอประสาทตา แบบกระจาย CRVO มีลักษณะเฉพาะคือเริ่มเฉียบพลันข้างเดียวและเลือดออกสม่ำเสมอในสี่จตุภาค ในขณะที่จอประสาทตาเสื่อมจากเบาหวาน เป็นแบบสองข้างและเรื้อรัง โดยมีรูปแบบการสร้างเส้นเลือดใหม่ที่แตกต่างกันกลุ่มอาการตาขาดเลือด : ภาวะขาดเลือดเรื้อรังจากโรคหลอดเลือดแดงคาโรติดอุดตันอาจทำให้พบลักษณะของจอประสาทตา คล้าย CRVO เลือดออกใน CRVO จะเฉียบพลันและมากกว่า ในขณะที่กลุ่มอาการตาขาดเลือดเลือดออกจะปานกลาง ความดันลูกตาต่ำ และมีเส้นเลือดใหม่ที่ม่านตา ปรากฏเร็ว
การรักษา CRVO ประกอบด้วยสองเสาหลัก: การรักษาภาวะจอประสาทตา บวมน้ำ และ การรักษาภาวะเส้นเลือดงอกใหม่
การฉีดยาต้าน VEGF เข้าแก้วตาเป็นการรักษาทางเลือกแรกสำหรับภาวะจอประสาทตา บวมน้ำที่เกิดจาก CRVO 9, 10) การทดลองทางคลินิกแบบสุ่มขนาดใหญ่หลายชิ้นยืนยันประสิทธิภาพของมัน เมื่อเทียบกับ BRVO จำนวนครั้งที่ฉียามากกว่า และในชนิดขาดเลือด กรณีที่หายขาดนั้นพบได้น้อย แต่ปัจจุบันนี้เป็นการรักษาที่มีแนวโน้มดีที่สุดในการฟื้นฟูการมองเห็น
รานิบิซูแมบ
การทดลอง CRUISE : ในกลุ่ม 0.5 มก. ค่าเฉลี่ยการดีขึ้น +14.9 ตัวอักษรหลัง 6 เดือน 47.7% ดีขึ้น ≥15 ตัวอักษร (กลุ่มหลอก: ดีขึ้น 0.8 ตัวอักษร, 16.9% ดีขึ้น ≥15 ตัวอักษร) 12)
ขนาดยา : 0.5 มก./0.05 มล. ฉีดเข้าแก้วตาทุกเดือน
การครอบคลุมของประกัน : ได้รับการอนุมัติสำหรับ “จอประสาทตา บวมน้ำจากหลอดเลือดดำจอประสาทตาอุดตัน ”
แอฟลิเบอร์เซปต์
การทดลอง COPERNICUS : ในกลุ่ม 2 มก. 56% ดีขึ้น ≥15 ตัวอักษร (กลุ่มหลอก 12%) 13)
การทดลอง GALILEO : ยืนยันความเหนือกว่ากลุ่มหลอกเช่นกัน 14)
ขนาดยา : 2 มก./0.05 มล. ฉีดเข้าแก้วตาทุกเดือน
การครอบคลุมของประกัน : ได้รับการอนุมัติสำหรับ “จอประสาทตา บวมน้ำจากหลอดเลือดดำจอประสาทตาอุดตัน ”
ฟาริซิแมบ
การทดลอง COMINO (CRVO /hemi-CRVO , n=729): BCVA พื้นฐาน 50.5 ตัวอักษร, CST 711.6 μm ในกลุ่ม 6 มก. ค่าเฉลี่ยการดีขึ้น +16.9 ตัวอักษรที่สัปดาห์ที่ 24 56.6% ดีขึ้น ≥15 ตัวอักษร บรรลุความไม่ด้อยกว่าเมื่อเทียบกับแอฟลิเบอร์เซปต์ 11)
การเปลี่ยนแปลง CST : การลดลงของ CST ที่สัปดาห์ที่ 24 คือ ฟาริซิแมบ -461.6 μm เทียบกับแอฟลิเบอร์เซปต์ -448.8 μm อัตราการหายของการรั่วของจอประสาทตา คือ ฟาริซิแมบ 44.4% เทียบกับแอฟลิเบอร์เซปต์ 30.0% 11)
ความปลอดภัย : อุบัติการณ์การอักเสบภายในลูกตา (IOI) เท่ากับ 2.2% สำหรับ faricimab เทียบกับ 1.1% สำหรับ aflibercept IOI รุนแรงรวมถึง uveitis 2 รายในกลุ่ม faricimab และ endophthalmitis ที่ไม่ติดเชื้อ 1 รายในกลุ่ม aflibercept11)
กลไกการออกฤทธิ์ : แอนติบอดีแบบคู่จำเพาะที่มีฤทธิ์ต้าน VEGF-A และต้าน Ang-2
ยาต้าน VEGF อื่นๆ และผลการทดลองทางคลินิกที่สำคัญแสดงไว้ด้านล่าง
Bevacizumab : การฉีดเข้าแก้วตา 1.25 มก./0.05 มล. ใช้นอกเหนือข้อบ่งชี้ที่ได้รับอนุมัติ4, 9) การทดลอง LEAVO (100 สัปดาห์, CRVO 463 ราย): การปรับปรุง +15.1 ตัวอักษรในกลุ่ม aflibercept, +12.5 ตัวอักษรในกลุ่ม ranibizumab, +9.8 ตัวอักษรในกลุ่ม bevacizumab Aflibercept แสดงให้เห็นว่าไม่ด้อยกว่า ranibizumab แต่การเปรียบเทียบกับ bevacizumab ไม่ได้ข้อสรุป16) ผู้ป่วย 52% ในกลุ่ม aflibercept, 47% ในกลุ่ม ranibizumab และ 45% ในกลุ่ม bevacizumab บรรลุการมองเห็น ดีขึ้น ≥15 ตัวอักษรการทดลอง SCORE2 (CRVO /hemi-CRVO 362 ราย): ที่ 6 เดือน (จุดสิ้นสุดหลัก) การมองเห็น เทียบเท่าระหว่าง bevacizumab และ aflibercept17) ผู้ป่วยที่ตอบสนองไม่ดีที่ 6 เดือนได้รับการรักษาช่วยเหลือด้วยการปลูกถ่าย dexamethasone ที่ 24 เดือน ทั้งสองกลุ่มมีแนวโน้มการมองเห็น ลดลงจาก 12 เดือนระยะเวลาการรักษา : ประมาณ 56–75% ของผู้ป่วย CRVO ต้องการการรักษาด้วยยาต้าน VEGF อย่างต่อเนื่องนานกว่า 5 ปี10) การมาตรวจตามนัดอย่างสม่ำเสมอในระยะยาวและการรักษาต่อเนื่องเป็นสิ่งจำเป็น การหยุดรักษาเป็นความเสี่ยงต่อการมองเห็น ลดลงสูตรการให้ยา : เริ่มต้นด้วยการฉีดทุกเดือน จากนั้นขยายช่วงเวลาด้วยวิธี treat-and-extend โดยพิจารณาจากการปรับปรุงของจอประสาทตา บวมน้ำในการตรวจ OCT สำหรับ faricimab กำลังพิจารณาขยายช่วงเวลาถึง 16 สัปดาห์11)
เลือกใช้เมื่อยาต้าน VEGF ไม่ได้ผลหรือไม่เหมาะสม
การฉีด triamcinolone acetonide เข้าแก้วตา (TAIV) : ในการศึกษา SCORE กลุ่มการรักษามาตรฐาน (การจี้ด้วยแสง ) แสดงการมองเห็น ดีขึ้น ≥15 ตัวอักษรใน 7%, กลุ่ม TAIV 1 มก. ใน 27% และกลุ่ม 4 มก. ใน 26% ที่ 12 เดือน อย่างไรก็ตาม จอประสาทตา บวมน้ำกลับเป็นซ้ำในมากกว่า 60% ของผู้ป่วย ต้องให้ยาเพิ่มเติม เนื่องจากกลุ่ม 4 มก. มีความดันลูกตา สูงและต้อกระจก ดำเนินไปอย่างมีนัยสำคัญ จึงแนะนำให้ใช้ 1 มก. หากฉีด10) การปลูกถ่าย dexamethasone แบบปลดปล่อยต่อเนื่อง (Ozurdex 0.7 มก.) : ในการทดลอง GENEVA (CRVO /BRVO 1267 ราย) การมองเห็น ดีขึ้นเริ่มตั้งแต่วันที่ 30 ถึงจุดสูงสุดที่ 90 วัน แต่ผลหายไปที่ 6 เดือน15) ที่ 1 ปี พบความดันลูกตา ≥25 มม.ปรอทใน 16% ความเสี่ยงของต้อกระจก และความดันลูกตา สูงสูงกว่าเมื่อเทียบกับยาต้าน VEGF เยื่อบุตาอักเสบ ระยะหลังเยื่อบุตาอักเสบ ระยะหลังหลังการปลูกถ่าย DEX เช่นกัน และอาการรู้สึกมีสิ่งแปลกปลอม ตาแดง และการมองเห็น ลดลงจำเป็นต้องได้รับการดูแลทันที 8)
ยาต้าน VEGF
ปัจจุบัน ยาต้าน VEGF ที่ได้รับการอนุมัติจาก FDA สำหรับอาการบวมน้ำที่จอประสาทตา จาก CRVO ได้แก่ ranibizumab, aflibercept (2 มก.) และ faricimab 10) Bevacizumab เป็นการใช้ยานอกข้อบ่งชี้ แต่การทดลองหลายชิ้นแสดงให้เห็นถึงประสิทธิภาพ Faricimab มีฤทธิ์ทำให้หลอดเลือดคงตัวผ่านกลไกต้าน Ang-2 และมีรายงานอัตราการหายของการรั่วซึมที่จอประสาทตา สูงกว่า aflibercept 11) ระหว่างปี 2021 ถึง 2024 ผลิตภัณฑ์ชีววัตถุคล้ายคลึง ranibizumab 2 ชนิด (ranibizumab-nuna, ranibizumab-eqrn) และผลิตภัณฑ์ชีววัตถุคล้ายคลึง aflibercept 4 ชนิด (aflibercept-jbvf, aflibercept-yszy, aflibercept-mrbb, aflibercept-ayyh) ได้รับการอนุมัติจาก FDA สำหรับอาการบวมน้ำที่จอประสาทตา จาก RVO ซึ่งขยายทางเลือกในอนาคต 10)
PRP (การจี้จอตาทั่วทั้งจอประสาทตา ) ใช้ในการจัดการการสร้างเส้นเลือดใหม่ใน CRVO ชนิดขาดเลือด 9) PRP ไม่ได้ช่วยให้การมองเห็น ดีขึ้น แต่ป้องกันการเกิดต้อหินจากเส้นเลือดใหม่ ผ่านการทำให้เส้นเลือดใหม่หดตัวและยับยั้งการดำเนินไป
ชนิดไม่ขาดเลือด : ไม่เกิดเส้นเลือดใหม่ ดังนั้นจึงไม่มีข้อบ่งชี้ในการทำ PRP ไม่แนะนำให้ทำ PRP เพื่อป้องกันชนิดขาดเลือด : ประมาณ 30% ของ CRVO ชนิดขาดเลือดเกิดเส้นเลือดใหม่ ดังนั้นอาจจำเป็นต้องทำ PRP ปัจจุบัน ยายับยั้ง VEGF สามารถควบคุมเส้นเลือดใหม่ได้ในระดับหนึ่ง ดังนั้นจึงถือว่าไม่สายเกินไปที่จะทำ PRP หลังจากตรวจพบเส้นเลือดใหม่ อย่างไรก็ตาม ในกรณีที่ขาดเลือดรุนแรงหรือผู้ป่วยสูงอายุ อาจพิจารณาทำ PRP เร็วขึ้นผลการวิจัยจาก CVOS : การศึกษา Central Vein Occlusion Study (CVOS) ได้ตรวจสอบการจี้จอตาแบบตารางสำหรับอาการบวมน้ำที่จอประสาทตา ใน CRVO แต่ไม่พบว่าช่วยให้การมองเห็น ดีขึ้น ดังนั้นจึงไม่แนะนำให้จี้จอตาแบบตารางสำหรับอาการบวมน้ำที่จอประสาทตา แนะนำให้จี้จอตาทั่วทั้งจอประสาทตา อย่างหนาแน่นเฉพาะเมื่อยืนยันว่ามีเส้นเลือดใหม่ที่ม่านตา หรือมุมตา 9, 10) การใช้ยาต้าน VEGF ร่วมกันอาจทำให้ทำ PRP ได้สมบูรณ์ง่ายขึ้น 10)
หลังจากที่ยายับยั้ง VEGF ได้รับการอนุมัติแล้ว ไม่ได้ทำเป็นทางเลือกแรก ไม่มีการทดลองทางคลินิกขนาดใหญ่สำหรับอาการบวมน้ำที่จอประสาทตา จาก CRVO และยังไม่มีหลักฐานที่ชัดเจน การผ่าตัด Radial optic neurotomy ที่เคยทำในอดีต พัฒนาขึ้นบนพื้นฐานทางทฤษฎีของการลดความดันที่ lamina cribrosa เพื่อลดความดันหลอดเลือดดำ แต่เนื่องจากอาจทำให้เกิดภาวะแทรกซ้อนรุนแรง เช่น ความบกพร่องของลานสายตา และเลือดออก ปัจจุบันจึงไม่ทำอีก
ในกรณีที่มีเลือดออกในน้ำวุ้นตา สามารถทำ PRP พร้อมกับการนำเลือดออกออกได้ นอกจากนี้ ในกรณีที่มีภาวะ vitreomacular traction syndrome (เยื่อเหนือจอประสาทตา , การดึงรั้งของน้ำวุ้นตา ต่อจอประสาทตา ) การผ่าตัดน้ำวุ้นตา อาจช่วยให้จอประสาทตา บวมดีขึ้นได้
CRVO ที่เกี่ยวข้องกับวัคซีนสเตียรอยด์ แบบ pulse (methylprednisolone 1 กรัม นาน 3 วัน) โดยความหนาของโฟเวียลดลงจาก 823 ไมครอนเหลือ 166 ไมครอน และการมองเห็น ฟื้นจาก 2/60 เป็น 6/96) ยาต้านการแข็งตัวของเลือด : อาจทำให้พยากรณ์โรคทางสายตาแย่ลง ไม่แนะนำให้ใช้4)
เพื่อประเมินประสิทธิภาพการรักษาและตรวจหาภาวะแทรกซ้อนตั้งแต่แรกเริ่ม ให้ติดตามผลตามกำหนดการดังต่อไปนี้
ชนิดที่ไม่ขาดเลือด : ประเมินซ้ำหลังเริ่มป่วย 4–6 สัปดาห์ จากนั้นติดตามทุก 1–3 เดือนตามสภาพของจอประสาทตา บวม ทำการประเมินปริมาณจอประสาทตา บวมด้วย OCT และตรวจวัดสายตาทุกครั้งชนิดขาดเลือด : ต้องมาตรวจทุกเดือนเป็นเวลา 6 เดือนหลังเริ่มป่วย9) ก่อนขยายม่านตา ให้ตรวจดูว่ามีเส้นเลือดใหม่ที่ม่านตา หรือไม่ และเฝ้าระวังเส้นเลือดใหม่ที่มุมตาโดยใช้ gonioscopy แม้หลังจากหยุดการรักษาด้วย anti-VEGF แล้ว ความเสี่ยงของการเกิดเส้นเลือดใหม่ยังคงอยู่ ดังนั้นให้ติดตามผลรวมถึงการตรวจมุมตา ต่อไปเฝ้าระวังการเปลี่ยนจากชนิดไม่ขาดเลือดเป็นชนิดขาดเลือด : ประมาณ 1 ใน 3 ของชนิดไม่ขาดเลือดจะเปลี่ยนเป็นชนิดขาดเลือดในระหว่างการดำเนินโรค ดังนั้นควรสังเกตมุมตาอยู่เสมอ การเปลี่ยนแปลงของ RAPD การมองเห็น ลดลงอย่างรวดเร็ว เลือดออกมากขึ้น เป็นสิ่งบ่งชี้ถึงการเปลี่ยนเป็นชนิดขาดเลือดระหว่างการรักษาด้วย anti-VEGF : ประเมินจอประสาทตา บวมด้วย OCT ทุก 1 เดือนหลังฉีด และฉีดซ้ำหากกลับเป็นซ้ำ หากคงที่ ให้ยืดระยะห่างการฉีดออกไปทีละน้อย (วิธี treat-and-extend)การจัดการทั่วร่างกาย : ติดตามความดันโลหิต น้ำตาลในเลือด และไขมันเป็นระยะร่วมกับอายุรกรรม เนื่องจาก CRVO มีความเสี่ยงต่อตาอีกข้าง (1% ต่อปี) การตรวจตาทั้งสองข้างเป็นประจำจึงสำคัญ10)
โรคต้อหินจากเส้นเลือดใหม่ ทำให้เกิดความเสียหายต่อลานสายตาที่ไม่สามารถฟื้นคืนได้ ดังนั้นในชนิดขาดเลือด ห้ามขาดการติดตามผลทุกเดือนเป็นเวลา 6 เดือน (รวมถึงการตรวจมุมตา )
หลังใส่ DEX implant ต้องระวังความเสี่ยงของความดันลูกตา สูง (16% สูงถึง ≥25 มม.ปรอท) และเยื่อบุตาอักเสบ ติดเชื้อภายในลูกตาที่เกิดช้า8, 15) หากรู้สึกผิดปกติ ควรรีบพบแพทย์
ยาต้านการแข็งตัวของเลือดและยาละลายลิ่มเลือดอาจทำให้เลือดออกในจอประสาทตา แย่ลง ไม่แนะนำให้ใช้4)
หากกำลังรับประทานยา PDE5 inhibitor ให้แจ้งจักษุแพทย์และแพทย์ผู้ดูแล และปรึกษาเกี่ยวกับการสามารถรับประทานยาต่อไปได้หรือไม่ 2)
การรักษาด้วยสเตียรอยด์ เพิ่มความเสี่ยงต่อการลุกลามของต้อกระจก และความดันลูกตา สูง ดังนั้นการติดตามความดันลูกตา เป็นประจำจึงเป็นสิ่งจำเป็น
Q
ต้องฉีด anti-VEGF กี่ครั้ง?
A
ในการทดลอง CRUISE มีการฉีด 6 ครั้งต่อเดือน และพบว่าการมองเห็น ดีขึ้นอย่างมีนัยสำคัญ 12) ในทางปฏิบัติ การรักษาเริ่มต้นด้วยการฉีดทุกเดือน จากนั้นขยายระยะห่างขณะยืนยันการดีขึ้นของจอประสาทตา บวมน้ำด้วย OCT รายงานระบุว่าประมาณ 56-75% ของผู้ป่วย CRVO ต้องการการรักษาต่อเนื่องนานกว่า 5 ปี 10) ดังนั้นการตรวจติดตามเป็นประจำในระยะยาวจึงเป็นสิ่งจำเป็น สำหรับ faricimab กำลังพิจารณาการขยายระยะห่างสูงสุดถึง 16 สัปดาห์ด้วยวิธี treat-and-extend 11)
ด้านหลัง lamina cribrosa หลอดเลือดแดงจอประสาทตา ส่วนกลางและหลอดเลือดดำจอประสาทตา ส่วนกลางมีปลอกหุ้มด้านนอกร่วมกัน (ปลอกเนื้อเยื่อเกี่ยวพัน) การหนาตัวและแข็งตัวของผนังหลอดเลือดแดงเนื่องจากหลอดเลือดแดงแข็งจะกดทับหลอดเลือดดำที่อยู่ติดกัน ทำให้เกิดความเสียหายต่อเยื่อบุผนังหลอดเลือด → การเกิดลิ่มเลือด → การอุดตัน 9, 10) ใน BRVO การอุดตันส่วนใหญ่เกิดขึ้นที่จุดไขว้ของหลอดเลือดแดง-ดำ ในขณะที่ CRVO การอุดตันมีลักษณะเฉพาะที่เกิดขึ้นใกล้ lamina cribrosa แต่กลไกการเกิดลิ่มเลือดถือว่าเหมือนกับ BRVO
องค์ประกอบทั้งสามของ Virchow (ความเสียหายของหลอดเลือด, การไหลเวียนเลือดชะงัก, ภาวะเลือดแข็งตัวมากเกินไป) ล้วนมีส่วนเกี่ยวข้อง ใน BRVO การกดทับที่จุดไขว้ของหลอดเลือดแดง-ดำเป็นสาเหตุหลักของการอุดตัน ในขณะที่ CRVO โครงสร้างที่เป็นเอกลักษณ์ซึ่งหลอดเลือดแดงและหลอดเลือดดำมีปลอกหุ้มร่วมกันในพื้นที่กายวิภาคที่แคบของ lamina cribrosa เป็นพื้นฐานของการเกิดการอุดตัน
การอุดตันของหลอดเลือดดำ → ความดันในหลอดเลือดดำเพิ่มขึ้น → การรั่วของส่วนประกอบในพลาสมา → จอประสาทตา บวมและเลือดออก ภาวะจอประสาทตา ขาดเลือด → ภาวะออกซิเจนต่ำ → การผลิต VEGF (vascular endothelial growth factor) มากเกินไป → การแย่ลงของจอประสาทตา บวมน้ำและการสร้างเส้นเลือดใหม่ (เส้นเลือดใหม่ที่ม่านตา , เส้นเลือดใหม่ที่จอประสาทตา ) 9, 10)
ในบรรดาโรคหลอดเลือดจอประสาทตา ทั้งหมด มีรายงานว่าระดับ Ang-2 (angiopoietin-2) สูงที่สุดใน RVO Ang-2 แข่งขันกับ Ang-1 ในการจับกับ Tie2 ยับยั้งการคงตัวของหลอดเลือดที่อาศัยสัญญาณ Ang-1/Tie2 11) นี่เป็นพื้นฐานของกลไกการออกฤทธิ์ของ faricimab ที่กำหนดเป้าหมายทั้ง VEGF-A และ Ang-2
กลไกนี้เป็นเหตุผลเชิงทฤษฎีสำหรับการรักษาด้วย anti-VEGF และ anti-Ang-2 ใน CRVO ชนิดขาดเลือด การผลิต VEGF สูงกว่าชนิดไม่ขาดเลือดอย่างมีนัยสำคัญ และการสร้างเส้นเลือดใหม่ที่ม่านตา มุมตา และจอประสาทตา ดำเนินไปอย่างรวดเร็ว ยายับยั้ง VEGF ไม่เพียงแต่ช่วยให้จอประสาทตา บวมน้ำดีขึ้น แต่ยังมีประสิทธิภาพในการทำให้เส้นเลือดใหม่หดตัว แต่จะกลับมาเป็นซ้ำเมื่อฤทธิ์ยาลดลง จึงจำเป็นต้องให้ยาอย่างต่อเนื่อง
ใน CRVO ความผิดปกติของการไหลเวียนเลือดดำทำให้เกิดความผิดปกติของการไหลเวียนในระดับหลอดเลือดแดงส่วนปลาย ในการตรวจ OCT B-scan จะเห็นเป็นแถบสะท้อนแสงสูงในชั้นแกรนูลาร์ชั้นในบริเวณพาราฟอฟเวีย (ลักษณะ PAMM ) ในภาพเอนเฟซชั้นตื้นจะไม่เด่นชัด แต่ในภาพเอนเฟซชั้นลึกจะเห็นบริเวณสะท้อนแสงสูงที่สอดคล้องกับจอประสาทตา ขุ่นได้ชัดเจน
ที่เกี่ยวข้องกับ COVID-19 : ความเสียหายของเยื่อบุผนังหลอดเลือดจากพายุไซโตไคน์ ภาวะก่อนเกิดลิ่มเลือด และการติดเชื้อโดยตรงของเซลล์เยื่อบุผนังหลอดเลือดร่วมกันทำให้เกิดการแข็งตัวของเลือดมากเกินไป 3) VITT (ลิ่มเลือดอุดตันหลังวัคซีน) : เกิดแอนติบอดีต่อตนเองต่อปัจจัยเกล็ดเลือด 4 (PF4) กระตุ้นเกล็ดเลือดและเกิดลิ่มเลือด 5) ยายับยั้ง PDE5 : ภายใต้ภาวะความดันโลหิตต่ำทั่วร่างกาย ทำให้หลอดเลือดดำจอประสาทตา ขยายและความเร็วเลือดลดลง เพิ่มความเสี่ยงต่อลิ่มเลือดในหลอดเลือดดำ 2) หัวใจห้องขวาล้มเหลว : การระบายเลือดดำทางขวาบกพร่องทำให้ความดันหลอดเลือดดำตาเพิ่มขึ้น อาจกระตุ้นให้เกิด CRVO ทั้งสองข้าง 1)
Q
ทำไมจึงเรียกว่า "ต้อหิน 90 วัน"?
A
ใน CRVO ชนิดขาดเลือด การผลิต VEGF จำนวนมากเนื่องจากจอประสาทตา ขาดเลือดเป็นบริเวณกว้างกระตุ้นให้เกิดเส้นเลือดใหม่ที่ม่านตา ภาวะรูบีโอซิสม่านตา เกิดขึ้นใน 45-80% ของกรณีขาดเลือด และเส้นเลือดใหม่เหล่านี้ไปอุดตันมุมช่องหน้าม่านตา ทำให้เกิดต้อหิน ชนิดเส้นเลือดใหม่ มักปรากฏภายใน 2-4 เดือน (ประมาณ 90 วัน) หลังเริ่มมีอาการ จึงเรียกว่า “ต้อหิน 90 วัน” 9, 10) การตรวจมุมตา อย่างสม่ำเสมอเป็นสิ่งจำเป็นสำหรับการตรวจพบตั้งแต่เนิ่นๆ และการรักษาด้วย PRP และการต้าน VEGF มีผลต่อพยากรณ์การมองเห็น
รายงานเกี่ยวกับความเสี่ยงของการอุดตันของหลอดเลือดดำจอประสาทตา หลังการติดเชื้อ COVID-19 สะสมเพิ่มขึ้น
RiaziEsfahani H และคณะ (2024) รายงานกรณี hemi-CRVO ในผู้ป่วยอายุน้อยที่มีประวัติติดเชื้อ COVID-19 3) ซึ่งบ่งชี้ว่าความเสี่ยงของ RVO อาจคงอยู่เป็นเวลาหลายเดือนหลังการติดเชื้อ
ในการทบทวนผู้ป่วย RVO หลังวัคซีน 20 ราย พบว่า 7 รายเป็นผู้ที่มีอายุน้อยกว่า 40 ปี 6) อัตราการเกิดลิ่มเลือดหลังฉีดวัคซีน ChAdOx1 (AstraZeneca) คือ 1.13 ต่อ 100,000 โดส และมีการเสนอว่ากลไกการแข็งตัวของเลือดมากเกินไปผ่าน VITT 5, 6)
Torkashvand A และคณะ (2023) รายงานผู้ป่วยที่มี CRVO ร่วมกับการอุดตันของหลอดเลือดแดงจอตาส่วนกลางหลังจากรับประทานซิลเดนาฟิล 2) มีการบันทึกความหนาแน่นของหลอดเลือดที่ลดลงใน OCTA และความสนใจมุ่งไปที่ผลของสารยับยั้ง PDE5 ต่อการไหลเวียนของจอตา
ความก้าวหน้าในเทคนิคการถ่ายภาพมุมกว้างช่วยให้การประเมินขอบเขตของภาวะขาดเลือดบริเวณรอบนอกมีความแม่นยำมากขึ้น 9, 10) บริเวณจอตาส่วนรอบนอกที่ไม่มีการไหลเวียนซึ่งประเมินได้ยากด้วย FA มาตรฐานสามารถตรวจพบได้ด้วย FA มุมกว้าง ซึ่งช่วยเพิ่มความแม่นยำในการทำนายความเสี่ยงของการเปลี่ยนจากชนิดที่ไม่ขาดเลือดไปเป็นชนิดขาดเลือด OCTA สามารถประเมินการขยายตัวของพื้นที่ FA Z และการลดลงของความหนาแน่นของเส้นเลือดฝอยในเชิงปริมาณโดยไม่ต้องใช้สารทึบรังสี และมีการรายงานประโยชน์ในการติดตามผู้ป่วย RVO อย่างไรก็ตาม ในปัจจุบัน ข้อจำกัดด้านขอบเขตการถ่ายภาพทำให้ไม่สามารถแทนที่ FA ได้อย่างสมบูรณ์ 9)
กำลังมีการวิจัยการตรวจหา RVO อัตโนมัติจากภาพถ่ายจอตาสีโดยใช้อัลกอริทึมการเรียนรู้เชิงลึก และมีการรายงานความสามารถในการแยกแยะที่ดี 10) คาดว่าจะนำไปประยุกต์ใช้ในการคัดกรองและการแพทย์ทางไกล ในอนาคต
ระหว่างปี 2021 ถึง 2024 FDA ได้อนุมัติผลิตภัณฑ์ชีววัตถุคล้ายคลึงของ ranibizumab 2 ชนิด (ranibizumab-nuna [Byooviz], ranibizumab-eqrn [Cimerli]) และผลิตภัณฑ์ชีววัตถุคล้ายคลึงของ aflibercept 4 ชนิด (aflibercept-jbvf [Yesafili], aflibercept-yszy [Opuviz], aflibercept-mrbb [Ahzantive], aflibercept-ayyh [Pavblu]) สำหรับข้อบ่งชี้ภาวะจอตาบวมน้ำที่เกี่ยวข้องกับ RVO 10) การแพร่หลายของชีววัตถุคล้ายคลึงคาดว่าจะช่วยเพิ่มการเข้าถึงการรักษาและลดค่าใช้จ่ายทางการแพทย์
ในการทดลอง COMINO ของ faricimab หลังจาก 24 สัปดาห์ (ส่วนที่ 2: 24-72 สัปดาห์) ผู้ป่วยทั้งหมดถูกเปลี่ยนไปใช้ faricimab 6 มก. ในสูตร T&E (ช่วงห่างสูงสุด 16 สัปดาห์) ข้อมูลความยั่งยืนและความปลอดภัยระยะยาวที่ 72 สัปดาห์จะถูกเผยแพร่ในอนาคต และคาดว่าจะมีผลลัพธ์สำคัญเกี่ยวกับความเป็นไปได้ในการยืดระยะห่างการให้ยาในการรักษา RVO 11)
มีรายงานผู้ป่วยที่ตรวจพบความผิดปกติของหัวใจห้องขวาหลังจาก CRVO ทั้งสองข้าง ซึ่งเน้นย้ำถึงความสำคัญของการทำงานร่วมกันแบบสหสาขาวิชากับศัลยกรรมหัวใจและอายุรศาสตร์โรคหัวใจ 1)
Matsuo T, et al. Sequential bilateral central retinal vein occlusion with differential long-term outcomes following cardiac surgery. Cureus. 2025;17(12):e100045.
Torkashvand A, et al. Central retinal vein and artery occlusion associated with sildenafil. J Med Case Rep. 2023;17:399.
RiaziEsfahani H, et al. Hemicentral retinal vein occlusion in a patient with COVID-19 history. J Med Case Rep. 2024;18:50.
Staropoli PC, et al. Central retinal vein occlusion associated with COVID-19 and MTHFR mutation in a 15-year-old male. Am J Ophthalmol Case Rep. 2022;26:101522.
Sonawane NJ, et al. Central retinal vein occlusion post-COVID-19 vaccination. Indian J Ophthalmol. 2022;70:308-9.
Dutta Majumder P, et al. Retinal venous occlusion following COVID-19 vaccination: third dose and review. Indian J Ophthalmol. 2022;70:2191-4.
Zhao J, et al. Chylous aqueous humor caused by hyperlipidemia. Medicine. 2023;102:e34972.
Tripathi AN, et al. Atypical delayed-onset endophthalmitis following intravitreal dexamethasone implant. Rom J Ophthalmol. 2024;68(4):343-8.
Flaxel CJ, et al. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2020;127:P288-P320.
Flaxel CJ, et al. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024;131:P288-P332.
Tadayoni R, et al. Efficacy and Safety of Faricimab for Macular Edema due to Retinal Vein Occlusion: 24-Week Results from the BALATON and COMINO Trials. Ophthalmology. 2024.
Campochiaro PA, et al. Ranibizumab for macular edema following central retinal vein occlusion: six-month primary end point results of a phase III study (CRUISE). Ophthalmology. 2010;117(6):1124-1133.e1. doi:10.1016/j.ophtha.2010.02.022. PMID:20381871.
Boyer D, et al. Vascular endothelial growth factor Trap-Eye for macular edema secondary to central retinal vein occlusion: six-month results of the phase 3 COPERNICUS study. Ophthalmology. 2012;119(5):1024-1032. doi:10.1016/j.ophtha.2012.01.042. PMID:22440275.
Holz FG, et al. VEGF Trap-Eye for macular oedema secondary to central retinal vein occlusion: 6-month results of the phase III GALILEO study. Br J Ophthalmol. 2013;97(3):278-284. doi:10.1136/bjophthalmol-2012-301504. PMID:23298885.
Haller JA, et al. Randomized, sham-controlled trial of dexamethasone intravitreal implant in patients with macular edema due to retinal vein occlusion (GENEVA). Ophthalmology. 2010;117(6):1134-1146.e3. doi:10.1016/j.ophtha.2010.03.032. PMID:20417567.
Hykin P, et al. Clinical effectiveness of intravitreal therapy with ranibizumab vs aflibercept vs bevacizumab for macular edema secondary to central retinal vein occlusion (LEAVO). JAMA Ophthalmol. 2019;137(11):1256-1264. doi:10.1001/jamaophthalmol.2019.3305. PMID:31465100; PMCI D:PMC6865295.
Scott IU, et al. Effect of bevacizumab vs aflibercept on visual acuity among patients with macular edema due to central retinal vein occlusion: the SCORE2 randomized clinical trial. JAMA. 2017;317(20):2072-2087. doi:10.1001/jama.2017.4568. PMID:28492910; PMCI D:PMC5710547.
日本眼科学会. 眼底血管造影実施基準(改訂版). 日眼会誌. 2011;115(9):675-681.