TD-OCT (รุ่นที่ 1)
ความยาวคลื่น: 810 นาโนเมตร
ความเร็ว: 400 A-scan/วินาที
ความละเอียดตามแนวแกน: ประมาณ 10 ไมโครเมตร
รุ่นแรกที่ใช้กระจกอ้างอิงเคลื่อนที่เพื่อเปลี่ยนความยาวเส้นทางแสงเพื่อให้ได้ภาพตัดขวาง ปัจจุบันถูกแทนที่ด้วย SD-OCT เป็นส่วนใหญ่

เครื่องตรวจวัดชั้นตาด้วยแสง (Optical Coherence Tomography; OCT) เป็นอุปกรณ์วินิจฉัยภาพที่ใช้ปรากฏการณ์การแทรกสอดของแสงอินฟราเรดใกล้เพื่อให้ได้ภาพตัดขวางของจอตาและส่วนหน้าของตาแบบไม่รุกราน ความละเอียดประมาณ 2-5 ไมโครเมตร ซึ่งสูงกว่าอัลตราซาวนด์ตาประมาณ 100 เท่า ช่วยประเมินโครงสร้างละเอียดของจอตาและเส้นประสาทตาได้ด้วยความละเอียดสูง มีประโยชน์ในการตรวจพบโรคตาต่างๆ ตั้งแต่ระยะแรกและติดตามผล
หลังจากที่ Huang และคณะนำเสนอในปี 1991 OCT ก็แพร่หลายอย่างรวดเร็วในสาขาจักษุวิทยา ปัจจุบันถือเป็นการตรวจมาตรฐานในหลายด้าน เช่น โรคจอตา โรคต้อหิน โรคส่วนหน้าของตา และประสาทจักษุวิทยา ค่าคะแนนประกันถูกกำหนดไว้ที่ 187 คะแนนสำหรับการวิเคราะห์ภาพสามมิติของจอตา
OCT มีสามรุ่นหลัก ลักษณะของแต่ละรุ่นแสดงไว้ด้านล่าง
TD-OCT (รุ่นที่ 1)
ความยาวคลื่น: 810 นาโนเมตร
ความเร็ว: 400 A-scan/วินาที
ความละเอียดตามแนวแกน: ประมาณ 10 ไมโครเมตร
รุ่นแรกที่ใช้กระจกอ้างอิงเคลื่อนที่เพื่อเปลี่ยนความยาวเส้นทางแสงเพื่อให้ได้ภาพตัดขวาง ปัจจุบันถูกแทนที่ด้วย SD-OCT เป็นส่วนใหญ่
SD-OCT (รุ่นที่ 2)
ความยาวคลื่น: 840 นาโนเมตร
ความเร็ว: 40,000 ถึง 100,000 A-scan/วินาที
ความละเอียดตามแนวแกน: 3-7 ไมโครเมตร
รุ่นที่สองที่ใช้สเปกโตรมิเตอร์และการแปลงฟูริเยร์เพื่อเก็บข้อมูลความลึกพร้อมกัน เป็นมาตรฐานทางคลินิกในปัจจุบัน เหมาะสำหรับการประเมินจุดรับภาพและหัวประสาทตาอย่างแม่นยำ อุปกรณ์ตัวแทน: Cirrus (Carl Zeiss), Spectralis (Heidelberg), RS-3000 (Nidek), 3D-OCT (Topcon)
SS-OCT (รุ่นที่ 3)
ความยาวคลื่น: 1050 นาโนเมตร
ความเร็ว: 100,000–400,000 การสแกน A/วินาที
ความละเอียดตามแนวแกน: ประมาณ 5 μm
รุ่นที่สามที่ใช้เลเซอร์กวาดความยาวคลื่นและเครื่องตรวจจับสมดุลคู่ ข้อดีคือสามารถมองเห็นโครงสร้างลึกเช่นคอรอยด์ได้ดีเนื่องจากความยาวคลื่นยาว และไม่จำเป็นต้องใช้ EDI-OCT
OCT เป็นการตรวจที่ไม่รุกล้ำและไม่สัมผัส ไม่เจ็บปวดเลย อาจต้องใช้ยาหยอดตาขยายม่านตา แต่เพียงส่องแสงโดยไม่สัมผัสกระจกตาหรือจอประสาทตา ระยะเวลาการตรวจปกติเพียงไม่กี่นาที
| โหมดการถ่ายภาพ | คุณลักษณะและการใช้งาน |
|---|---|
| การสแกนแบบกากบาท | การสแกนพื้นฐานผ่านรอยบุ๋มจอตา ทำเป็นอันดับแรก |
| 5 เส้น | ชิ้นบางเพื่อตรวจสอบโครงสร้างขนาดเล็ก (เช่น การยืนยันรูจอตา) |
| การสแกนแนวรัศมี | ยืนยันติ่งเนื้อใน PCV, ประเมินรอยโรคที่อยู่นอกศูนย์กลาง |
| แผนที่จอตา | แผนที่ความหนาจอตา ประเมินประสิทธิภาพการรักษาภาวะจอตาบวมจากเบาหวานและ RVO |
| การวิเคราะห์ต้อหิน (cpRNFL/GCA) | ความหนาของ RNFL และ GCL+IPL การวินิจฉัยต้อหินและการประเมินการดำเนินโรค |
พื้นที่การตรวจแบ่งเป็น OCT ส่วนหลัง (จอตา, รอบหัวประสาทตา, ส่วนรอบนอก) และ OCT ส่วนหน้า (AS-OCT; กระจกตา, ช่องหน้าลูกตา, มุมตา)
ขั้นตอนการถ่ายภาพพื้นฐานมีดังนี้:
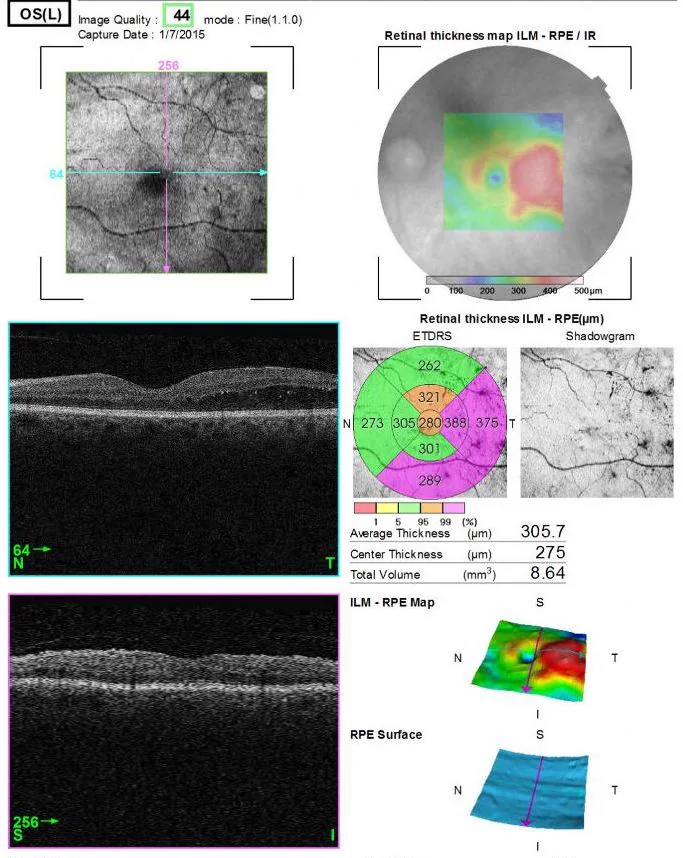
ในการสแกนโฟเวีย สิ่งสำคัญคือการได้ภาพตัดขวางที่ไม่เห็นรอยบุ๋มโฟเวียและไม่เห็นชั้นในของจอประสาทตา ในโรคจุดรับภาพ ศูนย์กลางอาจเคลื่อนเนื่องจากความไม่มั่นคงในการจ้อง และการเข้าใจโครงสร้างปกติของจอประสาทตาช่วยพัฒนาทักษะการตรวจและการวินิจฉัย
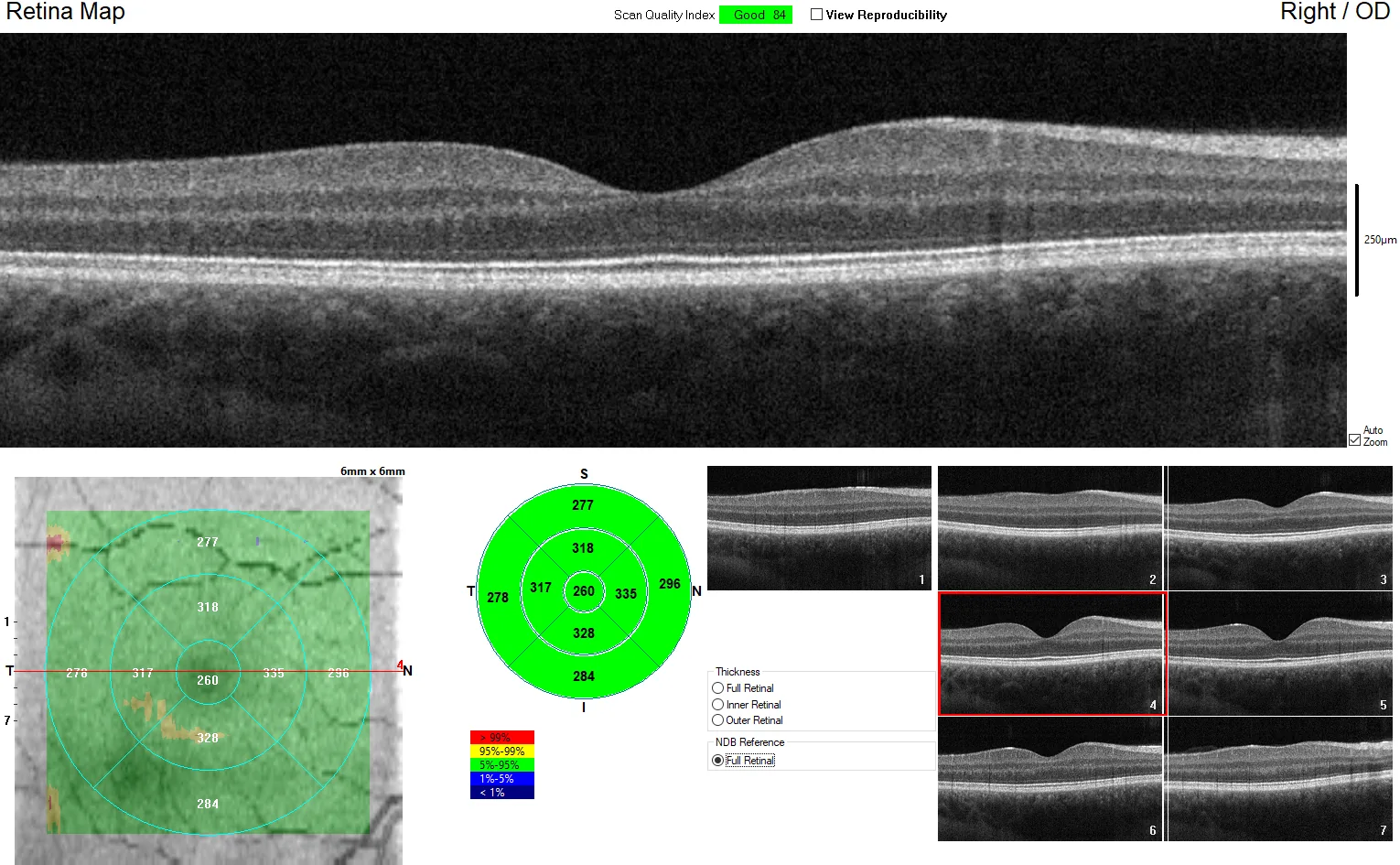
โครงสร้างชั้นปกติในการสแกนโฟเวีย (จากด้านในออกด้านนอก) ประกอบด้วย 13 ชั้นดังนี้:
วุ้นตา → เยื่อลิมิตติ้งชั้นใน (ILM) → ชั้นเส้นใยประสาท (RNFL) → ชั้นเซลล์ปมประสาท (GCL) → ชั้นเพล็กซิฟอร์มชั้นใน (IPL) → ชั้นนิวเคลียร์ชั้นใน (INL) → ชั้นเพล็กซิฟอร์มชั้นนอก (OPL) → ชั้นนิวเคลียร์ชั้นนอก (ONL) → เยื่อลิมิตติ้งชั้นนอก (ELM) → โซนอิลลิปซอยด์ (EZ) → โซนอินเตอร์ดิจิเทชัน (IZ) → เยื่อบุผิวสีจอประสาทตา (RPE) → คอรอยด์
เนื่องจากคุณสมบัติการสะท้อนของแต่ละชั้นสะท้อนถึงสภาพพยาธิสภาพ การระบุชั้นที่แม่นยำจึงเป็นพื้นฐานของการแปลผล
| โรค | ผลการตรวจ OCT ที่เป็นตัวแทน |
|---|---|
| รูที่จุดรับภาพ | ความบกพร่องของจอประสาทตาทุกชั้น ± VMT |
| เยื่อเหนือจอตา (ERM) | ชั้นสะท้อนแสงสูงเหนือเยื่อลิมิตติ้งชั้นใน |
| แรงดึงแก้วตา-จอตา (VMT) | การหลุดลอกบางส่วนของแก้วตาหลังร่วมกับแรงดึงจอตา |
| จอตาบวมจากเบาหวาน | จอตาหนาตัว, จอตาบวมแบบถุงน้ำ, DRIL, ของเหลวใต้จอตา |
| หลอดเลือดดำจอตาอุดตัน (RVO) | จอตาบวมแบบถุงน้ำ, ของเหลวใต้จอตา |
| จอตาเสื่อมตามอายุ (AMD) | เส้นเลือดใหม่คอรอยด์ (ชนิด 1/2/3), การหลุดลอกของชั้นเยื่อบุผิวเม็ดสี |
| โรคคอรอยด์อักเสบชนิดเซรุ่มกลางจอตา (CSC) | จอตาประสาทรับความรู้สึกหลุดลอก, คอรอยด์หนาตัวใน EDI-OCT |
| การฉีกขาดของ RPE | การหายไปอย่างเฉียบพลันของ RPE และโครงสร้างชั้นนอก |
รูจอตา แสดงเป็นข้อบกพร่องตลอดความหนาของจอตา SD-OCT เป็นการตรวจที่มีความไวและความจำเพาะสูงที่สุดในการวินิจฉัยรูจอตา1).
เยื่อเหนือจอตา (ERM) ถูกมองว่าเป็นชั้นสะท้อนแสงสูงเหนือเยื่อลิมิตติ้งอินเทอร์นา2) เกี่ยวกับการมองเห็นหลังผ่าตัด มีรายงานว่า 80% ของกรณีได้รับการมองเห็นดีขึ้นสองบรรทัดขึ้นไปหลังการผ่าตัดวุ้นตา2)
ใน เบาหวานขึ้นจอตาชนิดมีน้ำใต้จอประสาทตา การวัดความหนาของจอตาแบบปริมาณด้วย OCT กลายเป็นตัวบ่งชี้ในการเริ่มการรักษาด้วย anti-VEGF และการตัดสินใจรักษาซ้ำ3) DRIL (การไม่เป็นระเบียบของชั้นจอตาชั้นใน) เป็นเครื่องหมายสำคัญสำหรับการพยากรณ์การมองเห็นที่ไม่ดี
ใน RVO OCT ช่วยให้ประเมินปริมาณน้ำใต้จอประสาทตาและตรวจพบการเปลี่ยนแปลงที่รอยต่อระหว่างวุ้นตาและจอตาได้4)
ใน AMD การลอกของ RPE ถูกจำแนกเป็นชนิดเซรุ่ม ไฟโบรวาสคิวลาร์ และดรูซีนอยด์ และ CNVM สามารถจำแนกเป็นชนิดที่ 1 (ใต้ RPE) ชนิดที่ 2 (เหนือ RPE) และชนิดที่ 3 (เส้นเลือดใหม่ในจอตา)5)
เนื่องจากสภาวะการถ่ายภาพ
สิ่งรบกวนแบบกระจก (Mirror artifact): เนื่องจากข้อผิดพลาดในการตั้งค่าช่วงการสแกน ภาพจริงจะกลับด้านและซ้อนทับกัน
Vignetting: สัญญาณอ่อนลงบริเวณรอบนอก ขึ้นอยู่กับมุมตกกระทบของแสง
ข้อผิดพลาดนอกช่วง (Out-of-range error): โครงสร้างที่อยู่นอกช่วงความลึกที่ตั้งไว้จะถูกแสดงแบบพับกลับ
ปัจจัยผู้ป่วย
สิ่งรบกวนจากการกระพริบตา (Blink artifact): เกิดข้อบกพร่องในแนวนอนเนื่องจากการกระพริบตาระหว่างการสแกน
การเคลื่อนไหวของลูกตา: การจ้องที่ไม่ดีทำให้ภาพเลื่อนหรือบิดเบี้ยว
การเคลื่อนตำแหน่ง (Misalignment): เนื่องจากการเปลี่ยนแปลงตำแหน่งศีรษะระหว่างการสแกน
ปัจจัยซอฟต์แวร์
OCT มีความแม่นยำในการวินิจฉัยที่ดีเยี่ยมโดยเฉพาะโรคของจอประสาทตาส่วนกลางและขั้วหลัง แต่ไม่เหมาะสำหรับการตรวจหารอยโรคจอประสาทตาส่วนปลาย (เช่น จอประสาทตาเสื่อมแบบตาข่าย จอประสาทตาฉีกขาด เป็นต้น) นอกจากนี้ หากมีต้อกระจกหรือขุ่นของวุ้นตาอย่างรุนแรง คุณภาพของภาพจะลดลงและความน่าเชื่อถือในการวินิจฉัยลดลง สำหรับรอยโรคส่วนปลาย จะใช้การถ่ายภาพจอประสาทตามุมกว้างและการตรวจด้วยจักษุแพทย์ทางอ้อม
SD-OCT เป็นเทคนิคการถ่ายภาพวินิจฉัยแบบไม่สัมผัสและไม่รุกรานเพื่อประเมินความเสียหายทางโครงสร้างของโรคต้อหินอย่างเป็นกลาง และได้รับการยอมรับว่ามีประโยชน์สูงในการวินิจฉัยโรคต้อหิน 6) มีประโยชน์อย่างยิ่งในการวินิจฉัยโรคต้อหินก่อนลานสายตา เนื่องจากสามารถตรวจพบการเปลี่ยนแปลงทางโครงสร้างก่อนที่ข้อบกพร่องของลานสายตาจะปรากฏ 6)7)
ความหนาของ RNFL
หลักการวัด: การวัดปริมาณความหนาระหว่างเยื่อจำกัดชั้นใน (ILM) และขอบเขตของ RNFL
แผนที่ TSNIT: แสดงความหนาของ RNFL บนวงกลมขนาด 3.4 มม. รอบศูนย์กลางของเส้นประสาทตา ตามลำดับ: T (ขมับ) → S (บน) → N (จมูก) → I (ล่าง) → T (ขมับ)
รูปแบบปกติ: แสดงยอดสองยอดในทิศทางบนและล่าง (สะท้อนการกระจายทางกายวิภาคของมัดเส้นใยรูปโค้ง) 6)
ความสามารถในการตรวจหาโรคต้อหิน: ความไว 83% และความจำเพาะ 88% สำหรับความหนา RNFL เฉลี่ย (ที่ระดับ 5%) ที่ระดับ 1% ความจำเพาะ 100% และความไว 65%
พารามิเตอร์ ONH
การวิเคราะห์จานประสาทตา: การตรวจจับจานประสาทตา แอ่ง และขอบจานโดยอัตโนมัติ
เกณฑ์เยื่อบรูช: กำหนดขอบจานที่จุดสิ้นสุดของเยื่อบรูช และคำนวณระยะทางที่สั้นที่สุดถึง ILM
ตัวบ่งชี้ที่มีความสามารถในการวินิจฉัยสูง: ความหนาของขอบแนวตั้ง พื้นที่ขอบ และอัตราส่วน C/D แนวตั้งมีความสามารถในการวินิจฉัยสูงที่สุด 7)
BMO-MRW: การประเมินความกว้างของขอบประสาทตาโดยใช้ช่องเปิดของเยื่อบรูชเป็นเกณฑ์ มีความสามารถในการทำซ้ำได้ดีเยี่ยม 6)
การวิเคราะห์เซลล์ปมประสาท (GCA)
วัตถุที่วัด: ความหนาของชั้นเซลล์ปมประสาท (GCL) และชั้นข่ายประสาทชั้นใน (IPL) รอบจอตา
ชื่อเรียกตามเครื่อง: Cirrus เรียก GCIPL (GCL+IPL), Optovue เรียก GCC (RNFL+GCL+IPL)
พารามิเตอร์ที่มีประโยชน์: ค่าต่ำสุด, ส่วนขมับล่าง และค่าเฉลี่ย มีประโยชน์มากที่สุดในการวินิจฉัย 6)7)
ความสัมพันธ์กับพื้นเอฟเฟกต์: พารามิเตอร์จอตาแสดงพื้นเอฟเฟกต์ช้ากว่าความหนา RNFL จึงมีประโยชน์ในการประเมินระยะลุกลาม 6)
การเปรียบเทียบกับฐานข้อมูลตาปกติมีประโยชน์ แต่ต้องระวังผลบวกลวงและผลลบลวงจากปัจจัยต่อไปนี้
มีสองแนวทางในการประเมินการดำเนินของโรคต้อหิน: การวิเคราะห์เหตุการณ์และการวิเคราะห์แนวโน้ม
GPA ของ Cirrus ผสานรวมทั้งสองแนวทาง7) ขีดจำกัดความแปรปรวนที่ยอมรับได้สำหรับความหนา RNFL เฉลี่ยระหว่างการตรวจคือ 3.89 ไมโครเมตร และการลดลงที่สามารถทำซ้ำได้ตั้งแต่ 4 ไมโครเมตรขึ้นไปบ่งชี้ถึงการเปลี่ยนแปลงที่มีนัยสำคัญทางสถิติ
ในโรคต้อหินระยะลุกลาม ความหนา RNFL จะคงที่และไม่ค่อยลดลงต่ำกว่า 50 ไมโครเมตรเนื่องจากเนื้อเยื่อที่ไม่ใช่ประสาท เช่น เกลียและหลอดเลือดยังคงอยู่6)7) “ผลกระทบพื้น” นี้ลดประโยชน์ทางคลินิกของ SD-OCT ในระยะสุดท้าย ทำให้การประเมินการดำเนินโรคด้วยการตรวจลานสายตาเป็นหลัก พารามิเตอร์จอประสาทตาส่วนกลาง (GCIPL) เกิดผลกระทบพื้นช้ากว่าความหนา RNFL จึงยังคงมีประโยชน์ในระยะลุกลาม6)
ในตาที่มีสายตาสั้นมาก การเปรียบเทียบกับฐานข้อมูลปกติมีข้อจำกัด เนื่องจากมัดเส้นใย RNFL เลื่อนไปทางด้านขมับ แม้แต่ตาปกติก็อาจถูกประเมินว่า “บาง” ในกรณีเช่นนี้ การเปรียบเทียบตามลำดับกับค่าพื้นฐานของผู้ป่วยเองมีประสิทธิภาพ การประเมินการบางลงแบบค่อยเป็นค่อยไปทำได้โดยการตรวจ SD-OCT หลายครั้งติดต่อกัน ควรทราบว่าความหนา RNFL ลดลงตามธรรมชาติเมื่ออายุมากขึ้นประมาณ 0.52 ไมโครเมตรต่อปี ดังนั้นต้องพิจารณาการลดลงตามธรรมชาตินี้ด้วย
OCT กำลังขยายตัวอย่างรวดเร็วในสาขาประสาทจักษุวิทยา9) ความหนา RNFL รอบหัวประสาทตา (cpRNFL) และ GCIPL จอประสาทตาส่วนกลาง (ชั้นเซลล์ปมประสาท + ชั้นข่ายประสาทชั้นใน) เป็นพารามิเตอร์หลัก และสามารถตรวจพบการเปลี่ยนแปลงก่อนที่อาการทางคลินิกหรือความผิดปกติทางการมองเห็นจะปรากฏชัดเจน9)
| โรค | ผลการตรวจระยะเฉียบพลัน | ผลการตรวจระยะเรื้อรัง |
|---|---|---|
| ประสาทตาอักเสบ | RNFL หนาขึ้น (บวมของแอกซอน) หรือปกติ | RNFL และ GCIPL บางลง (6 เดือนหลังเริ่มมีอาการ) |
| โรคปลอกประสาทเสื่อมแข็ง (MS) | cpRNFL ลดลงแม้ไม่มีอาการ | อัตราการฝ่อของ RNFL และ GCIPL เพิ่มขึ้นในชนิดลุกลาม |
| NMOSD | Papilledema | RNFL บางรุนแรง (<30 μm), จุดรับภาพบวมแบบไมโครซิสติก (40% ใน AQP4 บวก) 9) |
| โรคเส้นประสาทตาถูกกดทับ (เช่น เนื้องอกต่อมใต้สมอง) | GCIPL บางสองชั้นทางด้านจมูก | RNFL ฝ่อรูปผีเสื้อ (สอดคล้องกับ hemianopsia ข้างขมับทั้งสองข้าง) |
| NAION | ประเมิน RNFL ยากเนื่องจาก papilledema, GCIPL บางเกิดขึ้นก่อน | บางในแนวราบด้านล่างจมูก |
| Drusen ของหัวประสาทตา (ODD) | EDI-OCT เป็นมาตรฐานทองคำในการตรวจหา | ปริมาตร ODD มาก → สัมพันธ์กับ RNFL บางและความบกพร่องของลานสายตา |
| ภาวะคั่งของจานประสาทตา (papilledema) | cpRNFL เพิ่มขึ้น | GCIPL บางลง >10μm → การมองเห็นแย่ลงหลังจาก 1 ปี 9) |
โรคประสาทตาอักเสบและโรคปลอกประสาทเสื่อมแข็ง (MS): การบางลงของ RNFL และ GCIPL เป็นตัวบ่งชี้ทางชีวภาพที่ได้รับการยอมรับ 9) แม้ในผู้ป่วย MS ที่ไม่มีอาการทางตา ก็พบการลดลงของ cpRNFL และการศึกษาหลังการเสียชีวิตยืนยันรอยโรคทำลายไมอีลินของเส้นประสาทตาใน 99% ของผู้ป่วย MS ความหนาของ cpRNFL สัมพันธ์กับค่าสายตาที่ดีที่สุดที่แก้ไขแล้ว ความไวต่อคอนทราสต์ การมองเห็นสี และการฝ่อของสมอง
NMOSD: มีลักษณะเฉพาะคือการฝ่อของเส้นประสาทตาอย่างรุนแรง โดยมีความถี่ของจอประสาทตาบวมน้ำแบบถุงเล็ก (microcystic macular edema) สูงกว่า MS (5%) อย่างมีนัยสำคัญ คือประมาณ 40% ในผู้ป่วยที่ตรวจพบ AQP4 บวก 9) ในโรคประสาทตาอักเสบที่เกี่ยวข้องกับ MOG-IgG GCIPL จะถูกสงวนไว้ค่อนข้างดี ในขณะที่เกี่ยวข้องกับ AQP4-IgG จะสูญเสียอย่างเด่นชัด 9)
ดรูเซนของจานประสาทตา (ODD): EDI-OCT เป็นมาตรฐานทองคำในการตรวจหา ODD 9) ODD ปรากฏเป็นโครงสร้างสะท้อนต่ำเหนือ lamina cribrosa ที่มีขอบสะท้อนสูง และมีความสามารถในการตรวจจับดรูเซนที่ถูกฝังอยู่เหนือกว่าอัลตราซาวนด์ B-scan การเรืองแสงเอง และ CT ควรแยก PHOMS (โครงสร้างรูปไข่สะท้อนสูงรอบจานประสาทตา) เป็นปรากฏการณ์ที่แยกจาก ODD 9)
โรคเส้นประสาทตาถูกกดทับ: ความหนา RNFL ปกติก่อนผ่าตัด (≥70μm) เป็นปัจจัยทำนายที่สำคัญสำหรับการมองเห็นและลานสายตาที่ดีขึ้นหลังผ่าตัด 9) และการประเมิน OCT ก่อนผ่าตัดใช้ในการทำนายพยากรณ์โรค
เนื่องจากอัลกอริทึมการแบ่งส่วนและฐานข้อมูลปกติแตกต่างกันระหว่างเครื่องมือ การเปรียบเทียบตัวเลขระหว่างเครื่องมือต่างชนิดกันจึงไม่สามารถทำได้ สำหรับการประเมินตามระยะเวลา แนะนำให้ใช้เครื่องมือชนิดเดียวกัน 9)
OCT อาศัยหลักการของอินเตอร์เฟอโรมิเตอร์แบบไมเคิลสัน แสงอินฟราเรดใกล้ (ความยาวคลื่น 840-1050 นาโนเมตร) ถูกแบ่งออกเป็นลำแสงวัดและลำแสงอ้างอิง ซึ่งส่องไปยังตัวอย่าง (จอตา) และกระจกอ้างอิงตามลำดับ เมื่อแสงสะท้อนจากทั้งสองถูกรวมกลับเข้าด้วยกัน จะเกิดรูปแบบการแทรกสอด (interferogram) ซึ่งใช้คำนวณความเข้มของการสะท้อนที่แต่ละความลึก โปรไฟล์ความเข้มของการสะท้อนในทิศทางความลึกนี้เรียกว่า A-scan และการเรียง A-scan ตามแนวขวางจะเกิดเป็น B-scan (ภาพตัดขวาง)
ในโรคต้อหินและโรคเส้นประสาทตา จะประเมินสามชั้นต่อไปนี้เป็นลำดับแรก 9)
เมื่อ RGC เสียหาย RNFL จะฝ่อลง ประมาณ 50% ของ RGC ทั้งหมดกระจุกตัวอยู่ในบริเวณศูนย์กลาง 20° ของจอประสาทตาส่วนกลาง และแม้ในโรคต้อหินระยะเริ่มต้น ประมาณ 50% ของ RGC อาจหายไปแล้ว 6) SD-OCT ประเมินการสูญเสียแอกซอนของ RGC ผ่านความหนาของ RNFL และการบางลงของชั้นในรวมถึงตัวเซลล์ผ่าน GCA
ความแตกต่างหลักอยู่ที่ความยาวคลื่นที่ใช้และความสามารถในการมองเห็นโครงสร้างลึก SD-OCT ใช้ย่าน 840 นาโนเมตร ในขณะที่ SS-OCT ใช้ย่าน 1050 นาโนเมตร ความยาวคลื่น 1050 นาโนเมตรกระเจิงโดยเม็ดสีเมลานินน้อยกว่าและทะลุผ่าน RPE ได้ง่ายกว่า ดังนั้น SS-OCT จึงเหนือกว่าในการสังเกตคอรอยด์และตาขาว นอกจากนี้ ความเร็วในการถ่ายภาพของ SS-OCT สูงกว่า SD-OCT ทำให้สแกนมุมกว้างได้ง่าย ในทางกลับกัน ความละเอียดตามแนวแกนของทั้งสองอยู่ที่ประมาณ 5-7 ไมโครเมตร ไม่มีความแตกต่างมากนัก
ด้วยความสามารถในการสแกนมุมกว้างความเร็วสูงของ SS-OCT ที่ความยาวคลื่น 1050 นาโนเมตร การประเมินสเปกตรัมของโรคคอรอยด์หนา (pachychoroid disease spectrum) จึงก้าวหน้าขึ้น ความแม่นยำในการประเมินคอรอยโดพาทีชนิดเซรุ่มส่วนกลาง, โรคหลอดเลือดคอรอยด์ชนิดโพลิปอยด์ (PCV) และภาวะหลอดเลือดฝอยขยายบริเวณพาราฟอฟเวียดีขึ้น ซึ่งช่วยให้เข้าใจพยาธิสรีรวิทยา นอกจากนี้ ความพยายามในการประเมินภาพตัดขวางบริเวณกว้างรวมถึงจอประสาทตาส่วนปลายในการถ่ายภาพเดียวกันกับจอประสาทตาส่วนกลางกำลังดำเนินอยู่
AI วินิจฉัยอัตโนมัติสำหรับโรคต้อหิน โรคจอประสาทตาเสื่อมตามอายุ และโรคจอประสาทตาบวมจากเบาหวานได้รับการพัฒนา และรายงานว่ามีความแม่นยำในการวินิจฉัยที่ดีขึ้น ผ่านการวิเคราะห์ภาพ OCT โดยใช้การเรียนรู้เชิงลึก การปรับปรุงความแม่นยำในการแบ่งส่วนและการสร้างรายงานอัตโนมัติกำลังถูกนำไปใช้ในทางปฏิบัติ 6)7).
จำเป็นต้องมีการศึกษาระยะยาวเพื่อสร้างประโยชน์ของ OCT ในฐานะเครื่องมือคัดกรองและติดตามในโรคระบบประสาทเสื่อม เช่น อัลไซเมอร์และพาร์กินสัน 9) การบางลงของ RNFL และ GCIPL ในผู้ป่วยโรคพฤติกรรมการนอนหลับแบบ REM กำลังได้รับความสนใจในฐานะตัวบ่งชี้แทนสำหรับโรคพาร์กินสันระยะเริ่มต้น 9).
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Macular Hole Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern®. 2020.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Suspect Preferred Practice Pattern®. 2020.
Lo C, Vuong LN, Micieli JA. Recent advances and future directions on the use of optical coherence tomography in neuro-ophthalmology. Taiwan J Ophthalmol. 2021;11(2):107-131.