ชนิดทั่วไป
กลุ่มผู้ป่วย: ผู้ชายอายุ 30-40 ปี มักเป็นข้างเดียว
พยาธิวิทยา: จอประสาทตาลอกแบบเซรุ่มเฉพาะที่บริเวณจุดรับภาพ
การดำเนินโรค: ส่วนใหญ่หายได้เองภายใน 3-4 เดือน การพยากรณ์โรคทางสายตาโดยทั่วไปดี

จอประสาทตาอักเสบชนิดเซรุ่มส่วนกลาง (Central Serous Chorioretinopathy; CSC) เป็นโรคที่มีการลอกตัวของจอประสาทตาแบบเซรุ่ม (SRF) ในบริเวณจุดรับภาพ ในการตรวจฟลูออเรสซีนแองจิโอกราฟี (FA) จะพบการรั่วของฟลูออเรสซีนที่ระดับเยื่อบุผิวรับแสง (RPE) ถือเป็นโรคจอประสาทตาที่พบบ่อยเป็นอันดับสี่รองจากจอประสาทตาเสื่อมตามอายุ เบาหวานขึ้นจอประสาทตา และหลอดเลือดดำจอประสาทตาอุดตัน Von Graefe บรรยายโรคนี้ว่า “จอประสาทตาอักเสบส่วนกลางที่เกิดซ้ำ” ในปี 1866 และ Gass และคณะตั้งชื่อปัจจุบันในปี 1967 ก่อนหน้านี้ในญี่ปุ่น มักหมายถึงเฉพาะกรณีทั่วไปที่ทำให้เกิดจอประสาทตาลอกเฉพาะที่บริเวณจุดรับภาพ (เรียกว่าจอประสาทตาอักเสบส่วนกลาง) แต่ปัจจุบันจำแนกเป็นสามชนิด กรณีส่วนใหญ่หายได้เอง แต่ในกรณีที่ SRF คงอยู่ การพยากรณ์โรคทางสายตาอาจแย่ลง
ทางระบาดวิทยา อุบัติการณ์คือ 9.9 ต่อผู้ชาย 100,000 คน และ 1.7 ต่อผู้หญิง 100,000 คน โดยอัตราส่วนชาย:หญิงประมาณ 8:14) ในการศึกษา 250 ตา อายุเฉลี่ย 46.6 ปี และ 88.4% เป็นผู้ชาย3)
โรคนี้มีสามชนิดดังนี้:
ชนิดทั่วไป
กลุ่มผู้ป่วย: ผู้ชายอายุ 30-40 ปี มักเป็นข้างเดียว
พยาธิวิทยา: จอประสาทตาลอกแบบเซรุ่มเฉพาะที่บริเวณจุดรับภาพ
การดำเนินโรค: ส่วนใหญ่หายได้เองภายใน 3-4 เดือน การพยากรณ์โรคทางสายตาโดยทั่วไปดี
ชนิดเรื้อรัง
กลุ่มผู้ป่วย: พบมากในผู้สูงอายุ มักเป็นทั้งสองข้าง มีแนวโน้มเพิ่มขึ้นเมื่อเร็วๆ นี้
พยาธิสภาพ: ความผิดปกติของ RPE อย่างกว้างขวาง มักเกิดซ้ำ
การดำเนินโรค: SRF คงอยู่นาน ≥6 เดือน ต้องได้รับการรักษาอย่างจริงจัง 5)
จอประสาทตาหลุดแบบตุ่มน้ำ
กลุ่มผู้ป่วย: พบมากในผู้ใช้สเตียรอยด์ขนาดสูง สอดคล้องกับโรคที่เคยเรียกว่า multiple posterior pole retinal pigment epitheliopathy ในญี่ปุ่น
พยาธิสภาพ: ชนิดรุนแรงร่วมกับจอประสาทตาหลุดแบบตุ่มน้ำ ร่วมกับ PED ขนาดใหญ่และจุดขาวหลายจุด
การดำเนินโรค: SRF มักลามลงไปถึงส่วนล่างของจอตา การพยากรณ์โรคการมองเห็นอาจไม่ดี
อัตราการกลับเป็นซ้ำสูงถึง 50% ภายใน 1 ปี โรคนี้ถือเป็นส่วนหนึ่งของสเปกตรัมโรคคอรอยด์หนา (กลุ่มโรคที่มีลักษณะคอรอยด์หนา) 3)9)
ในกรณีทั่วไป มักหายได้เองภายใน 3-4 เดือน การพยากรณ์โรคการมองเห็นโดยทั่วไปดี อย่างไรก็ตาม อัตราการกลับเป็นซ้ำสูงถึง 50% ภายใน 1 ปี หาก SRF คงอยู่นาน >6 เดือน ถือเป็นเรื้อรังและต้องได้รับการรักษา เช่น PDT ในกลุ่มคอรอยด์หนา อัตราการหายเองต่ำกว่า (28.8%) เมื่อเทียบกับกลุ่มที่ไม่หนา (48%) และอัตราการกลับเป็นซ้ำสูงกว่า (31.2% เทียบกับ 10.4%) จึงต้องระวัง 3)
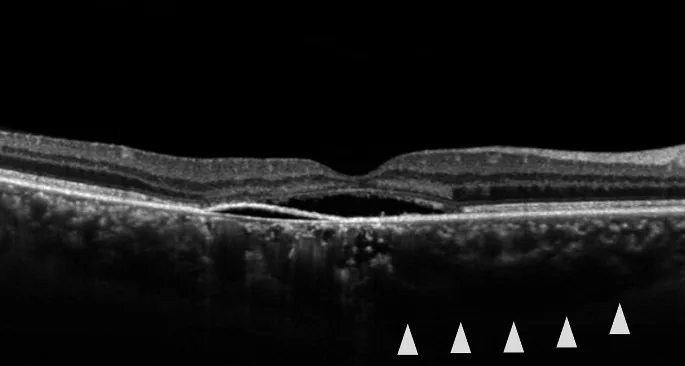
เมื่อของเหลวใต้จอประสาทตาถูกดูดซึม จุดบอดกลางและภาพบิดเบี้ยว (Metamorphopsia) จะดีขึ้นค่อนข้างเร็ว ในขณะที่ภาพเล็กและความไวต่อความแตกต่างลดลงอาจคงอยู่ ในชนิดเรื้อรัง มักเกิดซ้ำบ่อยและหลายกรณีมีสายตาไม่ดี ในกรณีทั่วไป มักเป็นข้างเดียว ในขณะที่ชนิดเรื้อรังและจอประสาทตาลอกแบบตุ่มน้ำ มักเป็นสองข้าง
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit lamp) และการตรวจภาพต่างๆ พบอาการแสดงดังต่อไปนี้
ในชนิดเรื้อรัง ความเสียหายของชั้นเยื่อบุผิวรงควัตถุเป็นบริเวณกว้าง และอาจพบจอประสาทตาลอกที่ยื่นลงด้านล่างร่วมกับแถบฝ่อของชั้นเยื่อบุผิวรงควัตถุ ในจอประสาทตาลอกแบบตุ่มน้ำ จอประสาทตามักลอกรุนแรงและลามไปถึงส่วนล่างของอวัยวะรับภาพ ร่วมกับการลอกของชั้นเยื่อบุผิวรงควัตถุขนาดใหญ่และรอยด่างขาวหลายจุด
สาเหตุพื้นฐานของโรคนี้ยังไม่ทราบแน่ชัด แต่เชื่อว่าการเพิ่มการซึมผ่านของหลอดเลือดคอรอยด์เป็นสาเหตุหลัก ความเครียดและสเตียรอยด์เป็นที่ทราบว่ามีความสัมพันธ์กับการเกิดและการกำเริบของโรค มีรายงานปัจจัยเสี่ยงดังต่อไปนี้
| ปัจจัยเสี่ยง | ความแข็งแรงของความสัมพันธ์ | ข้อสังเกตพิเศษ |
|---|---|---|
| สเตียรอยด์ | OR 37.11) | ทุกช่องทางการให้ยา |
| บุคลิกภาพแบบ A | ปานกลาง | เกี่ยวข้องกับความเครียด |
| การตั้งครรภ์ | 0.008% ต่อปี7) | มักหายเองหลังคลอด |
| OSA | 61% ของผู้ป่วย9) | การทำงานของระบบซิมพาเทติกมากเกินไป |
| สารยับยั้ง PDE5 | รายงานผู้ป่วย8) | หายเมื่อหยุดยา |
การเกิดโรคอธิบายด้วยทฤษฎีหลายปัจจัย (multi-hit theory)9) เชื่อว่าเกิดใน 3 ขั้นตอน: ① ปัจจัยทางกายวิภาคที่เอื้อ (ความยาวแกนตาสั้น ตาขาวหนา การระบายเลือดดำ vortex ไม่สมมาตร ฯลฯ) ② เหตุการณ์กระตุ้น (สเตียรอยด์ ความเครียด OSA ฯลฯ) ③ การเสียสมดุล
สเตียรอยด์เป็นปัจจัยเสี่ยงที่สำคัญที่สุดของโรคนี้ และความเสี่ยงจะเพิ่มขึ้นในทุกเส้นทางการให้ยา รวมถึงยาหยอดตา การสูดดม การฉีด และการรับประทาน มีรายงานอัตราส่วนออดส์ (Odds Ratio) สูงมากถึง 37.1 1) หากได้รับการวินิจฉัยว่าเป็นโรคนี้และกำลังใช้สเตียรอยด์ ควรปรึกษาแพทย์ผู้ดูแลและพิจารณาลดขนาดยาหรือหยุดยาให้มากที่สุด หากได้รับสเตียรอยด์เนื่องจากโรคทางระบบ จำเป็นต้องประสานงานกับแผนกอื่นเพื่อจัดการเป็นรายกรณี
การวินิจฉัยโรคนี้ใช้การตรวจ FA และ OCT ร่วมกันเป็นพื้นฐาน ลักษณะของการตรวจหลักแสดงไว้ด้านล่าง
| การตรวจ | ลักษณะเฉพาะ | บทบาทหลัก |
|---|---|---|
| FA | การรั่วของฟลูออเรสซีนแบบจุด | ระบุจุดรั่วและวางแผนการรักษา |
| IA (ICG) | การเรืองแสงมากเกินไปของคอรอยด์ | ประเมินความผิดปกติของคอรอยด์และการวินิจฉัยแยกโรค |
| OCT | แสดงภาพ SRF และการลอกตัวของเยื่อบุผิวเม็ดสี | ติดตามผลและวัดปริมาณ |
รายละเอียดของการตรวจแต่ละอย่างมีดังนี้
ไม่มีการรักษาด้วยยาที่เป็นที่ยอมรับสำหรับโรคนี้ การจี้ด้วยเลเซอร์บริเวณจุดรั่วซึมจากการตรวจฟลูออเรสซีนแองจิโอกราฟีเป็นวิธีการรักษาเดียวที่ยอมรับโดยทั่วไปในปัจจุบัน และแผนการรักษาขึ้นอยู่กับชนิด ระยะ และตำแหน่งของจุดรั่วซึม
ในชนิดเฉียบพลันทั่วไป มักมีแนวโน้มที่จะหายได้เอง ในระยะเฉียบพลันของผู้ป่วยรายแรก ให้รอการดูดซึมของเหลวใต้จอประสาทตาตามธรรมชาติเป็นเวลา 4-6 เดือน ในกรณีทั่วไป มักดูดซึมหมดภายใน 3-4 เดือน และพยากรณ์โรคด้านการมองเห็นดี อัตราการหายเองในกลุ่มที่ไม่มีความหนาของคอรอยด์คือ 48% ในขณะที่กลุ่มที่มีความหนาของคอรอยด์ต่ำกว่าคือ 28.8% 3)
หากอาการ主观รุนแรงและผู้ป่วยต้องการให้ดีขึ้นเร็ว การจี้ด้วยเลเซอร์ก็เป็นข้อบ่งชี้แม้ในกรณีเฉียบพลันทั่วไป หากกำลังใช้สเตียรอยด์ ให้ลดขนาดหรือหยุดให้มากที่สุด หากให้สเตียรอยด์เนื่องจากโรคทางระบบ ให้จัดการแต่ละกรณีโดยร่วมมือกับแผนกอื่น
ในกรณีที่จอประสาทตาลอกนานเกิน 4-6 เดือนนับจากเริ่มมีอาการ กรณีกลับเป็นซ้ำ กรณีรุนแรง หรือกรณีที่ตาอีกข้างก็มีความบกพร่องทางการมองเห็นจากโรคนี้ (ชนิดเรื้อรังหรือจอประสาทตาลอกแบบตุ่มพอง) จำเป็นต้องให้การรักษาเพื่อให้ของเหลวใต้จอประสาทตาถูกดูดซึมเร็วขึ้น เนื่องจากพยากรณ์โรคการมองเห็นไม่ดีเนื่องจากความเสียหายของจุดรับภาพ
ข้อบ่งชี้เมื่อจุดรั่วซึมอยู่ห่างจากรอยบุ๋มจอประสาทตาตั้งแต่ 500 ไมครอนขึ้นไป และอย่างน้อยอยู่นอกบริเวณหลอดเลือดของรอยบุ๋ม จี้โดยตรงที่จุดรั่วซึมที่ระบุได้จากการตรวจฟลูออเรสซีนแองจิโอกราฟี (เส้นผ่านศูนย์กลาง 200 ไมครอน, 0.2 วินาที, 70-120 มิลลิวัตต์) ระดับการจี้คือ การจี้แบบอ่อนที่ให้จุดจี้สีขาวเทาในชั้นลึกของจอประสาทตา การรั่วซึมระหว่างหัวประสาทตาและจุดรับภาพไม่เป็นปัญหาหากจี้แบบอ่อน หากมีการรั่วซึมภายในรอยลอกของเยื่อบุผิวรับสี ให้จี้เฉพาะจุดรั่วซึมเท่านั้น
เมื่อการจี้ด้วยเลเซอร์ได้ผล จอประสาทตาลอกจะยุบลงภายในไม่กี่สัปดาห์ อย่างไรก็ตาม การดีขึ้นของอาการ主观มักใช้เวลานานกว่า ภาวะแทรกซ้อน ได้แก่ การยิงถูกจุดรับภาพโดยผิดพลาด การเกิดเส้นเลือดใหม่ในคอรอยด์หลังการผ่าตัด (ซึ่งเกิดขึ้นได้ง่ายกว่าด้วยการจี้แบบคลื่นยาว ระยะเวลาสั้น จุดเล็ก)
ใช้เลเซอร์สีเหลือง 577 นาโนเมตร ฉายแสงด้วยการตั้งค่า 240 มิลลิวัตต์ เส้นผ่านศูนย์กลางจุด 200 ไมครอน 200 มิลลิวินาที รอบการทำงาน 5% 4) พลังงานถูกส่งไปยังเยื่อบุผิวรับสีอย่างจำเพาะ ดังนั้นจึงไม่เกิดแผลเป็น สามารถฉายแสงใต้รอยบุ๋มจอประสาทตาได้โดยตรง
Bodea F และคณะ (2024) รายงานว่าในผู้ป่วยโรคคอริโอเรติโนพาทีชนิดเซรุ่มส่วนกลางที่ได้รับการรักษาด้วย MPLT มีการลดลงของของเหลวใต้จอประสาทตาภายใน 2 สัปดาห์ และหายไปภายใน 6 สัปดาห์ 4)
สำหรับโรคนี้ในระหว่างตั้งครรภ์ เลเซอร์ไมโครพัลส์ถือเป็นทางเลือกการรักษาที่ปลอดภัยเพียงทางเดียว 7)
การสังเกตอาการ
ข้อบ่งใช้: ทางเลือกแรกสำหรับกรณีเฉียบพลันทั่วไป
ระยะเวลา: 4–6 เดือน รอการดูดซึมตามธรรมชาติ
ข้อควรระวัง: ระหว่างใช้สเตียรอยด์ ควรพิจารณาลดขนาดหรือหยุดยาโดยประสานงานกับแผนกอื่น
PDT (การรักษาด้วยแสงไดนามิก)
ข้อบ่งใช้: ทางเลือกแรกสำหรับจอประสาทตาอักเสบชนิดเซรุ่มกลางเรื้อรัง
วิธีการ: แนะนำให้ใช้ PDT แบบ half-dose (half-fluence)
หลักฐาน: การทดลอง PLACE และ SPECTRA พิสูจน์ประสิทธิภาพ (อัตราการหายของของเหลวใต้จอประสาทตาใน 12 สัปดาห์ 78% เทียบกับ eplerenone 17%)9)
เลเซอร์ไมโครพัลส์
ลักษณะเด่น: ไม่เกิดแผลเป็น สามารถฉายใต้รอยบุ๋มจอตาได้โดยตรง
ข้อดี: การรักษาเดียวที่ใช้ได้ในระหว่างตั้งครรภ์7)
ผล: ของเหลวใต้จอประสาทตาลดลงใน 2 สัปดาห์ หายใน 6 สัปดาห์4)
ใช้ในกรณีที่ไม่สามารถจี้ด้วยเลเซอร์ได้ เช่น จุดรั่วในบริเวณหลอดเลือดจอตาส่วนกลาง หรือชนิดเรื้อรัง แนะนำให้ใช้ half-dose PDT (ครึ่งขนาดปกติ) หรือ half-fluence PDT (ครึ่งพลังงานเลเซอร์) ร่วมกับ verteporfin (visudyne) เป็นทางเลือกแรกสำหรับจอประสาทตาอักเสบชนิดเซรุ่มกลางเรื้อรัง9)
ผลลัพธ์ของการทดลองทางคลินิกหลักมีดังนี้9)
ยาต้านตัวรับมิเนอรัลคอร์ติคอยด์ ใช้ในขนาด 50 มก./วัน ในการทดลอง VICI (การทดลองแบบสุ่ม ปกปิดสองด้าน ควบคุมด้วยยาหลอก) หลังจากให้ยา 12 เดือน eplerenone ไม่แสดงความแตกต่างอย่างมีนัยสำคัญในการปรับปรุง BCVA เมื่อเทียบกับยาหลอก9) ถือว่ามีประสิทธิภาพน้อยกว่า PDT และมีรายงานผู้ป่วยที่ไม่ตอบสนองแม้หลังจากรักษา 10 เดือน5)
วิธีการรักษาใหม่ที่เกี่ยวข้องกับการฉายแสง LED สีเหลือง 590 นาโนเมตรและ LED สีแดง 625 นาโนเมตร อย่างละ 6 นาที5) มีรายงานผู้ป่วยที่ BCVA ดีขึ้นจาก 20/80 เป็น 20/25 และความหนาจอประสาทตาส่วนกลางลดลงจาก 752 ไมครอนเป็น 296 ไมครอน (ที่ 1 เดือน) ในผู้ป่วยที่มีจอประสาทตาชั้นรับภาพลอกตัวแบบเซรosus เรื้อรังที่เกี่ยวข้องกับ CSC ซึ่งไม่ตอบสนองต่อ eplerenone5)
อุบัติการณ์ของโรคนี้ระหว่างตั้งครรภ์รายงานอยู่ที่ 0.008% ต่อปี 7) ส่วนใหญ่จะหายได้เองภายใน 3 เดือนหลังคลอด หากจำเป็นต้องรักษา เลเซอร์ไมโครพัลส์ (MPLT) ถือเป็นทางเลือกที่ปลอดภัยเพียงทางเดียวในระหว่างตั้งครรภ์ และสามารถฉายแสงได้โดยไม่เกิดแผลเป็นแม้ใต้รอยบุ๋มจอตา 7)
ในกรณีเฉียบพลันทั่วไป การสังเกตอาการเป็นเวลา 4-6 เดือนเป็นพื้นฐาน สำหรับชนิดเรื้อรังที่มี SRF คงอยู่นานกว่า 6 เดือน การรักษาด้วยแสงครึ่งขนาด (half-dose PDT) เป็นทางเลือกแรก 9) การทดลอง SPECTRA แสดงอัตราการหายของ SRF อย่างสมบูรณ์ที่ 12 สัปดาห์เท่ากับ 78% ในกลุ่ม PDT เทียบกับ 17% ในกลุ่ม eplerenone ซึ่งแตกต่างอย่างมีนัยสำคัญ หากจุดรั่วอยู่ภายนอกบริเวณหลอดเลือดของรอยบุ๋มจอตา จะใช้เลเซอร์จี้แข็งตัว (จี้แบบอ่อน) หากอยู่ใต้รอยบุ๋มจอตาโดยตรงหรือระหว่างตั้งครรภ์ จะเลือกเลเซอร์ไมโครพัลส์ Eplerenone ไม่แสดงการปรับปรุง BCVA อย่างมีนัยสำคัญเมื่อเทียบกับยาหลอกในการทดลอง VICI 9)
กลไกการเกิดโรคนี้ อธิบายโดยกลไกที่ซับซ้อนซึ่งเน้นที่ “การเพิ่มขึ้นของการซึมผ่านของหลอดเลือดคอรอยด์” จากการศึกษา IA เชื่อว่ารอยโรคปฐมภูมิอยู่ที่คอรอยด์ และความเสียหายของ RPE เกิดขึ้นเป็นลำดับรอง ยังไม่ทราบแน่ชัดว่าทำไมรอยโรคจึงเกิดขึ้นที่คอรอยด์ ความเครียดและสเตียรอยด์เป็นที่ทราบกันว่าสัมพันธ์กับการเกิดและการกำเริบของโรค
ในการตรวจ FA จะเห็นการรั่วของฟลูออเรสซีนจากเยื่อบุผิวรงควัตถุและการสะสมของสีใต้จอตา การศึกษา OCT แสดงให้เห็นว่าคอรอยด์หนากว่าในโรคนี้เมื่อเทียบกับตาปกติ ซึ่งพิสูจน์ความผิดปกติของคอรอยด์ทางสัณฐานวิทยา
Cheung CMG และคณะ (2025) อธิบายการเกิดโรคนี้ด้วยทฤษฎีหลายปัจจัย 9)
ตาที่เป็น CSC มีตาขาวส่วนหน้าและส่วนหลังหนากว่าตาปกติอย่างมีนัยสำคัญ 9) หลอดเลือดดำวอร์ติโคสเจาะทะลุตาขาวในแนวเฉียง (ระยะในตาขาวประมาณ 4 มม.) ดังนั้นตาขาวที่หนาอาจเพิ่มความต้านทานการไหลออกของหลอดเลือดดำและทำให้เกิดภาวะคั่งเลือดในคอรอยด์ 9) ใน 62% ของตา CSC พบการสะสมของของเหลวในช่องเหนือคอรอยด์ (loculation of fluid) และ 19% พบการรั่วซึมของซิลิโอคอรอยด์ (ciliochoroidal effusion) 9) ใน CSC ที่เกิดจากสเตียรอยด์ ตาขาวจะบางกว่า CSC ที่ไม่ทราบสาเหตุ ซึ่งบ่งชี้ว่าตาขาวมีบทบาทแตกต่างกันในพยาธิสภาพ 9)
มีการเสนอการจำแนกประเภทใหม่โดยอาศัยการถ่ายภาพหลายรูปแบบ 9)
ในแต่ละหมวดหมู่มีประเภทย่อย: ปฐมภูมิ / กลับเป็นซ้ำ / หายไป CSC แบบซับซ้อนมีความเสี่ยงสูงต่อการเกิดเส้นเลือดใหม่ในคอรอยด์ (MNV) เมื่อเทียบกับ CSC แบบง่าย ค่าสัมประสิทธิ์ความสอดคล้องระหว่างผู้เชี่ยวชาญจอประสาทตา 10 คนคือ κ=0.57 (ปานกลาง) และการจำแนกประเภทกำลังได้รับการปรับปรุงอย่างต่อเนื่อง 9)
พบพาคิดรูเซนในผู้ป่วย CSC มากกว่า 40% 9) ตา CSC ที่มีพาคิดรูเซนมีความผิดปกติของ RPE ที่กว้างขวางกว่า และมีรูปร่างและการกระจายตัวแตกต่างจากดรูเซนชนิดอ่อนทั่วไป มีการแสดงความสัมพันธ์ระหว่างความหนาของชั้น Haller และการบางลงของเส้นเลือดฝอยคอรอยด์ 9)
PBM เป็นการรักษาแบบใหม่ที่ไม่ใช้เวอร์เทพออร์ฟิน โดยฉายแสงผสมระหว่าง LED สีเหลือง 590 นาโนเมตรและ LED สีแดง 625 นาโนเมตร 5) คาดหวังให้เป็นการรักษาทางเลือกในสถานการณ์ที่ขาดแคลนเวอร์เทพออร์ฟิน
การมีลักษณะพาคิคอรอยด์มีความสำคัญมากขึ้นในฐานะปัจจัยพยากรณ์โรคของโรคนี้ ในกลุ่มพาคิคอรอยด์ อัตราการกลับเป็นซ้ำสูงกว่า (31.2% เทียบกับ 10.4%) และอัตราการหายเองต่ำกว่า (28.8% เทียบกับ 48%) เมื่อเทียบกับกลุ่มที่ไม่ใช่พาคิคอรอยด์ 3) การมีลักษณะพาคิคอรอยด์เป็นตัวบ่งชี้สำคัญในการกำหนดแนวทางการรักษา
มีรายงานการเกิดโรคนี้ครั้งแรกหรือกลับเป็นซ้ำหลังการฉีดวัคซีน COVID-19 สะสมมากขึ้น 6) มีข้อเสนอว่าการกระตุ้นแกน HPA โดยวัคซีนและฤทธิ์คล้ายฮอร์โมนสเตียรอยด์อาจเกี่ยวข้อง