中心性漿液性脈絡膜 視網膜 病變(CSC )是一種在黃斑部 引起漿液性視網膜剝離 (SRF)的疾病,螢光素 眼底血管造影(FA )可見RPE 層級的螢光滲漏。
好發於30~40歲男性,男女比約為8:1。
類固醇 是最大的危險因子(OR 37.1),所有給藥途徑均有發病風險。大多數典型病例在3-4個月內自行緩解,但如果SRF持續超過6個月,則作為慢性型需要積極治療。
慢性型的第一線治療是半劑量PDT (光動力療法 )。PLACE試驗顯示其顯著優於微脈衝雷射 ,SPECTR A試驗顯示12週時SRF完全消退率為78%,而依普利酮為17%9) 。
它是厚脈絡膜 疾病譜的一部分,厚脈絡膜 組的自然消退率低於非厚脈絡膜 組(28.8% vs 48%)3) 。
FA 和OCT 的結合是診斷的基礎,IA有助於評估脈絡膜 異常和鑑別診斷。 中心性漿液性脈絡膜 視網膜 病變(Central Serous Chorioretinopathy; CSC )是一種在黃斑部 發生漿液性視網膜剝離 (SRF)的疾病。螢光素 眼底血管造影(FA )顯示視網膜色素上皮 (RPE )層次的螢光滲漏。它被認為是繼年齡相關性黃斑部 病變、糖尿病視網膜病變 和視網膜靜脈阻塞 之後第四常見的視網膜 疾病。1866年von Graefe將其描述為「中心性復發性視網膜 炎」,1967年Gass等人命名了現在的病名。在日本,以前通常僅指黃斑部 局限性視網膜剝離 的典型病例(所謂中心性視網膜 炎),但現在分為三種亞型。許多病例可自行癒合,但SRF持續存在的病例視力 預後可能惡化。
流行病學上,男性發生率為每10萬人9.9例,女性為1.7例,男女比例約為8:14) 。一項250隻眼的研究顯示平均年齡46.6歲,男性佔88.4%3) 。
本病有以下三種亞型。
典型型
患者族群 :以30-40歲男性為主。通常單眼發病。
病理 :黃斑部 局限性漿液性視網膜剝離 。
病程 :大多數在3-4個月內自行吸收。視力 預後通常良好。
慢性型
患者族群 :多見於老年人。常為雙眼發病。近期有增加趨勢。
病理生理 :廣泛的RPE 損傷。常反覆發作。
病程 :SRF持續6個月以上。需要積極治療5) 。
泡狀視網膜剝離
患者族群 :多見於大量使用類固醇 的病例。相當於日本以前稱為多發性後極部視網膜色素上皮 病變的疾病。
病理生理 :伴有泡狀視網膜剝離 的重症型。伴有大型RPE 剝離(PED )和多發性白色斑紋。
病程 :SRF的範圍常波及眼底下方,視力 預後可能較差。
復發率很高,一年內高達50%。本病被認為是厚脈絡膜 疾病譜(以脈絡膜 增厚為特徵的疾病群)的一部分3) 9) 。
Q
能自然痊癒嗎?
A
典型病例常在3~4個月內自然緩解,視力 預後一般良好。但一年內復發率高達50%。若SRF持續6個月以上,則視為慢性型,需要PDT 等治療。在厚脈絡膜 組中,自然消退率低於非厚脈絡膜 組(28.8% vs 48%),復發率也更高(31.2% vs 10.4%),需注意3) 。
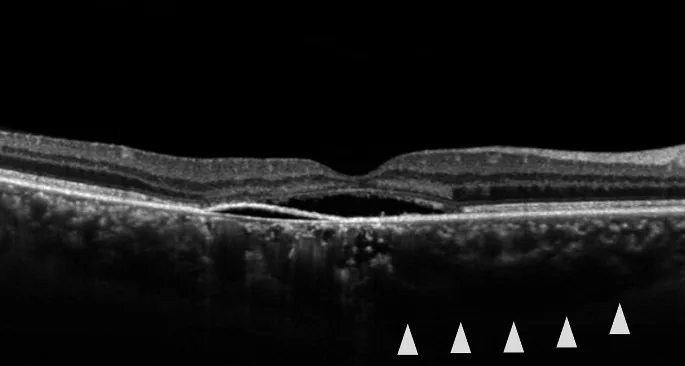
中心性漿液性脈絡膜視網膜病變的OCT。黃斑部可見漿液性視網膜剝離和輕度PED。 Koizumi H, et al. Central serous chorioretinopathy and the sclera: what we have learned so far. Jpn J Ophthalmol. 2024. Figure 4. PM
CI D: PMC11420308. License: CC BY.
黃斑部 OCT 顯示中心凹下伴有視網膜下液 的淺層漿液性視網膜剝離 。還可見RPE 小隆起和提示脈絡膜 增厚的表現,顯示了中心性漿液性脈絡膜 視網膜 病變的臨床影像。
視力 下降遠視 化(hyperopic shift)。視物變形 :物體看起來扭曲。與中心暗點 一樣,是患者不適的症狀,可能影響駕駛和工作。小視症 :物體看起來比實際小。中心暗點 對比敏感度 下降色覺異常 (後天性藍黃色覺異常 )。
當視網膜下液 被吸收後,中心暗點 和變視症 會相對較早改善。另一方面,小視症和對比敏感度 下降可能持續存在。慢性型容易復發,視力 不良的病例較多。典型病例多為單眼性,而慢性型和泡狀視網膜剝離 多為雙眼性。
透過裂隙燈 顯微鏡和各種影像檢查可觀察到以下所見。
漿液性視網膜剝離 (SRF)黃斑部 無出血的圓形或橢圓形隆起。視網膜色素上皮剝離 (PED )OCT 上最多63%可見。沉澱物 :剝離視網膜 後面的白色點狀沉積物。多見於色素上皮剝離和漿液性視網膜剝離 的好發部位。視網膜 下纖維蛋白沉積(白色斑紋)脈絡膜 增厚OCT (增強深度成像OCT )評估。正常為250~300μm,而本病為350~450μm以上。厚脈絡膜 組的中心凹下脈絡膜 厚度(SFCT)據報導為406.6±80.8μm 3) 。部分病例可達500μm。Haller層血管擴張和Sattler層變薄 :EDI-OCT 可確認的脈絡膜 結構特徵性變化 3) 。
慢性型中,色素上皮損傷廣泛,有時可見伴有色素上皮萎縮索並向下延伸的視網膜剝離 。泡狀視網膜剝離 中,視網膜剝離 嚴重,常波及眼底下方,伴有大型色素上皮剝離和多發性白色斑紋。
本病的根本原因尚未明確,但脈絡膜 血管通透性亢進被認為是本質。已知壓力和類固醇 與本病的發病和惡化有關。以下風險因素已被報導。
風險因子 關聯強度 備註 類固醇 OR 37.11) 所有給藥途徑 A型性格 中等 壓力相關 懷孕 0.008%/年7) 產後自然緩解常見 OSA 61%的患者9) 交感神經亢進 PDE5抑制劑 病例報告8) 停藥後消退
類固醇 全身性紅斑狼瘡 (SLE )患者使用類固醇 後發病的報告,OR值為37.1(95% CI 6.2–221.8),極高1) 。類固醇 與本病的發生和惡化有關,因此對於正在使用的患者,考慮停藥或減量非常重要。需與其他科別協作,根據個別病例處理。精神科藥物 :有服用喹硫平(非典型抗精神病藥)後發病的報告。停藥2週後最佳矯正視力 改善,2個月後完全消退2) 。PDE5抑制劑 :有服用他達拉非5mg後發病,停藥3個月後消退的病例報告8) 。懷孕 :懷孕期間的發病率為每年0.008%7) 。OSA(阻塞性睡眠呼吸中止症) :61%的患者有OSA9) 。COVID-19疫苗 :有接種後復發的報告,認為與HPA軸活化有關6) 。幽門螺旋桿菌感染 :53–69%的患者有幽門螺旋桿菌感染,OR值為4.6。
發病機制以多因素假說(multi-hit theory)解釋9) 。認為分為三個階段:①解剖學易感因素(短眼軸 、鞏膜 增厚、渦靜脈引流不對稱等),②誘發事件(類固醇 、壓力、OSA等),③代償失調。
避免壓力,保持規律生活。
正在使用類固醇 藥物的患者,請勿自行停藥,如出現眼部症狀請諮詢醫師。
如有睡眠呼吸中止症,接受適當治療(如CPAP)非常重要。
吸菸可能會增加風險,因此建議戒菸。
Q
類固醇與中心性漿液性脈絡膜視網膜病變有什麼關係?
A
類固醇 是本病最大的風險因子,無論是點眼、吸入、注射或口服,所有給藥途徑都會增加風險。據報告,勝算比高達37.11) 。如果確診本病且正在使用類固醇 ,請與主治醫師討論,並盡可能考慮減量或停藥。如果因全身性疾病而使用類固醇 ,則需要每例患者與其他科室協作處理。
本病的診斷以FA 和OCT 的組合為基礎。主要檢查的特點如下所示。
檢查 特徵性所見 主要作用 FA 點狀螢光素 滲漏 確定滲漏點和治療計劃 IA(ICG) 脈絡膜 高螢光評估脈絡膜 異常和鑑別診斷 OCT 顯示SRF和色素上皮剝離 追蹤和定量
各項檢查的詳細內容如下。
螢光素眼底血管攝影 (FA )RPE 的點狀螢光素 滲漏,攝影早期出現點狀強螢光,隨時間擴大並積聚在視網膜 下。滲漏形態有噴出型 和圓形增大 兩種。典型的滲漏模式為墨漬樣(31%)和煙囪樣(12%)。典型病例滲漏點常為單個,而大泡性視網膜剝離 常可見多個滲漏點。慢性型可見顆粒狀強螢光和晚期瀰漫性弱螢光滲漏,常難以識別單個滲漏點。靛青綠血管攝影(IA/ICG) :攝影中期可見脈絡膜 強螢光(異常脈絡膜 組織染色)。此徵象見於所有類型,但與典型病例相比,慢性型和大泡性視網膜剝離 範圍更廣、程度更強,且為雙眼性。有助於評估厚脈絡膜 變化及鑑別診斷(CNV /PCV )。OCT 視網膜剝離 尤為有效。還可觀察到光感受器外節線性延長(冰柱樣改變)。EDI-OCT (頻域OCT 的脈絡膜 觀察模式)可準確評估脈絡膜 厚度。正常中心凹下脈絡膜 厚度為250300μm,而本病為350450μm(部分病例超過500μm),形態學上也證實了脈絡膜 異常。OCTA (OCT血管攝影 )脈絡膜 微血管的血流障礙(陰影效應)6) 。眼底自發螢光(FAF ) :急性期呈強螢光,慢性期呈廣泛弱螢光。有助於評估RPE 損傷範圍。慢性CSC 中可見邊緣強螢光的帶狀弱螢光(萎縮帶),有助於推測病程和確認視網膜下液 向下移動。
滲出型年齡相關性黃斑部 病變(尤其是息肉狀脈絡膜血管病變 ;PCV ) :通過ICG攝影確認息肉狀病變。50歲以上患者是特別重要的鑑別診斷。特發性脈絡膜新生血管 :發生於年輕患者時需鑑別。IA有助於鑑別。Vogt-小柳-原田病 (VKH)全葡萄膜炎 症狀、多發性漿液性視網膜剝離 。視盤小凹 黃斑 病變視盤小凹 相關的SRF。狼瘡性脈絡膜 視網膜 病變 :女性、活動性SLE 、雙眼性SRF需與本病鑑別1) 。視網膜 血管病視網膜靜脈阻塞 、糖尿病黃斑 病變等引起黃斑部 視網膜剝離 的疾病鑑別。脈絡膜 腫瘤高血壓及妊娠高血壓症候群 :可繼發性引起黃斑部 SRF。裂孔性視網膜剝離 視網膜剝離 病例中需要鑑別。
目前尚無針對本病的既定藥物治療。對螢光素眼底血管攝影 (FA )上的螢光滲漏點進行雷射光凝是目前唯一普遍接受的治療方法,治療方針根據類型、分期和滲漏點位置決定。
典型的急性型有自然緩解趨勢,初發急性期可等待4-6個月讓視網膜下液 自然吸收。典型病例常在3-4個月內完全吸收,視力 預後良好。非厚脈絡膜 組的自然消退率為48%,而厚脈絡膜 組僅為28.8%3) 。
如果自覺症狀嚴重且患者希望早期改善,即使是急性典型病例也可考慮光凝治療。若正在使用類固醇 ,應盡可能減量或停用。若因全身疾病使用類固醇 ,需與相關科室協作個別處理。
對於發病後4-6個月以上仍持續剝離的病例、復發病例、重症病例,或對側眼因本病殘留視力 障礙的病例(慢性型、大疱性視網膜剝離 ),需要透過治療促進視網膜下液 早期吸收,因為黃斑 損傷會導致視力 預後不良。
適用於滲漏點距中心凹500μm以上且至少位於中心凹無血管區之外的情況。直接光凝FA 上確定的滲漏點(200μm光斑、0.2秒、70-120mW)。光凝強度應為弱光凝,在視網膜 深層產生淡灰白色光凝斑 。即使滲漏位於視盤黃斑 之間,弱光凝也無問題。若滲漏位於色素上皮剝離內,僅需光凝滲漏點。
光凝有效時,視網膜剝離 在數週內消退。但自覺症狀的改善通常需要更長時間。併發症包括中心凹誤照、術後脈絡膜新生血管 (CNV )形成(長波長、短時間、小光斑光凝更易發生)等。
使用577nm黃色雷射。設定參數為240mW、200μm光斑、200ms、5%工作週期進行照射4) 。由於能量選擇性作用於RPE ,不形成疤痕。可直接照射中心凹下方。
Bodea F等人(2024)報告,接受MPLT治療的中心性漿液性脈絡膜 視網膜 病變患者,治療後2週SRF減少,6週消退4) 。
對於妊娠期本病,微脈衝雷射 被認為是唯一安全的治療選擇7) 。
觀察追蹤
適應症 :急性典型病例的第一線治療。
期間 :4-6個月。等待自然吸收。
注意 :使用類固醇 期間,應與其他科室協調考慮減量或停藥。
PDT(光動力療法)
適應症 :慢性中心性漿液性脈絡膜 視網膜 病變的第一線治療。
方法 :推薦半劑量(半光通量)PDT 。
證據 :PLACE試驗和SPECTR A試驗(12週SRF消退率78% vs 依普利酮17%)證明了其有效性9) 。
微脈衝雷射
特點 :無疤痕,可直接照射中心凹下方。
優勢 :是唯一可在妊娠期使用的治療方法7) 。
效果 :2週時SRF減少,6週時消退4) 。
用於滲漏點位於中心凹無血管區或慢性型等無法進行雷射光凝的病例。使用維替泊芬(Visudyne)的半劑量PDT (常規劑量的一半)或半光通量PDT (一半雷射輸出)被推薦為慢性中心性漿液性脈絡膜 視網膜 病變的第一線治療9) 。
主要臨床試驗結果如下9) 。
PLACE試驗 :半劑量PDT 在SRF消退率、BCVA改善、視網膜 敏感度和RPE 剝離高度等所有指標上均顯著優於微脈衝雷射 (HS ML)。SPECTR A試驗 :半劑量PDT 相比依普利酮,SRF完全消退率顯著較高(12週時:78% vs 17%)。12個月時,初始PDT 組的BCVA優於依普利酮→延遲PDT 組。REPLACE試驗 :HS ML無效的患者交叉至半劑量PDT 後改善。交叉1年後,PDT 組SRF完全消退率為78%(32眼中),HS ML組為67%(10眼中)。僅PDT 組視網膜 敏感度改善。SPECS試驗 :依普利酮無效的患者交叉至半劑量PDT 後改善。交叉3個月後,PDT 組SRF完全消退率為87.5%(37眼中),HS ML組為22.2%(9眼中)。PDT 實施時機的重要性視力 改善的可能性越低。據報導,每延遲1週,可能性降低4%,因此適時介入很重要9) 。對57隻半劑量PDT 眼的分析未發現中心凹萎縮病例9) 。
礦物皮質激素受體拮抗劑。每日50mg使用。在VICI 試驗 (多中心隨機雙盲安慰劑對照試驗)中,治療12個月後,依普利酮在BCVA改善方面與安慰劑相比無顯著差異9) 。其效果被認為不如PDT ,有病例報告顯示即使治療10個月仍無效5) 。
一種新療法,使用590nm黃色LED和625nm紅色LED各照射6分鐘5) 。有病例報告顯示,對於依普利酮無效的慢性中心性漿液性脈絡膜 視網膜 病變伴漿液性色素上皮剝離,最佳矯正視力 從20/80改善至20/25,中心視網膜 厚度從752μm減少至296μm(1個月時)5) 。
類固醇 眼藥水或全身給藥可能加重或延長病程,原則上應避免使用。使用維替泊芬的PDT 可能出現藥物供應問題。PBM作為替代方案正在研究中5) 。
依普利酮需注意高鉀血症等副作用。
慢性型視功能障礙持續時,建議儘早考慮在專業機構治療。
Q
懷孕期間發生中心性漿液性脈絡膜視網膜病變該怎麼辦?
A
據報導,妊娠期本病的發生率為0.008%/年7) 。多數病例在產後3個月內自然緩解。如果需要治療,微脈衝雷射 (MPLT)被認為是妊娠期唯一安全的選擇,並且可以直接照射到中心凹下方而不留疤痕7) 。
Q
選擇哪種治療方法?
A
對於急性典型病例,基本是觀察4-6個月。對於SRF持續超過6個月的慢性型,半劑量PDT 是第一線選擇9) 。SPECTR A試驗顯示,12週時SRF完全消退率在PDT 組為78%,依普利酮組為17%,差異顯著。如果滲漏點在中心凹無血管區外側,選擇雷射光凝(弱凝固);在中心凹正下方或妊娠期,選擇微脈衝雷射 。依普利酮在VICI 試驗中與安慰劑相比,BCVA改善無顯著差異9) 。
本病的發病機轉以「脈絡膜 血管通透性增加」為中心,由複合機轉解釋。根據IA研究,原發病灶在脈絡膜 ,繼發性引起RPE 損傷。為什麼脈絡膜 會發生病變,目前仍有許多不明之處。已知壓力和類固醇 與本病的發生和惡化有關。
脈絡膜 血管(主要是Haller層擴張血管)通透性增加脈絡膜 間質壓升高、脈絡膜 增厚RPE 外側血-視網膜屏障 破壞RPE 幫浦功能下降SRF在視網膜 下腔積聚
在FA 上表現為色素上皮的螢光滲漏和視網膜 下染料積存。OCT 研究顯示,本病患者脈絡膜 較正常眼增厚,形態學上也證明了脈絡膜 異常。
Cheung CMG等人(2025)用多重打擊理論解釋本病的發病機轉9) 。
解剖學易感性 :短眼軸 、鞏膜 增厚、渦靜脈引流分布不對稱等。本病在近視 眼中罕見,眼球形態參與發病機制。誘發事件 :類固醇 、壓力、OSA、藥物使用等。無明顯誘因的病例也不少見。代償機制的活化 :Haller層血管擴張、渦靜脈吻合形成(約90%的厚脈絡膜 疾病譜中存在10) )。代償失調 :脈絡膜 毛細血管缺血→RPE 損傷→外層視網膜 萎縮→惡性循環9) 。
CSC 眼的前部和後部鞏膜 顯著厚於正常眼9) 。由於渦靜脈斜行穿過鞏膜 (鞏膜 內走行約4mm),鞏膜 增厚可能增加靜脈流出阻力,導致脈絡膜 充血 9) 。62%的CSC 眼可見脈絡膜 上腔液體積聚(loculation of fluid),19%可見睫狀體 脈絡膜 滲出(ciliochoroidal effusion)9) 。在類固醇 誘發的CSC 中,鞏膜 比特發性CSC 更薄,提示鞏膜 在發病機制中的作用可能不同9) 。
PDE5抑制劑(如他達拉非) :通過增加cGMP/NO擴張和增厚脈絡膜 血管,誘發本病8) 。喹硫平 :推測通過D1受體介導的血管擴張機制2) 。
基於多模態影像的新分類已被提出9) 。
簡單型 :RPE 異常總面積≤2 DA(視盤面積)複雜型 :RPE 異常總面積>2DA或多灶性非典型型 :大泡型、RPE 撕裂、合併其他視網膜 疾病
每個類別內又分為初發、復發和消退亞類。複雜型CSC 發生脈絡膜新生血管 (MNV)的風險高於簡單型CSC 。10名視網膜 專家之間的一致性κ=0.57(中等),分類仍在持續改進中9) 。
超過40%的CSC 患者存在厚玻璃膜疣 9) 。伴有厚玻璃膜疣 的CSC 眼RPE 異常更廣泛,其形態和分佈與傳統軟性玻璃膜疣 不同。已顯示Haller層增厚與脈絡膜 毛細血管變薄相關9) 。
PBM作為一種不使用維替泊芬的新療法備受關注。它採用590nm黃色LED和625nm紅色LED組合照射5) 。在維替泊芬供應不足的情況下,它被期待作為替代治療。
厚脈絡膜 表現的有無作為本病的預後預測因子日益重要。與非厚脈絡膜 組相比,厚脈絡膜 組的復發率更高(31.2% vs 10.4%),自然消退率更低(28.8% vs 48%)3) 。厚脈絡膜 表現的有無是決定治療方案的重要指標。
COVID-19疫苗接種後本病發病和復發的報告不斷積累6) 。提示疫苗可能通過激活HPA軸和類固醇 激素樣作用參與其中。
Rao Q, Wang R, Liu C, et al. Systemic lupus erythematosus combined with central serous chorioretinopathy treated with glucocorticoids. J Int Med Res. 2023;51(3):03000605231163716.
Durmaz Engin C, Güngör SG, Yıldız Şeker DY. Central serous chorioretinopathy following oral quetiapine. GMS Ophthalmol Cases. 2023;13:Doc13.
Bhattacharyya S, Ghorpade A, Mandal S, et al. Presentation and outcome of central serous chorioretinopathy with and without pachychoroid. Eye (Lond). 2024;38:127-131.
Bodea F, Munteanu M, Balica NC, et al. Micropulse Laser Therapy in Central Serous Chorioretinopathy. Clin Pract. 2024;14:2484-2490.
Iovino C, Coppola M, Gioia AD, et al. Photobiomodulation therapy for serous pigment epithelial detachment in chronic central serous chorioretinopathy. Retinal Cases Brief Rep. 2025;19:766-770.
Sanjay S, Leo SW, Au Eong KG. Recurrent central serous chorioretinopathy following COVID-19 vaccination. Am J Ophthalmol Case Rep. 2022;27:101644.
Ochinciuc R, Roșca C, Zaharia IM, et al. Central serous chorioretinopathy in pregnancy. Rom J Ophthalmol. 2022;66(4):382-385.
Alsarhani A, Alsulaiman R, Aljehani M, et al. Central serous chorioretinopathy associated with Tadalafil. Case Rep Ophthalmol. 2022;13:1008-1011.
Cheung CMG, Lai TYY, Gomi F, et al. Pathogenesis and management of pachychoroid disease spectrum. Eye (Lond). 2025;39:819-834.
Ochinciuc U, Pop RM, Mălāescu GD, et al. Vortex vein anastomosis in pachychoroid spectrum disease. Clin Ophthalmol. 2023;17:53-62.
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。