乾性角結膜炎

全身性紅斑性狼瘡(SLE)的眼部症狀
一目了然的要點
Section titled “一目了然的要點”1. 什麼是全身性紅斑性狼瘡(SLE)?
Section titled “1. 什麼是全身性紅斑性狼瘡(SLE)?”全身性紅斑性狼瘡(SLE)是一種由於免疫系統慢性過度活化而導致全身多器官發炎的自體免疫疾病。它被列為經典的五大膠原病之一。
好發於2030多歲的女性。男女比例約為1:81:9,女性占絕對多數。亞洲人較多,白種人較少。盛行率約為每10萬人50~100人。
SLE的診斷標準演變如下。
- 美國風濕病學會(ACR)標準(1997年最終修訂):11項臨床和免疫學項目中符合4項或以上即可診斷
- SLICC標準(2012年):擴展至17項,符合4項或以上即可診斷
- 歐洲風濕病聯盟/美國風濕病學會標準(2019年):抗核抗體(ANA)陽性為必要條件,加權總分≥10分即可診斷
根據美國風濕病學會修訂的診斷標準,在病程中符合以下11項中的4項或以上即可診斷:蝶形紅斑、盤狀紅斑、光敏感、口腔潰瘍、關節炎、漿膜炎、腎臟病變、神經系統病變、血液學異常、免疫學異常、抗核抗體陽性。
此外,在葡萄膜炎診療指引中,SLE被視為膠原病相關葡萄膜炎的鑑別診斷疾病1)。需結合眼部表現和全身症狀,並與風濕免疫科協作評估。
不包含。約30%的患者出現眼部症狀,但眼部症狀本身不屬於SLE的診斷標準項目。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”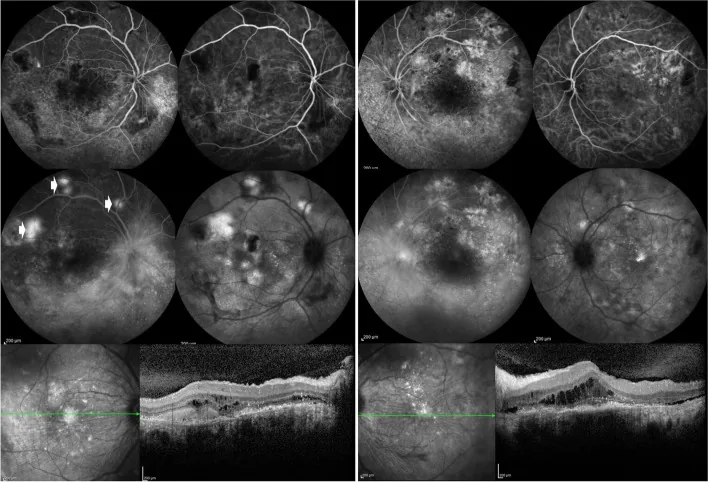
約33%至50%的患者出現眼部主訴。症狀從輕度刺激感到嚴重視力下降不等。
- 乾澀感和異物感:最常見的主訴。由繼發性乾燥症候群引起的乾眼症所致。伴有灼熱感、視力模糊,傍晚症狀加重。
- 視力下降:發生於狼瘡性視網膜病變和視神經炎。從無症狀的眼底變化到急劇的視力下降,表現多樣。
- 眼痛:視神經炎的特徵是眼球運動時加重的眼眶周圍疼痛。
- 畏光(刺眼):伴隨乾眼症或眼前段發炎出現。
- 色覺異常:視神經炎幾乎全部病例均出現紅綠色覺障礙。
SLE的眼部病變多樣,可累及眼球幾乎全層。
| 部位 | 主要所見 |
|---|---|
| 眼前段 | 乾性角結膜炎、鞏膜炎、上鞏膜炎 |
| 眼後段 | 軟性滲出、視網膜出血、血管閉塞 |
| 神經眼科 | 視神經炎、眼球運動障礙 |
狼瘡性視網膜病變是最重要的後段病變。通常為雙眼性,多見於疾病活動性高的時期。
- 軟性白斑(棉絮斑):最常見的視網膜表現
- 視網膜出血和Roth斑:由局部循環障礙引起
- 微動脈瘤和硬性滲出:基於微血管病變
- 血管迂曲和鞘形成:血管炎的徵象
- 動靜脈阻塞:也可能發生視網膜中央動脈阻塞(CRAO)和視網膜中央靜脈阻塞(CRVO)
- 漿液性視網膜剝離和視網膜色素上皮剝離:推測與脈絡膜循環障礙或口服類固醇有關
抗心磷脂抗體陽性與狼瘡性視網膜病變,尤其是阻塞性病變相關2)。
- 乾燥性角結膜炎:約30%的患者出現。為淚液分泌減少型乾眼。
- 鞏膜炎:前部瀰漫性或結節性鞏膜炎見於少數患者。對類固醇反應良好。壞死性鞏膜炎可能重症化。
- 盤狀病變:累及眼瞼時可引起瘢痕性眼瞼內翻或眼瞼外翻。
神經眼科表現
Section titled “神經眼科表現”- 視神經炎:約1%發生。可見視盤蒼白或水腫、相對性傳入性瞳孔障礙(RAPD)。
- 眼球運動障礙:中樞神經系統病變導致動眼神經和展神經受損。約30%出現。
合併葡萄膜炎的情況意外地少見。SLE可能合併虹膜睫狀體炎,但通常較輕微。如果出現葡萄膜炎,應考慮其他原因。
3. 原因與風險因素
Section titled “3. 原因與風險因素”已鑑定出80多個與SLE相關的基因位點變異。易感基因和保護基因的複雜平衡參與發病。
- 紫外線(UV)暴露:作為光過敏誘發SLE發病
- 病毒抗原暴露:感染可成為誘因
- 藥物:使用普魯卡因胺、肼屈嗪、氯丙嗪等
- 其他:手術、外傷、精神壓力
女性佔絕對多數,提示雌激素及其他荷爾蒙的參與。育齡期高發支持這一假說。
視網膜病變的風險因素
Section titled “視網膜病變的風險因素”狼瘡性視網膜病變與疾病控制不佳相關。抗心磷脂抗體陽性在閉塞性病變的發生中起重要作用2)。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”SLE的診斷建議以下檢查:
- 血液檢查:全血細胞計數(CBC)、基礎代謝面板(BMP)
- 免疫學檢查:抗核抗體(ANA)、抗dsDNA抗體、抗磷脂抗體
- 發炎標誌物:紅血球沉降速率(ESR)、CRP、C3/C4值
- 其他:抗SS-A抗體、抗SS-B抗體(評估繼發性乾燥症)
特別是抗核抗體在活動期大多數病例呈陽性,有助於掌握病情。作為葡萄膜炎篩檢,也應確認葡萄膜炎診療指南建議的基本項目(HLA-B27、胸部X光、梅毒血清反應、QFT-3G、ACE、ANA)1)。
乾性角結膜炎的評估
Section titled “乾性角結膜炎的評估”- 淚液半月面測量:小於1mm為異常
- 淚膜破裂時間(TBUT):小於10秒為異常
- 角結膜染色:使用螢光素、玫瑰紅或麗絲胺綠
- Schirmer試驗:無麻醉下≥15mm為正常,點眼麻醉下≥5mm為正常
視網膜病變的評估
Section titled “視網膜病變的評估”- 眼底檢查:散瞳下評估棉絮狀白斑、出血和血管異常
- 螢光眼底造影(FFA):對評估視網膜血管炎和血管阻塞很重要。可檢測滲漏、毛細血管擴張、阻塞和微血管瘤
- 吲哚青綠(ICG)造影:檢測FFA無法顯示的脈絡膜病變,表現為脈絡膜過螢光
- OCT-A(光學同調斷層掃描血管攝影):可能有助於監測亞臨床視網膜病變的視網膜結構變化(研究階段)
視神經炎的評估
Section titled “視神經炎的評估”- 螢光眼底造影:確認視盤周圍毛細血管的擴張、填充缺損和過螢光滲漏
- 釓增強MRI:檢測視神經或視交叉的增大和增強
SLE的多樣症狀需要與其他疾病鑑別。
- 其他自體免疫疾病:類風濕性關節炎、混合性結締組織病、修格連氏症候群
- 血管炎:結節性多動脈炎、貝西氏病
- 視網膜病變的鑑別:糖尿病視網膜病變(HbA1c升高)、高血壓視網膜病變(動靜脈交叉現象)、類肉瘤病(常伴葡萄膜炎)
5. 標準治療方法
Section titled “5. 標準治療方法”SLE眼部症狀的治療最重要的是控制原發病。與風濕免疫科醫師的協作必不可少。
原發病治療的基礎是全身性糖皮質激素給藥。
- 無眼或中樞神經系統症狀時:潑尼松龍(PSL)30~40 mg/日
- 有眼或中樞神經系統症狀時:PSL 1 mg/kg/日,給藥3~4週後,根據症狀和發炎標誌物逐漸減量
- 活動性狼瘡視網膜病變:甲潑尼龍1 g/日×3天靜脈滴注(脈衝療法),之後從潑尼松片40~60 mg/日開始逐漸減量
對於因視網膜血管炎導致進行性血管阻塞的病例,需要抗凝血治療。華法林片2~5 mg/日,調整至PT-INR 1.5~2。
對於類固醇效果不充分或類固醇抵抗的病例,使用以下藥物:
生物製劑(最新)
Section titled “生物製劑(最新)”- 貝利木單抗(Benlysta®):BLyS/BAFF抑制劑。SLE適應症。BLISS-52試驗證實可顯著降低疾病活動性3)
- 阿尼魯單抗(Saphnelo®):抗IFNAR1抗體(I型IFN受體抑制劑)。2022年在日本核准。顯著改善中重度SLE的疾病活動性4)
- 伏環孢素(鈣調神經磷酸酶抑制劑):用於狼瘡性腎炎
廣泛用於減少SLE的復發。眼科方面需注意視網膜毒性(參見「羥氯喹的眼毒性」一節)。
眼部局部治療
Section titled “眼部局部治療”視網膜病變的治療
Section titled “視網膜病變的治療”- 視網膜光凝固術:螢光眼底攝影確認視網膜新生血管時,為預防玻璃體出血立即施行。對廣泛的視網膜血管閉塞也進行預防性治療。
- 玻璃體手術:用於增殖性玻璃體視網膜病變。
- 血漿分離交換術:用於重症病例。
- 漿液性視網膜剝離:通過螢光眼底攝影確認視網膜色素上皮層的螢光滲漏點,對該滲漏點進行視網膜光凝固術。
視神經炎的治療
Section titled “視神經炎的治療”- 甲基普立朗靜脈脈衝療法:每日1克,連用3天,之後口服普立朗每日1毫克/公斤,逐漸減量。
- 類固醇抵抗:多達三分之一的病例會出現。環磷醯胺靜脈脈衝療法持續6個月。
- 復發:約37%的患者在類固醇減量過程中出現復發,需要再次治療。
羥氯喹的眼毒性
Section titled “羥氯喹的眼毒性”羥氯喹與視網膜色素上皮(RPE)中的黑色素結合,可能引起黃斑部病變。
黃斑部病變的危險因子:
- 終身累積劑量≥1000克(氯喹≥450克)
- 每日劑量≥5毫克/公斤(2016年AAO修訂建議)5)
- 肝功能或腎功能減退
- 肥胖、65歲以上、既往黃斑部病變
毒性徵象:
- 雙側旁中心視野缺損
- 內節外節接合處消失(SD-OCT上的「飛碟」徵)
- 進行性色素變化(經典的「牛眼樣」黃斑病變)
篩檢建議(AAO 2016年修訂)5):
開始治療後5年內僅需基線檢查。5年後建議每年進行Humphrey 10-2視野檢查、SD-OCT和眼底自發螢光檢查。存在高風險因子時,應在5年前開始篩檢。如果發現黃斑病變,應停用藥物。
開始治療後5年內僅需基線檢查,但5年後建議每年進行眼底檢查。Humphrey 10-2視野檢查和SD-OCT是主要的篩檢方法。存在高風險因子(腎功能下降、高劑量、長期使用)的患者應更早開始檢查5)。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”全身性免疫異常
Section titled “全身性免疫異常”SLE的病理基礎是自身耐受喪失和自身抗體過度產生。
- 自身耐受破壞:遺傳和環境因素導致對自身抗原的免疫耐受喪失
- T細胞異常:輔助T細胞過度活化,調節性免疫細胞減少
- B細胞成熟異常:B細胞成熟加快,凋亡受抑制。漿細胞壽命延長,產生過量自身抗體
- 第一型干擾素路徑活化:透過BLyS/BAFF介導的B細胞過度活化
- 免疫複合物形成:自身抗體與核、核內和細胞質自身抗原結合,導致發炎性細胞因子釋放
- 組織損傷:慢性發炎、免疫複合物沉積和凋亡細胞清除缺陷導致組織和器官損傷
血管病變的病理學
Section titled “血管病變的病理學”SLE的病理特徵是小血管和毛細血管的纖維素樣壞死性血管炎。纖維素樣物質由纖維蛋白、免疫複合物和補體組成。
視網膜病變的發病機制
Section titled “視網膜病變的發病機制”狼瘡性視網膜病變的病理生理涉及雙重機制。
- 免疫複合物型血管炎:免疫複合物沉積在血管內皮上,激活補體並釋放發炎介質,導致無灌注和缺血。
- 血栓性機制:抗磷脂抗體症候群的發生導致視網膜血管血栓形成。抗心磷脂抗體陽性與閉塞性狼瘡性視網膜病變相關2)。
當無灌注區域擴大時,可能出現新生血管,進而發展為增殖性玻璃體視網膜病變,甚至新生血管性青光眼。
乾性角結膜炎的機制
Section titled “乾性角結膜炎的機制”除了慢性發炎和免疫複合物沉積外,繼發性乾燥症候群的發生是主要原因。自體免疫攻擊淚腺導致淚液分泌減少。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”OCT-A監測亞臨床視網膜病變
Section titled “OCT-A監測亞臨床視網膜病變”光學同調斷層掃描血管攝影(OCT-A)是一種新的影像診斷方法,可以非侵入性評估傳統螢光眼底造影難以檢測的亞臨床視網膜微血管變化。它有望應用於SLE視網膜病變的早期發現和監測,但其有效性仍處於尚未充分研究的階段。
CAR-T療法
Section titled “CAR-T療法”在針對難治性SLE的CD19靶向CAR-T療法,少數治療抵抗性患者報告了無藥物緩解6)。對眼部併發症的長期影響是未來的課題。
生物製劑的應用
Section titled “生物製劑的應用”阿尼魯單抗(I型IFN受體抑制劑)可改善活動性SLE的疾病控制,並有望對眼部併發症產生間接效果4)。眼科領域的個別療效數據仍在累積中。
8. 參考文獻
Section titled “8. 參考文獻”-
日本眼炎症学会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
-
Stafford-Brady FJ, Urowitz MB, Gladman DD, Easterbrook M. Lupus retinopathy. Patterns, associations, and prognosis. Arthritis Rheum. 1988;31:1105-1110.
-
Navarra SV, Guzmán RM, Gallacher AE, et al. Efficacy and safety of belimumab in patients with active systemic lupus erythematosus: a randomised, placebo-controlled, phase 3 trial (BLISS-52). Lancet. 2011;377:721-731.
-
Morand EF, Furie R, Tanaka Y, et al. Trial of anifrolumab in active systemic lupus erythematosus. N Engl J Med. 2020;382:211-221.
-
Marmor MF, Kellner U, Lai TYY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 Revision). Ophthalmology. 2016;123:1386-1394.
-
Mackensen A, Müller F, Mougiakakos D, et al. Anti-CD19 CAR T cell therapy for refractory systemic lupus erythematosus. Nat Med. 2022;28:2124-2132. doi:10.1038/s41591-022-02017-5.
