青光眼前期至開角期
虹膜紅變:瞳孔緣出現微細的新生血管簇。正常血管在虹膜實質內呈放射狀走行,而新生血管在虹膜表面呈不規則、迂曲的圖案。
房角新生血管:可見越過鞏膜突延伸至小樑網上的樹枝狀細血管。眼壓正常至輕度升高。
纖維血管膜:覆蓋小樑網增殖,導致繼發性開角型青光眼。

新生血管性青光眼(NVG)是一種以眼前房隅角纖維血管組織增生為特徵的重症續發性青光眼。視網膜缺血是主要原因,導致VEGF(血管內皮生長因子)增加,虹彩和隅角形成新生血管。纖維血管組織的形成和收縮導致周邊虹彩前粘連(PAS),最終引起不可逆的隅角閉塞。
自20世紀上半葉開始,就有關於視網膜缺血伴虹彩紅變的報導,1960年代以後「新生血管性青光眼」這個術語得以確立。在此之前,曾使用出血性青光眼、充血性青光眼、血栓性青光眼等多種名稱,但現在統一為NVG。
最常見的病因是增殖性糖尿病視網膜病變(PDR)和視網膜靜脈阻塞(RVO),約佔所有病例的三分之二。其他原因包括視網膜剝離、視網膜動脈阻塞和眼缺血症候群(OIS)1)。一項大型回顧性研究(129隻眼)顯示,病因的分佈為:增殖性糖尿病視網膜病變53%、視網膜靜脈阻塞29%、視網膜剝離7%、視網膜動脈阻塞6%、眼缺血症候群2%2)。
病理核心是VEGF介導的前段新生血管形成。Wakabayashi等人對41例繼發於缺血性視網膜疾病的虹膜新生血管和新生血管性青光眼連續病例進行了玻璃體內注射貝伐珠單抗,幾乎所有病例在給藥後48小時內觀察到虹膜新生血管消退12)。這種快速的新生血管消退證實了VEGF在前段新生血管形成中的主要作用。
眼壓輕度升高時無症狀。隨著眼壓升高,出現視物模糊、虹視、眼痛。如果病情急劇惡化,可能伴有類似急性閉角型青光眼發作的劇烈眼痛、頭痛、噁心、嘔吐。另一方面,如果糖尿病視網膜病變或視網膜靜脈阻塞等原發病導致的視力下降先於眼壓升高,則對眼壓升高的自覺症狀可能不明顯。當眼壓極度升高時,會發生大皰性角膜病變,患者可能因異物感和眼痛就診。
本病的分期廣泛採用Shields的四期分類。各期的臨床所見如下。
青光眼前期至開角期
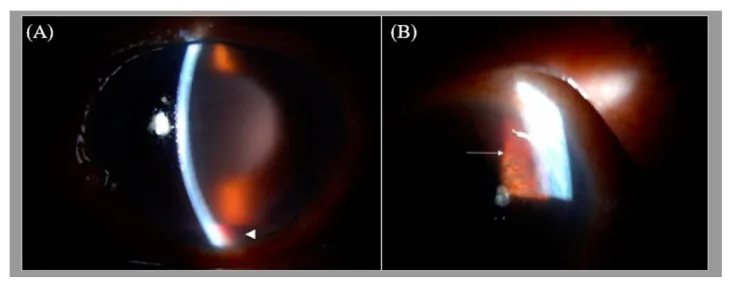
虹膜紅變:瞳孔緣出現微細的新生血管簇。正常血管在虹膜實質內呈放射狀走行,而新生血管在虹膜表面呈不規則、迂曲的圖案。
房角新生血管:可見越過鞏膜突延伸至小樑網上的樹枝狀細血管。眼壓正常至輕度升高。
纖維血管膜:覆蓋小樑網增殖,導致繼發性開角型青光眼。
閉角期至絕對期
葡萄膜外翻:纖維血管膜收縮導致虹膜後方的色素層向前表面翻轉。虹膜表面變得平滑。
周邊虹膜前粘連進展:虹膜被帳篷狀拉向小樑網,導致粘連性隅角閉塞。眼壓顯著升高。
絕對期青光眼:視功能恢復極為困難。高眼壓引起的眼痛成為主要症狀。
一項針對129隻眼的回顧性研究顯示,新生血管性青光眼診斷時,25%為開放隅角,30%為部分閉塞,45%為完全閉塞2)。完全閉塞眼的視力更差(中位數20/4375),眼壓更高(中位數59 mmHg)2)。僅憑臨床所見無法準確預測隅角狀態,因此所有病例均需進行隅角鏡檢查2)。
| 原發疾病 | 頻率 |
|---|---|
| 增殖性糖尿病視網膜病變 | 53%2) |
| 視網膜靜脈阻塞 | 29%2) |
| 視網膜剝離 | 7%2) |
| 視網膜動脈阻塞 | 6%2) |
| 眼缺血症候群 | 2%2) |
在視網膜靜脈阻塞中,缺血型CRVO約在3個月內易發生虹膜新生血管,常被稱為「100天青光眼」(90-day glaucoma)。在增殖性糖尿病視網膜病變中,長期視網膜無灌流區域的累積促進VEGF產生,前段新生血管傾向緩慢進展。眼缺血症候群由於存在內頸動脈閉塞或狹窄,需要透過頸動脈超音波和頭部MRA等進行輔助診斷。
Temkar等人(2023)報告了一例30歲男性因外傷性內頸動脈海綿靜脈竇瘻管(CCF)伴視網膜動靜脈複合阻塞而發展為NVG的病例4)。靜脈淤滯和動脈功能不全導致的嚴重視網膜缺血是NVG發病的機制。
Zakaria等人(2023)報告了一例睫狀視網膜動脈保留型CRAO患者在2週內發展為NVG的病例3)。CRAO中18.2%發生新生血管化,平均在8.5週出現3)。
Fliney等人(2021)報告了一例20歲男性以NVG為首發表現的脈絡膜惡性黑色素瘤病例7)。腫瘤產生的VEGF和FGF是NVG的原因。約2%的脈絡膜黑色素瘤出現眼壓升高,其中大部分為NVG7)。
增殖性糖尿病視網膜病變是NVG最常見的病因,約佔所有NVG的53%2)。但並非所有糖尿病患者都會發展為NVG,血糖控制和通過視網膜光凝管理視網膜缺血對預防發病至關重要。在無灌流區域變得廣泛之前進行全視網膜光凝是抑制前段新生血管發生的關鍵。
早期發現虹膜新生血管是診斷的關鍵。由於散瞳藥會引起血管收縮,使新生血管不易觀察,因此在未散瞳狀態下進行裂隙燈顯微鏡檢查和隅角鏡檢查非常重要10)。在高倍鏡下觀察瞳孔緣,不要漏診早期虹膜新生血管至關重要。
隅角鏡檢查中,可見新生血管越過鞏膜突延伸到小樑網上。有時由於全周周邊虹膜前粘連,隅角內可能無法直接看到新生血管,但如果存在虹膜新生血管,應考慮本病並開始治療。在糖尿病視網膜病變或視網膜靜脈阻塞的追蹤中,需要定期在未散瞳狀態下觀察瞳孔緣,以檢測微小的新生血管。
需要與表現為虹膜紅變的疾病進行鑑別。Fuchs虹膜異色性虹膜睫狀體炎可在虹膜表面出現異常血管,但通常不伴有隅角關閉,且通常不出現纖維血管膜收縮引起的葡萄膜外翻。ICE症候群(虹膜角膜內皮症候群)通常為單眼,伴有角膜內皮異常,並呈現虹膜實質萎縮、虹膜孔形成、瞳孔偏位等特徵性表現,因此可以區分。與炎症性續發性青光眼的鑑別可參考前房細胞和角膜後面沉著物的有無。
治療策略是改善視網膜缺血和控制眼壓並行10)。僅處理一方面無法使病情穩定,需要根據病期將兩者結合。
全視網膜光凝固術(PRP)
抗VEGF藥物
開放隅角期:透過玻璃體內注射VEGF抑制劑使新生血管消退後,再進行PRP
快速消退:Wakabayashi等人的41例連續病例中,IVB給藥後48小時內虹膜新生血管消退12)
術前給藥:術前合併使用抗VEGF藥物可減少術中及術後併發症10)14)(證據等級2B)
抗VEGF藥物的玻璃體內注射(intravitreal bevacizumab: IVB)是新生血管性青光眼藥物治療的核心。一項關於貝伐珠單抗玻璃體內注射的隨機對照試驗報告,與對照組相比,IVB單藥治療NVG顯著促進了眼壓下降和新生血管消退13)。新生血管抑制期一般為3至6週,在此期間完成PRP是理想的。在日本,貝伐珠單抗玻璃體內注射屬於仿單標示外使用,因此必須經過各醫療機構的倫理委員會批准。
按照原發性開放隅角青光眼進行藥物治療10)。抑制房水生成的β阻斷劑和碳酸酐酶抑制劑理論上有效性較高。前列腺素類似物和α2腎上腺素受體激動劑也可合併使用。口服碳酸酐酶抑制劑應在確認無腎功能障礙後進行。高滲劑的靜脈輸注旨在暫時降低眼壓,但效果持續時間短,腎功能減退患者有急性腎衰竭風險,需謹慎。硫酸阿托品滴眼液和皮質類固醇滴眼液可能對消炎和緩解疼痛有效10)。
副交感神經受體激動劑毛果芸香鹼(縮瞳藥)通常無效,並可能因破壞血-房水屏障而導致病情惡化,因此不推薦使用10)11)。
根據病期的治療選擇指南如下。
在IVB使用之前,小梁切除術術中及術後常伴有大量前房出血,常導致濾過功能不全。術前進行IVB可減少圍手術期前房出血,眼壓控制在21 mmHg以下的成功率約為60%。預後不良因素包括年齡小於50歲和有玻璃體手術史。特別是在年輕患者中,周邊虹膜前粘連快速進展的閉角期病例,術後效果往往不佳。近年來微創玻璃體手術的普及減少了結膜疤痕,也有助於提高小梁切除術的療效。
絲裂黴素C合併小梁切除術是首選,最好在新生血管消退後進行10)。對於小梁切除術仍無法降低眼壓或存在活動性新生血管的病例,可選擇引流閥植入術(特別是Ahmed青光眼閥扁平部植入)9)。對於視功能預後不良的眼,進行睫狀體光凝術。無論哪種情況,術前進行全視網膜光凝和抗VEGF藥物治療可減少圍手術期併發症10)14)。
視網膜缺血導致供氧不足時,視網膜細胞釋放VEGF、IL-6等血管生成因子。正常情況下,VEGF水平與抗血管生成因子色素上皮衍生因子(PEDF)保持平衡。當這種平衡向VEGF優勢傾斜時,內皮細胞的活化、增殖和遷移得到促進,導致眼前段新生血管形成。已知房水中VEGF濃度在NVG眼中比健康眼高出數十倍以上,與眼前段新生血管的發生直接相關。
新生血管性青光眼的新生血管壁薄,缺乏肌層,緊密連接缺失,通透性增高。這些新生血管伴有由肌成纖維細胞增殖形成的纖維血管膜。最初,纖維血管膜覆蓋小梁網,增加房水流出阻力,表現為繼發性開角型青光眼。隨後,膜的收縮導致虹膜表面變平、葡萄膜外翻和周邊虹膜前粘連形成,最終導致房角不可逆關閉1)。
初期,纖維血管膜覆蓋小樑網,形成續發性開放隅角青光眼1)11)。隨後,膜收縮導致周邊虹膜前粘連,轉變為粘連性閉塞隅角青光眼。在有水晶體眼中,隅角閉塞更容易進展2),一旦到達此階段,常規濾過手術單獨難以實現長期眼壓控制。只要基礎視網膜缺血持續存在,新生血管和纖維血管膜收縮就會繼續進展,因此通過PRP或抗VEGF療法抑制缺血狀態是治療的根本。
Wang等人(2024)對129隻NVG眼進行研究,探討診斷時隅角狀態的預測因子2)。完全閉塞眼的視力和眼壓均更嚴重,但僅憑臨床特徵無法準確預測隅角狀態。急診就診的病例中完全閉塞的頻率更高,有PRP或玻璃體手術史的眼也傾向於更多隅角閉塞2)。
Soman等人(2022)報告了一例由COVID-19相關視網膜病變引起的快速發作NVG病例5)。一名50歲男性在感染COVID-19三週後出現雙眼視網膜血管病變,右眼在兩週內進展為NVG。其機制被認為是血栓前狀態相關的視網膜血管損傷。通過抗青光眼藥物和PRP,新生血管完全消退,眼壓恢復正常5)。
ALKhamees等人(2023)報告了一名患有Pierson症候群(LAMB2突變)的11歲女孩,出現自發性前房出血、玻璃體出血和新生血管性青光眼8)。觀察到繼發於視網膜缺血的虹膜和隅角新生血管,最終需要睫狀體光凝術,但眼球仍進展為眼球癆8)。