假性水晶體 眼青光眼 是指白內障 術後植入人工水晶體 的眼睛發生的青光眼 ,而無水晶體 眼青光眼 是指未植入人工水晶體 的無水晶體 狀態發生的青光眼 。兩者均屬於續發性青光眼 1) 2) 3) 。青光眼 診療指南第5版將白內障術後青光眼 列為獨立分類項目,在成人和兒童中都是臨床上重要的併發症1) 。
根據發病機轉,大致分為開放隅角 型和閉塞隅角 型6) 。開放隅角 型機轉包括黏彈性物質 殘留、術後發炎、水晶體 顆粒、色素分散、類固醇 青光眼 和鬼影細胞青光眼 。閉塞隅角 型機轉包括瞳孔阻滯 、玻璃體 脫出、周邊虹膜前粘連 和UGH症候群 。白內障 術後發炎性青光眼 由發炎細胞和蛋白質導致的小樑網阻塞、小樑炎、周邊虹膜前粘連 形成等多種機轉重疊發生6) 。
術後一過性眼壓 升高在術後第1天見於29%至50%的患者4) 。但大多數在數日內自然緩解。標準囊外摘除術後慢性青光眼 的盛行率據報導為2.1%至4%。無水晶體 眼術後慢性青光眼 的盛行率約為3%。隨著超音波乳化 術的普及,無水晶體 眼的發生率顯著下降,但在後囊破裂或人工水晶體 植入困難的情況下仍可能發生。
白內障 術後眼壓 波動的機轉因發生時間而異。
時間 主要機轉 術後數小時至1天 黏彈性物質 (OVD )殘留術後1至7天 發炎、出血、水晶體 顆粒 術後1至7週 類固醇 眼藥水引起的眼壓 升高術後數週至數月 UGH症候群 (IOL 偏位)術後數月至數年 色素分散、周邊虹膜前粘連 術後長期 虹膜 摩擦症候群
小兒白內障術後青光眼 是重要的併發症,先天性白內障 術後發生率為18%至26%。在出生後9個月內手術時,發生率高達50%2) 。可能伴有房水 流出通道發育異常,風險持續終生1) 。年輕手術、小角膜 、小眼球為危險因子。
在IRIS Registry超過750萬例的大規模數據中,白內障 術後持續性假性晶體虹膜 睫狀體 炎(PUPPI)的發生率為1.68%5) 。糖尿病患者發病風險升高1.87倍5) 。
Q
現代白內障手術後還會發生青光眼嗎?
A
即使是現代的小切口超音波乳化 術,術後眼壓 升高仍可能發生。但通常為一過性,轉為慢性青光眼 的比例較低,約2%至4%。徹底清除黏彈劑、輕柔操作組織、術後早期監測眼壓 可將風險降至最低。對於已有青光眼 的患者,術後早期眼壓 升高可能加重視神經病變 ,因此需要按照「原因和風險因素」一節 所述進行謹慎管理4) 。
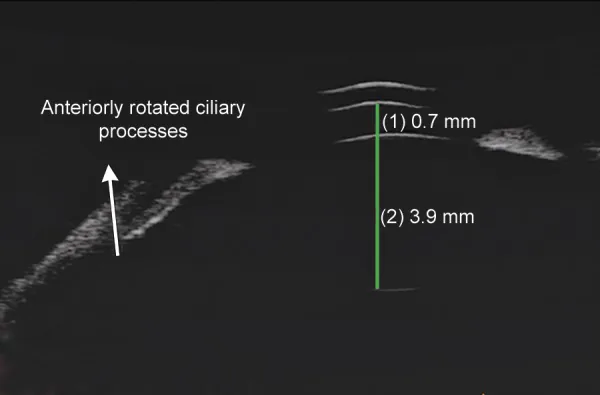
人工水晶體植入眼青光眼中顯示淺前房和睫狀突前旋的UBM影像 Parivadhini A, et al. Management of Secondary Angle Closure Glaucoma. J Curr Glaucoma Pract. 2014. Figure 1C. PM
CI D: PMC4741163. License: CC BY.
眼前段
UBM 顯示
前房 明顯變淺和睫狀突前旋。該影像顯示了
白內障 術後
人工水晶體 植入眼或無
水晶體 眼
青光眼 中所見的
前房 變窄的診斷性表現。
術後早期一過性眼壓 升高 :可能出現眼痛 、視力 模糊、角膜水腫 導致的視力 下降。若由黏彈劑殘留或發炎引起,症狀在術後數小時至數天內出現。慢性病程 :與一般青光眼 一樣,早期無症狀;隨著進展,患者自覺視野缺損 (暗點)。往往直到視野損害嚴重時才被發現。急性瞳孔阻滯 :表現為劇烈眼痛 、頭痛、噁心,與急性青光眼 發作症狀相似。可見虹膜 膨隆和明顯的前房 變淺。UGH症候群 前房 出血導致的一過性視力 下降。反覆出現視力 模糊和充血 。類固醇 青光眼 類固醇 眼藥水期間,眼壓 常無症狀性升高,可能僅透過定期眼壓測量 發現。
開放隅角機制的發現
黏彈性物質 殘留前房 內可見黏彈性物質 殘留。分散型比凝聚型更容易進入小樑網,更難清除,更容易引起眼壓 升高。
術後發炎 :前房 內發炎細胞和閃輝增加。過度發炎可導致小樑網阻塞和纖維化2) 3) 。
類固醇 青光眼 類固醇 眼藥水期間眼壓 升高。效價順序:地塞米松 ≥ 倍他米松 > 氟米龍。具有劑量依賴性,年輕人反應更明顯。
水晶體 顆粒前房 內漂浮白色顆粒。囊外摘除術或YAG雷射 後囊切開術後,殘留的皮質或核碎片可阻塞小樑網。
色素分散 :虹膜 透照缺損 和小樑網色素沉著。單片式IOL 置於睫狀溝時尤其成問題。
閉塞隅角機制的發現
瞳孔阻滯 虹膜 膨隆和前房 變淺。可發生於前房 型IOL 或睫狀溝IOL 2) 。
UGH症候群 葡萄膜炎 、青光眼 和前房 出血三聯徵。IOL 的支撐部直接接觸並摩擦虹膜 或周圍組織,引起發炎。釋放的虹膜 色素堵塞小樑網,導致色素性青光眼 2) 3) 。
虹膜 摩擦症候群虹膜 萎縮和復發性前房 出血。發生於睫狀溝植入的後房型IOL 的支撐部或光學部邊緣持續摩擦虹膜 或隅角 血管。使用抗凝血藥物的患者更容易出血。
玻璃體 脫出前房 內玻璃體 導致急性隅角 關閉。
周邊虹膜前粘連 前房 變淺導致慢性隅角 關閉。
白內障 術後眼壓 升高的機制多種多樣2) 3) 。眼壓 峰值的原因是多因素的,包括手術創傷、水晶體 物質殘留、OVD 殘留、已有的流出道障礙、虹膜 色素釋放、前房 出血和發炎4) 。
主要風險因素包括以下內容。
既有青光眼 :術後眼壓 升高會加劇視神經 損傷。合併剝落症候群(PEX )的患者術後24小時內眼壓 升高的風險尤其高4) 9) 。IOL 放置不當IOL 的睫狀溝放置有較高的色素分散和UGH症候群 風險。單件式IOL 囊外植入可能導致UGH症候群 。術後類固醇 眼藥水 :眼壓 升高取決於類固醇 的效力和劑量。地塞米松和倍他米松的升眼壓 作用比氟米龍強。曲安奈德 可導致眼壓 持續升高9至12個月。兒童白內障 手術 :尤其是9個月以下嬰兒的手術,青光眼 風險顯著增高2) 。小角膜 和小眼球也是獨立的危險因子。後囊膜破裂 玻璃體 脫出和晶狀體碎片殘留。剝落症候群和懸韌帶脆弱 :由於IOL 不穩定,增加色素分散和UGH症候群 的風險4) 。Nd:YAG雷射後囊膜切開術 :可引起一過性眼壓 升高2) 3) 。晶狀體顆粒可能遷移並阻塞小樑網。已有青光眼 或高度近視 的患者風險更高。使用抗凝血藥物 :在虹膜 摩擦症候群中更容易發生前房 出血。IOL 材料和形狀IOL 在囊外植入時更容易引起UGH症候群 。三片式IOL 的支撐部角度和長度不同,虹膜 接觸的風險也不同。
進行以下檢查以確定眼壓 升高的機制。
隅角檢查 隅角 開放或關閉、是否存在周邊虹膜前粘連 、小樑網色素沉著程度,以及確認晶狀體顆粒或剝落物質。裂隙燈顯微鏡檢查 前房 發炎、出血、黏彈劑殘留以及IOL 的位置和穩定性。重要的是評估IOL 偏移或傾斜、與囊袋 收縮的關聯以及睫狀溝固定IOL 的正位。同時評估Elschnig珍珠、後囊膜纖維化和囊袋 收縮。UBM (超音波生物顯微鏡 )IOL 支撐部與虹膜 /睫狀體 的接觸關係。有助於確認UGH症候群 和虹膜 摩擦症候群。眼壓測量 Goldmann壓平眼壓計 是標準方法1) 。也使用回彈式iCare和Tono-Pen。角膜水腫 時需注意測量精度。使用角膜 厚度校正值進行評估。視神經 和視野評估青光眼 的進展以及檢測新的青光眼 性變化。OCT 測量視網膜神經纖維層 (RNFL )厚度有助於檢測早期變化。前房 閃輝值測量雷射閃輝儀 可定量評估前房 發炎。有助於術後發炎的縱向監測。
鑑別診斷時,需系統性地排除以下各機制。
鑑別診斷 特徵性表現 黏彈劑殘留 術後數小時至1天發病;自行消退 類固醇 青光眼 使用類固醇 期間發生;停藥後恢復正常 水晶體 顆粒性青光眼 前房 內白色顆粒漂浮;一過性UGH症候群 復發性前房 出血;色素播散 虹膜 摩擦症候群虹膜 萎縮、復發性前房 出血惡性青光眼 前房 普遍變淺、後方偏移
類固醇性青光眼 的診斷:在使用類固醇 的患者中出現高眼壓 ,停用類固醇 後眼壓 恢復正常即可確診。眼壓 恢復正常的時間與類固醇 使用時間成正比。使用曲安奈德 後,眼壓 升高可持續9至12個月,因此需要長期追蹤。
水晶體 顆粒性青光眼 的診斷:除了囊外摘除術或外傷後數天至數週的高眼壓 外,還需確認前房 內漂浮有疑似水晶體 物質的大白色顆粒。常伴有前房 發炎,但需與水晶體 溶解性青光眼 和水晶體 過敏性青光眼 鑑別。
Q
如何診斷UGH症候群?
A
UGH症候群 以葡萄膜炎 、青光眼 和前房 出血三聯徵為特徵2) 3) 。復發性前房 出血是最具特徵性的表現。UBM 檢查確認IOL 支撐部與虹膜 或睫狀體 接觸至關重要。前房 型IOL 或睫狀溝放置的IOL 較易發生,但若存在假性剝落症候群導致的懸韌帶不穩定,囊袋 內IOL 也可能發生。需與虹膜新生血管 及其他出血原因鑑別。虹膜 摩擦症候群的主要表現是虹膜 萎縮,雖然也有復發性前房 出血,但IOL 偏位的作用更大。
根據眼壓 升高的機制選擇治療非常重要1) 2) 3) 。
黏彈劑殘留或術後發炎引起的暫時性眼壓 升高,通常透過青光眼 眼藥水(β阻斷劑、碳酸酐酶抑制劑 眼藥水)或口服碳酸酐酶抑制劑 (乙醯唑胺 )等保守治療即可緩解。若眼壓 顯著升高(40 mmHg以上),可考慮前房穿刺 減壓11) 。有報告指出,術後早期預防性使用碳酸酐酶抑制劑 或β阻斷劑可抑制術後5小時及以後的眼壓 升高4) 。
白內障 術後、外傷後或YAG雷射 後囊切開術後,水晶體 物質逸出,堵塞小樑網導致眼壓 升高。通常在術後數天內發生,眼壓 升高程度與殘留水晶體 碎片量成正比。多為暫時性。
抗發炎及降眼壓 藥物 :類固醇 眼藥水與降眼壓 藥物聯合使用前房 沖洗完全清除水晶體 皮質 :若皮質殘留,則完全清除
這是白內障 術後使用類固醇 眼藥水期間常見的機轉。小樑細胞中細胞外基質產生增加和細胞骨架改變導致眼壓 升高。
減少或停用類固醇 :盡可能減少或停用類固醇 。需根據原發疾病的發炎控制情況判斷。降眼壓 藥物 :各種眼藥水、口服碳酸酐酶抑制劑 手術治療 (藥物控制不佳或視功能損害進展時):
小樑切開術 小樑切除術 眼壓 時選擇使用曲安奈德 病例 :清除玻璃體 內殘留物或切除Tenon囊下團塊可能有效
有報告指出,流出道重建術比POAG 可獲得更大的降眼壓 效果(證據等級1B)1)
也有報告指出雷射小樑成形術 有效1)
根據IOL 與虹膜 的接觸狀態進行階段性治療。
當IOL 與虹膜 未沾黏時 :散瞳 後採仰臥位,嘗試自然復位。散瞳 後未恢復虹膜 與囊袋 嚴重沾黏或IOL脫位 至前房 IOL IOL 縫線固定或鞏膜 內固定後瞳孔夾持 復發瞳孔阻滯 ,虹膜 切除術有效支撐腳進入前房 並接觸角膜內皮 :盡快復位
長期使用類固醇 眼藥水和阿托品眼藥水效果不佳。確診後,摘除刺激虹膜 的IOL 是首選 。摘除後,植入縱徑較短的IOL ,或進行IOL 縫線固定或鞏膜 內固定。
急性病例 :參照急性青光眼 發作,進行甘露醇靜脈滴注和頻繁毛果芸香鹼點眼無水晶體 眼 :雷射虹膜 周邊切開術(LPI )或手術前段玻璃體切除術 人工水晶體 眼玻璃體 破碎術可能有效惡性青光眼 玻璃體切除術 2)
對於開放隅角 機轉,參照原發性開放隅角青光眼 進行藥物治療1) 。
前列腺素類藥物 :降眼壓 效果顯著,常作為一線藥物使用β受體阻斷劑 碳酸酐酶抑制劑 多佐胺 、布林佐胺 ,口服乙醯唑胺 α2受體激動劑 :溴莫尼定
如果藥物治療無法控制,則進行手術治療2) 3) 。
開放隅角 機轉 :考慮流出道重建術。對於類固醇性青光眼 ,小樑切開術 是首選。閉塞隅角 機轉 :考慮隅角 黏連分離術或小樑切除術 。人工水晶體 眼小樑切除術 的效果比有水晶體 眼差,青光眼引流裝置 (管分流手術)也是一種選擇2) 3) 。兒童術後青光眼 :按照原發性先天性青光眼 (PCG)進行治療1) 。由於手術效果不佳,最終可能需要帶板的管分流手術1) 。
Q
白內障術後慢性青光眼如何處理?
A
首先確定眼壓 升高的機轉。如果是開放隅角 機轉,則按照POAG 進行藥物治療1) 。如果是閉塞隅角 機轉,考慮LPI 或隅角 黏連分離術。對於類固醇性青光眼 ,減少或停用類固醇 最為重要;如果需要手術,小樑切開術 是首選。如果藥物治療不足,則進行手術,但在人工水晶體 眼中,小樑切除術 效果不佳,因此考慮使用青光眼引流裝置 2) 。如果是由IOL 相關問題(色素分散、UGH症候群 )引起,則更換IOL 是根本性治療。
Q
白內障術後使用青光眼眼藥水時有哪些注意事項?
A
奧米德內帕(艾貝里斯 )禁用於植入IOL 或無水晶體 眼,不能使用。即使單眼為有水晶體 眼,也屬於患者單位禁忌,因此不能處方艾貝里斯 。其他PG製劑(拉坦前列素、曲伏前列素等)、β阻斷劑、碳酸酐酶抑制劑 、α2受體激動劑可按照POAG 使用1) 。術後使用類固醇 眼藥水期間,存在類固醇性青光眼 的風險,因此需密切觀察類固醇 的效力、劑量、持續時間以及眼壓 變化。
白內障 手術後眼壓 升高是由於房水 流出通道的一過性或持續性障礙所致2) 3) 。
在開放角機制中,黏彈性物質 、發炎細胞、色素顆粒、水晶體 顆粒、鬼影細胞等阻塞小樑網。對小樑網的持續刺激會導致纖維化,並導致房水 流出阻力慢性增加。
黏彈性物質 OVD 顆粒小,容易進入小樑網間隙,因此與凝聚型相比,術後眼壓 升高的風險更高。凝聚型易於整塊去除,但如果殘留於隅角 ,同樣會升高眼壓 。
類固醇 青光眼 眼壓 升高作用與類固醇 的抗炎強度成正比:地塞米松 ≥ 倍他米松 > 氟米龍。具有劑量依賴性,年輕人反應更顯著。曲安奈德 在眼內長期殘留,導致眼壓 持續升高9-12個月。
色素分散 :IOL 的支撐部或光學部邊緣接觸虹膜 後面,機械性剝離虹膜 色素上皮。釋放的色素顆粒積聚在小樑網,增加房水 流出阻力。單片式丙烯酸IOL 置於睫狀溝時尤其成問題。
虹膜 與玻璃體 前界膜的粘連(無水晶體 眼)或IOL 引起的瞳孔阻滯 (前房 型IOL 、睫狀溝IOL 、反向植入IOL )阻礙房水 流入前房 2) 。術後淺前房 和發炎促進周邊虹膜前粘連 形成,導致慢性閉塞隅角 青光眼 。
UGH症候群 的病理生理IOL 囊外固定或不對稱固定時,支撐部直接接觸虹膜 或周圍組織。虹膜 摩擦導致虹膜 色素堵塞小樑網,引起色素性青光眼 。虹膜 損傷嚴重時可合併虹膜 睫狀體 炎和前房 出血2) 3) 。過去在前房 型IOL 中更常見,但現在後房型IOL 囊袋 內固定已成為標準,其發生率很低。單片式丙烯酸IOL 囊外植入時可能發生。
虹膜 摩擦症候群的病理生理IOL 的支撐部或光學部邊緣持續摩擦虹膜 或隅角 血管。過去認為多見於成角環或長軸徑IOL ,但實際上IOL 偏位往往是原因。繼發性高眼壓 表現為虹膜 色素播散或前房 出血。在目前囊袋 內固定為標準的情況下,非常罕見。
白內障 手術後,由於移除水晶體 導致前房 加深和隅角 開放,眼壓 會下降8) 10) 。閉鎖性隅角 青光眼 的眼壓 下降更為顯著4) 。即使在開放性隅角 青光眼 ,術前眼壓 較高的病例也顯示出較大的眼壓 下降10) 。Poley等人(2009)報告指出,一年時的眼壓 下降可維持十年8) 。
Hayashi等人(2001)研究了青光眼 患者白內障 手術後的眼壓 控制,顯示超音波乳化 術及人工水晶體 植入可顯著降低眼壓 7) 。
Acharya等人(2024)分析了IRIS Registry超過750萬例病例,報告持續性假性水晶體 眼葡萄膜炎 (PUPPI)的發生率為1.68%,糖尿病(IRR 1.87)、種族和性別是危險因子5) 。
在兒童期需要白內障 手術的病例中,可能伴有房水 流出道的發育異常1) 。水晶體 移除引起的前眼部解剖變化也參與其中。無論無水晶體 眼或假性水晶體 眼,開放性隅角 或閉鎖性隅角 青光眼 都可能發生。由於中央角膜 較厚,可能出現表面上的高眼壓 ,需注意1) 。
近年來前眼部光學同調斷層掃描 (OCT )和UBM 的進步,使得術後隅角 和虹膜 -人工水晶體 關係的評估更加精確。透過定量評估人工水晶體 與虹膜 的接觸、傾斜和偏心,有望實現UGH症候群 和虹膜 摩擦症候群的早期診斷和預防性介入。前眼部OCT 可以非接觸、非侵入性地高解析度顯示隅角 結構,有助於術後隅角 變化的縱向監測。
人工水晶體 設計和尺寸計算演算法的改進顯著降低了色素分散和UGH症候群 的風險。基於眼軸長度 和前房 深度優化人工水晶體 尺寸,以及材料和支撐腳設計的改進正在推進。然而,針對剝落症候群和高度近視 相關的懸韌帶脆弱 等難以預測的風險因子的對策仍是未來的挑戰。
隨著MIGS (微創青光眼手術 )的發展,透過白內障 手術合併MIGS 進行術後眼壓 管理的選擇正在擴大。對於已有青光眼 的患者,在白內障 手術同時植入MIGS 裝置有望改善術後眼壓 控制。
對於小兒白內障術後青光眼 ,已有長管引流裝置的長期成效報告,對於僅靠藥物治療困難的病例,這是一個重要的治療選擇2) 。
Acharya等人(2024)利用IRIS Registry中超過750萬患者的數據,計算出PUPPI的發生率為1.68%5) 。糖尿病(IRR 1.87)、女性及非洲裔是獨立的風險因子,顯示了大規模真實世界數據對術後併發症監測的實用性。
Levkovitch-Verbin等人(2008)研究了青光眼 或PEX 患者白內障 術後24小時內的眼壓 升高,並報告了術後早期眼壓 監測的重要性9) 。
Chen等人(2015)作為AAO 的報告,系統性回顧了白內障 超聲乳化術後的眼壓 變化,確認了青光眼 患者的中期眼壓 降低效果10) 。
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. 2020.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
European Society of Cataract & Refractive Surgeons. ESCRS Clinical Guidelines: Cataract Surgery.
Acharya B, Hyman L, Tomaiuolo M, et al. Prolonged undifferentiated postoperative pseudophakic iridocyclitis. Ophthalmology. 2024.
Bodh SA, Kumar V, Raina UK, et al. Inflammatory glaucoma. Delhi J Ophthalmol. 2011;21:37-41.
Hayashi K, Hayashi H, Nakao F, et al. Effect of cataract surgery on intraocular pressure control in glaucoma patients. J Cataract Refract Surg. 2001;27:1779-86.
Poley BJ, Lindstrom RL, Samuelson TW, et al. Intraocular pressure reduction after phacoemulsification with intraocular lens implantation in glaucomatous and nonglaucomatous eyes. J Cataract Refract Surg. 2009;35:1946-55.
Levkovitch-Verbin H, Habot-Wilner Z, Burla N, et al. Intraocular pressure elevation within the first 24 hours after cataract surgery in patients with glaucoma or exfoliation syndrome. Ophthalmology. 2008;115:104-8.
Chen PP, Lin SC, Junk AK, et al. The effect of phacoemulsification on intraocular pressure in glaucoma patients: a report by the American Academy of Ophthalmology. Ophthalmology. 2015;122:1294-307.
Hildebrand GD, Wickremasinghe SS, Tranos PG, et al. Efficacy of anterior chamber decompression in controlling early intraocular pressure spikes after uneventful phacoemulsification. J Cataract Refract Surg. 2003;29:1087-92.