原發性先天性青光眼(PCG)是一種罕見的先天性疾病,由於前房 角發育異常(小樑發育不全)導致房水 流出受阻,眼壓 升高,屬於發育性青光眼 的早發型。
白種人發生率為每12,000至18,000名新生兒中有1例,近親結婚時發生率增加5至10倍1) 。日本報告每10萬名新生兒中有1.8至2.4例。
畏光 、流淚和眼瞼痙攣 的「三徵」是典型的早期症狀,眼壓 升高可導致牛眼(buphthalmos)和Haab紋1) 。CYP1B1是最常見的致病基因,但基因檢測僅能確定約24-40%病例的病因7) 。
首選治療是手術(隅角 切開術或小樑切開術 ),在出生後1個月至2歲期間進行隅角 切開術的成功率為94%,效果良好。
藥物治療作為輔助手段,例如口服乙醯唑胺 5-10 mg/kg,每6-8小時一次2) 。
早期診斷和治療可獲得良好的視功能。約60%的手術成功病例維持矯正視力 0.5以上。
需要終身進行眼壓 管理、屈光 矯正和弱視 治療1) 。
發育性青光眼 (developmental glaucoma)是由於房水 流出道發育異常引起的青光眼 的總稱,根據發病時間分為早發型和晚發型。早發型發育性青光眼 相當於傳統的「原發性先天性青光眼」,眼壓 升高的原因僅限於小樑網的發育異常。晚發型發育性青光眼 由於隅角 發育異常程度較輕,發病較晚,隅角鏡檢查 難以發現異常,通常也沒有角膜 直徑擴大或Haab紋。
原發性先天性青光眼(primary congenital glaucoma; PCG)是一種罕見的疾病,由遺傳決定的小樑網和前房 角異常導致眼壓 升高,不伴有其他眼部或全身發育異常。以前曾使用小樑發育不全(trabeculodysgenesis)、隅角 發育不全(goniodysgenesis)和原發性嬰兒型青光眼 等術語,但2013年兒童青光眼 研究網絡(CGRN)的國際分類將其統一為原發性先天性青光眼1) 。
原發性先天性青光眼是原發性兒童青光眼 中最常見的類型,根據發病時間分為以下四型1) 。
新生兒期發病 (0-1個月):最嚴重的類型。嬰兒期發病 (1個月以上至24個月):最常見,好發於出生後3-9個月。遲發型(延遲認知型) (2歲以上):發病越晚,症狀和體徵越不明顯。自然停止型 :極為罕見。眼壓 正常,但可見牛眼和Haab紋等原發性先天性青光眼的典型表現。
白種歐洲人的發生率為每12,000至18,000名新生兒中有1例1) 。在東歐部分地區,發生率高達每1,250人中有1例。存在近親結婚時,發生率增加5至10倍1) 。65%至80%的病例為雙眼性,男女比例約為3:2,男性居多1) 。
原發性先天性青光眼占所有眼病患者的不到0.01%,但據估計占全球兒童失明的5%。75%為雙眼性,65%為男童,80%在出生後1年內發病。
在ANZRAG的大型隊列(290例兒童青光眼 )中,PCG最常見,占57.6%(167/290例),其中嬰兒期發病的PCG最多,占53.3%(89/167例)。PCG的男女比例為1.46:1,診斷年齡中位數為0.25歲(IQR 0至0.6歲)7) 。
先天性青光眼 除了原發性先天性青光眼外,還包括續發性類型。世界青光眼 協會(WGA)對兒童續發性青光眼 的4種分類如下所示。
分類 主要疾病 伴有先天性眼部異常的青光眼 Axenfeld-Rieger異常、Peters異常 、先天性無虹膜 等 伴有先天性全身異常的青光眼 唐氏症 候群、Sturge-Weber症候群、神經纖維瘤病 等續發於後天性疾病或藥物的青光眼 葡萄膜炎 後、類固醇 誘導性等先天性白內障 術後青光眼 手術時年齡小、小眼球為危險因子
Q
原發性先天性青光眼的發生頻率為何?
A
在白人中,每12,000至18,000名新生兒中有1例,但在近親結婚多的地區,可上升至每1,250人中有1例。65%至80%為雙眼發病1) 。
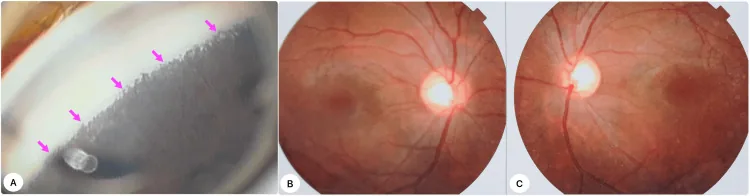
原發性先天性青光眼之前房角鏡所見與雙眼眼底照片。顯示虹膜前附著與視神經盤凹陷擴大。 Iqbal MI, et al. A Landmark Case of Childhood Glaucoma Care in Bangladesh: Gonioscopy-Assisted Transluminal Trabeculotomy in Primary Congenital Glaucoma. Cureus. 2025. Figure 1. PM
CI D: PMC11934033. License: CC BY.
左圖為前房 角鏡照片,顯示虹膜 前附著導致前房 角發育異常。中圖與右圖為雙眼眼底照片,可見視神經 盤凹陷擴大。這些對應於本文「主要症狀與臨床所見」章節討論的原發性先天性青光眼之臨床所見。
原發性先天性青光眼患者因眼壓 升高導致角膜水腫 ,出現刺激症狀,表現為以下「臨床三聯徵」中的一項或多項1) 。
畏光 怕光 ,在戶外瞇眼。溢淚 :無眼分泌物的流淚為特徵。與鼻淚管阻塞 的鑑別很重要。眼瞼痙攣
角膜水腫 /混濁導致的視力 下降、進行性近視 和散光 也會發生。在嬰幼兒中,監護人常注意到「眼白 」、「眼大」或「眼發藍」而就醫。
角膜所見
Haab條紋 :Descemet膜的水平至斜向斷裂,是先天性青光眼 的強力指標1) 。
角膜 直徑增大青光眼 。
角膜水腫 與混濁
眼球與視神經所見
牛眼(buphthalmos) :因眼壓 升高導致整個眼球擴大。角膜 擴大可持續至約3歲,鞏膜 伸展可持續至約10歲。
視神經 盤凹陷青光眼 。眼壓 正常化後凹陷可能改善(逆轉)。
眼軸長度 增加1) 。
關於Haab條紋:當角膜 直徑迅速增大時,Descemet膜無法充分伸展而產生撕裂。這些撕裂稱為Haab條紋,會導致角膜 散光 ,阻礙視力 發育。
角膜 直徑正常值參考:新生兒約為9.5–10.5 mm,至1歲左右增至10.0–11.5 mm。出生後不久超過12.0 mm時,應高度懷疑本病。
診斷標準(依據青光眼 診療指引)
青光眼 診療指引規定,滿足以下四項中至少一項即可診斷:
兩次或以上測量眼壓 ≥22 mmHg
杯盤比增大(≥0.3,或雙眼差≥0.2)
存在提示青光眼 的視野缺損
角膜 直徑或眼軸長度 增大
根據EGS第6版,符合以下5項中至少2項即可診斷為原發性先天性青光眼1) 。
眼壓 角膜 表現角膜水腫 、角膜 直徑增大(新生兒≥11 mm,1歲≥12 mm,任何年齡>13 mm)視神經 盤凹陷進行性近視 :與年齡不相稱的眼軸 增長隅角 表現虹膜 高位附著、殘留葡萄膜組織、小樑發育不全
Q
孩子只是眼睛大,也可能是青光眼嗎?
A
任何年齡角膜 直徑超過13 mm時,青光眼 的可能性極高。在自然停止型原發性先天性青光眼中,儘管眼壓 正常,仍可能出現牛眼和Haab紋,需要作為疑似青光眼 進行追蹤。
大多數原發性先天性青光眼為散發性(無家族史),但約10%~40%為家族性,呈體染色體隱性遺傳 ,外顯率為40%~100%1) 。連鎖分析已鑑定出5個基因座。
主要致病基因如下:
基因 基因座 染色體 功能 CYP1B1 GLC3A 2p22-p21 脂肪酸/維生素代謝酶 LTBP2 GLC3D 14q24.2-q24.3 潛在型TGF-β結合蛋白 TEK/TIE2 GLC3E 9p21 Schlemm管發育信號
CYP1B1 (GLC3A):最常見的致病基因。在胎兒和成人的神經上皮和睫狀體 中表現,代謝眼部發育必需的化合物。CYP1B1缺陷小鼠出現嚴重的小樑網萎縮。CYP1B1突變病例通常發病較早,雙眼受累,病程典型。LTBP2 (GLC3D):在小樑網和睫狀突中表現,但在眼中的作用尚未完全闡明。TEK/TIE2 (GLC3E):血管生成素/TEK信號通路對Schlemm管的發育至關重要,TEK基因剔除小鼠缺乏Schlemm管。MYOC :可能參與高達5.5%的原發性先天性青光眼病例。EFEMP1 也被報告為候選基因1) 。
根據ANZRAG隊列的基因診斷率報告,總體24.7%(125/506例)獲得分子診斷。在PCG中,30.4%(41/135例)可實現分子診斷,包括CYP1B1雙等位基因突變15.6%(21例)、TEK雜合突變5.9%(8例)、CPAM D8 3.7%(5例)、FOXC1雜合突變3.7%(5例)。基於基因診斷的PCG亞型重新分類發生在10.4%的病例中(FOXC1突變重新分類為ARS,CPAM D8突變重新分類為ASD )7) 。CYP1B1雙等位基因突變在PCG女性中較常見(66.7% vs 33.3%,P=0.02)7) 。
透過基因檢測確定病因的機率約為24-40%。建議進行基因檢測以排除其他先天異常並用於計畫生育1) 。
近親結婚被認為是疾病嚴重程度和預後不良的因素1) 。原發性先天性青光眼患者的第二個孩子患病的機率通常低於3%,但如果已有兩個孩子患病,假設體染色體隱性遺傳 ,則機率升至25%。
Q
是否應該接受基因檢測?
A
EGS指南建議從排除其他先天異常和計畫生育的角度進行基因檢測1) 。ANZRAG隊列顯示PCG的基因診斷率為30.4%,基因診斷導致10.4%的病例亞型重新分類7) 。檢測陰性不能排除原發性先天性青光眼,但可能有助於診斷準確性和適當管理。
原發性先天性青光眼的診斷通常可以在眼壓測量 不準確的情況下臨床做出。Haab紋的存在是先天性青光眼 的強指標1) 。
眼壓測量 眼壓 計(包括回彈式眼壓 計)進行測量1) 。注意:哭鬧的兒童可能出現假性高值,全身麻醉藥物會導致假性低值。回彈式眼壓 計也可用於居家測量1) 。全身麻醉下使用的所有藥物都會降低眼壓 。唯一的例外是分離性麻醉藥鹽酸氯胺酮,它可能使眼壓 輕度升高。如果在七氟烷麻醉下眼壓 為20 mmHg,清醒時眼壓 將超過30 mmHg。有觀點認為七氟烷麻醉下正常上限為15 mmHg或12 mmHg。角膜 直徑和厚度測量角膜 直徑;如果超過年齡相應的正常範圍,則懷疑眼壓 控制不良。中央角膜 厚度即使沒有水腫也可能增加,並可能影響眼壓測量 值1) 。眼軸長度 測量近視 進展和眼軸長度 增加提示青光眼 進展。隅角檢查 角膜 混濁導致隅角鏡檢查 困難,超音波生物顯微鏡 (UBM )很有用。視神經 盤評估眼壓 降低後常可見杯凹改善。特別是1歲以下通過手術治療獲得良好眼壓 控制的病例中,約50%的杯盤比減少0.2以上,表明兒童視神經 盤杯凹具有可逆性,與成人不同。視力 和屈光 檢查散光 、角膜 混濁和Haab紋可導致弱視 ,因此在追蹤期間應定期進行屈光 檢查,與眼壓測量 並行。
可能與原發先天性青光眼 混淆的疾病如下所示1) 。
鑑別疾病 鑑別要點 結膜炎 有眼部分泌物和充血 ;角膜 直徑正常 鼻淚管阻塞 有眼部分泌物;角膜 直徑正常 PPM D角膜 後表面的囊泡樣改變CHED 雙眼角膜水腫 ,眼壓 正常 X連鎖巨角膜 角膜 直徑增大,眼壓 正常出生時外傷 外傷史,Haab紋通常垂直
手術是首選治療方法2) 。原因是原發性先天性青光眼由隅角 發育異常引起,可透過手術解決;嬰幼兒藥物療效難以確認;且存在依賴照護者遵從性的問題2) 。藥物治療作為圍手術期或術後輔助手段使用2) 。
應在具有足夠小兒眼科和青光眼 治療經驗的機構進行,需要包括再次手術、長期追蹤和弱視 治療在內的綜合管理2) 。
小樑切開術 (trabeculotomy)角膜 透見困難的情況下也可施行2) 。需要製作結膜 瓣和鞏膜 瓣,可能使未來的濾過手術 變得困難。使用微導管 的360°小樑切開術 也有嘗試2) 。出生後2個月內發病的病例成功率為78%,略低;但此後發病的病例成功率為96%,效果良好。隅角 切開術(goniotomy)角膜 透明的病例2) 。一次手術可切開90-120°,最多可從不同部位進行3次操作2) 。出生後1個月至2歲發病的成功率為94%,尤其良好。但出生後1個月內發病的病例成功率為26%,2歲以後發病的病例為38%,較低。對於出生後3-12個月發病的原發性先天性青光眼,隅角 切開術和小樑切開術 的成功率相似(70-90%)2) 。術式選擇取決於術者經驗。失敗的危險因素是隅角 發育不良的程度和前段過度擴張2) 。
濾過手術 (trabeculectomy)隅角 手術無效的病例2) 。原發性先天性青光眼患者的鞏膜 薄,製作瓣膜困難,即使合併抗代謝藥物 ,濾過泡形成也可能困難。1年成功率為50-87%,較成人差2) 。帶引流管的植入物手術(GDD) :用於濾過手術 無效的病例。一項針對Ahmed瓣膜和Baerveldt植入物的32項研究、1221隻眼的統合分析顯示,術前平均眼壓 31.8±3.4 mmHg,術後12個月平均眼壓 降至16.5 mmHg(95% CI 15.517.6)8) 。成功率隨時間下降:12個月87%(95% CI 0.830.91),24個月77%(95% CI 0.71~0.83),120個月37%。Ahmed組和Baerveldt組的成功率無顯著差異8) ,主要併發症包括前房 變淺13.6%、低眼壓 11.7%、脈絡膜 滲出8.3%。睫狀體破壞術 眼壓 時考慮使用2) 。
藥物治療是輔助治療,旨在術前短期降低眼壓 和術後控制眼壓 2) 。參照原發性開放隅角青光眼 聯合使用藥物,但需注意以下事項。
嬰幼兒相對於體重和體表面積,劑量容易過大,因此應盡可能從低濃度藥物開始。
口服乙醯唑胺 (碳酸酐酶抑制劑 ) :按510 mg/kg每68小時給藥一次。對術前緊急降低眼壓 有效2) 。β受體阻斷劑 α2腎上腺素受體促效劑 (如溴莫尼定)在2歲以下兒童中絕對禁忌。可引起神經精神症狀(嗜睡、心搏過緩、低血壓等)1) 2) 。前列腺素FP受體促效劑 在兒童中的效果較成人弱2) 。兒童葡萄膜鞏膜 流出道發育不全,無反應者較多,但被認為比β受體阻斷劑 有稍好的降眼壓 效果。點眼藥水從淚囊、鼻黏膜直接進入全身循環,因此兒童即使一滴也容易引起嚴重的全身性副作用。建議指導點眼後壓迫淚囊部。
必須終身監測眼壓 ,並透過屈光 矯正和弱視 治療支持最佳的視覺發育1) 。
Q
為什麼首選手術而非藥物治療?
A
原發性先天性青光眼的原因是隅角 發育異常,可透過手術解決。在嬰幼兒中,藥物效果難以確認,且存在順從性問題。此外,兒童可使用的藥物有限,例如α₂受體激動劑的禁忌症和前列腺素類藥物的效果減弱2) 。
原發性先天性青光眼的眼壓 升高是由於前房 隅角 發育異常導致房水 流出受阻所致1) 。
在1950至60年代,曾認為原因是覆蓋隅角 的非穿孔性膜(Barkan膜),但後續的組織學調查否定了這種膜的存在。目前認為流出障礙源於小樑網本身。
正常情況下,妊娠第三孕期睫狀體 和周邊虹膜 會向後移動,遠離角膜 和鞏膜 。在原發性先天性青光眼中,小樑網內膠原樑的過度或過早積累阻礙了這種後移,導致虹膜 根部和睫狀肌保持前附著,阻塞小樑網或壓迫Schlemm管。
Rao(2025)對4名原發性先天性青光眼患者的小樑網標本進行了組織學分析,報告了近小管網(JCM)和角膜 鞏膜 網的擴大、小樑網樑的增厚、紡錘形核的增加(提示上皮間質轉化),以及JCM內存在兩個形態不同的區域3) 。這些發現提示原發性先天性青光眼中小樑網各區域的異常分化和分化異質性。
GAT T(gonioscopy-assisted transluminal trabeculotomy)是一種相對較新的技術,透過角膜 切口在隅角 鏡下將微導管 或縫線插入Schlemm管,切開全周小樑網。其在成人青光眼 中的有效性正在確立,並逐漸應用於兒童。
Song等人(2022)報告了一例對3歲原發性先天性青光眼男童實施GAT T的病例。虹膜 覆蓋了整個隅角 直至Schwalbe線,正常隅角 結構不可見,但透過鉤操作剝離虹膜 以識別Schlemm管,成功實施了GAT T。術後6個月眼壓 穩定4) 。
Elhusseiny等人(2023)報告了6名有青光眼 手術史的原發性先天性青光眼患者7隻眼接受GAT T的1年結果。平均眼壓 從術前的25.7±5.9 mmHg顯著下降至12個月後的12.0±1.5 mmHg。完全成功率為85.7%(6/7眼),包括限定性成功在內為100%,沒有眼睛需要額外青光眼 手術。未觀察到嚴重併發症5) 。
Dada等人(2022)報告了一種針對伴有角膜 混濁的原發性先天性青光眼的新技術,使用23G雷射內視鏡探頭在可視化隅角 結構的同時進行隅角 切開術6) 。傳統上,隅角 切開術需要透明角膜 ,但藉助內視鏡輔助,即使在角膜 混濁眼中也可能可行。
對於有家族史或近親結婚較多地區等高風險族群,未來產前基因篩檢可能作為一種預防措施出現。在ANZRAG隊列中,基因診斷使10.4%的PCG亞型得到重新分類,表明基因診斷有助於更精確的診斷和適當的管理7) 。期待未來大型國際隊列的證據累積。
一項關於兒童青光眼 患者QOL的系統性回顧發現,使用了10種患者報告結果指標(PROMs),但目前尚無針對兒童青光眼 的特異性問卷9) 。IVI _C、CVAQC和LVP-FVQ-II作為視覺特異性兒童量表獲得了相對較高的評分(5/7分)。兒童青光眼 患者對未來存在擔憂(就業、家庭計畫、對手術的恐懼),現有PROMs未能充分涵蓋9) 。開發兒童青光眼 特異性PROMs是未來的挑戰。
手術成功病例的長期視力 預後相對良好。無論是隅角 切開術還是小樑切開術 ,約60%的成功病例保持矯正視力 0.5以上。
盡早進行屈光 檢查和屈光 矯正,並頻繁進行屈光 檢查以應對度數變化。
Haab紋引起的角膜 散光 可導致弱視 ,因此應同時進行散光 管理和弱視 治療。
必須終身監測眼壓 。
兒童青光眼 患者的健康相關QoL(HRQoL)與先天性心臟病或急性淋巴性白血病患兒相當(PedsQL 4.0評分約76-79/100)。視力 良好組、原發型和單眼性患者的QoL較好;手術次數、點眼次數和雙眼性與QoL降低相關9) 。
Q
手術後的長期視力預後如何?
A
手術成功案例中,約60%可維持矯正視力 0.5以上。但終身眼壓 管理、屈光 矯正和弱視 治療不可或缺。處理Haab紋引起的角膜 散光 和進行性近視 是維持視功能的關鍵。需要GDD手術的案例,12個月成功率為87%,24個月為77%,隨時間推移而下降,因此長期追蹤是必需的8) 。
European Glaucoma Society. European Glaucoma Society Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025;109(Suppl 1):S1-S270.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
Rao A. Histopathological changes in the trabecular meshwork in primary congenital glaucoma. Am J Ophthalmol Case Rep. 2025;38:102340.
Song Y, Zhang X, Weinreb RN. Gonioscopy-assisted transluminal trabeculotomy in primary congenital glaucoma. Am J Ophthalmol Case Rep. 2022;25:101366.
Elhusseiny AM, Aboulhassan RM, El Sayed YM, et al. Gonioscopy-assisted transluminal trabeculotomy following failed glaucoma surgery in primary congenital glaucoma: one-year results. Case Rep Ophthalmol Med. 2023;2023:6761408.
Dada T, Satpuke K, Bukke AN, et al. Endoscope-assisted goniotomy in primary congenital glaucoma with corneal opacification. BMJ Case Rep. 2022;15:e252958.
Knight LSW, Ruddle JB, Taranath DA, et al. Childhood and early onset glaucoma classification and genetic profile in a large Australasian disease registry. Ophthalmology. 2024;131(1):62-73.
Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: a systematic review and meta-analysis. J AAPOS. 2023;27(3):139.e1-139.e10.
Stingl JV, Cascant Ortolano L, Azuara-Blanco A, Hoffmann EM. Systematic review of instruments for the assessment of patient-reported outcomes and quality of life in patients with childhood glaucoma. Ophthalmol Glaucoma. 2024;7(4):391-400.