淚點閉鎖症
定義:上下淚點狹窄或閉合的狀態。
主要原因:燒傷或化學腐蝕後的疤痕、Stevens-Johnson症候群、眼類天皰瘡。
藥物性:噻嗎洛爾、多佐胺、毛果芸香鹼等青光眼眼藥水,IDU(抗病毒藥),S-1(蒂斯旺®)。

淚道(淚點→淚小管→淚囊→鼻淚管→下鼻道開口)的通過障礙(狹窄或阻塞)導致流淚的疾病稱為淚道阻塞。其中,鼻淚管入口及之後的阻塞稱為鼻淚管阻塞(NLDO)。
裂隙燈檢查可見淚液半月面增高,螢光素染色清除延遲提示淚道阻塞可能。通過淚道沖洗試驗確診。
根據阻塞部位,大致分為以下四種類型。
淚點閉鎖症
定義:上下淚點狹窄或閉合的狀態。
主要原因:燒傷或化學腐蝕後的疤痕、Stevens-Johnson症候群、眼類天皰瘡。
藥物性:噻嗎洛爾、多佐胺、毛果芸香鹼等青光眼眼藥水,IDU(抗病毒藥),S-1(蒂斯旺®)。
淚小管阻塞症
定義:淚小管(上/下)阻塞的狀態。
矢部·鈴木分類:Grade 1(總淚小管阻塞,有交通)/Grade 2(上下無交通,可插入7~8mm以上)/Grade 3(比Grade 2更近端的阻塞)。
特徵:抗癌藥物相關者多為雙側性、上下同時受損。
總淚小管阻塞症
鼻淚管阻塞症
自2018年淚道內視鏡納入健保給付後1),可觀察阻塞部位的纖維化程度及黏膜發炎情形,提高了對總淚小管或鼻淚管阻塞的鑑別準確性。沖洗試驗估計的阻塞部位與淚道內視鏡所見的一致率約為70%1),內視鏡直接觀察具有重要意義。
溢淚不僅包括淚道阻塞,也包括淚液分泌過多(如乾眼引起的反射性溢淚)。淚道沖洗有逆流則可判斷為阻塞。透過BUT測量或Schirmer試驗評估淚液分泌量進行鑑別。
使用S-1(Tegafur/Gimeracil/Oteracil鉀複方製劑,TS-1®)抗癌治療期間發生的淚點及淚小管阻塞常較嚴重。建議早期置管。抗癌藥相關淚道阻塞中,淚點及淚小管病變約占60%1)。抗癌藥使用期間拔管易再阻塞,因此建議在用藥期間持續留置淚道管1)。
矢部·鈴木分類用於淚小管阻塞的嚴重程度分級1)。
| 分級 | 定義 | 治療方法 |
|---|---|---|
| 第1級 | 可插入探針≥11 mm;上下淚點間交通存在(總淚小管阻塞) | DEP/SEP,置管時間2~10個月 |
| 第2級 | 上下淚點間無交通;可插入探針≥7~8 mm | DEP/SEP(難度高),也可考慮CDCR |
| 第3級 | 阻塞位置比第2級更近端 | DEP/SEP困難,嘗試金屬探針,考慮CDCR |
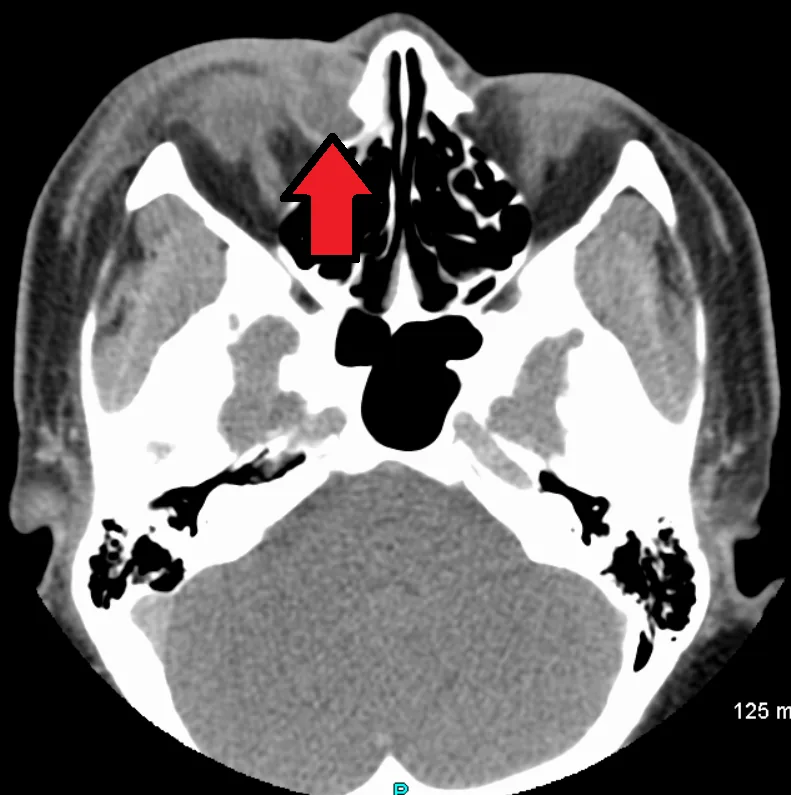
鼻淚管阻塞是成人溢淚的最常見原因。多見於女性和老年人,鼻淚管的解剖性狹窄被認為是原因之一。錐形束CT淚道造影分析顯示,眶上緣-內總淚點-鼻淚管開口的角度在92%的病例中呈前屈曲3),這種形態特徵被認為有助於阻塞的風險。
鼻淚管阻塞的原因包括慢性發炎、年齡相關變化,以及Stevens-Johnson症候群、眼類天皰瘡、藥物性(青光眼眼藥水、抗病毒藥、抗癌藥)等。
| 檢查 | 可檢測的資訊 | 侵襲性 | 健保給付 |
|---|---|---|---|
| 淚道沖洗(通水檢查) | 有無阻塞及回流方向 | 低 | 有 |
| 染料消失試驗 | 淚液清除率降低 | 低 | 有 |
| 淚囊造影 | 阻塞部位、淚囊擴大、顯影劑中斷 | 中 | 有 |
| 淚道內視鏡 | 直接觀察阻塞部位、纖維化、黏膜發炎 | 中 | 自2018年起 |
| 眼眶及鼻竇CT | 淚囊窩、鼻腔形狀、鼻竇炎、腫塊 | 中等 | 有(術前) |
淚道內視鏡檢查於2018年納入健保給付1),對診斷阻塞部位的纖維化程度、黏膜發炎及淚道內腫塊有幫助。若懷疑淚道外病變,則合併使用CT或MRI。
淚囊攝影有時難以判斷顯影劑是否到達阻塞部位1),其角色主要是對淚道內視鏡直接觀察的補充。
流淚的原因大致分為「淚道通過障礙(分泌量正常但無法排出)」和「淚液分泌過多(刺激導致淚液增加)」。淚道阻塞是最常見的原因,但乾眼引起的反射性流淚、結膜炎、角膜炎等也會導致流淚。透過BUT測量和Schirmer測試評估淚液分泌量,並透過淚道沖洗確認有無通過障礙來進行鑑別。
自2018年起已納入健保。淚道內視鏡可直接觀察阻塞部位,有助於診斷纖維化程度、黏膜發炎及淚道內腫瘤。對於通水試驗難以判斷的阻塞部位詳細分類(如總淚小管阻塞與鼻淚管阻塞的鑑別、淚囊-鼻淚管移行部阻塞與下部膜性鼻淚管阻塞的區別等)尤其有用。
根據阻塞部位、嚴重程度及患者意願選擇治療方法。
急性期/初期處理如下:
在點眼麻醉下,用淚點擴張針或尖刀切開並擴張淚點。留置淚點塞24週後取出,若再次閉塞,則留置淚小管矽膠管12個月後取出。
逐步擴張淚點(由細到粗)後留置淚管可預防再次閉塞。留置時間為17個月,拔管後312個月的成功率據報導為81.8~100%1)。
用4%鹽酸利多卡因溶液進行淚道內麻醉後,用淚點擴張針充分擴張淚小管。從淚點小心插入雙頭或導管型矽膠管,同時確認阻塞部位的觸感,留置1~2個月後取出。
使用DEP(淚道內視鏡直接穿破法)或SEP(鞘引導內視鏡下穿破法)穿破阻塞部位1)。
置管時間為2~10個月。據報導,術後878天Kaplan-Meier法的通暢率為94%1)。
難度顯著增加,若DEP/SEP穿通困難,則嘗試用細金屬探針穿通1)。若上下淚小管均無法開放,則考慮CDCR(結膜淚囊鼻腔吻合術)。
用DEP或SEP穿通阻塞部位,通過SGI(鞘引導插管)或G-SGI置入導管1)。
直接置管有22%的黏膜下誤置報告1),推薦使用SGI/G-SGI方法。置管時間為2~12個月。拔管後1年手術成功率為70~87%1)。DSI(直接矽膠插管)的成功率較低,約52.5%(拔管後8~30個月)1),拔管後3000天的通暢率為64%,有長期復發風險的報告1)。復發危險因子包括淚囊炎病史、病程長、阻塞距離長、男性1)。
適用於長期溢淚、眼部分泌物症狀且患者希望手術的情況。急性淚囊炎時,在切開引流、抗生素消炎後制定手術計畫。對於不希望根治手術的患者,可通過探通或置管推遲手術時間,但需事先充分說明鼻淚管阻塞的置管術效果不佳。
外路DCR手術步驟:
外路DCR的成功率為90~99%1),多數報告顯示再阻塞率低於10%。有報告指出,由於骨窗較小,內路(內視鏡下)DCR的效果略差。
| 術式 | 成功率 | 留置/暢通時間 | 主要適應症 |
|---|---|---|---|
| 直接矽膠管插入(DSI) | 約52.5%(8~30個月後) | 留置2~12個月 | 鼻淚管阻塞(輕度) |
| 淚道內視鏡下導管置入(DEP/SEP+SGI) | 70~87%(1年後) | 留置2~12個月 | 鼻淚管阻塞/淚小管阻塞 |
| DCR鼻外法 | 90~99%1) | — | 鼻淚管阻塞(根治) |
| DEP/SEP(第1級淚小管阻塞) | 暢通率94%(878天後) | 留置2~10個月 | 總淚小管阻塞 |
淚道內視鏡手術及淚管置管相關的主要併發症如下所示1)。
S-1(TS-1®)引起的淚道阻塞常發生在淚點和淚小管,且易加重,因此建議早期行矽膠管置入術。化療期間拔管易再阻塞,故治療期間最好維持置管。如出現症狀,請及時諮詢眼科醫師。
因阻塞部位和術式而異。淚點置管:17個月;淚小管淚道內視鏡下治療(DEP/SEP):210個月;鼻淚管置管術:2~12個月。未來有望根據淚道內視鏡所見確定最佳拔管時機。
鼻淚管入口處阻塞最常見。慢性發炎、年齡相關變化和解剖狹窄共同參與。
阻塞發生後,淚液和分泌物在阻塞近端(淚囊側)積聚。積聚的黏液成為細菌培養基,導致Moraxella lacunata、S. mitis、綠膿桿菌、α溶血性鏈球菌等過度生長,進展為慢性淚囊炎1)。淚液清除減少也會導致角膜和結膜的慢性改變。
一項使用錐狀束CT淚道造影分析淚道形態的報告顯示,眼眶上緣-內總淚點-鼻淚管開口的角度在92%的病例中向前彎曲3),這種形態特徵被認為影響器械插入鼻淚管的難度以及阻塞的形成。
淚道內視鏡有兩種規格:外徑0.9毫米、觀察像素10,000(2012年改進型)和外徑0.7毫米、3,000像素的操作優先型1)。2020年,景深得到改善,可適應1.5至7毫米的觀察距離。主要使用尖端10毫米處向上彎曲27°的彎曲型,根據病例選擇使用直型和雙彎曲型1)。
淚囊結石由慢性炎症和分泌物滯留形成4)。淚道內腫瘤有時通過淚道內視鏡發現,有惡性黑色素瘤、乳頭狀瘤和肉芽腫的報告1)。由於在DCR手術時的病理檢查中約1.0%(佔所有腫瘤的69%)發現惡性腫瘤,因此建議對手術標本進行組織病理學檢查5)。