DEP(直接內視鏡探通)
操作:將淚道內視鏡探頭本身作為探條,直接穿破閉塞部位。
特點:操作簡單。可同時進行觀察和穿破,但由於不使用鞘管,插管需另行SGI法。
適應症:閉塞部位明確且能確保穿破方向的病例。

淚道插管術(淚管插管術)是針對淚點、淚小管、總淚小管、鼻淚管的阻塞或狹窄,留置矽膠管以重新開通並維持淚道暢通的手術方式。根據阻塞部位不同,操作技術差異很大,各自有相應的手術入路。
在日常眼科診療中,主訴溢淚的患者常存在淚道狹窄或阻塞。裂隙燈檢查發現淚液半月面增高,螢光素染色清除延遲,則提示淚道阻塞可能性大,通過淚道沖洗檢查可確診。
淚道置管術的主要目的是在阻塞的淚道中留置矽膠管一段時間,以恢復管腔暢通,促進黏膜自然再生。這不是根治性手術,效果因阻塞部位和嚴重程度而異。
對於鼻淚管阻塞,DCR(淚囊鼻腔吻合術)作為根治性治療,成功率達90–99% 3),但置管術是一種創傷更小的選擇,有時作為根治手術前的橋接治療。術前需向患者充分說明鼻淚管阻塞置管的效果不佳。
隨著淚道內視鏡(外徑0.7–0.9 mm,6000–10000像素纖維鏡)的發展,可以直接觀察阻塞部位並進行穿通和置管 1)。DEP(直接內視鏡探通)和SEP(鞘引導內視鏡探通)等穿通方法,以及SGI(鞘引導插管)和G-SGI等置管方法已普及,降低了黏膜下誤插的風險 1)。
淚道阻塞根據阻塞部位大致分為四型。
| 阻塞部位 | 主要原因 | 置管時間 | 成功率 |
|---|---|---|---|
| 淚點阻塞 | SJS、化學腐蝕後疤痕、慢性炎症 | 1–2個月 | 81.8–100%1) |
| 淚小管阻塞(第1級) | 發炎性疤痕、EKC後 | 2至10個月 | 94%(878天後)1) |
| 淚小管阻塞(第2-3級) | 抗癌藥物相關、廣泛疤痕 | 個別判斷 | 難治 |
| 鼻淚管阻塞 | 老化、感染、原因不明 | 2至12個月 | 70至87%(1年後)1) |
淚點阻塞主要由燒傷、化學腐蝕後、Stevens-Johnson症候群(SJS)、眼類天皰瘡等慢性發炎引起的疤痕所致。青光眼眼藥水(噻嗎洛爾、多佐胺等)和TS-1(替加氟、吉美嘧啶、奧替拉西鉀)等藥物性原因也是重要因素。
淚小管和總淚小管阻塞由發炎性疤痕和術後沾黏引起。採用矢部·鈴木分類(第1-3級)評估嚴重程度,治療難度差異很大。
鼻淚管阻塞是從淚囊到下鼻道開口處的阻塞,其中鼻淚管入口處阻塞最為常見。它被認為是老年人及女性中常見的後天性淚道疾病。
淚小管阻塞的嚴重程度評估採用矢部·鈴木分類1)。根據阻塞的程度和部位,治療難度差異很大,因此術前準確分類非常重要。
| 分級 | 定義 | 治療難度 |
|---|---|---|
| 1級 | 可插入探針≥11mm,上下淚點間交通存在(總淚小管阻塞) | 標準 |
| 2級 | 上下淚點間無交通,可插入探針≥7~8mm | 高 |
| 3級 | 阻塞位置比2級更近端 | 非常高 |
無論阻塞部位為何,以下主要症狀共通存在。
使用TS-1(Tegafur/Gimeracil/Oteracil鉀複方製劑)或5-FU(Fluorouracil)進行抗癌治療期間發生的淚道阻塞容易重症化。淚點及淚小管受累約佔60%1),建議早期置管。抗癌治療期間拔管容易再次阻塞,因此治療持續期間最好維持置管1)。抗癌藥相關淚道阻塞常為雙側性、上下淚小管同時受累,尤其難治2)。
後天性鼻淚管阻塞是成人流淚症的主要原因之一,好發於女性及老年人。年齡相關的淚道纖維化及發炎性變化被認為是主要背景因素。
先天性鼻淚管阻塞常見於新生兒及嬰兒期,但90%以上在1歲前自然痊癒,因此以觀察為主。對於1歲後仍殘留的病例或伴有復發性淚囊炎的病例,可考慮探通或淚道內視鏡手術1)。
TS-1及5-FU等抗癌藥引起的藥物性淚道阻塞有一定發生頻率,阻塞進展後容易成為難治病例2)。建議從給藥早期開始觀察流淚症狀,一旦確認阻塞,應盡快置管1)。
**淚道沖洗檢查(通水檢查)**是最基本的確定診斷方法,鼻淚管阻塞時可見淚囊內黏液從淚點逆流。此檢查創傷小,可在門診進行。
淚囊造影顯示顯影劑在鼻淚管入口處及以後中斷,並可見淚囊擴張。有助於估計阻塞層級,但與內視鏡所見的一致率約為70% 1)。
淚道內視鏡檢查是使用外徑0.7~0.9mm的纖維內視鏡直接觀察淚道內腔的檢查方法,於2018年被納入健保 1)。有助於準確確定阻塞部位(鑑別總淚小管阻塞或鼻淚管阻塞)、評估纖維化程度與黏膜發炎、發現淚道內腫瘤。通水檢查對阻塞部位的估計與淚道內視鏡所見的一致率約為70%,因此內視鏡直接觀察具有重要意義 1)。
術前CT(眼眶與鼻竇)用於手術適應症病例,以評估淚囊窩與鼻腔的形態以及有無鼻竇炎。
它是一種使用外徑0.7~0.9mm的超細纖維內視鏡直接觀察淚道內腔的裝置。可以準確確定阻塞部位,並在內視鏡下進行穿通與置管。與通水檢查的一致率約為70%,淚道內視鏡能提供更準確的診斷。此檢查於2018年被納入健保,對於評估阻塞部位的纖維化程度、黏膜發炎與淚道內腫瘤特別有用。
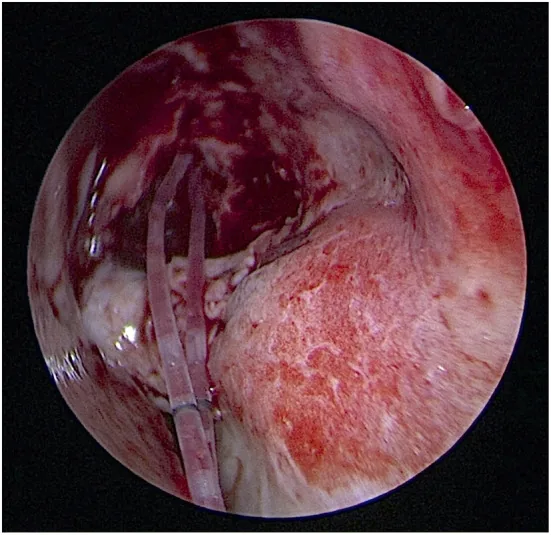
治療方法根據阻塞部位、嚴重程度以及患者的狀況與意願選擇。
在點眼麻醉下,用淚點擴張針或尖刀切開並擴張淚點。留置淚點塞2-4週後拔除,若再次閉塞,則重新切開淚點,留置淚小管矽膠管1-2個月後拔除。拔管後3-12個月的成功率據報告為81.8-100% 1)。
用4%鹽酸利多卡因進行淚道內麻醉後,用淚點擴張針充分擴張淚小管。從淚點插入雙頭或導管型矽膠管,但需仔細感受閉塞部位的阻力,逐步推進管尖,切勿強行操作。金屬探針有形成假道的風險,需特別謹慎。留置時間一般為1-2個月。
淚道內視鏡下的治療:使用DEP或SEP穿破閉塞部位,通過SGI/G-SGI插入矽膠管1)。第1級(總淚小管閉塞)在878天後的暢通率為94%,效果良好1)。第2級和第3級難度顯著增加,穿破困難時需考慮中止手術。
經淚點入路不可行的總淚小管閉塞:採用皮膚切口入路。沿前淚嵴做15-20mm皮膚切口,切開淚囊,在顯微鏡直視下確認總淚點位置後穿破閉塞部位。內眥腱的高度可作為總淚點位置的參考。
術前需向患者充分說明鼻淚管閉塞的插管手術效果不佳。合併慢性淚囊炎時再閉塞率高達45-80%。合併急性淚囊炎時,需先切開引流並使用抗生素消炎後再制定手術計畫。
使用DEP或SEP穿破閉塞部位,通過SGI/G-SGI將矽膠管引導至鼻腔並插入。留置時間2-12個月。拔管後1年成功率為70-87% 1),拔管後3000天的暢通率為64%,存在長期復發風險1)。復發風險因素包括淚囊炎病史、病程長、閉塞距離長和男性1)。
DEP(直接內視鏡探通)
操作:將淚道內視鏡探頭本身作為探條,直接穿破閉塞部位。
特點:操作簡單。可同時進行觀察和穿破,但由於不使用鞘管,插管需另行SGI法。
適應症:閉塞部位明確且能確保穿破方向的病例。
SEP(鞘管引導內視鏡探通)
操作:將鐵氟龍淚道鞘作為外套管安裝,用鞘尖端穿破阻塞部位。
特點:可在觀察管腔的同時進行穿破。穿破後可直接過渡到SGI引導的插管。
適應症:需要仔細確認穿破方向的病例。可降低黏膜下誤入的風險。
SGI(鞘引導插管) 是將鞘留置在淚道內,將導管連接在鞘內,然後從鼻腔拔出鞘,將導管引導至鼻腔的方法。直接插管(DSI)據報導有22%的黏膜下誤入率1),因此推薦SGI方法。
G-SGI 是SGI的改良方法,無需鼻腔內操作。鞘上設有割線,可從淚點側拔出鞘,從而減少鼻腔器械插入相關的疼痛和併發症風險。
插入內視鏡時,要注意淚小管的垂直部和水平部等結構。向外牽拉眼瞼使淚小管變直,可從上淚點幾乎直線到達淚囊。灌流液應緩慢注入,避免快速灌流壓引起疼痛。
因阻塞部位而異。淚點或淚小管阻塞留置12個月,鼻淚管阻塞留置212個月。長期留置(9個月以上)會增加淚點撕裂(起司線效應)和肉芽形成的風險,因此適時拔管很重要。未來有望根據淚道內視鏡所見確定最佳拔管時機。
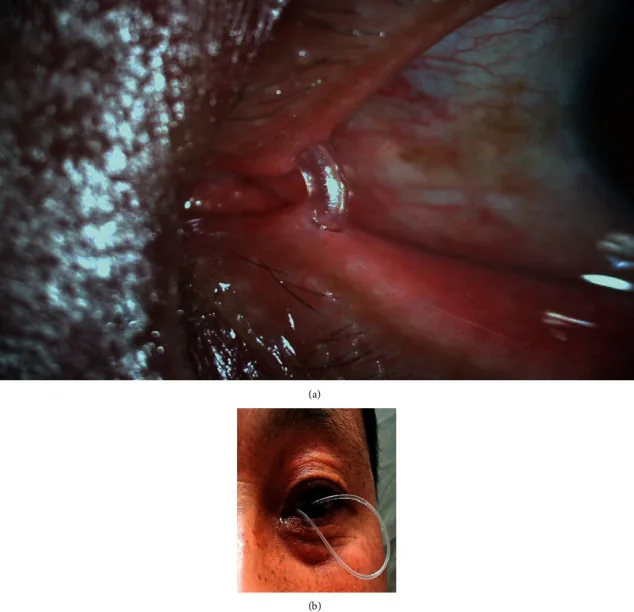
淚道內視鏡手術及置管相關的主要併發症如下所示1)。
| 併發症 | 發生時間 | 處理 |
|---|---|---|
| 黏膜裂孔形成 | 術中 | 確認皮下水腫並中止手術 |
| 黏膜下誤插入 | 術中至術後早期 | 淚道內視鏡確認、再次手術、拔管 |
| 起司切割效應 | 術後(長期留置) | 適當管理留置時間(少於9個月) |
| 肉芽形成 | 術後(長期留置) | 類固醇眼藥水 / 早期拔管 |
| 淚囊炎 / 感染性角膜炎 | 術後(長期留置) | 抗生素給藥 / 拔管 |
| 眼眶蜂窩組織炎樣皮膚腫脹 | 術後早期 | 靜脈抗生素 / 立即拔管 |
黏膜裂孔形成是淚道內視鏡操作中最需注意的術中併發症。若發生皮下積水(眼瞼腫脹),應立即停止手術。
黏膜下誤插入好發於淚囊下部的鼻背側。可能導致術後鼻出血或眼眶蜂窩組織炎。透過SGI/G-SGI法可降低發生率,但一旦發生,常需拔管和再次手術。
起司線效應是指淚點向淚小管水平方向呈裂隙狀撕裂的併發症。過度淚點切開或擴張是誘因。據報導,留置9個月以上時3例中全部發生1),因此必須在適當時間內拔管。
肉芽形成發生在與導管接觸的部位。透過類固醇眼藥水管理,拔管後1個月內多可消失。
淚囊炎 / 感染性角膜炎由長期留置導致細菌增殖(Moraxella lacunata、鏈球菌、綠膿桿菌等)引起。除抗生素給藥外,有時需要拔管。
眼眶蜂窩織炎樣皮膚腫脹是因黏膜下誤插入導致淚囊內細菌擴散至眼眶所致。需要靜脈注射抗生素並立即拔除導管。
拔管後定期進行淚道沖洗以確認通暢性。對於鼻淚管阻塞,長期存在再阻塞風險,因此需持續追蹤觀察流淚症狀是否復發。再阻塞時考慮重新插管或轉為DCR。
淚液從淚點經淚小管(上、下)→總淚小管→淚囊→鼻淚管→下鼻道開口(Hasner瓣)排入鼻腔。任何部位阻塞都會導致流淚和眼部分泌物。
淚小管從淚點開始,先垂直部(約2mm)後水平部(約8mm),上下淚小管匯合形成總淚小管。理解這一結構是內視鏡操作的基礎。
淚點及淚小管阻塞主要由Stevens-Johnson症候群、眼類天皰瘡、慢性炎症導致的黏膜瘢痕形成或外傷後沾黏引起。TS-1、5-FU等抗癌藥通過直接損傷淚小管上皮並引發炎症反應導致阻塞。這些藥物性阻塞主要發生在淚小管,雙側性和上下同時受累的頻率較高2)。
鼻淚管阻塞由年齡相關性纖維化、慢性炎症、感染、外傷、鼻竇疾病等多因素引起,但多數原因不明。鼻淚管入口處的解剖性狹窄被認為與之相關。阻塞發生後,淚囊內積聚淚液和黏液,導致細菌過度生長(Moraxella lacunata、鏈球菌、綠膿桿菌等),進而發展為慢性淚囊炎。
淚小管阻塞即使開通後也可能再次阻塞。預後取決於阻塞程度、炎症原因和活動性。復發風險因素包括淚囊炎病史、病程長、阻塞段長和男性1)。
隨著G-SGI(無需鼻腔內操作的SGI改良法)的普及,與鼻腔器械插入相關的疼痛和併發症風險正在降低1)。
淚道內視鏡畫素數(從6000提升至10000畫素)和焦深(1.5-7mm)的改善,使得能夠詳細觀察阻塞部位並進行術後監測1)。未來有望根據淚道內視鏡所見決定最佳拔管時機1)。
淚道內視鏡下探通術治療先天性鼻淚管阻塞已有高治癒率的報導,2022年先天性鼻淚管阻塞診療指引也建議使用該方法1)。
對於上下淚小管均無法開放的難治性病例,Jones管(CDCR)或結膜淚囊吻合術(淚囊移位術)正在作為選項進行探討1)。結膜淚囊吻合術後1年所有病例的溢淚症狀均有改善1)。
抗癌藥物相關淚道阻塞的留置時間最佳化也是一個課題;從預防再阻塞的角度,建議在持續治療期間不要拔管2)。