DEP(直接内镜探通)
操作:将泪道内镜探头本身作为探条,直接穿破闭塞部位。
特点:操作简单。可同时进行观察和穿破,但由于不使用鞘管,插管需另行SGI法。
适应症:闭塞部位明确且能确保穿破方向的病例。

泪道插管术(泪管插管术)是针对泪点、泪小管、总泪小管、鼻泪管的阻塞或狭窄,留置硅胶管以重新开通并维持泪道通畅的手术方式。根据阻塞部位不同,操作技术差异很大,各自有相应的手术入路。
在日常眼科诊疗中,主诉溢泪的患者常存在泪道狭窄或阻塞。裂隙灯检查发现泪液半月面增高,荧光素染色清除延迟,则提示泪道阻塞可能性大,通过泪道冲洗检查可确诊。
泪道置管术的主要目的是在阻塞的泪道中留置硅胶管一段时间,以恢复管腔通畅,促进黏膜自然再生。这不是根治性手术,效果因阻塞部位和严重程度而异。
对于鼻泪管阻塞,DCR(泪囊鼻腔吻合术)作为根治性治疗,成功率达90–99% 3),但置管术是一种创伤更小的选择,有时作为根治手术前的桥接治疗。术前需向患者充分说明鼻泪管阻塞置管的效果不佳。
随着泪道内镜(外径0.7–0.9 mm,6000–10000像素纤维镜)的发展,可以直接观察阻塞部位并进行穿通和置管 1)。DEP(直接内镜探通)和SEP(鞘引导内镜探通)等穿通方法,以及SGI(鞘引导插管)和G-SGI等置管方法已普及,降低了黏膜下误插的风险 1)。
泪道阻塞根据阻塞部位大致分为四型。
| 阻塞部位 | 主要原因 | 置管时间 | 成功率 |
|---|---|---|---|
| 泪点阻塞 | SJS、化学腐蚀后瘢痕、慢性炎症 | 1–2个月 | 81.8–100%1) |
| 泪小管阻塞(1级) | 炎症性瘢痕、EKC后 | 2至10个月 | 94%(878天后)1) |
| 泪小管阻塞(2-3级) | 抗癌药物相关、广泛瘢痕 | 个体判断 | 难治 |
| 鼻泪管阻塞 | 老化、感染、原因不明 | 2至12个月 | 70至87%(1年后)1) |
泪点阻塞主要由烧伤、化学腐蚀后、Stevens-Johnson综合征(SJS)、眼类天疱疮等慢性炎症引起的瘢痕所致。青光眼滴眼液(噻吗洛尔、多佐胺等)和TS-1(替加氟、吉美嘧啶、奥替拉西钾)等药物性原因也是重要因素。
泪小管和总泪小管阻塞由炎症性瘢痕和术后粘连引起。采用矢部·铃木分类(1-3级)评估严重程度,治疗难度差异很大。
鼻泪管阻塞是从泪囊到下鼻道开口处的阻塞,其中鼻泪管入口处阻塞最为常见。它被认为是老年人及女性中常见的后天性泪道疾病。
泪小管阻塞的严重程度评估采用矢部·铃木分类1)。根据阻塞的程度和部位,治疗难度差异很大,因此术前准确分类非常重要。
| 分级 | 定义 | 治疗难度 |
|---|---|---|
| 1级 | 可插入探针≥11mm,上下泪点间交通存在(总泪小管阻塞) | 标准 |
| 2级 | 上下泪点间无交通,可插入探针≥7~8mm | 高 |
| 3级 | 阻塞位置比2级更近端 | 非常高 |
无论阻塞部位如何,以下主要症状普遍存在。
使用TS-1(替加氟/吉美嘧啶/奥替拉西钾复方制剂)或5-FU(氟尿嘧啶)进行抗癌治疗期间发生的泪道阻塞容易重症化。泪点和泪小管受累约占60%1),建议早期置管。抗癌治疗期间拔管容易再次阻塞,因此治疗持续期间最好维持置管1)。抗癌药相关性泪道阻塞常为双侧性、上下泪小管同时受累,尤其难治2)。
获得性鼻泪管阻塞是成人流泪的主要原因之一,好发于女性和老年人。年龄相关的泪道纤维化和炎症性改变被认为是主要背景因素。
先天性鼻泪管阻塞常见于新生儿和婴儿期,但90%以上在1岁前自然痊愈,因此以观察为主。对于1岁后仍残留的病例或伴有复发性泪囊炎的病例,可考虑探通或泪道内镜手术1)。
TS-1和5-FU等抗癌药引起的药物性泪道阻塞有一定发生频率,阻塞进展后容易成为难治病例2)。建议从给药早期开始观察流泪症状,一旦确认阻塞,应尽快置管1)。
**泪道冲洗检查(通水检查)**是最基本的确定诊断方法,鼻泪管阻塞时可见泪囊内黏液从泪点反流。该检查创伤小,可在门诊进行。
泪囊造影显示造影剂在鼻泪管入口处及以后中断,并可见泪囊扩张。有助于估计阻塞水平,但与内镜所见的一致率约为70% 1)。
泪道内镜检查是使用外径0.7~0.9mm的纤维内镜直接观察泪道内腔的检查方法,于2018年被纳入医保 1)。有助于准确确定阻塞部位(鉴别总泪小管阻塞还是鼻泪管阻塞)、评估纤维化程度和黏膜炎症、发现泪道内肿物。通水检查对阻塞部位的估计与泪道内镜所见的一致率约为70%,因此内镜直接观察具有重要意义 1)。
术前CT(眼眶和鼻窦)用于手术适应症病例,以评估泪囊窝和鼻腔的形态以及有无鼻窦炎。
它是一种使用外径0.7~0.9mm的超细纤维内镜直接观察泪道内腔的装置。可以准确确定阻塞部位,并在内镜下进行穿通和置管。与通水检查的一致率约为70%,泪道内镜能提供更准确的诊断。该检查于2018年被纳入医保,对于评估阻塞部位的纤维化程度、黏膜炎症和泪道内肿物特别有用。
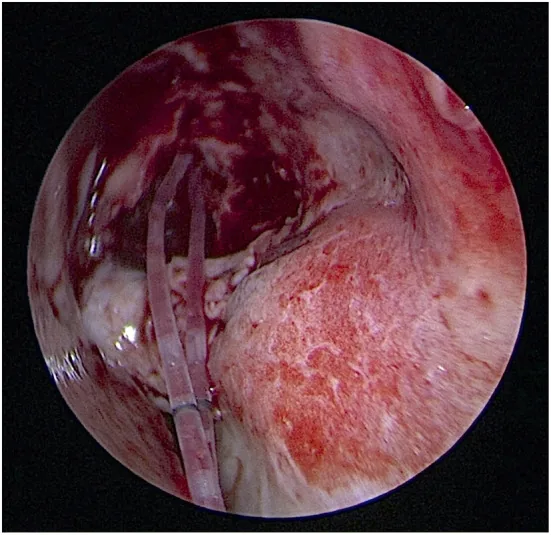
治疗方法根据阻塞部位、严重程度以及患者的状况和意愿选择。
在点眼麻醉下,用泪点扩张针或尖刀切开并扩张泪点。留置泪点塞2-4周后拔除,若再次闭塞,则重新切开泪点,留置泪小管硅胶管1-2个月后拔除。拔管后3-12个月的成功率据报道为81.8-100% 1)。
用4%盐酸利多卡因进行泪道内麻醉后,用泪点扩张针充分扩张泪小管。从泪点插入双头或导管型硅胶管,但需仔细感受闭塞部位的阻力,逐步推进管尖,切勿强行操作。金属探针有形成假道的风险,需特别谨慎。留置时间一般为1-2个月。
泪道内镜下的治疗:使用DEP或SEP穿破闭塞部位,通过SGI/G-SGI插入硅胶管1)。1级(总泪小管闭塞)在878天后的通畅率为94%,效果良好1)。2级和3级难度显著增加,穿破困难时需考虑中止手术。
经泪点入路不可行的总泪小管闭塞:采用皮肤切口入路。沿前泪嵴做15-20mm皮肤切口,切开泪囊,在显微镜直视下确认总泪点位置后穿破闭塞部位。内眦腱的高度可作为总泪点位置的参考。
术前需向患者充分说明鼻泪管闭塞的插管手术效果不佳。合并慢性泪囊炎时再闭塞率高达45-80%。合并急性泪囊炎时,需先切开引流并使用抗生素消炎后再制定手术计划。
使用DEP或SEP穿破闭塞部位,通过SGI/G-SGI将硅胶管引导至鼻腔并插入。留置时间2-12个月。拔管后1年成功率为70-87% 1),拔管后3000天的通畅率为64%,存在长期复发风险1)。复发风险因素包括泪囊炎病史、病程长、闭塞距离长和男性1)。
DEP(直接内镜探通)
操作:将泪道内镜探头本身作为探条,直接穿破闭塞部位。
特点:操作简单。可同时进行观察和穿破,但由于不使用鞘管,插管需另行SGI法。
适应症:闭塞部位明确且能确保穿破方向的病例。
SEP(鞘管引导内镜探通)
操作:将特氟龙泪道鞘作为外套管安装,用鞘尖端穿破阻塞部位。
特点:可在观察管腔的同时进行穿破。穿破后可直接过渡到SGI引导的插管。
适应症:需要仔细确认穿破方向的病例。可降低黏膜下误入的风险。
SGI(鞘引导插管) 是将鞘留置在泪道内,将导管连接在鞘内,然后从鼻腔拔出鞘,将导管引导至鼻腔的方法。直接插管(DSI)据报道有22%的黏膜下误入率1),因此推荐SGI方法。
G-SGI 是SGI的改良方法,无需鼻腔内操作。鞘上设有割线,可从泪点侧拔出鞘,从而减少鼻腔器械插入相关的疼痛和并发症风险。
插入内镜时,要注意泪小管的垂直部和水平部等结构。向外牵拉眼睑使泪小管变直,可从泪点上点几乎直线到达泪囊。灌流液应缓慢注入,避免快速灌流压引起疼痛。
因阻塞部位而异。泪点或泪小管阻塞留置12个月,鼻泪管阻塞留置212个月。长期留置(9个月以上)会增加泪点撕裂(奶酪丝效应)和肉芽形成的风险,因此适时拔管很重要。未来有望根据泪道内镜所见确定最佳拔管时机。
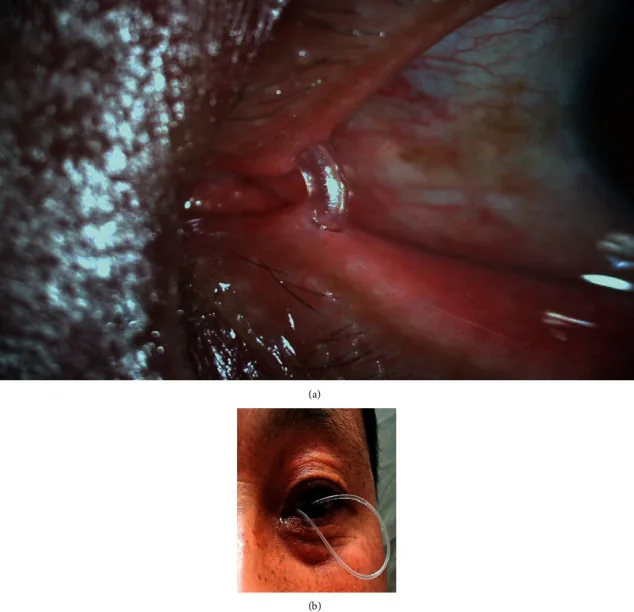
泪道内镜手术及置管相关的主要并发症如下所示1)。
| 并发症 | 发生时间 | 处理 |
|---|---|---|
| 黏膜裂孔形成 | 术中 | 确认皮下水肿并中止手术 |
| 黏膜下误插入 | 术中至术后早期 | 泪道内镜确认、再次手术、拔管 |
| 奶酪切割效应 | 术后(长期留置) | 合理管理留置时间(少于9个月) |
| 肉芽形成 | 术后(长期留置) | 类固醇滴眼液 / 早期拔管 |
| 泪囊炎 / 感染性角膜炎 | 术后(长期留置) | 抗生素给药 / 拔管 |
| 眼眶蜂窝织炎样皮肤肿胀 | 术后早期 | 静脉抗生素 / 立即拔管 |
黏膜裂孔形成是泪道内镜操作中最需注意的术中并发症。若发生皮下水肿(眼睑肿胀),应立即停止手术。
黏膜下误插入好发于泪囊下部的鼻背侧。可导致术后鼻出血或眼眶蜂窝织炎。通过SGI/G-SGI法可降低发生率,但一旦发生,常需拔管和再次手术。
奶酪丝效应是指泪点向泪小管水平方向呈裂隙状撕裂的并发症。过度泪点切开或扩张是诱因。据报道,留置9个月以上时3例中全部发生1),因此必须在适当时间内拔管。
肉芽形成发生在与导管接触的部位。通过类固醇滴眼液管理,拔管后1个月内多可消失。
泪囊炎 / 感染性角膜炎由长期留置导致细菌增殖(Moraxella lacunata、链球菌、铜绿假单胞菌等)引起。除抗生素给药外,有时需要拔管。
眼眶蜂窝织炎样皮肤肿胀是由于黏膜下误插入导致泪囊内细菌扩散至眼眶所致。需要静脉注射抗生素并立即拔除导管。
拔管后定期进行泪道冲洗以确认通畅性。对于鼻泪管阻塞,长期存在再阻塞风险,因此需持续随访观察流泪症状是否复发。再阻塞时考虑重新插管或转为DCR。
泪液从泪点经泪小管(上、下)→总泪小管→泪囊→鼻泪管→下鼻道开口(Hasner瓣)排入鼻腔。任何部位阻塞都会导致流泪和眼部分泌物。
泪小管从泪点开始,先垂直部(约2mm)后水平部(约8mm),上下泪小管汇合形成总泪小管。理解这一结构是内镜操作的基础。
泪点及泪小管阻塞主要由Stevens-Johnson综合征、眼类天疱疮、慢性炎症导致的黏膜瘢痕形成或外伤后粘连引起。TS-1、5-FU等抗癌药通过直接损伤泪小管上皮并引发炎症反应导致阻塞。这些药物性阻塞主要发生在泪小管,双侧性和上下同时受累的频率较高2)。
鼻泪管阻塞由年龄相关性纤维化、慢性炎症、感染、外伤、鼻窦疾病等多因素引起,但多数原因不明。鼻泪管入口处的解剖性狭窄被认为与之相关。阻塞发生后,泪囊内积聚泪液和黏液,导致细菌过度生长(Moraxella lacunata、链球菌、铜绿假单胞菌等),进而发展为慢性泪囊炎。
泪小管阻塞即使开通后也可能再次阻塞。预后取决于阻塞程度、炎症原因和活动性。复发风险因素包括泪囊炎病史、病程长、阻塞段长和男性1)。
随着G-SGI(无需鼻腔内操作的SGI改良法)的普及,与鼻腔器械插入相关的疼痛和并发症风险正在降低1)。
泪道内窥镜像素数(从6000提升至10000像素)和焦深(1.5-7mm)的改善,使得能够详细观察阻塞部位并进行术后监测1)。未来有望根据泪道内窥镜所见确定最佳拔管时机1)。
泪道内窥镜下探通术治疗先天性鼻泪管阻塞已有高治愈率的报道,2022年先天性鼻泪管阻塞诊疗指南也建议使用该方法1)。
对于上下泪小管均无法开放的难治性病例,Jones管(CDCR)或结膜泪囊吻合术(泪囊移位术)正在作为选择进行探讨1)。结膜泪囊吻合术后1年所有病例的溢泪症状均有改善1)。
抗癌药物相关泪道阻塞的留置时间优化也是一个课题;从预防再阻塞的角度,建议在持续治疗期间不要拔管2)。