DEP(direct endoscopic probing)
手技:涙道内視鏡プローブそのものをブジーとして使用し、閉塞部を直接穿破する。
特徴:シンプルな手技。観察と穿破を同時に行えるが、シースを用いないためチューブ挿入はSGI法を別途要する。
適応:閉塞部位が明瞭で穿破方向が確保できる症例。

涙道チューブ挿入術(涙管チューブ挿入術)は、涙点・涙小管・総涙小管・鼻涙管の閉塞・狭窄に対してシリコンチューブを留置し、涙道の通過性を再開通・維持する手術術式である。閉塞部位により手技が大きく異なり、それぞれに適した手術アプローチが存在する。
眼科日常診療において流涙を訴える患者では涙道狭窄や閉塞を認める場合が多い。細隙灯検査で涙液メニスカスの高位を認め、フルオレセイン染色のクリアランスが遅延していれば涙道閉塞の可能性が高く、涙洗(通水)検査で確定診断を行う。
涙道チューブ挿入術の主目的は、閉塞した涙道にシリコンチューブを一定期間留置することで管腔の開通を図り、自然治癒的な粘膜再生を促すことである。根治的な術式ではなく、閉塞部位・重症度によって成績に差がある。
鼻涙管閉塞に対してはDCR(涙囊鼻腔吻合術)が根治的治療として成功率90〜99%と優れているが3)、チューブ挿入術はより低侵襲な選択肢として根治手術の前段階(ブリッジ治療)に位置づけられる場合がある。なお、鼻涙管閉塞に対するチューブ留置の成績は良好でないことを術前に患者へ十分説明する必要がある。
涙道内視鏡(外径0.7〜0.9mm、6,000〜10,000画素のファイバースコープ)の開発により、閉塞部位を直接観察しながら穿破・チューブ挿入が可能となった1)。DEP(direct endoscopic probing)やSEP(sheath-guided endoscopic probing)による穿破法、SGI(sheath-guided intubation)やG-SGIによるチューブ挿入法が普及し、粘膜下誤挿入のリスクが軽減された1)。
涙道閉塞は閉塞部位によって4型に大別される。
| 閉塞部位 | 主な原因 | チューブ留置期間 | 成功率 |
|---|---|---|---|
| 涙点閉塞 | SJS・化学腐食後瘢痕・慢性炎症 | 1〜2か月 | 81.8〜100%1) |
| 涙小管閉塞(grade 1) | 炎症性瘢痕・EKC後 | 2〜10か月 | 94%(878日後)1) |
| 涙小管閉塞(grade 2-3) | 抗癌剤関連・広範瘢痕 | 個別判断 | 難治 |
| 鼻涙管閉塞 | 加齢・感染・原因不明 | 2〜12か月 | 70〜87%(1年後)1) |
涙点閉塞は熱傷・化学腐食後・Stevens-Johnson症候群(SJS)・眼類天疱瘡などの慢性炎症による瘢痕が主な原因である。緑内障点眼薬(チモロール・ドルゾラミド等)やTS-1(テガフール・ギメラシル・オテラシルカリウム)などの薬剤性も重要な原因となる。
涙小管・総涙小管閉塞は炎症性瘢痕・術後癒着によって生じる。矢部・鈴木分類(grade 1〜3)で重症度を評価し、治療難易度が大きく異なる。
鼻涙管閉塞は涙囊から下鼻道開口部にかけての閉塞で、鼻涙管入口部閉塞が最多である。高齢者・女性に多い後天性涙道疾患として知られる。
涙小管閉塞の重症度評価には矢部・鈴木分類が用いられる1)。閉塞の程度・部位によって治療難易度が大きく異なり、術前の正確な分類が重要である。
| Grade | 定義 | 治療難易度 |
|---|---|---|
| Grade 1 | ブジー11mm以上挿入可、上下涙点間交通あり(総涙小管閉塞) | 標準 |
| Grade 2 | 上下涙点間交通なし、ブジー7〜8mm以上挿入可 | 高い |
| Grade 3 | Grade 2よりも近位で閉塞 | 非常に高い |
閉塞部位にかかわらず、主症状として以下が共通して認められる。
TS-1(テガフール・ギメラシル・オテラシルカリウム配合剤)や5-FU(フルオロウラシル)による抗癌治療中に生じた涙道閉塞は重症化しやすい。涙点・涙小管障害が約60%を占め1)、早期のチューブ挿入が推奨される。抗癌剤使用中にチューブを抜去すると再閉塞しやすいため、治療継続中はチューブ留置を維持することが望ましい1)。抗癌剤関連涙道閉塞は両側性・上下涙小管同時障害が多く、特に難治である2)。
後天性鼻涙管閉塞は成人流涙症の主要原因のひとつであり、女性・高齢者に好発する。加齢に伴う涙道の線維化・炎症性変化が主な背景とされる。
先天性鼻涙管閉塞は新生児・乳児期に多く認められるが、90%以上が1歳までに自然治癒するため、経過観察が基本である。1歳以降も残存する症例や反復性涙囊炎を伴う場合にはプロービングや涙道内視鏡下手術が考慮される1)。
TS-1や5-FUなどの抗癌剤による薬剤性涙道閉塞は一定頻度で生じ、閉塞が進行すると難治例となりやすい2)。投与開始早期から流涙症状を観察し、閉塞が確認された時点で速やかにチューブ挿入を行うことが推奨される1)。
**涙洗検査(通水検査)**は最も基本的な確定診断法であり、鼻涙管閉塞では涙囊内の粘液が涙点から逆流する所見が観察される。侵襲が低く外来で施行可能である。
涙囊造影では造影剤が鼻涙管入口部以降で途絶し、涙囊拡大所見がみられる。閉塞レベルの推定に有用だが、内視鏡所見との一致率は約70%程度である1)。
涙道内視鏡検査は外径0.7〜0.9mmのファイバースコープで涙道内腔を直接観察する検査法であり、2018年に保険収載された1)。閉塞部位の正確な特定(総涙小管閉塞か鼻涙管閉塞かの鑑別)、線維化の程度・粘膜炎症の評価、涙道内腫瘤の発見に有用である。通水検査による閉塞部位推定と涙道内視鏡所見の一致率は70%前後であり、内視鏡による直接観察の意義は大きい1)。
術前CT(眼窩・副鼻腔)は手術適応症例において涙囊窩・鼻腔の形状、副鼻腔炎の有無を確認するために行う。
外径0.7〜0.9mmの極細ファイバースコープで涙道内腔を直接観察する装置です。閉塞部位の正確な特定と内視鏡下での穿破・チューブ挿入が可能です。通水検査との一致率は70%前後であり、涙道内視鏡でより正確な診断が得られます。2018年に保険収載されており、閉塞部の線維化の程度・粘膜炎症・涙道内腫瘤の評価に特に有用です。
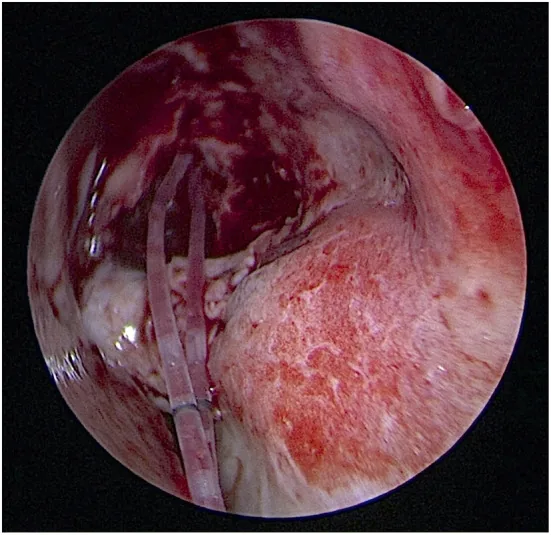
治療法は閉塞部位・重症度・患者の状態と希望に応じて選択する。
点眼麻酔下に涙点拡張針または尖刃で涙点を切開・拡張する。2〜4週間の涙点プラグ留置後に抜去し、再閉塞が認められた場合は涙点を再切開したうえで涙小管シリコンチューブを1〜2か月留置後に抜去する。チューブ抜去後3〜12か月の成功率は81.8〜100%と報告されている1)。
4%リドカイン塩酸塩液による涙道内麻酔を行ったのち、涙点拡張針で十分に涙小管を拡張する。涙点からヌンチャク型またはカテーテルタイプのシリコンチューブを挿入するが、閉塞部位の感触を慎重に確かめながら少しずつチューブ先端を進め、無理をしてはならない。金属ブジーは誤道形成のリスクがあり特に慎重に扱う。留置期間は1〜2か月が基本である。
涙道内視鏡下での治療はDEPまたはSEPで閉塞部を穿破し、SGI/G-SGIでチューブを挿入する1)。Grade 1(総涙小管閉塞)では878日後の開存率が94%と良好な成績が報告されている1)。Grade 2・3では難易度が格段に高く、穿破困難時は手術を中止する判断も必要である。
経涙点アプローチが不能な総涙小管閉塞では皮膚切開からのアプローチを行う。前涙囊稜に沿って15〜20mmの皮膚切開をおき、涙囊を切開したうえで顕微鏡直視下に総涙点の位置を確認しながら閉塞部を穿孔する。内眼角腱の高さが総涙点位置の目安となる。
鼻涙管閉塞に対するチューブ挿入術の成績は良好でないことを術前に患者へ十分に説明する。慢性涙囊炎を合併した場合の再閉塞率は45〜80%と高い。急性涙囊炎合併例では切開排膿・抗菌薬による消炎後に手術計画を立てる。
DEPまたはSEPで閉塞部を穿破し、SGI/G-SGIでチューブを鼻腔へ誘導して挿入する。チューブ留置期間は2〜12か月。抜去後1年の成功率は70〜87%1)、チューブ抜去後3,000日の開存率は64%と長期的な再発リスクがある1)。再発リスク因子として涙囊炎既往・長期罹病期間・長い閉塞距離・男性が挙げられる1)。
DEP(direct endoscopic probing)
手技:涙道内視鏡プローブそのものをブジーとして使用し、閉塞部を直接穿破する。
特徴:シンプルな手技。観察と穿破を同時に行えるが、シースを用いないためチューブ挿入はSGI法を別途要する。
適応:閉塞部位が明瞭で穿破方向が確保できる症例。
SEP(sheath-guided endoscopic probing)
手技:テフロン製涙道シースを外筒として装着し、シース先端で閉塞部を穿破する。
特徴:管腔を観察しながら穿破可能。穿破後そのままSGIによるチューブ挿入へ移行できる。
適応:穿破方向の慎重な確認が必要な症例。粘膜下誤挿入リスクを低減できる。
**SGI(sheath-guided intubation)**はシースを涙道内に留置し、チューブをシース内に接続後、鼻腔よりシースを引き抜いてチューブを鼻腔へ誘導する方法である。チューブの直接挿入(DSI)では22%に粘膜下誤挿入が報告されており1)、SGIによる方法が推奨される。
G-SGIはSGIの変法で、鼻腔内操作を必要としない術式である。シースに割線を入れることで涙点側からシースを抜去できる設計となっており、鼻腔への器具挿入に伴う疼痛・合併症リスクを低減できる。
内視鏡を挿入する際は涙小管の垂直部・水平部といった構造を意識する。眼瞼を外側へ牽引し涙小管を直線化することで、上涙点からほぼ直線的に涙囊へ到達できる。灌流液は少しずつ流し、急激な灌流圧は疼痛を誘発するため避ける。
閉塞部位により異なります。涙点・涙小管閉塞では1〜2か月、鼻涙管閉塞では2〜12か月の留置が報告されています。長期留置(9か月以上)ではチーズワイヤリング(涙点裂傷)や肉芽形成のリスクが高まるため、適切な時期での抜去が重要です。涙道内視鏡所見をもとに最適な抜去時期を判断することが今後期待されています。
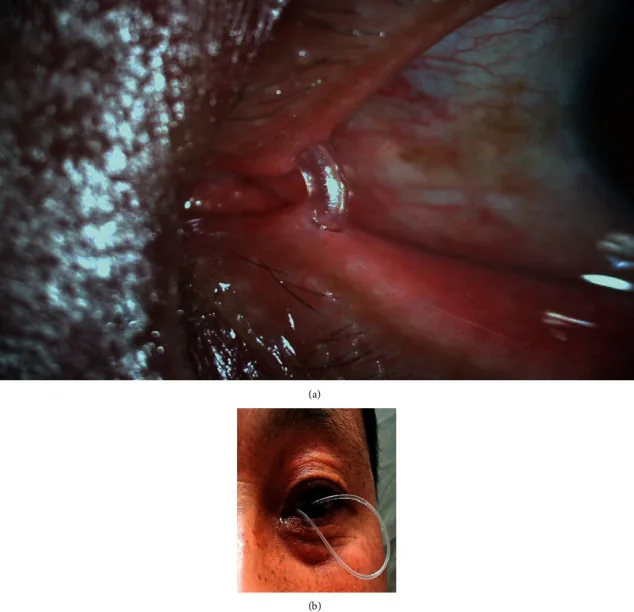
涙道内視鏡手術およびチューブ留置に伴う主な合併症を以下に示す1)。
| 合併症 | 発生時期 | 対処 |
|---|---|---|
| 粘膜裂孔形成 | 術中 | 皮下水腫を確認し手術中止 |
| 粘膜下誤挿入 | 術中〜術後早期 | 涙道内視鏡で確認・再手術・チューブ抜去 |
| チーズワイヤリング | 術後(長期留置) | 留置期間の適正管理(9か月未満) |
| 肉芽形成 | 術後(長期留置) | ステロイド点眼・チューブ早期抜去 |
| 涙囊炎・感染性角膜炎 | 術後(長期留置) | 抗菌薬投与・チューブ抜去 |
| 眼窩蜂巣炎様皮膚腫脹 | 術後早期 | 抗菌薬点滴・チューブ即時抜去 |
粘膜裂孔形成は涙道内視鏡操作中に最も注意すべき術中合併症である。皮下水腫(眼瞼浮腫)が生じた場合は直ちに手術を中止する。
粘膜下誤挿入は涙囊下部の鼻背側に好発する。術後鼻出血や眼窩蜂巣炎の原因となる。SGI/G-SGI法により発生率を低減できるが、発生した場合はチューブ抜去と再手術が必要になることが多い。
チーズワイヤリングは涙点が涙小管の水平部方向にスリット状に裂ける合併症である。過剰な涙点切開・拡張が誘因となる。9か月以上の長期留置では3例中3例で発生したとの報告1)があり、適切な期間での抜去が必須である。
肉芽形成はチューブとの接触部位に生じる。ステロイド点眼で管理し、抜去後1か月以内に消失することが多い。
涙囊炎・感染性角膜炎は長期留置による細菌増殖(Moraxella lacunata・連鎖球菌・緑膿菌等)が原因である。抗菌薬投与に加えてチューブ抜去が必要になることがある。
眼窩蜂巣炎様皮膚腫脹は粘膜下誤挿入によって涙囊内細菌が眼窩内へ波及することで生じる。抗菌薬点滴とチューブの即時抜去が必要である。
チューブ抜去後は定期的な涙道洗浄で通過性を確認する。鼻涙管閉塞では長期経過で再閉塞リスクがあるため、流涙症状の再燃がないか経過観察を継続する。再閉塞時はチューブ再挿入またはDCRへの移行を検討する。
涙液は涙点から涙小管(上・下)→総涙小管→涙囊→鼻涙管→下鼻道開口部(Hasner弁)の経路で鼻腔へ排出される。いずれかの部位に閉塞が生じると流涙・眼脂として発症する。
涙小管は涙点から垂直部(約2mm)→水平部(約8mm)へ移行し、上下涙小管は合流して総涙小管となる。この構造を理解することが内視鏡操作の基本となる。
涙点・涙小管の閉塞はStevens-Johnson症候群・眼類天疱瘡・慢性炎症による粘膜瘢痕形成、または外傷後の癒着が主な機序である。TS-1・5-FUなどの抗癌剤は涙小管上皮の直接傷害と炎症反応により閉塞を引き起こす。これらの薬剤性閉塞は涙小管主体に生じ、両側性・上下同時障害の頻度が高い2)。
鼻涙管閉塞は加齢性の線維化・慢性炎症・感染・外傷・副鼻腔疾患など複合的要因で生じるが、多くは原因不明である。鼻涙管入口部の解剖学的狭小が関与すると考えられている。閉塞が生じると涙囊内に涙液・粘液が貯留し、細菌の過剰増殖(Moraxella lacunata・連鎖球菌・緑膿菌等)が起こり慢性涙囊炎へ進展する。
涙小管閉塞は一度開通しても再閉塞することがある。閉塞の程度・炎症の原因・活動性によって予後が左右される。再発リスク因子として涙囊炎既往・長期罹病期間・長い閉塞距離・男性が挙げられる1)。
G-SGI(鼻腔内操作不要のSGI変法)の普及により、鼻腔への器具挿入に伴う疼痛・合併症リスクが低減されつつある1)。
涙道内視鏡の画素数向上(6,000→10,000画素)と焦点深度の改善(1.5〜7mm対応)により、閉塞部位の詳細な観察と術後モニタリングが可能となった1)。涙道内視鏡所見をもとにした最適なチューブ抜去時期の決定が今後期待されている1)。
先天鼻涙管閉塞に対する涙道内視鏡下プロービングは高い治癒率が報告されており、先天鼻涙管閉塞診療ガイドライン(2022年)でも使用が提案されている1)。
上下涙小管とも開放不可の難治例に対して、Jones tube(CDCR)や結膜涙囊吻合術(涙囊移動術)が選択肢として検討されている1)。結膜涙囊吻合術は術後1年で全例に流涙改善が報告されている1)。
抗癌剤関連涙道閉塞における留置期間の最適化も課題であり、治療継続中はチューブを抜去しないことが再閉塞予防の観点から推奨されている2)。