放線菌性(最多)
起因菌: Actinomyces israelii
嫌気性・グラム陽性糸状菌。涙小管内の嫌気的環境に最も適応しており、硫黄顆粒(sulfur granule)を形成する。菌石は放線菌コロニーにカルシウムが沈着して成長する。

涙小管炎(canaliculitis)は、涙道系を構成する涙小管(上涙小管・下涙小管)に生じる慢性感染性炎症である。起因菌の多くは涙小管内に菌石(concretion / dacryolith)を形成する放線菌(Actinomyces israelii)であり、まれにPropionibacterium、連鎖球菌などの細菌や真菌(Aspergillus、Candida)によっても起こる。
涙道は涙点→涙小管(上下)→総涙小管→涙囊→鼻涙管の順に連続する構造であり、涙小管炎はこの涙道系の中で涙小管に限局した感染である。下涙小管に好発し、中高年女性に多い。
片眼性の難治性結膜炎として眼科外来を受診することが多く、適切な診断・治療に至るまでに時間を要する場合がある。涙点の特徴的な変化(拡張・発赤・分泌物の圧出)に気づくことが早期診断のポイントとなる。
放線菌性(最多)
起因菌: Actinomyces israelii
嫌気性・グラム陽性糸状菌。涙小管内の嫌気的環境に最も適応しており、硫黄顆粒(sulfur granule)を形成する。菌石は放線菌コロニーにカルシウムが沈着して成長する。
細菌性
起因菌: Propionibacterium, Nocardia, 連鎖球菌, 黄色ブドウ球菌, 緑膿菌
Nocardia は好気性放線菌に分類される。Fusobacterium は嫌気性菌であり、これらも菌石を形成しうる。
真菌性
起因菌: Aspergillus, Candida
まれであるが難治性となりやすい。抗真菌薬(ピマリシン点眼等)の追加が必要となる場合がある。
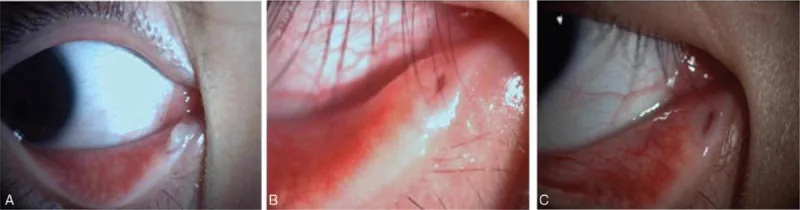
主訴は充血、眼脂、流涙であり、片眼性の慢性結膜炎に類似した症状を示す。多くの場合、下涙小管に病変が生じる。初期には慢性結膜炎として抗菌薬点眼が処方されるが改善せず、難治性の経過をたどることが多い。
| 所見 | 内容 | 臨床的意義 |
|---|---|---|
| 涙点の拡張(punch-out appearance) | 涙点が拡大し、発赤を呈する | 最も特徴的な所見。涙小管炎を疑う端緒となる |
| 涙点周囲の腫脹 | 涙小管の走行に一致した索状腫脹 | 涙小管内の炎症・菌塊の存在を示唆 |
| 圧迫による分泌物排出 | 涙点圧迫で膿性・硫黄顆粒様の分泌物が排出される | 病的特異性が高い(pathognomonic)所見 |
| 瞼結膜の炎症 | 充血・肥厚・乳頭増殖 | 難治性結膜炎像 |
涙点圧迫による硫黄顆粒様分泌物の排出は涙小管炎に高い特異度を持つ所見であり、この所見が確認できれば臨床診断がほぼ確定する。
肉眼で黄色〜白色の顆粒状物質として観察される菌塊であり、放線菌のコロニーにカルシウム塩が沈着したものである。「硫黄」は外見の色・形状からつけられた名称であり、硫黄そのものではない。顕微鏡下では放線菌の糸状菌体が密集した構造が確認できる。
硫黄顆粒が涙小管内に停留・成長して形成される結石様物質である。菌石が涙小管内に存在すると慢性炎症が持続し、抗菌薬単独では治癒しない原因となる。
中高年女性に多く、片眼性の難治性結膜炎として眼科外来を受診するパターンが多い。下涙小管に好発することが知られている。明確な人口動態データは限られているが、流涙・眼脂を主訴とする患者において慢性結膜炎との鑑別が重要である。
涙道閉塞症例においては涙道内に結石(dacryolith)が高率に合併する。涙道内視鏡診療の手引きによれば、涙囊結石は鼻涙管閉塞症例の7.5%に合併するとされており1)、涙道系全体を通じて結石形成の素因が存在しうることを示している。
ドライアイ治療のために使用される涙点プラグが涙小管内に迷入し、異物反応・炎症の核として涙小管炎を惹起する症例がある1)。涙点プラグ留置歴のある患者が難治性結膜炎を呈する場合は、プラグ迷入による涙小管炎を念頭に置く必要がある。
片眼性の難治性結膜炎が続く場合、涙小管炎を積極的に疑うことが重要である。外来での診断手順を以下に示す。
Step 1: 涙点の視診 涙点の発赤・拡張(punch-out appearance)の有無を確認する。
Step 2: 涙点圧迫テスト 涙小管の走行に沿って涙点を圧迫し、分泌物の排出を確認する。膿性・硫黄顆粒様の分泌物が排出されれば涙小管炎の臨床診断が確立する。
Step 3: 涙道洗浄 涙道洗浄を実施する。涙小管炎では涙道に閉塞を認めないことが多い。涙囊炎では涙道閉塞を伴うことが多いため、通過性の確認は鑑別に有用である。
Step 4: 微生物学的検査 涙小管内から排出された膿性分泌物を採取し、グラム染色・塗抹鏡検・嫌気培養を実施して起炎菌を同定する。
| 検査 | 方法・判定 | 意義 |
|---|---|---|
| グラム染色 | グラム陽性・枝分かれ糸状菌体(放線菌の特徴) | 放線菌性を迅速に推定可能 |
| 嫌気培養 | 嫌気条件下での培養 | 放線菌は嫌気性のため嫌気培養が必要 |
| 好気培養 | 通常培養 | Nocardia・Candida・Aspergillus 等の検出 |
放線菌の塗抹鏡検所見は特徴的であり、グラム陽性の枝分かれした糸状の菌体を確認することで放線菌性涙小管炎の推定診断が可能となる。
涙道内視鏡(dacryoendoscopy)は涙小管内の菌石・炎症所見を直接観察できる。菌石の正確な位置・大きさを確認し、完全摘出の確認に有用である1)。涙道内視鏡ガイド下での菌石除去は直視下操作が可能であり、術後の再発予防に寄与する2)。
| 鑑別疾患 | 特徴的所見 | 涙道洗浄 | 鑑別ポイント |
|---|---|---|---|
| 涙小管炎 | 涙点拡張・硫黄顆粒排出・索状腫脹 | 通過 | 片眼性難治性結膜炎 + 涙点所見 |
| 涙囊炎 | 涙囊部腫脹・涙囊圧迫で大量の膿逆流 | 閉塞 | 涙道閉塞・涙囊部の腫脹が主体 |
| 慢性結膜炎 | 瞼結膜の充血・肥厚 | 正常 | 両眼性が多い・涙点所見なし |
| 霰粒腫 | 眼瞼皮下の無痛性腫瘤 | 正常 | 眼瞼腫瘤中心・涙点所見なし |
涙小管炎は涙点周囲の腫脹・涙点拡張が特徴で、涙道洗浄では閉塞を認めないことが多い。一方、涙囊炎は涙囊部(内眼角下方)の腫脹が主体であり、涙囊を圧迫すると涙点から大量の膿が逆流し、涙道洗浄では閉塞が確認される。涙点の局所所見(拡張・圧迫時の分泌物排出)の有無が最大の鑑別点となる。
涙小管内の菌塊(菌石)を完全に物理的除去することが治療の根幹である。菌石は抗菌薬が浸透しにくい密な菌塊構造をしており、抗菌薬点眼単独では菌塊ごと除去できず、治癒に至らない。外科的切開・掻爬が必須となる。
Step 1: 涙小管切開・菌塊除去
局所麻酔下に涙小管切開(canaliculotomy)を施行する。
鋭匙(curette)で涙小管内容物を徹底的に掻爬し、菌塊・菌石を完全に郭清する。菌塊残存は再発の最大原因となるため、完全除去が最重要である。
涙道内視鏡を用いる場合は直視下に菌石の摘出と完全除去の確認が可能である1)。
Step 2: 術後抗菌薬点眼・涙小管洗浄
ニューキノロン系点眼を術後継続する。
レボフロキサシン点眼液0.5%(クラビット®)を1日4〜6回投与する。ニューキノロン系点眼による涙小管洗浄も術後管理として有用である。
真菌性涙小管炎の場合は抗真菌薬(ピマリシン点眼等)の追加を考慮する。
Step 3: 全身抗菌薬・経過観察
放線菌性にはペニシリン系全身投与を数週間行う。
アモキシシリン250〜500mg(サワシリン®等)を1日3回、数週間継続する。術後は繰り返し涙道洗浄を行い、再発を予防する。培養結果に基づいて抗菌薬を適宜調整する。
涙小管切開(canaliculotomy)
菌塊の完全除去が最重要であり、不完全切除による菌塊残存は再発の主因となる。
涙道内視鏡下の菌石除去
涙道内視鏡を用いることで、菌石の正確な位置を直接観察しながら摘出できる。完全摘出の確認が可能であり、再発防止に有用とされる2)。
迷入涙点プラグへの対応
涙点プラグの迷入が原因の場合は、涙点切開による摘出または涙道内視鏡下に鼻腔内への排出を試みる1)。
| 薬剤 | 用量・用法 | 適応 |
|---|---|---|
| レボフロキサシン点眼液0.5%(クラビット®) | 1日4〜6回 | 術後継続・涙小管洗浄 |
| アモキシシリンカプセル250mg(サワシリン®等) | 1日3回、数週間 | 放線菌性(全身投与) |
| ピマリシン点眼(ナタマイシン点眼) | 1日4〜6回 | 真菌性(必要に応じて) |
菌塊の不完全摘出による再発には再手術(再切開・掻爬)を行う。涙道閉塞が進行した場合は涙管チューブ留置またはDCR(涙囊鼻腔吻合術)が必要となることもある。
通常は点眼単独では治癒しない。涙小管内に形成された菌塊(菌石)は密な構造をしており、抗菌薬が菌塊内部の菌体に到達しにくいためである。局所麻酔下に涙小管を切開し、鋭匙で菌塊を物理的に完全除去することが治療の根幹である。術後に抗菌薬点眼(ニューキノロン系)と全身投与(放線菌性はペニシリン系)を組み合わせることで治癒率が高まる。
菌塊を完全に除去できれば予後良好であり、再発は少ない。一方、菌塊の摘出が不完全で涙小管内に菌石が残存すると再発しやすい。涙道内視鏡を用いることで菌石の完全摘出を確認でき、再発防止に有用とされる。再発した場合は再切開・掻爬を行う。
涙小管は涙点に始まり、眼瞼縁に沿って水平に走行する。上涙小管・下涙小管それぞれの長さは約8〜10mmであり、合流して総涙小管(common canaliculus)を形成した後、涙囊に開口する。涙小管の内腔は扁平であり、正常では直径約0.5〜1mmである。
涙小管の内腔は外気との交通が限られており、嫌気的な環境が形成されやすい。Actinomyces israelii は偏性ないし通性嫌気性菌であり、この環境に適応して増殖しやすい。一般的な開放部位(皮膚・結膜)では増殖しにくい放線菌が、涙小管内では優位に定着できるのはこの解剖学的特性による。
菌石の構造は密なコロニーにカルシウムが沈着した固体に近い形態であり、抗菌薬分子が菌塊内部の菌体に到達しにくい。また菌塊表面のバイオフィルム様構造が薬剤の浸透を妨げる。このため、抗菌薬点眼単独では表面の菌体を部分的に除去できても菌塊全体の除去は達成できず、投薬中止後に再増殖・再燃が起こりやすい。外科的に菌塊を物理的に除去することが唯一の根本的治療となる理由はここにある。
涙道内視鏡は細径ファイバースコープを涙道内に挿入して直視下に涙道内腔を観察する技術である1)。涙小管炎においては菌石の存在・位置・大きさを直接確認でき、完全摘出の確認が可能となる2)。従来の盲目的な涙小管切開・掻爬に比べ、より確実な菌石除去が期待される。涙道内視鏡診療の手引きにおいても、涙小管結石を伴う涙小管炎では結石の完全摘出が治癒に直結するとされており1)、内視鏡技術の普及が治療成績向上に寄与している。
ドライアイ治療として広く使用される涙点プラグの迷入が涙小管炎の原因となる症例が報告されている1)。プラグが涙小管内に脱落した後、異物として炎症・感染の核となる。涙点プラグ留置例で難治性結膜炎が生じた場合は本病態を念頭に置く必要がある。対応としては涙点切開による摘出または涙道内視鏡下の鼻腔内排出が選択される。
日本涙道・涙液学会涙道内視鏡診療の手引き作成委員会. 涙道内視鏡診療の手引き. 日本眼科学会雑誌. 2023;127(10):896-917.
Ali MJ, Alam MS, Naik MN. Dacryoendoscopic features in a case of canaliculitis with concretions. Ophthalmic Plast Reconstr Surg. 2017;33:228-229.