
霰粒腫
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 霰粒腫とは
Section titled “1. 霰粒腫とは”霰粒腫(chalazion)は、瞼板(けんばん)の脂腺であるマイボーム腺に分泌物が梗塞・貯留し、その変性した内容物に対して異物反応として慢性肉芽性炎症を生じた疾患である。感染を伴わない非感染性の炎症である点が麦粒腫(ものもらい)と根本的に異なる。
マイボーム腺は瞼板内に存在する脂腺であり、涙液油層の主成分であるmeibum(脂質成分)を分泌する。その分泌液は涙液の蒸発を防ぎ、眼表面の安定化に寄与する。マイボーム腺の導管が梗塞すると、分泌物が腺管内に貯留して霰粒腫形成の基盤となる。
霰粒腫は小児・成人ともに発症する。小児では眼瞼皮膚(前葉組織)が脆弱なため、病巣が皮膚側へ浸潤・拡大する傾向がやや強い。
MGD(マイボーム腺機能不全)との関連が強く、霰粒腫は局所的なMGDとみなすこともできる。多発・繰り返す霰粒腫では、脂漏性皮膚炎や酒さ(rosacea)の合併を考慮する。これらはいずれもMGDの危険因子であり、霰粒腫の再発に関与する。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”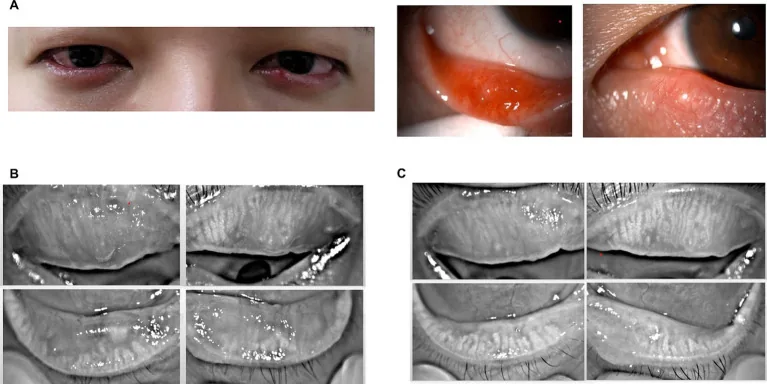
慢性期(典型像)
Section titled “慢性期(典型像)”典型的な霰粒腫では、眼瞼皮下に粟粒大〜大豆大の円形で硬い腫瘤を触知する。限局性の発赤・腫脹を認めるが自発痛はない。腫瘤は瞼板中に存在して可動性がなく、皮膚との癒着もみられない。
感染を併発した急性期には、眼瞼の浮腫・腫脹・発赤・脂質の漏出がみられ、疼痛を伴う。この時期は内麦粒腫との臨床的鑑別が困難となる。自然吸収されない場合には、腫脹・発赤が軽減する一方で眼瞼中央に無痛性の結節(慢性肉芽腫)が形成される。
- 結膜側への自壊: ポリープ状肉芽腫が結膜面から突出する
- 皮膚側への自壊: 肉芽組織が皮膚面に露出する
皮膚側への自壊は特に小児で多くみられる。
放置された霰粒腫では眼瞼の著しい腫脹・変形により、眼瞼下垂や睫毛内反を呈する場合がある。
小児の特記事項
Section titled “小児の特記事項”小児は眼瞼皮膚(前葉組織)が脆弱なため、肉芽腫性炎症が皮膚側に浸潤・拡大する傾向が強い。腫瘤の摘出を躊躇している間に眼瞼皮膚の壊死が進行するリスクがあり、適切な時期に治療を開始することが重要である。
3. 分類と病型
Section titled “3. 分類と病型”霰粒腫は病態・経過によって以下の4病型に分類される。
| 病型 | 主な特徴 | 鑑別ポイント |
|---|---|---|
| 典型的(慢性期)霰粒腫 | 無痛性・硬い腫瘤、発赤なし | 弾性に富む、皮膚との癒着なし |
| 急性霰粒腫 | 疼痛・発赤・腫脹を伴う | 内麦粒腫との鑑別困難 |
| 自壊型(結膜側) | ポリープ状肉芽腫を形成 | 結膜面からの肉芽突出 |
| 自壊型(皮膚側) | 肉芽が皮膚面に露出 | 小児に多い |
典型的(慢性期)霰粒腫は発赤や疼痛がなく、硬い無痛性腫瘤が特徴である。触診では弾性に富み、皮膚との癒着はみられない。
急性霰粒腫は感染の併発により炎症が急性化した状態で、疼痛・発赤・眼瞼腫脹を伴う。内麦粒腫との臨床的鑑別は困難であることが多い。急性期が消退すると典型的霰粒腫に移行する。
自壊型は内容物が自然に流出した状態であり、結膜側へ自壊するとポリープ状肉芽腫が形成される。皮膚側への自壊は特に小児で多く、眼瞼外観の変形を招くことがある。
4. 診断と検査方法
Section titled “4. 診断と検査方法”眼瞼皮下の硬い腫瘤を触知する。弾性に富み、皮膚との癒着はない。腫瘤は瞼板中に固着し可動性がない点が特徴である。
眼瞼を翻転して結膜面を観察する。結膜面の膨隆・発赤の確認、結膜側への自壊(ポリープ状肉芽腫)の有無を評価する。
細隙灯顕微鏡検査
Section titled “細隙灯顕微鏡検査”角膜への圧迫による乱視・角膜上皮障害の程度を評価する。大きな霰粒腫では角膜圧迫による不正乱視が生じることがある。
脂腺癌(meibomian gland carcinoma)との鑑別 — 最重要
脂腺癌は短期間の経過観察では霰粒腫と鑑別することが大変難しい。以下の所見があれば脂腺癌を強く疑う。
- 皮膚面または結膜面の表面が凹凸不整で不規則な増殖パターン
- 走行血管の口径不同や走行異常
- 上眼瞼に多い(下眼瞼よりも上眼瞼に好発する)
- 脂肪を含むため黄白色の色調を呈する
- 切開時の内容物が粥状を呈さず、黄白色の小粒状腫瘤である
薬剤への反応を観察するとともに、摘出時には必ず病理組織検索を行う。
その他の鑑別疾患:
- 内麦粒腫: 急性霰粒腫と症状が類似する。細菌感染による急性化膿性炎症
- 眼瞼血管腫(深在性): 小児では鑑別を要する。透光性・青色調の腫瘤
- 涙囊炎: 小児では内眼角付近の腫瘤として鑑別を要する
繰り返す霰粒腫ではMGD(マイボーム腺機能不全)・脂漏性皮膚炎・酒さ(rosacea)の合併を考慮する。これらはMGDの危険因子であり、霰粒腫の多発・再発に関与する。また、上眼瞼に多い再発例や黄白色の非粥状内容物を呈する例では脂腺癌との鑑別が重要であり、摘出時には必ず病理組織検査を行う姿勢が求められる。
5. 標準的な治療法
Section titled “5. 標準的な治療法”5-1. 保存的治療
Section titled “5-1. 保存的治療”温罨法(おんあっぽう)
温水で温めたタオルなどを眼瞼に10分ほど押し当て、その後眼瞼をマッサージする。加えて眼瞼のシャンプーによる洗浄を行うと、瞼縁の異常分泌物を一掃するだけでなく、擦過洗浄が眼瞼マッサージにもなるため温罨法の治療効果を高める。温罨法は初期・軽度の霰粒腫に適応となる。
ステロイド局所注射
- 薬剤: トリアムシノロン(トリアムシノロンアセトニド)
- 用量: 0.25〜0.1mL
- 投与経路: 眼瞼腫脹部位の結膜下へ注入
- 効果判定: 施行後1〜2週で腫瘤の縮小が認められれば再度施行する
初期・軽度の霰粒腫では温罨法に加えてステロイド注射を行う。線維化が進んだ腫瘤には効果が限定的となる。メタアナリシス(Aycinena ら 2016, Ophthalmic Plast Reconstr Surg[³])では、ステロイド注射の1回成功率は約60%、1〜2回で約72%である一方、切開掻爬術(I&C)の1回成功率は約78%、1〜2回で約87%と報告され、外科治療のほうが奏効率および再発抑制で優位とされている。一方、原発性霰粒腫を対象としたランダム化比較試験(Ben Simon ら 2011, Am J Ophthalmol[⁴])では、両者の有効性に有意差を認めなかった報告もあり、症例特性に応じた選択が望ましい。
5-2. 小児の保存的治療
Section titled “5-2. 小児の保存的治療”小児では全身麻酔が必要となるため、外科処置の敷居が高い。まず保存的治療を試みることが多い。
- 抗菌点眼薬を試みてもよい
- ステロイド点眼は有効であるが、眼圧上昇に注意しながら低濃度のものを使用する
- 多発・繰り返す例では急性期から抗菌点眼薬と抗菌薬(セフェム系)内服を併用する
5-3. 外科的治療(霰粒腫摘出術)
Section titled “5-3. 外科的治療(霰粒腫摘出術)”保存的治療で改善しない場合や、腫瘤が大きく外観・機能に影響する場合は外科的切除の適応となる。
麻酔
2%リドカイン塩酸塩(キシロカイン®)を用いて、結膜下および眼瞼皮下に浸潤麻酔を行う。
経結膜アプローチ(標準術式)
皮膚に切開を加えないため、皮膚瘢痕を残さない利点がある。
- 狭瞼器で霰粒腫を挟み込む
- 眼瞼を翻転させ結膜面を露出する
- 霰粒腫の部位を確認する
- 腫瘤中央に眼瞼縁に垂直な方向で2〜3mmの小切開を加える
- 貯留していた粥状物(脂肪と細胞崩壊産物の混合物)が流出する
- ガーゼや鋭匙にて粥状物を掻き出す
- 有鉤鑐子と剪刀で残存する膠原線維を十分に切除する
経眼瞼皮膚アプローチ
皮膚側への浸潤が強い例や、自壊例で皮膚の広範な処置が必要な場合に選択する。
- 狭瞼器を装着する
- 霰粒腫近傍の皮膚を眼瞼縁と平行な方向で1.5〜2cm程度切開する
- 皮下組織・眼輪筋を剝離する
- 腫瘤の直上で霰粒腫前壁を露出させる
- 眼瞼縁と平行に切開して内部の粥状物を排出する
- 有鉤鑐子と剪刀で膠原線維郭清を実施する
5-4. 小児手術の注意点
Section titled “5-4. 小児手術の注意点”- 小児は眼瞼皮膚(前葉組織)が脆弱なため、肉芽腫性炎症が皮膚側に浸潤・拡大しやすい
- 腫瘤摘出を躊躇すると、眼瞼皮膚の壊死が進行するリスクがある
- 小児では原則として全身麻酔下で手術を行う
- 多発・繰り返す例は急性期から抗菌点眼薬と抗菌薬(セフェム系)の内服を開始する
摘出検体の病理組織検査
霰粒腫と脂腺癌を短期間の経過観察で鑑別することは困難である。摘出した組織は必ず病理組織検索に提出する。特に以下の例では脂腺癌の可能性を念頭に置く。
- 上眼瞼に生じた腫瘤
- 再発を繰り返す例
- 切開時に粥状でなく黄白色の小粒状内容物を呈する例
初期・軽度の霰粒腫であれば温罨法と眼瞼マッサージで改善する例がある。保存療法の成功率は約80%とされる。温水で温めたタオルを眼瞼に10分ほど当て、その後眼瞼をマッサージする。眼瞼のシャンプーを加えると効果が増強する。ただし線維化が進んだ腫瘤には保存療法の効果が限定的となり、外科的切除が必要となる。
標準的な術式は経結膜アプローチである。2%リドカイン塩酸塩の浸潤麻酔下に、眼瞼を翻転させて結膜面を露出し、腫瘤中央に眼瞼縁に垂直な2〜3mmの小切開を加える。粥状物をガーゼや鋭匙で掻き出した後、有鉤鑐子と剪刀で残存膠原線維を十分に郭清する。皮膚に切開を加えないため皮膚瘢痕を残さない。手術中の疼痛は局所麻酔により最小限に抑えられる。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”マイボーム腺の正常機能
Section titled “マイボーム腺の正常機能”マイボーム腺は瞼板内に存在する脂腺(皮脂腺の一種)であり、涙液油層の主成分であるmeibum(脂質)を分泌する。meibumは涙液表面に油層を形成し、涙液の蒸発を防いで眼表面の安定化に寄与する。マイボーム腺は上下眼瞼それぞれに約20〜30腺存在し、眼瞼縁の小孔から開口している。
霰粒腫の発症機序
Section titled “霰粒腫の発症機序”- マイボーム腺の導管が梗塞する(MGDとの関連が強い)
- 導管内に分泌物が蓄積する。マイボーム腺分泌物は脂肪と角質を含む細胞崩壊産物の混合物である
- 蓄積した変性内容物に対して異物反応が惹起される
- 類上皮細胞・多核巨細胞・リンパ球浸潤を伴う慢性肉芽性炎症が発生する
- 膠原線維が増殖し、線維化が進行して肉芽腫(霰粒腫)が完成する
この発症機序において細菌感染は関与しない点が本疾患の本質的な特徴である。
霰粒腫の病理組織では、好中球・リンパ球・形質細胞の浸潤と毛細血管の増生よりなる肉芽組織が主体を占める。一部に泡沫状マクロファージや類上皮細胞も認められる。肉芽組織の周囲を縁取るように、膠原組織からなる結合組織が存在する。これが慢性期の霰粒腫で触れる硬い腫瘤の組織学的基盤となる。
MGDとの関係
Section titled “MGDとの関係”霰粒腫はマイボーム腺の局所的なMGDともいえる。全般的なMGDの存在は、複数の腺管の梗塞リスクを高め、霰粒腫の多発・再発につながる。脂漏性皮膚炎や酒さ(rosacea)はMGDの重要な危険因子であり、これらを合併する患者では霰粒腫が繰り返し発生しやすい。多発・再発例では背景疾患の管理も重要となる。
赤外線マイボグラフィを用いた前向き研究(Li ら 2020, BMC Ophthalmol[⁵])では、霰粒腫が治癒した後でも該当部位にマイボーム腺の脱落が残存し、その範囲は治療法(保存療法 vs 外科治療)によらず腫瘤の大きさに依存することが示されている。また Hanna ら(2022, Int Ophthalmol[⁶])は、霰粒腫摘出術後にマイボグラフィで罹患眼瞼全体のマイボーム腺指標が改善することを報告しており、外科治療がMGD改善にも寄与する可能性を示唆している。
7. 予後と経過
Section titled “7. 予後と経過”保存療法の予後
保存療法の成功率は80%前後の報告が多い(Wu ら 2018, Acta Ophthalmol[¹])。ただし腫瘤に線維化をきたした症例では眼瞼の硬結を完全に除去できない。温罨法・眼瞼清拭の継続はMGD管理として再発予防にも有効である(Tashbayev ら 2024, Curr Eye Res[²])。
外科治療の予後
外科治療の予後は通常良好である。ただし膠原線維の郭清が不十分な場合、術後に眼瞼の硬結が残存して患者クレームとなりやすい。十分な郭清が術後成績の鍵となる。
再発について
MGDが背景にある場合は再発リスクが高い。術後も温罨法・眼瞼清拭の継続を指導することが再発予防に重要である。多発・再発例では脂漏性皮膚炎・酒さの管理も並行して行う。
脂腺癌の見逃しリスク
脂腺癌との鑑別を逃すと予後不良となる。全例で摘出検体を病理検査に提出する姿勢が重要である。特に上眼瞼・再発例・非粥状内容物を呈する例では高い警戒が求められる。
小児の注意点
皮膚側への浸潤傾向に注意する。手術時期を逸すると眼瞼皮膚の壊死リスクが高まる。全身麻酔下での手術が必要であるが、適切な時期に介入することで良好な予後が期待できる。
8. 参考文献
Section titled “8. 参考文献”-
Wu AY, Gervasio KA, Gergoudis KN, Wei C, Oestreicher JH, Harvey JT. Conservative therapy for chalazia: is it really effective? Acta Ophthalmol. 2018;96(4):e503-e509. doi:10.1111/aos.13675. PMID: 29338124. PMCID: PMC6047938.
-
Tashbayev B, Chen X, Utheim TP. Chalazion Treatment: A Concise Review of Clinical Trials. Curr Eye Res. 2024;49(2):109-118. doi:10.1080/02713683.2023.2279014. PMID: 37937798.
-
Aycinena ARP, Achiron A, Paul M, Burgansky-Eliash Z. Incision and Curettage Versus Steroid Injection for the Treatment of Chalazia: A Meta-Analysis. Ophthalmic Plast Reconstr Surg. 2016;32(3):220-224. doi:10.1097/IOP.0000000000000483. PMID: 26035035.
-
Ben Simon GJ, Rosen N, Rosner M, Spierer A. Intralesional triamcinolone acetonide injection versus incision and curettage for primary chalazia: a prospective, randomized study. Am J Ophthalmol. 2011;151(4):714-718.e1. doi:10.1016/j.ajo.2010.10.026. PMID: 21257145.
-
Li J, Li D, Zhou N, Qi M, Luo Y, Wang Y. Effects of chalazion and its treatments on the meibomian glands: a nonrandomized, prospective observation clinical study. BMC Ophthalmol. 2020;20(1):278. doi:10.1186/s12886-020-01557-z. PMID: 32652956. PMCID: PMC7353760.
-
Hanna S, Hartstein M, Mukari A, Shor S, Habib G, Hamed Azzam S. Global improvement in meibomian glands after chalazion surgery demonstrated by meibography. Int Ophthalmol. 2022;42(8):2591-2598. doi:10.1007/s10792-022-02307-4. PMID: 35412124.
