結節型(56%)
黄色調の結節性腫瘤:腫瘍細胞内の脂質による黄色外観が特徴。上眼瞼縁に好発し、表面不整で易出血性の腫瘍血管を伴う。
眼瞼翻転による観察:眼瞼を翻転して結膜側も確認することが重要。
脂腺癌(sebaceous carcinoma, SGC)は、眼瞼の脂腺—マイボーム腺、ツァイス腺、涙丘脂腺、眉毛皮膚脂腺—から発生する稀で悪性度の高い腫瘍である。眼瞼では最も重要な悪性腫瘍のひとつであり、マイボーム腺由来が大部分を占める。上眼瞼にはマイボーム腺が約50個、下眼瞼に約25個あるため、上眼瞼に好発する。
欧米と東アジアで疾患の位置づけが大きく異なる。眼瞼悪性腫瘍全体に占める割合は、欧米では基底細胞癌が80〜95%を占め、脂腺癌はわずか1〜3%にとどまる1)。一方、アジア系では脂腺癌の比率が著しく高い。
以下にアジアと欧米の疫学の違いを示す。
| 地域・集団 | 最多疾患 | 脂腺癌の割合 |
|---|---|---|
| 欧米 | 基底細胞癌 80〜95% | 1〜3% |
| インド(536例) | 脂腺癌 53% | 53%1) |
| 中国(1,086例) | 基底細胞癌 38% | 32%1) |
| 日本(38例) | 基底細胞癌 40% | 29%1) |
ただし、アジア人で脂腺癌の「割合」が高いのは基底細胞癌の割合が相対的に低いためであり、脂腺癌の「発生率」自体は白人の方が高い(2.03 vs アジア/太平洋系1.07/100万)1)。アジア人で眼瞼悪性腫瘍がある場合、それが脂腺癌である確率は非アジア人の6.21倍(範囲3.8〜10.1)に達する1)。本邦では眼瞼悪性腫瘍のうち基底細胞癌に次ぐ頻度である。
発症年齢は主に50歳代以降であり、平均年齢は57〜72歳、インド系では平均58歳と報告されている1)。眼瞼以外にも25%の症例で頭頸部・他の皮膚・生殖器に発生しうる。
ミュア・トール症候群:脂腺系腫瘍と内臓悪性腫瘍(胃腸・子宮内膜・泌尿器)を合併する常染色体優性遺伝疾患。DNAミスマッチ修復遺伝子(MLH1、MSH2、MSH6)の変異が背景にあり、ミュア・トール症候群患者の24%に脂腺癌を生じる。ミュア・トール症候群の脂腺癌は散発例より侵襲性が低いとされる。
ミュア・トール症候群の可能性を考慮する必要がある。ミュア・トール症候群は脂腺系腫瘍と大腸癌などの内臓悪性腫瘍が合併する遺伝疾患であり、MLH1・MSH2・MSH6の免疫染色で発現消失が認められた場合は消化器科などへの紹介が推奨される。
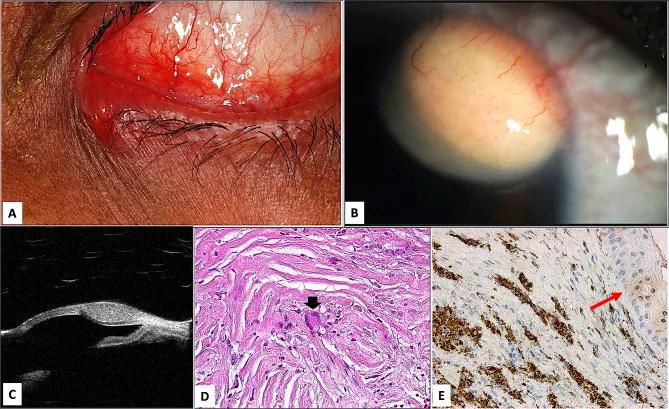
結節型(56%)
黄色調の結節性腫瘤:腫瘍細胞内の脂質による黄色外観が特徴。上眼瞼縁に好発し、表面不整で易出血性の腫瘍血管を伴う。
眼瞼翻転による観察:眼瞼を翻転して結膜側も確認することが重要。
びまん型(7%)
腫瘤を形成しない上皮内浸潤:マイボーム腺開口部から瞼縁皮膚や瞼結膜に薄く広がる型。
睫毛脱落(まつ毛禿):びまん型に特徴的な所見のひとつ。診断が最も遅れやすい。
腫瘍の発生部位は脂腺癌の59%が上眼瞼、29%が下眼瞼、内眼角3%、外眼角2%である1)。
パジェット様進展:主病巣から離れた瞼球結膜上皮内へ腫瘍細胞がシート状に増殖拡大する特徴的なパターン。瞼結膜全面を覆う花火状の腫瘍血管と腫瘍細胞増生を呈し、スキップ病変を形成しうる。
仮面症候群(great masquerader):霰粒腫・慢性眼瞼炎・基底細胞癌・扁平上皮癌・上輪部角結膜炎・眼瘢痕性類天疱瘡に類似する。結節性病変は霰粒腫と誤認されやすく、切開後に再発増大を繰り返す。眼窩蜂窩織炎として受診した例も報告されている3)。
アジア人で眼瞼悪性腫瘍がある場合に脂腺癌である確率は非アジア人の6.21倍である1)。ただしこれは相対的な割合の話であり、脂腺癌の発生率(人口あたり)自体は白人(2.03/100万)の方がアジア/太平洋系(1.07/100万)より高い。アジア人で基底細胞癌が少ないため、相対的に脂腺癌の比率が高く見える。
高い疑いの目(high index of suspicion)を持つことが最重要である。以下の場合に脂腺癌を積極的に疑う。
霰粒腫と思われても、掻爬内容物は必ず病理検査に提出する。 抗菌薬眼軟膏投与による改善の有無でパジェット様進展と眼瞼縁炎を鑑別できる場合がある。
脂腺癌が疑われる場合、以下の画像検査で転移・浸潤の評価を行う。
腫瘍サイズと眼瞼/眼窩浸潤に基づいてT1〜T4に分類される2)。
| T分類 | 定義 |
|---|---|
| T1 | 腫瘍長径 ≤10 mm |
| T2 | 腫瘍長径 >10〜20 mm |
| T3 | 腫瘍長径 >20 mm |
| T4 | 眼窩・副鼻腔等への浸潤 |
第8版では第7版と比較しT1の定義が拡大(5 mm以下→10 mm以下)され、ダウンステージングが生じることが示されている2)。
現在の標準的な免疫組織化学マーカーを以下に示す。
| マーカー | 特徴 |
|---|---|
| アディポフィリン | 細胞内脂質滴関連タンパク。脂腺分化の感度が高く実用的3) |
| アンドロゲン受容体 | 眼瞼の脂腺癌で一般に陽性 |
| 上皮膜抗原(EMA) | 陽性 |
ミュア・トール症候群スクリーニング:MLH1・MSH2・MSH6の免疫組織化学染色で発現消失の有無を確認する。
脂腺系腫瘍(脂腺癌・脂腺腫など)と内臓悪性腫瘍(特に大腸癌)を合併している場合にミュア・トール症候群を疑う。病理組織標本でMLH1・MSH2・MSH6の免疫染色による発現消失が確認された場合は、消化器科・婦人科などへの精査紹介が推奨される。
外科的切除が治療の主体である。
日本の標準(眼瞼限局例):
モース顕微鏡手術または完全周辺・深部断端評価法(CCPDMA):欧米での第一選択治療。組織をすべて水平断で評価し断端の腫瘍細胞を確認しながら切除する方法である。
インドの治療プロトコール(参考):T1〜T3腫瘍は4 mm安全域での広範切除+凍結切片制御→眼瞼再建。T4腫瘍は術前化学療法(3週ごとの5-フルオロウラシル+シスプラチン/カルボプラチン)または眼窩内容除去術を考慮する2)。
眼窩浸潤例、巨大で深く浸潤した病変、広範な球結膜波及例で施行される。AJCC病期別の施行率はT1 3%、T2 3%、T3 8%、T4 63%と報告されている2)。
日本では3 mm以上の安全域をとって切除することが標準とされている。欧米ではモース顕微鏡手術または完全周辺・深部断端評価法が第一選択であり、組織を全断端で評価しながら切除する。T4腫瘍や眼窩浸潤例では眼窩内容除去術が検討される。
脂腺癌は脂腺の腺上皮から発生する悪性腫瘍である。発生部位の内訳はマイボーム腺由来92%、ツァイス腺6%、涙丘2%と報告されている2)。
組織学的に脂腺細胞(空胞化した細胞質を持つ、脂質に富む細胞)と未分化基底様細胞が混在し、分化度は高分化から低分化まで様々である。腫瘍細胞内の脂質が黄色調の肉眼的外観をもたらす。
パジェット様進展のメカニズム:主腫瘍から離れた部位の上皮—瞼結膜・球結膜・皮膚—へ悪性細胞が個々に移動して増殖するパターン。スキップ病変を形成し、肉眼的に病変がないように見える部位にも腫瘍細胞が存在しうる。このため結膜マッピング生検による広がりの把握が治療に不可欠となる。
ミュア・トール症候群の分子機序:DNAミスマッチ修復遺伝子(MLH1、MSH2、MSH6、PMS2)の変異による常染色体優性遺伝疾患。変異によりDNA複製エラーの修復機能が喪失し、腫瘍抑制遺伝子に変異が蓄積することで脂腺系腫瘍が生じる。
Morawala(2023)は119例の脂腺癌を対象にAJCC第8版T分類を検討し、T分類が予後予測に有用であることを示した2)。T4腫瘍のリンパ節転移ハザード比2.38、遠隔転移ハザード比4.30、転移関連死ハザード比6.62であった。また第8版ではT1の定義が第7版の5 mm以下から10 mm以下に変更され、ダウンステージングが生じることが確認された。
Li & Finger(2021)はT2bN0M0の眼窩脂腺癌に対し、切除+冷凍凝固+超厚型羊膜移植後に高線量率小線源治療(2,000 cGy/5回)+電子線外部放射線療法(36 Gy/20回)の合計56 Gyを照射した5)。1年後視力20/20、放射線網膜症・視神経障害なし。ただし頸部リンパ節転移を生じた。
Adachi(2022)は97歳の手術不能耳前部脂腺癌に対し、60 Gy/30 frの電子線治療+過酸化水素含浸ガーゼを施行した4)。8か月後に肉眼的完全寛解。有害事象はGrade 2放射線皮膚炎のみ。過酸化水素の放射線増感効果が示唆されるが、少数例の報告であり今後の検証が必要である。
Kaliki S, Bothra N, Bejjanki KM, Nayak A, Ramappa G, Mohamed A, et al. Malignant Eyelid Tumors in India: A Study of 536 Asian Indian Patients. Ocular oncology and pathology. 2019;5(3):210-219. doi:10.1159/000491549. PMID:31049330; PMCID:PMC6489076.
Morawala A, Mohamed A, Krishnamurthy A, Jajapuram SD, Kaliki S. Sebaceous gland carcinoma: analysis based on the 8(th) edition of American Joint Cancer Committee classification. Eye (Lond). 2023;37(4):714-719. doi:10.1038/s41433-022-02025-2. PMID:35347292; PMCID:PMC9998849.
Ramachandran V, Tumyan G, Loya A, Treat K, Vrcek I. Sebaceous Carcinoma Masquerading As Orbital Cellulitis. Cureus. 2022;14(2):e22288. doi:10.7759/cureus.22288. PMID:35350510; PMCID:PMC8933264.
Adachi A, Oike T, Tamura M, Ota N, Ohno T. Radiotherapy With Hydrogen Peroxide-Soaked Gauze for Preauricular Sebaceous Carcinoma. Cureus. 2022;14(7):e27464. doi:10.7759/cureus.27464. PMID:35923494; PMCID:PMC9339371.
Li F, Stewart RD, Finger PT. Interstitial Brachytherapy for Orbital Sebaceous Carcinoma. Ophthalmic plastic and reconstructive surgery. 2021;37(6):e215-e217. doi:10.1097/IOP.0000000000002031. PMID:34314398; PMCID:PMC8565506.