結節型
外観:真珠光沢を帯びた丘疹・結節。表面に毛細血管拡張を認める。
中央部:病変が拡大するにつれ中央が陥凹し、潰瘍を形成することがある(結節潰瘍型)。
組織学的特徴:柵状配列(peripheral palisading)を示す腫瘍細胞島と裂隙が特徴的である。
基底細胞癌は表皮の基底細胞が真皮に向かって腫瘍性増殖をきたした悪性腫瘍である。表皮付属器の原基が由来と考えられている。眼瞼悪性腫瘍の中で最も頻度が高く、細胞増殖能は他の悪性腫瘍より低く、遠隔転移をきたさない低悪性度腫瘍である。好発部は下眼瞼で、瞼縁・睫毛部付近に発症しやすい。内眼角や外眦部にもみられる。
基底細胞癌は非黒色腫皮膚癌の約80%を占め1)、全皮膚悪性腫瘍の70〜80%にあたる。2) 欧米では眼瞼悪性腫瘍の82〜91%を占めるが8)、アジアでは11〜65%と地域差がある。8) インドの536例を対象とした研究では、基底細胞癌は眼瞼悪性腫瘍の24%を占め、平均発症年齢は60歳であった。8)
発生率はヨーロッパで過去10年に5%増加している。2) 死亡率は1%未満と低い。6) 眼瞼での発生部位の内訳は下眼瞼59%、内眥13〜30%、上眼瞼15〜16%、外眥3〜5%とされる。8)
遠隔転移は極めて稀である。転移率は0.0028〜0.55%とされ1)、死亡率も1%未満6)であり、低悪性度腫瘍に分類される。ただし局所浸潤性は強く、放置すると深部組織へ進展する。特に潰瘍型・内眼角型は眼窩内深部まで浸潤することがある。
眼瞼悪性腫瘍に共通する一般的特徴として以下の7項目が知られている。
これらの所見が1項目以上認められる眼瞼病変では悪性腫瘍を疑い、積極的に生検を行う必要がある。
初期は無症状であることが多い。病変の進行に伴い以下の症状が出現する。
結節型と潰瘍型が臨床的に最も多く認められる。インドの多施設研究では結節潰瘍型51%・結節型42%であった。8) 腫瘍径中央値は12mm、厚さ4mmと報告されている。8)
中心潰瘍または中心の陥凹を特徴とする。色素細胞の増生を伴って黒色や褐色を呈することが多いが、部分的に黒色の例、黒色調がみられない例もある。表皮原発であるため、瞼結膜面に病変はみられない。
結節型
外観:真珠光沢を帯びた丘疹・結節。表面に毛細血管拡張を認める。
中央部:病変が拡大するにつれ中央が陥凹し、潰瘍を形成することがある(結節潰瘍型)。
組織学的特徴:柵状配列(peripheral palisading)を示す腫瘍細胞島と裂隙が特徴的である。
硬化型(浸潤型)
外観:瘢痕様の平坦な硬結。境界不明瞭で白色〜黄色調を示す。
浸潤:深部浸潤傾向が強く、眼窩へ進展するリスクが高い。
予後:再発率が高く、高リスク亜型として分類される。morpheaform型・微小結節型・basosquamous型も同様に高リスクである。
内眥部の病変は眼窩深部への浸潤傾向があるため、眼窩進展の評価が特に重要である。色素性基底細胞癌はインド人で55%と高率に認められる一方、パリでは1%、地中海では45%と人種差がある。8)
病理組織学的には腫瘍細胞はCK5/6陽性・CK14陽性・CK20陰性・BerEP4陽性を示す。3)
下眼瞼が最多(50〜66%)であり、次いで内眥(13〜30%)に多い。8) 上眼瞼は15〜16%、外眥は3〜5%と少ない。内眥部は眼窩深部へ浸潤する傾向があるため注意を要する。
基底細胞癌の主な原因と発症リスクを高める要因を以下に示す。
転移リスクを高める因子を以下に示す。
| リスク因子 | 備考 |
|---|---|
| 腫瘍サイズ(5cm超で転移率25%、10cm超で50%) | 最大の因子1) |
| 男性 | 性差あり1) |
| 再発基底細胞癌 | 再発例で転移リスク上昇1) |
| 神経周囲浸潤 | 組織学的所見1) |
| 頭皮・耳介の原発 | 転移傾向が増大7) |
| 放射線治療歴・免疫抑制 | 治療関連因子1) |
日焼け止め・帽子・サングラスによる紫外線防御が一次予防として有効である。紫外線(特にUVB)が最大の環境因子であるため、日常的な紫外線対策が推奨される。
確定診断には切開生検による組織学的検査が必須である。臨床・病理学的一致率は基底細胞癌で86%と報告されている。8)
組織では好塩基性の腫瘍細胞が大小の胞巣を作って増殖する。胞巣辺縁における核の索状配列(peripheral palisading)が特徴的である。腫瘍島と周囲間質の間に裂隙を形成し、シート状または浸潤性の増殖パターンを示す高リスク亜型(morpheaform型・浸潤型・微小結節型)では再発リスクが高い。
術中の迅速病理検査で切除断端での腫瘍細胞の有無を確認したうえで欠損部を再建する。ただし迅速診断は最終診断ではない。永久標本で腫瘍細胞を取り除けていたかどうかを必ず確認する必要がある。
眼瞼BCCの進行度評価にはAJCC第8版のTNM分類が用いられる。9)
N0(所属リンパ節転移なし)、M0(遠隔転移なし)の早期例が大多数であり、pT1N0M0の根治切除で予後良好である。
基底細胞癌と鑑別すべき主な疾患を以下に示す。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| Trichoblastoma | PHLDA1+、CK20+、AR−3) |
| 脂腺癌 | AR びまん性+、EMA+、pagetoid spread3) |
| 眼瞼母斑 | 良性、色素沈着、軟らかい質感、小児期から存在 |
| 脂漏性角化症 | 良性、角質増殖、表面粗糙、疣状 |
基底細胞癌は眼窩浸潤性悪性新生物の第3位(約10%)を占め3)、内眥部の病変では特に眼窩浸潤を念頭に置く必要がある。
外科切除が標準治療の基本である。結節型の多くは比較的境界が明瞭であり、安全域1〜2mmを確保すれば全摘出が可能な場合が多い。
切除方針は腫瘍の位置と発育形態によって異なる。
インドの多施設研究では94%で広範切除が実施され、再発率は3%、眼球温存率は94%であった。8) 眼窩摘出を要した症例は5%であった。8)
国際標準(NCCNガイドライン)では、低リスク基底細胞癌に4mmの臨床マージンが推奨されている。2) 再発基底細胞癌の5年再発率は11〜17%と高く、再手術や補助療法が必要になる場合がある。2)
Mohs micrographic surgery(MMS)は薄い層状に組織を切除し、切除した組織の全断端を水平断で術中に病理評価する手法である。14) 再発例・高リスク亜型・内眼角部病変に特に有用であり、初発例の5年再発率は1%前後と非常に低い。14) 欧米では眼周囲BCCの標準術式として広く普及している。15)
眼周囲BCCへのMohs手術のオーストラリアにおける7年間のデータベース解析では、1,000例超のうち再発率は1.0%で、組織学的に陽性断端のみが再発の独立リスク因子であった。14)
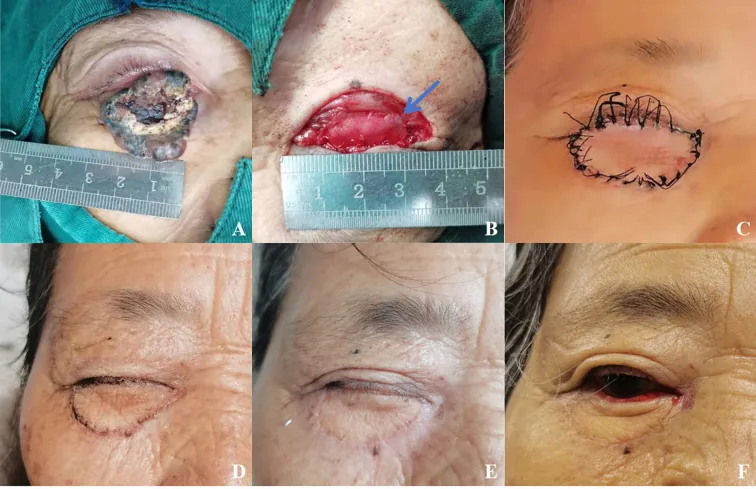
切除後の眼瞼欠損サイズに応じて再建術式を選択する。11)
| 欠損サイズ | 術式 |
|---|---|
| 1/4以下(小欠損) | 直接縫合 |
| 1/4〜1/2(中等度欠損) | Tenzel回転皮弁 |
| 1/2超・上眼瞼大欠損 | Cutler-Beard法(下眼瞼からのbridge flap) |
| 1/2超・下眼瞼大欠損 | Hughes法(上眼瞼瞼板結膜弁)+ 皮膚移植/皮弁 |
眼窩浸潤が確認された場合は眼窩郭清術(眼球を含む)または眼窩内容除去術が必要になることがある。10) 眼窩浸潤BCCの管理においては集学的アプローチが重要である。13)
全身状態不良・高齢者で根治切除に耐えられない場合に考慮される。再発率は初発基底細胞癌7.4%、再発基底細胞癌9.5%と報告されている。2) 局所制御率は腫瘍サイズ・浸潤深度の増大に伴い低下し、80〜85%となり、骨・軟骨浸潤時は50〜75%に低下する。1)
局所免疫療法
イミキモド5%クリーム:表在型基底細胞癌に対する局所免疫賦活薬。外科切除が困難な表在型病変に用いられる。
全身薬物療法
Vismodegib:ヘッジホッグ経路阻害薬(SMO阻害)。転移性基底細胞癌で奏効率30%、局所進行基底細胞癌で43%(Erivance試験)。1)
Sonidegib:ヘッジホッグ経路阻害薬。200mg/日投与で奏効率36%(BOLT試験)。1)
Cemiplimab:PD-1阻害薬。ヘッジホッグ経路阻害薬抵抗・不耐容例に承認。奏効率32%(第2相試験)。1)
局所進行例・転移例に対してはヘッジホッグ経路阻害薬(Vismodegib・Sonidegib)や免疫チェックポイント阻害薬(Cemiplimab)が用いられる。1) 放射線治療は根治切除が困難な症例に適応される。表在型基底細胞癌にはイミキモド5%クリームが選択肢となる。ただし外科切除が第一選択である。
結節型では安全域1〜2mm、瞼縁病変は瞼板ごと切除、潰瘍型はdeep marginを深くとることが推奨される。術中迅速凍結切片と永久標本での断端確認が重要である。全身状態不良・高齢者で根治切除が困難な場合は放射線治療を考慮する。
Mohs手術(Mohs micrographic surgery, MMS)は切除組織の全断端を水平断で術中に病理評価する手法である。14) 通常の外科切除と比べて組織温存率が高く、初発例の5年再発率は1%前後と非常に低い。再発例・高リスク亜型・内眼角部の病変など、断端評価が重要な場合に特に有用である。
基底細胞癌の発症にはヘッジホッグシグナル経路の異常活性化が中心的役割を果たす。正常状態ではPTCH1(Patched 1)タンパクがSMO(Smoothened)を抑制しており、ヘッジホッグリガンドが存在しない限りGLI転写因子は不活性状態に保たれる。
基底細胞癌ではPTCH遺伝子(9q22.3)の不活性化変異またはSMOの活性化変異により、SMOの恒常的活性化が生じる。その結果、GLI転写因子が核内に移行し、細胞増殖・生存・血管新生に関わる標的遺伝子の転写が亢進する。基底細胞癌の最大90%でこの経路の異常活性化が確認されている。1)4)
腫瘍は表皮付属器の原基に由来すると考えられている。腫瘍細胞は索状・島状構造を形成し、周辺に柵状配列(peripheral palisading)を示すことが病理組織学的特徴である。シート状あるいは浸潤性の増殖パターンを示す亜型(morpheaform型・浸潤型・微小結節型)は再発リスクが高く、高リスク組織型として分類される。1)6)
潰瘍型・内眼角型は局所浸潤性が特に強い。瞼板という解剖学的障壁がない内眼角では腫瘍が眼窩内深部まで浸潤し、眼窩摘出術を余儀なくされる場合がある。10)
Casey MCら(2021)は進行基底細胞癌に対するCemiplimabの第2相試験を報告した。1) ヘッジホッグ経路阻害薬に抵抗または不耐容となった局所進行・転移性基底細胞癌患者を対象として、奏効率32%、奏効持続期間は1年超を達成した。
Nivolumab(PD-1阻害薬)とIpilimumab(CTLA-4阻害薬)の併用療法は試験が進行中であり、今後の結果が注目される。1) 眼瞼腫瘍全般の最新動向として、光免疫療法や局所薬物療法の眼瞼BCCへの応用も研究されている。12)
転移性基底細胞癌の転移経路別予後を以下に示す。リンパ行性転移の生存中央値は87ヶ月1)4)、血行性転移は24ヶ月1)4)、骨転移は12ヶ月7)と報告されている。転移部位は、リンパ節が最多(60%)で、次いで肺(42%)、骨(10%)、皮膚(10%)の順である。7) 頭頸部原発の転移性基底細胞癌7症例のレビューでは、転移までの中央値は3年であった。4)
Ryan SEら(2024)は胸椎転移をきたした基底細胞癌に対して、手術・Vismodegib・放射線治療(25Gy/5回)の集学的アプローチを報告した。5) Vismodegibへの良好な反応が確認されており、転移性基底細胞癌に対するヘッジホッグ経路阻害薬の有効性を示す事例として注目される。
化学療法(白金製剤等)はヘッジホッグ経路阻害薬・免疫療法が無効の場合の第2〜3選択であり、役割は限定的である。1)7)