结节型
外观:珍珠光泽的丘疹/结节。表面可见毛细血管扩张。
中央部:随着病变扩大,中央凹陷,可能形成溃疡(结节溃疡型)。
组织学特征:特征性表现为栅栏状排列的肿瘤细胞岛和裂隙。

基底细胞癌是表皮基底细胞向真皮方向肿瘤性增殖形成的恶性肿瘤。被认为起源于表皮附属器的原基。它是眼睑恶性肿瘤中最常见的类型,细胞增殖能力低于其他恶性肿瘤,是一种低度恶性肿瘤,很少发生远处转移。好发于下眼睑,尤其是睑缘和睫毛附近,也可出现在内眦和外眦。
基底细胞癌约占非黑色素瘤皮肤癌的80%1),占所有皮肤恶性肿瘤的7080%2)。在欧美,它占眼睑恶性肿瘤的8291%8),但在亚洲,比例因地区而异,为11~65%8)。一项针对印度536例病例的研究显示,基底细胞癌占眼睑恶性肿瘤的24%,平均发病年龄为60岁8)。
在欧洲,过去10年发病率增加了5%2)。死亡率低于1%6)。眼睑发生部位的分布为:下眼睑59%、内眦1330%、上眼睑1516%、外眦3~5%8)。
远处转移极为罕见。转移率为0.0028~0.55%1),死亡率也低于1%6),属于低度恶性肿瘤。但局部浸润性强,若不治疗可向深部组织进展。尤其是溃疡型和内眦型,可能向眼眶深部浸润。
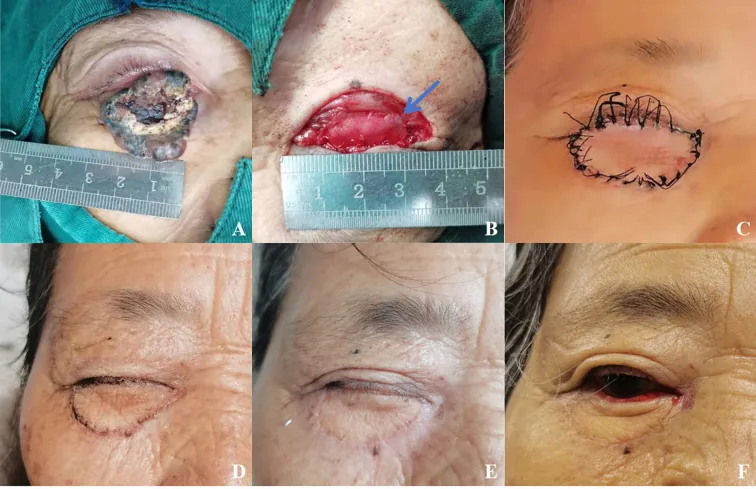
眼睑恶性肿瘤共通的以下7项一般特征已为人所知。
如果眼睑病变出现上述一项或多项表现,应怀疑恶性肿瘤,并积极进行活检。
早期通常无症状。随着病变进展,出现以下症状。
结节型和溃疡型在临床上最常见。印度的一项多中心研究中,结节溃疡型占51%,结节型占42%。8) 据报道,肿瘤直径中位数为12毫米,厚度为4毫米。8)
特征为中心性溃疡或中心凹陷。常因色素细胞增生而呈黑色或褐色,但部分病例呈部分黑色或未见黑色调。由于起源于表皮,眼睑结膜面未见病变。
结节型
外观:珍珠光泽的丘疹/结节。表面可见毛细血管扩张。
中央部:随着病变扩大,中央凹陷,可能形成溃疡(结节溃疡型)。
组织学特征:特征性表现为栅栏状排列的肿瘤细胞岛和裂隙。
硬化型(浸润型)
外观:瘢痕样扁平硬结。边界不清,呈白色至黄色调。
浸润:深部浸润倾向强,向眼眶进展的风险高。
预后:复发率高,被归类为高风险亚型。硬斑病样型、微结节型和基底鳞状细胞型同样为高风险。
内眦部病变有向眼眶深部浸润的倾向,因此眼眶进展的评估尤为重要。色素性基底细胞癌在印度人中高达55%,而在巴黎为1%,地中海地区为45%,存在种族差异。8)
病理组织学上,肿瘤细胞呈CK5/6阳性、CK14阳性、CK20阴性、BerEP4阳性。3)
下眼睑最多(5066%),其次为内眦(1330%)。8) 上眼睑占1516%,外眦占35%。内眦部有向眼眶深部浸润的倾向,需注意。
基底细胞癌的主要病因和增加发病风险的因素如下所示。
增加转移风险的因素如下所示。
| 风险因素 | 备注 |
|---|---|
| 肿瘤大小(超过5cm时转移率25%,超过10cm时50%) | 最大的因素 1) |
| 男性 | 存在性别差异1) |
| 复发性基底细胞癌 | 复发时转移风险增加1) |
| 神经周围浸润 | 组织学表现1) |
| 头皮或耳廓原发 | 转移倾向增加7) |
| 放疗史或免疫抑制 | 治疗相关因素1) |
使用防晒霜、帽子和太阳镜进行紫外线防护是有效的初级预防措施。由于紫外线(尤其是UVB)是最大的环境因素,建议日常进行紫外线防护。
确诊必须通过切开活检进行组织学检查。临床与病理的一致率在基底细胞癌中报告为86%。8)
组织学上,嗜碱性肿瘤细胞形成大小不等的巢状增殖。巢边缘的核栅栏状排列(peripheral palisading)是其特点。肿瘤岛与周围间质之间形成裂隙。高风险亚型(硬斑病样型、浸润型、微结节型)呈片状或浸润性生长模式,复发风险高。
术中通过快速病理检查确认切除边缘有无肿瘤细胞,然后重建缺损。但快速诊断并非最终诊断。必须通过永久标本确认肿瘤细胞是否已完全切除。
眼睑BCC的进展评估采用AJCC第8版TNM分类。9)
大多数为早期病例,无区域淋巴结转移(N0)和无远处转移(M0),pT1N0M0的根治性切除预后良好。
需要与基底细胞癌鉴别的主要疾病如下所示。
| 鉴别疾病 | 鉴别要点 |
|---|---|
| 毛母细胞瘤 | PHLDA1+、CK20+、AR−3) |
| 皮脂腺癌 | AR弥漫性+、EMA+、佩吉特样播散3) |
| 眼睑痣 | 良性、色素沉着、质地柔软、自幼存在 |
| 脂溢性角化病 | 良性、角化过度、表面粗糙、疣状 |
基底细胞癌是眼眶浸润性恶性肿瘤的第三位(约占10%)3),内眦部病变尤其需要考虑眼眶浸润。
手术切除是标准治疗的基础。大多数结节型边界相对清晰,通常可以通过1-2毫米的安全边缘实现完全切除。
切除策略取决于肿瘤的位置和生长形态。
印度的一项多中心研究中,94%的病例进行了广泛切除,复发率为3%,眼球保留率为94%。8) 需要眼眶内容物剜除的病例占5%。8)
国际标准(NCCN指南)建议低风险基底细胞癌采用4毫米的临床切缘。2) 复发性基底细胞癌的5年复发率高达11-17%,可能需要再次手术或辅助治疗。2)
莫氏显微手术(MMS)是一种将组织逐层切除,并在术中用水平切片对切除组织的全部边缘进行病理评估的技术。14) 对于复发病例、高风险亚型和内眼角病变尤其有用,初发病例的5年复发率极低,约为1%。14) 在欧美国家,它被广泛用作眼周基底细胞癌的标准术式。15)
澳大利亚一项为期7年的眼周基底细胞癌莫氏手术数据库分析,涉及超过1000例病例,显示复发率为1.0%,仅组织学阳性切缘是复发的独立危险因素。14)
根据切除后眼睑缺损的大小选择重建术式。11)
| 缺损大小 | 术式 |
|---|---|
| ≤1/4(小缺损) | 直接缝合 |
| 1/4至1/2(中等缺损) | Tenzel旋转皮瓣 |
| >1/2,上眼睑大缺损 | Cutler-Beard法(来自下眼睑的桥状皮瓣) |
| >1/2,下眼睑大缺损 | Hughes法(上眼睑睑板结膜瓣)+ 皮肤移植/皮瓣 |
如果确认有眼眶浸润,可能需要进行眼眶廓清术(包括眼球)或眼眶内容物剜除术。10) 在眼眶浸润性基底细胞癌的管理中,多学科方法非常重要。13)
对于全身状况不佳或高龄、无法耐受根治性切除的患者,可考虑放射治疗。据报道,原发性基底细胞癌的复发率为7.4%,复发性基底细胞癌为9.5%。2) 局部控制率随肿瘤大小和浸润深度增加而下降,降至80-85%,当有骨或软骨浸润时降至50-75%。1)
局部免疫治疗
咪喹莫特5%乳膏:用于浅表型基底细胞癌的局部免疫调节剂。适用于手术切除困难的浅表型病变。
全身药物治疗
Vismodegib:Hedgehog通路抑制剂(SMO抑制剂)。转移性基底细胞癌缓解率30%,局部晚期基底细胞癌43%(Erivance试验)。1)
Sonidegib:Hedgehog通路抑制剂。200mg/日给药缓解率36%(BOLT试验)。1)
Cemiplimab:PD-1抑制剂。获批用于对Hedgehog通路抑制剂耐药或不耐受的患者。缓解率32%(2期试验)。1)
对于局部晚期或转移性病例,可使用Hedgehog通路抑制剂(Vismodegib、Sonidegib)和免疫检查点抑制剂(Cemiplimab)。1) 放射治疗适用于根治性切除困难的病例。浅表型基底细胞癌可选择咪喹莫特5%乳膏。但手术切除是首选。
结节型建议安全边界1-2mm;睑缘病变需切除包括睑板;溃疡型建议深部切缘足够。术中冰冻切片和永久标本的切缘确认很重要。对于全身状况差或老年患者,若根治性切除困难,可考虑放射治疗。
Mohs手术(Mohs显微描记手术,MMS)是一种在术中对切除组织的所有切缘进行水平切片病理评估的技术。14) 与常规手术切除相比,组织保留率更高,初发病例的5年复发率非常低,约1%。对于复发病例、高风险亚型以及内眦部病变等切缘评估至关重要的病例尤其有用。
基底细胞癌的发生中,Hedgehog信号通路的异常激活起核心作用。正常情况下,PTCH1(Patched 1)蛋白抑制SMO(Smoothened),在没有Hedgehog配体的情况下,GLI转录因子保持非活性状态。
基底细胞癌中,PTCH基因(9q22.3)的失活突变或SMO的激活突变导致SMO持续激活。结果,GLI转录因子转移到细胞核,增强参与细胞增殖、存活和血管生成的靶基因转录。高达90%的基底细胞癌中证实了该通路的异常激活。1)4)
肿瘤被认为起源于表皮附属器的原基。肿瘤细胞形成索状或岛状结构,组织病理学特征为周边栅栏状排列。呈片状或浸润性生长模式的亚型(硬斑病样型、浸润型、微结节型)复发风险高,被归类为高风险组织学类型。1)6)
溃疡型和内眦型局部侵袭性特别强。在内眦部,由于缺乏睑板的解剖屏障,肿瘤可浸润至眼眶深部,有时不得不进行眼眶摘除术。10)
Casey MC等人(2021)报告了cemiplimab治疗晚期基底细胞癌的2期试验。1) 在对hedgehog通路抑制剂耐药或不耐受的局部晚期或转移性基底细胞癌患者中,缓解率为32%,缓解持续时间超过一年。
纳武利尤单抗(PD-1抑制剂)和伊匹木单抗(CTLA-4抑制剂)的联合疗法正在试验中,未来结果值得关注。1) 作为眼睑肿瘤的最新动态,光动力疗法和局部药物治疗在眼睑基底细胞癌中的应用也在研究中。12)
以下显示转移性基底细胞癌按转移途径的预后。淋巴转移的中位生存期为87个月1)4),血行转移为24个月1)4),骨转移为12个月7)。转移部位最常见的是淋巴结(60%),其次是肺(42%)、骨(10%)和皮肤(10%)。7) 对7例头颈部原发转移性基底细胞癌的回顾显示,转移的中位时间为3年。4)
Ryan SE等人(2024)报告了一例胸椎转移的基底细胞癌,采用手术、Vismodegib和放射治疗(25Gy/5次)的多学科方法。5) 已确认对Vismodegib反应良好,该病例作为转移性基底细胞癌中Hedgehog通路抑制剂有效性的示例值得关注。
化疗(如铂类药物)是Hedgehog通路抑制剂和免疫治疗无效时的二线或三线选择,作用有限。1)7)