浅表型(草莓状血管瘤)
深红色边界清晰的肿块:皮肤表面呈半球形隆起,呈鲜红色,外观典型。
皮肤表面及结膜的网状血管走行:皮肤表面和结膜面可见网状血管走行。这是与霰粒肿鉴别的重要所见。
非典型病例:也存在颜色变化小、隆起轻微的类型。

眼睑血管瘤是由血管内皮细胞增殖引起的良性肿瘤,发生于婴儿期者称为婴儿血管瘤(infantile hemangioma)。以往称为“草莓状血管瘤”或“毛细血管瘤”,但现根据ISSVA分类(国际血管异常研究学会,2018年修订)2)归类为婴儿血管瘤。而以往的“海绵状血管瘤”是不同疾病,归类为“静脉畸形”,属于血管畸形。
婴儿血管瘤是先天性的,出生后约2周开始增殖。1-2个月达到增殖高峰,持续增大至约1.5岁。之后数年内逐渐缩小。70%在学龄前后自然消退。少数病例迅速增大并浸润整个眼睑,导致睁眼困难。
ISSVA分类(2018年)2)将血管性病变大致分为“血管性肿瘤”和“血管畸形”。婴儿血管瘤是由于血管内皮细胞真正增殖而形成的肿瘤,被归类为“血管性肿瘤”。而静脉畸形是血管形成异常,被归类为“血管畸形”。两者在发病机制、自然病程和治疗策略上不同,因此准确分类对治疗选择很重要。
70%的婴儿血管瘤在学龄前后自然消退。出生后约2周开始增大,持续到约1.5岁,然后在数年内逐渐缩小。但是,导致睁眼困难的大型病变可能引起形觉剥夺性弱视,因此有时需要早期治疗而不等待自然消退。静脉畸形(旧称海绵状血管瘤)不会自然消退,因此管理策略不同。
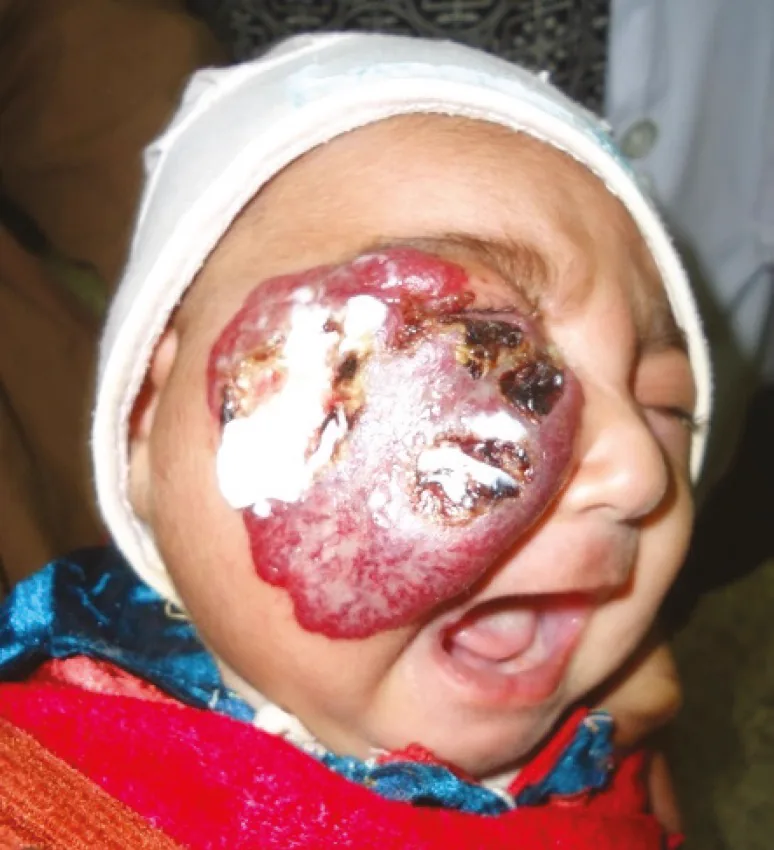
由于婴儿血管瘤发生于婴儿,自觉症状依靠家长观察。
婴儿血管瘤根据发生部位分为浅表型、深在型和混合型。
浅表型(草莓状血管瘤)
深红色边界清晰的肿块:皮肤表面呈半球形隆起,呈鲜红色,外观典型。
皮肤表面及结膜的网状血管走行:皮肤表面和结膜面可见网状血管走行。这是与霰粒肿鉴别的重要所见。
非典型病例:也存在颜色变化小、隆起轻微的类型。
深在型(皮下型)
皮下深层发生:皮肤表面发红不明显,但可触及皮下肿块。
青紫色皮肤变色:因静脉血透见,皮肤呈青紫色。边界不清晰。
混合型:也有浅表型和深在型合并的病例(混合型)。
出生后出现红色、边界清晰的隆起性病变是典型的婴儿血管瘤临床像。翻转眼睑观察结膜侧,确认有无网状血管走行对诊断很重要。
婴儿血管瘤由血管内皮细胞增殖引起。血管内皮生长因子(VEGF)已被证明参与增殖,这也是普萘洛尔作用机制的基础。
GLUT-1(葡萄糖转运蛋白1)是婴儿血管瘤的特征性免疫组织化学标志物3)。它与胎盘微血管具有共同的免疫表型,在静脉畸形中呈阴性。这一特性用于病理组织诊断中的鉴别。
许多病例仅凭临床发现即可诊断。
如果以上三点均具备,则可临床诊断为婴儿血管瘤。
当怀疑深部型或眼眶扩展时进行。
当临床诊断困难或为排除恶性时进行。
| 鉴别疾病 | 鉴别要点 |
|---|---|
| 眼睑淋巴管瘤 | 无自然消退,发生于眼表层和眼眶深部,GLUT-1阴性 |
| 霰粒肿 | 皮肤表面无血管走行,无血流信号 |
| 卡波西型血管内皮瘤 | 合并消耗性凝血病(Kasabach-Merritt综合征) |
| 横纹肌肉瘤 | 快速增大,发病较晚(婴幼儿至学龄期) |
| 斑痣性错构瘤病 | 早期病变范围固定,无增大趋势 |
由于自然消退倾向较高,多数病例首选观察。符合以下任一情况时考虑积极治疗:
如果有弱视风险,应尽早开始普萘洛尔治疗(最佳年龄:出生后5周至5个月)7)。
| 治疗方法 | 适应症 | 备注 |
|---|---|---|
| 观察 | 无弱视风险、小型病变 | 70%在学龄前消退 |
| 口服普萘洛尔 | 一线治疗(中至大型) | 2–3 mg/kg/天,儿科管理下 |
| 0.5%噻吗洛尔局部涂抹 | 表浅型、小型病变 | 每日两次(超说明书使用) |
| 脉冲染料激光(585–595 nm) | 浅表型 | 早期照射可早期消退 |
| 局部类固醇注射 | β受体阻滞剂不耐受病例 | 曲安奈德 3–5 mg/kg |
| 手术 | 消退后残留肿块 | 美容目的 |
β受体阻滞剂普萘洛尔是目前标准的一线药物7)。其作用机制推测为通过β2受体阻滞抑制VEGF和bFGF的产生、血管收缩以及诱导血管内皮细胞凋亡。
一项关于口服普萘洛尔的随机对照试验(NEJM, 2015)显示,普萘洛尔组(3 mg/kg/天,持续6个月)的治疗效果显著优于对照组7)。
噻吗洛尔滴眼液(0.5%)每日两次涂抹于血管瘤表面(超说明书使用)。已有报道对浅表型和小型病变有效11)。对于无法全身使用普萘洛尔的病例,这是一种选择。一旦确认效果,即停止使用。
脉冲染料激光(585–595 nm)对浅表型婴儿血管瘤有效8)。早期照射可促进早期消退并抑制隆起性变化。对表面红色病变有效,但对深部成分无效。
对于不耐受普萘洛尔或特定局部病变的患者,可使用曲安奈德(3–5 mg/kg)局部注射9)。这曾是首选治疗,但自普萘洛尔引入后,其适应症已受限。
需要注意因睁眼困难导致的形觉剥夺性弱视,以及因血管瘤压迫眼球和角膜变形引起的散光性弱视。持续评估肿瘤大小和形觉剥夺性弱视的风险,并进行屈光矫正和遮盖治疗。
主要副作用包括低血糖、心动过缓、低血压和支气管痉挛。低血糖在喂养不良或进食不足时更容易发生;建议在喂奶或进餐的同时服药。由于支气管痉挛的风险,哮喘和反应性气道疾病是禁忌症。为管理这些风险,建议在儿科专科医生指导下住院开始治疗。
婴儿血管瘤是血管内皮细胞真正增殖形成的肿瘤,与静脉畸形(血管畸形)的病理状态根本不同。VEGF(血管内皮生长因子)在肿瘤生长中起核心作用。普萘洛尔的β2受体阻断被认为通过抑制VEGF和bFGF的产生、血管收缩以及诱导凋亡来缩小肿瘤7)。
GLUT-1(葡萄糖转运蛋白1)阳性是婴儿血管瘤的特异性免疫表型,表明其与胎盘微血管有共同特征3)。这一特性支持了肿瘤起源于胎盘来源的血管内皮前体细胞的假说。GLUT-1在静脉畸形、淋巴管瘤和化脓性肉芽肿等其他血管病变中呈阴性,因此是鉴别诊断的实用标志物。
静脉畸形(旧称海绵状血管瘤)是血管形成异常(畸形),严格来说并非肿瘤。扩张的静脉血管腔形成团块,内壁覆盖扁平内皮细胞。GLUT-1阴性,几乎没有因生长因子引起的增殖性。不会自然消退,因此治疗适应证与婴儿血管瘤不同。
ISSVA分类(2018年修订版)2)提供了一个框架,将血管病变分为“血管性肿瘤”(血管内皮细胞增殖所致)和“血管畸形”(血管形成异常所致)。婴儿血管瘤属于“血管性肿瘤”,而静脉畸形和淋巴管畸形属于“血管畸形”。该分类对治疗决策具有直接意义。抑制血管内皮增殖的药物如普萘洛尔对血管性肿瘤有效,但对血管畸形效果有限。
眼睑的大型血管瘤压迫眼球时,会导致角膜不对称变形,产生不规则散光和屈光参差。如果这种散光未得到适当矫正,会阻碍视力发育,导致散光性弱视或屈光参差性弱视。形觉剥夺性弱视是由于睁眼困难导致光刺激本身被阻断所致。如果在视觉敏感期(出生至7-8岁)干预延迟,弱视可能变得不可逆。
阿替洛尔(选择性β1受体阻滞剂)作为普萘洛尔(非选择性β受体阻滞剂)的替代药物正在研究中。一项回顾性非劣效性研究10)显示,阿替洛尔(1 mg/kg/天)在治疗效果上不劣于普萘洛尔(2 mg/kg/天)。对于患有哮喘或反应性气道疾病而禁忌使用普萘洛尔的婴儿,阿替洛尔可能安全使用,未来前瞻性试验的结果值得关注。
一项关于噻吗洛尔马来酸盐凝胶(0.5%)局部涂抹的随机对照试验11)验证了其对出生后5至24周的表浅型婴儿血管瘤的有效性和安全性。局部吸收引起的全身性副作用风险较低,但仍需积累长期安全性数据。
西罗莫司(雷帕霉素)抑制mTOR通路,从而抑制血管内皮细胞增殖。一项前瞻性研究12)探讨了西罗莫司对难治性复合血管畸形(静脉畸形、淋巴管畸形、动静脉畸形的复合病例)的有效性和安全性,报告84%的复合血管畸形患者症状改善。虽然对婴儿血管瘤的适应症有限,但作为难治性血管畸形的新治疗选择备受期待。
Léauté-Labrèze C, Harper JI, Hoeger PH. Infantile haemangioma. Lancet. 2017;390(10089):85-94.
Wassef M, Blei F, Adams D, et al. Vascular anomalies classification: recommendations from the International Society for the Study of Vascular Anomalies. Pediatrics. 2015;136(1):e203-e214.
North PE, Waner M, Mizeracki A, et al. GLUT1: a newly discovered immunohistochemical marker for juvenile hemangiomas. Hum Pathol. 2000;31(1):11-22.
Metry D, Heyer G, Hess C, et al. Consensus statement on diagnostic criteria for PHACE syndrome. Pediatrics. 2009;124(5):1447-1456.
Kasabach HH, Merritt KK. Capillary hemangioma with extensive purpura. Am J Dis Child. 1940;59:1063-1070.
Dubois J, Patriquin HB, Garel L, et al. Soft-tissue hemangiomas in infants and children: diagnosis using Doppler sonography. AJR Am J Roentgenol. 1998;171(1):247-252. doi:10.2214/ajr.171.1.9648798. PMID:9648798.
Léauté-Labrèze C, Hoeger P, Mazereeuw-Hautier J, et al. A randomized, controlled trial of oral propranolol in infantile hemangioma. N Engl J Med. 2015;372(8):735-746.
Batta K, Goodyear HM, Moss C, et al. Randomised controlled study of early pulsed dye laser treatment of uncomplicated childhood haemangiomas. Lancet. 2002;360(9332):521-527.
Weiss AH, Kelly JP. Reappraisal of astigmatism induced by periocular capillary hemangioma and treatment with intralesional corticosteroid injection. Ophthalmology. 2008;115(2):390-397.
Bayart CB, Tamburro JE, Gee AW, et al. Atenolol versus propranolol for treatment of infantile hemangiomas during the proliferative phase: a retrospective noninferiority study. Pediatr Dermatol. 2017;34(4):413-421.
Chan H, McKay C, Adams S, et al. RCT of timolol maleate gel for superficial infantile hemangiomas in 5- to 24-week-olds. Pediatrics. 2013;131(6):e1739-e1747.
Adams DM, Trenor CC, Hammill AM, et al. Efficacy and safety of sirolimus in the treatment of complicated vascular anomalies. Pediatrics. 2016;137(2):e20153257.