规则散光的所见
顺规散光(WTR):陡峭主子午线在垂直方向。多见于年轻人,最为常见。
逆规散光(ATR):陡峭主子午线在水平方向。随年龄增长而增加,多见于老年白内障患者。
斜轴散光:陡峭主子午线在斜向。偏离0°或90°超过30度。
后角膜散光(PCA):平均0.3 D。陡峭子午线通常位于垂直方向;在顺规散光眼中,PCA部分抵消前部散光。在逆规散光眼中,PCA倾向于增加前部散光5)。

散光是指眼球的屈光面不是球面,不同子午线方向的屈光力不同,导致外界一点发出的光线在眼内不能聚焦于一点的屈光状态。在某条子午线上屈光力最强(强主子午线),与其垂直的方向上屈光力最弱(弱主子午线)。
眼球光学系统的总散光是角膜散光和晶状体散光的总和。大部分是角膜散光。存在晶状体半脱位时,晶状体散光会增强。
按散光轴分类(按主子午线方向分类):
| 分类 | 强主子午线方向 | 特征 |
|---|---|---|
| 顺规散光(WTR) | 垂直方向(60~120度) | 散光中最常见。多见于年轻人。 |
| 逆规散光(ATR) | 水平方向(0~30度、150~180度) | 随年龄增长而增加。 |
| 斜轴散光 | 斜向方向(31~59度、121~149度) | 水平及垂直以外的方向。 |
按屈光状态分类:
| 分类 | 定义 |
|---|---|
| 单纯近视性散光 | 一条焦线在视网膜上,另一条在视网膜前方 |
| 单纯远视性散光 | 一条焦线在视网膜上,另一条在视网膜后方 |
| 复合近视性散光 | 两条焦线均在视网膜前方 |
| 复合远视性散光 | 两条焦线均在视网膜后方 |
| 混合性散光 | 一条焦线在视网膜前方,另一条在视网膜后方 |
按病因分类:
| 分类 | 定义 |
|---|---|
| 规则散光 | 两条主子午线垂直(90度),每条子午线上屈光力均匀。可用柱镜矫正。 |
| 不规则散光(irregular astigmatism) | 两条主子午线不垂直,或同一子午线上屈光力不一致。不能用柱镜矫正。用硬性接触镜矫正。 |
一项对接受白内障手术患者的系统评价显示,47%的眼睛存在1.0 D以上的术前角膜散光。术前角膜散光≥1.0 D的病例约占1/3,这些是使用散光矫正型人工晶状体进行散光矫正的良好适应证。随着年龄增长,散光从顺规性向逆规性转变,因此接受白内障手术的老年患者中逆规性散光的比例较高。
散光也是屈光参差性弱视的重要原因。1.5 D以上的散光差(散光性屈光参差)或2.0 D以上的双眼散光会显著增加弱视风险7)。对于儿童,超过2 D的散光早期佩戴完全矫正眼镜可有效预防经线性弱视(meridional amblyopia)7)。
接受屈光手术的患者中散光的患病率也很高。SMILE手术候选者的平均散光度数约为1–2 D,手术计划中准确设定散光矫正轴位很重要2)。
散光的自觉症状因度数而异。
| 程度 | 主要症状 |
|---|---|
| 轻度(小于1 D) | 无症状或轻微眼疲劳 |
| 中度(1–3 D) | 视力下降、视疲劳、头痛。散光表上特定方向的线条看起来更暗。 |
| 高度(≥3 D) | 明显视力下降。儿童有发生经线性弱视的风险。 |
主要主诉是近距离工作时出现视疲劳、头痛和眼痛。尤其是远视性散光,由于调节负荷增加,视疲劳更为显著。不规则散光无法用柱镜完全矫正,需要硬性接触镜(HCL)矫正。
规则散光的所见
顺规散光(WTR):陡峭主子午线在垂直方向。多见于年轻人,最为常见。
逆规散光(ATR):陡峭主子午线在水平方向。随年龄增长而增加,多见于老年白内障患者。
斜轴散光:陡峭主子午线在斜向。偏离0°或90°超过30度。
后角膜散光(PCA):平均0.3 D。陡峭子午线通常位于垂直方向;在顺规散光眼中,PCA部分抵消前部散光。在逆规散光眼中,PCA倾向于增加前部散光5)。
不规则散光的所见
大多数角膜散光是由于先天性角膜形状不对称所致。角膜散光占眼球光学系统总散光的大部分。
年龄与散光的变化
年轻至中年人群中顺规散光(WTR)较多,但随着年龄增长,会向逆规散光(ATR)转变5)。这被认为是由于年龄增长导致晶状体周边硬化及眼睑压迫影响角膜子午线方向所致。接受白内障手术的老年患者中逆规散光相对较多。
不规则散光的原因
不规则散光可由圆锥角膜、角膜瘢痕(感染或外伤后)、翼状胬肉、角膜手术后及眼表疾病(干眼症、过敏)等引起。没有角膜地形图仪难以判断,评估不规则散光的存在必须进行角膜地形图检查。
术后散光的原因
白内障手术和角膜移植术后会发生术后散光。相关因素包括角膜缘松解切口(LRI)、飞秒激光弧形角膜切开术(FLACS-AK)和缝线诱发的散光。使用缝线的囊外白内障摘除术后散光可通过拆线减轻,但需注意可预测性较低。
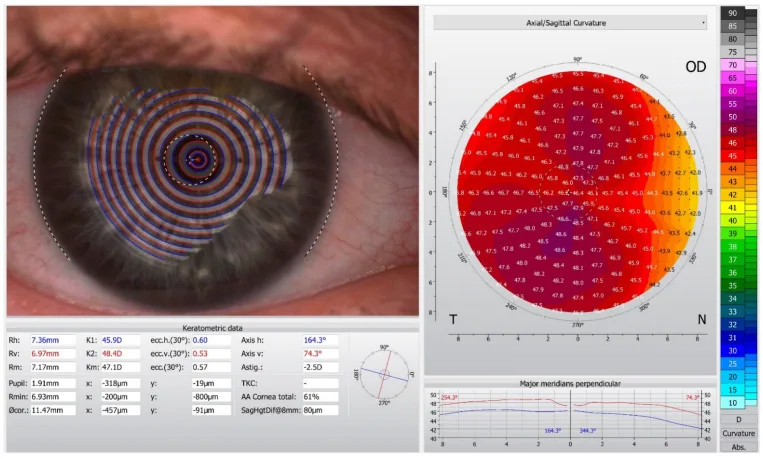
准确测量角膜散光是选择适当矫正方法和获得良好术后效果的基础。
| 测量设备 | 测量对象 | 用途/备注 |
|---|---|---|
| 自动验光角膜曲率计 | 前角膜散光和屈光值 | 筛查。测量角膜散光的量和轴。 |
| 光学生物测量仪(IOLMaster 700、Lenstar等) | 前角膜散光和眼轴长度 | IOL度数计算的标准设备 |
| 角膜地形图仪 | 前角膜形态(2D) | 鉴别规则和不规则散光所必需。确认是否存在不规则散光。 |
| 角膜断层扫描(Scheimpflug成像) | 前后角膜散光(TCA·3D) | 推荐用于高PCA病例。可获得PCA实测值。 |
检影法:客观屈光测量。在散瞳下进行精密检查时有用。
交叉柱镜法:用于精确测量散光轴和度数的自觉检查法。
角膜形态分析仪:评估不规则散光所必需。没有角膜形态分析仪很难判断不规则散光的有无。当角膜散光和屈光散光差异较大时,需检查植入的人工晶状体固定位置是否有问题。
散光的定量除了球镜度数、柱镜度数和轴位三个要素外,还使用Thibos的power vector分析。该方法用球镜等效度(M)、Jackson交叉柱镜分量(J0:垂直-水平散光)和Jackson交叉柱镜分量(J45:斜向散光)三个分量描述散光,三维评估治疗前后的散光变化9)。特别是在散光型IOL的术后评估中,残余散光和残余轴向的向量分析有助于估计轴位偏移量和规划再次手术。
Alpins法是一种用于评估散光型IOL、LASIK、LRI等散光矫正手术前后的统计分析方法。由目标诱导散光(TIA)、手术诱导散光(SIA)和残余散光(差异向量DV)三个向量组成,可计算矫正指数、误差指数、成功指数等9)。在术后评估中,其特点是不仅比较简单的散光度数,还能包括轴向变化进行综合评估。
白内障手术后,由于晶状体已被摘除,术后散光大部分为角膜散光。不应仅根据自动角膜曲率计的数值判断,而应使用角膜形态分析仪确认是否存在不规则散光6)。成人白内障PPP将术后残余散光的目标设定为0.5D以下6)。
术后散光评估流程(基于成人白内障PPP)
| 时间 | 评估内容 |
|---|---|
| 术后即刻至1周 | 确认IOL轴位(散光型IOL),评估缝线诱导散光 |
| 术后1个月 | 屈光暂定评估(因未稳定,可暂缓处方) |
| 术后3个月 | 稳定后残余散光评估。考虑配镜或追加治疗 |
| 残余散光≥0.75 D | 评估患者症状,考虑配镜或激光追加矫正 |
在涉及角膜缝线的手术(如白内障囊外摘除术)中,拆线可能减轻散光。现代超声乳化术后缝线相关散光较少,但适当的切口大小、位置和闭合是术后散光最小化的基础6)。
轴位标记(使用散光型IOL时):
术前在角膜缘进行基准标记,术中精确对准散光型IOL的轴位。数字眼球旋转追踪系统和术中像差仪有助于提高轴位标记精度8)。
术后散光评估步骤
白内障术后3个月或更晚,应确认以下内容6):
裂隙灯照明和眼前节OCT有助于检测散光型IOL植入后的轴位偏移。术后早期(1周内)确认轴位,旋转矫正成功率较高;3个月后晶状体囊纤维化可能导致重新定位困难4)。
角膜地形图对于检测不规则散光并将其与规则散光区分至关重要。散光型IOL仅矫正规则散光,不规则散光是禁忌证。在后角膜散光较高(PCA ≥0.5D)的病例中,考虑全角膜散光(TCA)进行IOL计算可提高准确性,建议使用Scheimpflug成像评估后角膜形态5)。
散光矫正方法的选择取决于散光类型(规则/不规则)、度数、病因、年龄和患者生活方式。
| 矫正方法 | 适应证 | 特点 |
|---|---|---|
| 眼镜(柱镜) | 规则散光 | 最常见。不适合不规则散光。注意子午线不等像视。 |
| 软性隐形眼镜(散光型SCL) | 规则散光(轻至中度) | 便利性高。旋转稳定性是挑战。 |
| 硬性接触镜(RGP) | 不规则散光、高度规则散光 | 在角膜前表面形成均匀的屈光面。矫正圆锥角膜不规则散光的主要方法。 |
| 巩膜镜(巩膜接触镜) | 高度不规则散光(如圆锥角膜末期) | 由巩膜支撑,对角膜接触少。矫正不规则散光效果优异。 |
儿童中,2D以上的散光有弱视(经线性弱视)风险,早期完全矫正并持续佩戴眼镜非常重要7)。若不等像视成为问题,可考虑降低柱镜度数或调整轴位(15度以内)。
屈光矫正手术矫正散光的效果可能随时间减弱。特别是逆规散光病例,随年龄增长逆规散光加重,可能需要再次手术。LASIK时需注意剩余角膜厚度。
基于证据的角膜屈光手术指南(SMILE)指出,等效球镜度数10D以下(近视10D以下,散光3D以下)为适应症2)。LASIK和PRK适用于近视性散光和远视性散光,但远视矫正的退行风险大于近视矫正1)。飞秒激光弧形角膜切开术(FLACS-AK)的5年结果显示,术前平均散光1.63 D术后显著降至0.53 D,5年后仍稳定在0.55 D3)。
SMILE矫正散光
SMILE(小切口透镜取出术)积极用于近视性散光。KLEx(角膜屈光透镜取出术)指南推荐最大散光矫正量为3D,设计强调剩余角膜厚度至少250 μm,并重视瓣厚加剩余基质床的总和2)。与LASIK相比,可避免瓣并发症,且在角膜神经保护和生物力学稳定性方面更优,但散光轴位的精确设定需要术者熟练。
远视矫正LASIK的退行率高于近视矫正,+4D以上的远视长期结果不稳定。远视性散光(复合远视性散光和混合散光)的手术前提是确认规则散光并进行彻底的术前角膜形态评估1)。
白内障手术也是植入人工晶体(IOL)的机会,可以在不增加额外创伤的情况下矫正散光。术后残余散光的目标是0.5 D以下。
| 矫正方法 | 适用散光量 | 特点 |
|---|---|---|
| 散光型人工晶体(Toric IOL) | ≥1.0 D(规则散光) | 可预测性最高。不规则散光为禁忌症。 |
| LRI(角膜缘松解切口) | 最大3.0 D(可预测性至1.5 D) | 无需昂贵设备。也可用于散光型IOL禁忌的病例。 |
| FLACS-AK(飞秒激光弧形切口) | 1.0~3.0 D | 切口精度高,可预测性优异。 |
| 准分子激光(LASIK/PRK) | 残余散光的二次矫正 | 可同时矫正球镜度数。注意剩余角膜厚度。 |
| 背驮式(附加镜片) | 残余屈光不正较大的病例 | 额外植入后房型人工晶状体 |
| 拆线 | 缝线诱导散光(囊外摘除术后) | 现代适应症有限 |
散光矫正型人工晶状体(Toric IOL)
IOL平面的柱镜度数为1.5~6.0 D,可矫正角膜平面0.75~4.75 D的散光。对于1.0 D以上的规则散光应考虑使用,超过2.0 D时有强有力的证据支持4)。
一项荟萃分析(13项试验)显示,与非散光矫正型IOL相比,散光矫正型IOL显著改善术后裸眼远视力(UDVA)(平均差 -0.07 logMAR,95% CI -0.10~-0.04),并降低未达到20/25或更好的风险4)。
轴位偏移的影响:每偏移1度,矫正效果降低约3.3%。偏移30度时矫正效果几乎消失,超过此度数后术后视功能可能比非散光矫正型IOL更差。
散光矫正型IOL的禁忌症:不规则散光(圆锥角膜、角膜瘢痕、角膜扩张)、悬韧带脆弱或断裂、后囊膜破裂、瞳孔散大不良、重度干眼、曾行巩膜扣带术的玻璃体视网膜手术或青光眼植入物手术。
FLACS-AK(飞秒激光弧形角膜切开术)
由于基于眼前节OCT测量结果设计激光照射方案,因此比手动切开的精度和深度均匀性更高。
Pham等人(2025)对34只眼进行了5年随访队列研究,显示FLACS-AK与白内障手术同时进行,术前平均角膜散光从1.63±0.886 D显著降至术后3个月的0.53±0.628 D(p=0.001),并在5年内保持稳定(5年后0.55±0.624 D)3)。UDVA达到20/25或更好的比例为67.6%,5年内无变化,MRSE在±0.50 D以内的比例在5年后达到91.2%3)。
每偏移1度,矫正效果降低约3.3%;偏移30度时效果几乎消失。偏移30度以上时,术后视功能可能比非散光型IOL更差。IOL旋转易发生在术后1小时至次日早期,因此手术结束时囊袋内固定的稳定性至关重要。长眼轴眼因IOL度数低、光学部薄而易旋转,有报告称同时植入囊袋张力环(CTR)有效。若确认轴位偏移,应尽早考虑重新定位手术。
进入散光眼的光线在陡峭主子午线方向形成前焦线,在平坦主子午线方向更后方形成后焦线。两条焦线之间形成最小弥散圆(Sturm光锥)。等效球镜是陡峭与平坦主子午线屈光度的平均值,对应于最小弥散圆位置的屈光状态。
眼球光学系统的总散光是角膜散光与晶状体散光之和。大部分为角膜散光,但晶状体半脱位时晶状体散光会增强。白内障摘除后晶状体散光消失,因此术后散光基本仅为角膜散光。
后角膜具有负屈光力,其陡峭子午线在多数眼中呈垂直方向。因此,PCA通常与前角膜散光方向相反。在顺规散光眼中,PCA部分抵消前部散光;在逆规散光眼中,PCA则叠加于前部散光之上。
Jin等人(2023)对62只高PCA(≥0.5 D)眼进行回顾性研究,报告称使用总角膜散光(TCA)计算散光型IOL时,逆规组(矫正指数1.14±0.29)和顺规组(矫正指数1.25±0.18)均出现术后过矫5)。逆规组误差量为0.22±0.52 D(p=0.03),顺规组为0.65±0.60 D(p=0.00),均显著偏向过矫方向5)。顺规眼的过矫可能导致轴位反转并诱发术后逆规散光,因此基于TCA的散光型IOL计算推荐用于逆规眼,但在顺规眼中需特别注意5)。
年轻人中顺规性散光(WTR)较多,但随着年龄增长会向逆规性散光(ATR)转变。这被认为是由于晶状体周边硬化及眼睑压迫导致角膜经线方向发生变化所致。这种转变是计算散光型人工晶状体度数及制定角膜缘松解切口计划时需要考虑的因素。
散光的ATR转变速度随年龄增长而加快,尤其在60岁以后变得显著。这种转变是人工晶状体计算时考虑未来散光变化(如目标残余散光略偏向顺规性)的依据4)。长眼轴眼(高度近视)中ATR转变往往更快,这些病例的散光型人工晶状体计算需要更谨慎的评估4)。
3D以上的散光可能存在经线性弱视,即强主经线方向的视力发育受到抑制。超过2D的散光,常规完全矫正对视力发育至关重要。早期发现和早期矫正有望获得良好的视力矫正效果。
弱视PPP(2022年修订版)将屈光参差性散光(单眼强散光)1.5D以上视为弱视风险因素,建议通过屈光筛查(照相筛查)早期发现7)。特别是斜轴散光(轴位在45°或135°附近),与中心视力相比,周边视力和运动视力更容易下降。
在散光的睫状肌麻痹下屈光检查中,准确评估柱镜度数和轴位至关重要。如果阿托品点眼前后柱镜度数或轴位变化较大,应怀疑晶状体散光的参与。无晶状体眼和人工晶状体眼中,角膜散光几乎占全部散光6)。
圆锥角膜是一种进行性角膜扩张症,表现为明显的不规则散光。使用Scheimpflug成像(如Pentacam)的断层扫描显示后表面隆起、变薄及Amsler网格阳性等特征性模式。KLEx(SMILE)指南将疑似圆锥角膜病例(如后表面最大高度≥16μm)列为禁忌症,要求严格的术前筛查2)。
针对圆锥角膜的不规则散光:
这是一种通过紫外线照射可在术后微调人工晶状体屈光力的镜片。术后确认残余屈光度后,通过光照射最终调整度数,有望提高散光矫正的精度4)。
这是一种在手术中实时测量无晶状体眼或有晶状体眼屈光状态,并指导最佳人工晶状体度数和轴向的系统。IA和Barrett Toric计算器在75%的眼中实现了小于0.5D的残余散光,超过了术前计算组的53%。实时修正有望降低再次手术的风险,但需要专用设备和额外时间4)。
基于术前详细角膜成像和患者特定屈光特征的个性化人工晶状体开发正在推进中。探索阐明屈光不正的遗传背景并根据个人眼部特征制定治疗计划的精准医疗方法4)。
KLEx指南中包含了SMILE与LASIK散光矫正效果比较的系统评价2)。SMILE的散光矫正精度(残余散光在0.5D以内的达成率)据报道为75-90%,与LASIK(70-85%)相当或略优。但也有一些报告指出LASIK在散光轴向的预测性上略更稳定。
SMILE散光矫正中轴向精度管理存在挑战,术前数字眼球旋转跟踪和术中列线图调整是提高精度的关键。由于飞秒激光照射位置的微小偏差直接导致残余散光,因此手术经验和技术熟练度必不可少2)。
散光矫正手术(LASIK、SMILE、散光型人工晶状体)后的长期过程中可能出现以下问题:
为尽量减少这些并发症,术前筛查(包括角膜地形图、角膜厚度测量和残余基质床计算)以及长期术后随访是必不可少的1)。
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-139.
Wang Y, Xie L, Yao K, et al. Evidence-based guidelines for keratorefractive lenticule extraction surgery. Ophthalmology. 2025. doi:10.1016/j.ophtha.2025.
Pham TMK, Nguyen XH, Pham TTT, Hoang TT. Five years follow-up outcomes of femtosecond laser-assisted cataract surgery on patients with preexisting corneal astigmatism. Int Med Case Rep J. 2025;18:373-379.
Mallareddy V, Daigavane S. Innovations and outcomes in astigmatism correction during cataract surgery: a comprehensive review. Cureus. 2024;16(8):e67828. doi:10.7759/cureus.67828
Jin T, Yu L, Li J, Zhou Y. Refractive outcomes of toric intra-ocular lens implantation in cases of high posterior corneal astigmatism. Indian J Ophthalmol. 2023;71(8):2967-71. doi:10.4103/IJO.IJO_3385_22
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022;129(1):P1-P126.
American Academy of Ophthalmology. Amblyopia Preferred Practice Pattern 2022 Update. Ophthalmology. 2023;130(3):P136-P178.
Kamari M, et al. Diagnosis of Dry Eye Disease Using Ocular Imaging Techniques. Diagnostics (Basel). 2021;11(8):1466.
Kanclerz P, Przewłócka K, Arnold RW. Agreement in non-cycloplegic and cycloplegic refraction between a photoscreener and a calibrated autorefractor. BMC Ophthalmol. 2024;24:130. doi:10.1186/s12886-024-03394-0