泪液分泌不足型
干燥综合征(Sjögren综合征):泪腺和唾液腺的慢性炎症性自身免疫性疾病。估计患者数50万~100万人。多见于40岁左右的中老年女性(男女比1:14)
非Sjögren型:年龄相关性泪腺功能减退、糖尿病、结节病、GVHD(移植物抗宿主病)等
药物性:抗组胺药、β受体阻滞剂、利尿剂、精神药物、口服避孕药等抑制泪液分泌

干眼综合征(dry eye syndrome)是一种由于多种因素导致泪膜稳定性下降的疾病。可引起眼部不适和视功能异常,并可能伴有眼表损伤。
**日本干眼研究会提出的定义(2016年修订)**如下所示。
“一种因多种因素导致泪膜稳定性下降的疾病,可引起眼部不适和视功能异常,并可能伴有眼表损伤。”
日本定义的特点在于将泪膜稳定性下降定位为病理核心。荧光素染色等检查中上皮损伤的阳性结果已被排除在诊断标准之外,从而能够可靠地诊断泪膜稳定性下降型干眼(BUT缩短型)。
旧定义(2006年,干眼研究会)将其描述为“由多种因素引起的泪液及角结膜上皮的慢性疾病,伴有眼部不适感和视功能异常”。日本分别在1995年、2006年和2016年三次修订诊断标准,作为干眼诊疗的先进国家受到国际认可7)。
TFOS DEWS II(2016年) 的定义为“以泪膜稳态丧失为特征的眼表多因素疾病,泪膜不稳定性和高渗透压、眼表炎症和损伤以及神经感觉异常在病因学中发挥作用”。日本定义以“泪膜稳定性下降”为首要,而国际定义则明确列出了泪液渗透压升高、眼表炎症和神经感觉异常。
日本患病率:
海外患病率:
40至50多岁人群最易患病,女性多见。它是眼科就诊的主要原因之一,且随着数字设备的普及呈增加趋势1)。
日本干燥综合征的估计患者数为50万至100万人,以40多岁为中心的中老年女性多见,男女比例约为1:14。干燥综合征分为原发性(约70%)和继发性(约30%,合并胶原病)两类。在胶原病中,类风湿关节炎常伴有重症干眼(继发性干燥综合征)。
干眼的症状多种多样。称为“泪膜功能障碍”更能反映实际情况。
不稳定的泪膜刺激角膜并向大脑发送信号,从而诱发反射性泪液分泌。然而,这种反射性泪液只是暂时性地增多,不足以恢复泪膜的稳定性,根本问题并未得到解决。这就是干眼症患者出现流泪的原因。
干眼大致分为泪液分泌不足型和蒸发亢进型,许多病例两者混合存在。此外,**水润不足型(BUT缩短型)**在亚洲人群中报道较多,其特点是即使泪液分泌量正常,泪液稳定性也显著降低。
泪液分泌不足型
干燥综合征(Sjögren综合征):泪腺和唾液腺的慢性炎症性自身免疫性疾病。估计患者数50万~100万人。多见于40岁左右的中老年女性(男女比1:14)
非Sjögren型:年龄相关性泪腺功能减退、糖尿病、结节病、GVHD(移植物抗宿主病)等
药物性:抗组胺药、β受体阻滞剂、利尿剂、精神药物、口服避孕药等抑制泪液分泌
蒸发过强型
其他原因包括LASIK/PRK术后(通常为一过性)、眼睑异常(兔眼、睑内翻)、神经营养性角膜病变(三叉神经功能障碍)、Stevens-Johnson综合征、维生素A缺乏症等。
TFOS Lifestyle报告(2023年)系统性地总结了现代生活方式增加干眼风险的机制8)。
数字环境风险:
化妆品与眼妆风险:
营养风险:
危险因素(日本干眼诊疗指南):
2型糖尿病与MGD:
屏幕工作时,眨眼次数从正常约每分钟16次显著降至5~7次,不完全眨眼(眼睑未能完全闭合的眨眼)也会增加9)。不完全眨眼时,脂质层无法均匀扩展到整个角膜表面,油层较薄部位泪液蒸发加剧。建议采用20-20-20法则(每20分钟,注视20英尺远处20秒),并有意识地进行完全眨眼9)。
同时满足以下两项即可确诊为干眼症。
根据2016年修订版,荧光素染色所見的上皮损伤不再作为确诊的必要条件。这一变更反映了日本的临床实际情况,即泪膜稳定性下降型干眼(BUT缩短型)占大多数。
在旧诊断标准(2006年版)中,满足「自觉症状、泪液异常、角结膜上皮损伤三大要素」者被诊断为干眼(确诊病例)。
日本干眼诊疗指南推荐使用在症状评估方面满足信度、效度和反应性的问卷7)。
满足以下4项中2项或以上即可诊断:
干眼症的症状与客观检查结果常不一致,因此开发了用于量化主观症状的问卷。TFOS DEWS III也将症状评估作为诊断和治疗效果评价的基础1)。日本干眼诊疗指南同样重视问卷的信度、效度和反应性7)。
OSDI(眼表疾病指数):由12个项目组成的问卷,作为临床试验中的患者报告结局(PRO)在国际上应用最为广泛。由「眼症状」「视觉相关功能」「环境触发因素」3个亚量表构成,0~12分为正常,13~22分为轻度,23~32分为中度,33~100分为重度。特异度为0.83,灵敏度为0.60。
SPEED(标准干眼评估问卷):由8个项目评估症状的频率和严重程度。0~28分。灵敏度0.90、特异度0.80,适用于日常临床中的纵向监测。
SANDE(干眼症状评估):仅含2个项目的最简洁问卷。使用视觉模拟量表(VAS)评估频率和严重程度。
请根据用途选择。OSDI有12个项目,可评估对生活质量的影响,作为临床试验的PRO已在国际上标准化1)。SPEED有8个项目,可快速实施,灵敏度高达0.90,适用于日常临床中的纵向监测。两者联合使用也有效。
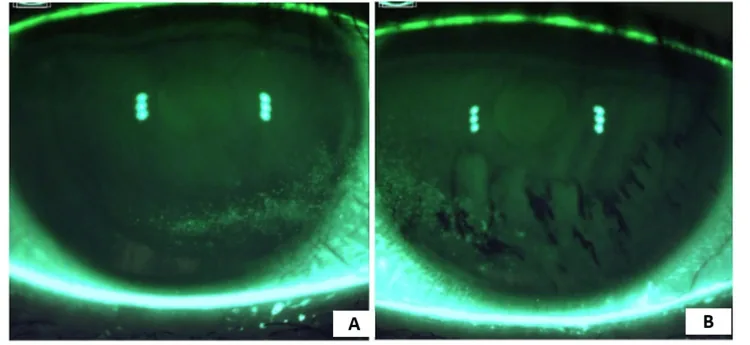
这是日本干眼研究会提出的日本独有的诊断分类。通过睁眼后泪膜破裂模式确定泪膜稳定性下降的原因,并直接与TFOT(分层治疗)相关联。
区域破裂
模式:睁眼后未见荧光素上移,大面积立即发生BUT。伴有黏液斑块/丝状物。
提示的病理状态:重度泪液缺乏型。上皮损伤也高度严重。
首选治疗:通过上下泪点栓植入增加泪液量。
线性破裂
点状破裂
模式:睁眼后立即出现类圆形破裂。泪液量基本正常。
提示的疾病状态:水湿润性低下型。由膜型黏蛋白(MUC16)表达异常导致的角膜水湿润性降低。
首选治疗:地夸磷索钠或瑞巴派特滴眼液
凹点状破裂
模式:在上方伸展的脂质层前端形成凹点(dimple),在水湿润不良区域出现横向线状破裂。
提示的疾病状态:水湿润性低下型
首选治疗:地夸磷索钠或瑞巴派特滴眼液
快速扩展
模式:小的线状破裂快速扩大。
提示的疾病状态:水湿润性低下型
一线治疗:地夸磷索钠或瑞巴派特滴眼液
随机破裂
BUT缩短型干眼是一种特殊类型,泪液量正常(Schirmer值正常),活体染色所见也几乎没有,但BUT显著缩短并呈现强烈自觉症状。其原因被认为是膜型黏蛋白表达异常导致的水润性下降。
这是一种泪液量正常(Schirmer值正常)但BUT缩短的干眼类型。在日本是最多的病型,以往在传统诊断标准中被归类为「疑似干眼」。2016年修订后被正式诊断为干眼,基于TFOD的治疗选择非常重要。地夸磷索钠和瑞巴派特被认为有效。
荧光素BUT(泪膜破裂时间):
非侵入性泪膜破裂时间(NIBUT): 由于荧光素滴眼本身会影响泪膜稳定性,因此开发了利用Placido盘反射像的非侵入性测量方法。灵敏度82–84%,特异度76–94%,红外照明可抑制反射性流泪5)。在日本国内,可使用Keratograph 5M(Oculus公司)和Idra(SBM公司)。
荧光素染色:检测角膜和结膜上皮异常的基本检查。NEI量表将角膜分为5个区域,每个区域评分03分(总分015分)5)。结膜上皮的屏障功能比角膜上皮更脆弱,干眼症中结膜上皮受到同等或更严重的损害。使用无蓝光滤光片可以更清晰地观察结膜上皮状态。
丽丝胺绿和孟加拉玫瑰红:染色结膜的死亡细胞和黏液。van Bijsterveld评分(孟加拉玫瑰红,满分9分)用于Sjögren综合征的眼科诊断标准(≥3分为阳性)。丽丝胺绿的毒性低于孟加拉玫瑰红,耐受性更好。
Schirmer试验: 使用带有1mm间隔刻度的5mm×35mm滤纸。
虽然重复性较差,但作为筛查手段是有用的。
泪河评估:眼表面总泪液量的75%~90%存在于泪河中。正常值约为0.2mm。在染色前观察可直接判断泪液量多少,有助于诊断泪液分泌不足型干眼。眼前节OCT(AS-OCT)可客观定量测量泪河高度(TMH)、面积和容积6)。
泪液渗透压:使用TearLab渗透压计测量。低于300 mOsm/L(双眼差异<8)为正常,300320为轻度,320340为中度,超过340为重度5)。
MMP-9检测(InflammaDry):一种检测泪液中MMP-9的即时检验(POCT),40 ng/mL以上为阳性。有助于判断是否开始抗炎治疗,但在过敏性结膜炎或感染中可能出现假阳性5)。
乳铁蛋白检测:乳铁蛋白是由泪腺腺泡细胞产生的抗菌、抗炎蛋白,干眼患者中其水平降低。可使用TearScan 270 MicroAssay System进行测量5)。
脂质层厚度(LLT): 使用LipiView干涉仪以干涉色单位(ICU)进行定量评估。测量范围为0~240 ICU。还配备不完全眨眼自动检测功能6)。
睑板腺成像(Meibography): 通过红外透射照明法使睑板腺结构可视化的检查。睑板腺缺失(dropout)分为4级(0级=0~25%缺失、1级=26~50%、2级=51~75%、3级=76~100%)进行评估6)。缺失程度和结构变化程度可作为MGD治疗方针的指导。
眼前节OCT(AS-OCT): 除可定量测量泪液半月板外,还可获取角膜厚度、上皮厚度图以及睑板腺的断面图像6)。
共聚焦激光扫描显微镜: 用于角膜的细胞水平评估。可评估神经纤维密度、炎症细胞密度和上皮细胞形态,有助于鉴别角膜神经病理性疼痛和神经营养性疾病6)。
Keratograph 5M(Oculus公司)
LipiView II(J&J Vision公司)
功能:通过干涉测量法进行睑板腺评估和脂质层定量评估。配备自动计算不完全眨眼的视频模块6)
这是日本干眼症研究会推荐的治疗概念。通过TFOD确定泪膜稳定性下降的原因,并根据维持相应泪膜层稳态的需要选择治疗。
TFOT 分层治疗对应表
| 治疗靶层 | 治疗方法 |
|---|---|
| 脂质层 | 热敷、眼睑清洁、少量眼膏、地夸磷索钠(促进脂质层扩散) |
| 水液层 | 人工泪液、泪点栓、透明质酸钠、地夸磷索钠 |
| 分泌型黏蛋白 | 地夸磷索钠、瑞巴派特 |
| 膜结合型黏蛋白 | 地夸磷索钠、瑞巴派特 |
| 上皮细胞(杯细胞) | 自体血清、瑞巴派特 |
| 眼表炎症 | 类固醇、瑞巴派特 |
以下为目前在日本已纳入医保并广泛使用的滴眼液。
0.1%/0.3% 玻璃酸钠滴眼液(Hyalein®): 用于角膜上皮保护和保湿。日本干眼诊疗指南「推荐」使用玻璃酸钠滴眼液7)。
3% 地夸磷索钠滴眼液(Diquas®/Diquas LX®): P2Y2受体激动剂。具有促进水分和黏蛋白分泌以及脂质层延展的作用。该药在日本研发。日本干眼诊疗指南给予「实施」推荐(强推荐)7)。
2% 瑞巴派特滴眼液UD(Mucosta®滴眼液UD): 具有促进黏蛋白分泌和抗炎作用。日本干眼诊疗指南给予「实施」推荐(强推荐)7)。
人工泪液(Soft Santear等,不含防腐剂): 治疗的基础。不含防腐剂的制剂更为理想。日本干眼诊疗指南「建议」(弱推荐)使用人工泪液7)。
0.3%氧氟沙星眼膏(Tarivid®眼膏): 不含防腐剂,油性成分在泪膜表面延展。在重症病例中作为保护剂使用。
反射性泪液分泌减少时,建议使用不含防腐剂的滴眼液。如果认为炎症与症状恶化有关,可考虑联合使用类固醇滴眼液。
轻度至中度:
重症:
环孢素滴眼液: 抑制T细胞介导的炎症。有0.05%(丽眼达®)和0.09%纳米乳剂(Cequa®)两种制剂1)。在2019年日本干眼诊疗指南制定时尚未纳入医保,但近年来部分制剂已获批7)。
立菲司特滴眼液(Xiidra®): 抑制LFA-1/ICAM-1相互作用,阻止T细胞活化及向眼表迁移1)。在国外已上市使用。
类固醇滴眼液: 用于急性加重期的短期炎症控制。日本干眼诊疗指南建议使用(需注意眼压升高)7)。
生活方式调整是干眼症管理的基础1)。建议控制数字设备使用时间、室内加湿、保证充足睡眠、摄入含欧米伽3脂肪酸的饮食1)。然而,DREAM试验(干眼评估与管理,535名参与者,多中心双盲随机对照试验)显示,欧米伽3脂肪酸(EPA 2000mg + DHA 1000mg/日)连续服用12个月与安慰剂相比,并未显著改善OSDI评分(组间差异-1.9,p=0.21)3)。高剂量欧米伽3脂肪酸补充剂的额外效果可能有限。带侧挡板的眼镜和保湿眼镜可减少蒸发、改善症状1)。
MGD是蒸发过强型干眼症的主要原因,需要积极治疗1)。
适用于滴眼液治疗效果不佳的泪液分泌不足型干眼症。日本干眼诊疗指南推荐使用泪点塞7)。
硅胶塞:
液体塞(Keeptear®,高研): 一种去端肽胶原液体塞。主要特点:
插入部位的选择:
并发症:溢泪、塞子移位、自然脱落、泪点扩大、角膜上皮损伤、肉芽形成、泪囊炎
BUT缩短型干眼可能会引起溢泪和视物模糊,需注意。此外,若眼表炎症处于活动期,建议在炎症得到控制后再行插入。
不。泪点栓子的适应症是滴眼液治疗效果不充分的泪液减少型干眼7)。伴有干燥综合征、Stevens-Johnson综合征、GVHD的重症病例也是良好的适应症。另一方面,在泪液量未必减少的BUT缩短型干眼中,可能会引起流泪和视物模糊,需要注意。此外,如果眼表炎症处于活动期,建议在炎症控制后再置入。
日本干眼诊疗指南建议不要使用NSAID滴眼液,并对一般干眼症建议不使用自体血清滴眼液7)。
泪膜从外向内依次为脂质层(源自睑板腺)、水液层(源自泪腺)和黏蛋白层(源自杯状细胞和角膜上皮)三层结构。该结构形成稳定的泪膜,承担保护角结膜、提供营养、维持屈光力及抗菌作用。
泪液量极度不足时,第一阶段无法完成,出现area break。湿润性差(膜型黏蛋白异常)时出现spot/dimple break,水液层蒸发过强时出现random break。
泪腺作为主泪腺,分泌泪液的水液层成分(水、电解质和蛋白质)2)。其分泌受副交感神经、交感神经和感觉神经的严格神经调控2)。
能够对环境变化做出快速反应,泪液电解质浓度的微小变化与干眼症相关2)。
膜型黏蛋白(MUC1/MUC16)维持角膜上皮的湿润性。当其表达受损时,磷脂(疏水性)细胞膜暴露,湿润性降低。这导致泪膜破裂时间缩短型干眼症的发生,并增加高阶像差。
泪膜不稳定形成以下恶性循环。
这种炎症级联反应的恶性循环导致干眼症的慢性化和进展。
DEWS II根据自觉症状的有无和眼表面所见的有无进行分类。自觉症状和眼表面所见均为阳性时诊断为干眼。存在眼表面所见但无自觉症状的情况被视为“神经麻痹状态(感觉功能不全)”,成为预防性管理的对象。
TFOS DEWS III(2025年)提出了基于诊断亚型(aqueous deficient / evaporative / mixed)的循证治疗算法1)。推荐根据不同病型组合泪液补充、泪液保留、泪液刺激、眼科补充剂和睑板腺治疗的系统性方法1)。
在白内障手术或LASIK前积极治疗干眼(尤其是蒸发过强型干眼/MGD),可以改善术后视觉结果和患者满意度1)。前瞻性研究报告显示,LASIK前的LipiFlow治疗可显著改善术后3个月的OSDI和BUT1)。TFOS DEWS III提出术前干眼管理应作为标准治疗1)。
莫替伐特雷普滴眼液0.3%(阿巴雷普®混悬滴眼液): 全球首个具有 TRPV1 拮抗作用 的干眼治疗药物。2025年12月持田制药在日本获得批准,2026年4月由千寿制药上市。通过抑制眼表伤害感受器TRPV1通道,直接抑制神经致敏引起的“刺痛感·异物感”等主观症状,这一点与泪液补充(人工泪液)、促进分泌(地夸磷索·瑞巴派特)、抗炎(环孢素)等现有药物不同。用法为 每次1滴·每日4次。Phase 2b试验(SJP-0132,日本国内多中心随机双盲剂量探索试验)显示DEQS(干眼相关生活质量评分)显著改善13),基于此结果,Phase 3-02试验获得了批准。虽然在泪液量和染色评分方面难以与现有药物拉开差距,但可作为 主观症状优势型(神经痛样症状) 和 现有治疗后症状残留病例 的新选择。
全氟己基辛烷(Miebo®):美国FDA于2023年批准的新型泪液稳定剂。针对蒸发过强型干眼,通过物理方式抑制泪液蒸发。在美国作为处方药使用,在其他地区可能被视为医疗器械。日本的批准状况需要确认1)。
鼻内电刺激(nasal neurostimulation):通过电刺激三叉神经诱发鼻泪反射,促进泪液分泌。TFOS DEWS III将其列为神经调节的治疗选择之一1)。
瓦伦尼克林鼻喷雾剂(Tyrvaya®):刺激三叉神经末梢的烟碱受体,诱导反射性泪液分泌。已在美国获批用于干眼症1)。
生物泪液替代物:自体血清、同种血清及富血小板血浆(PRP)正作为难治性病例的治疗选择进行研究1)。
低水平光疗(LLLT):已有研究报告其对睑板腺功能障碍具有抗炎作用1)。